Синдром тричера коллинза мкб 10
Содержание
- Синонимы диагноза
- Описание
- Симптомы
- Причины
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Другие названия и синонимы
Мандибулофациальный дизостоз, Синдром Тричера Коллинза-Франческетти, Челюстно-лицевой дизостоз.
Названия
Синдром Тричера Коллинза.
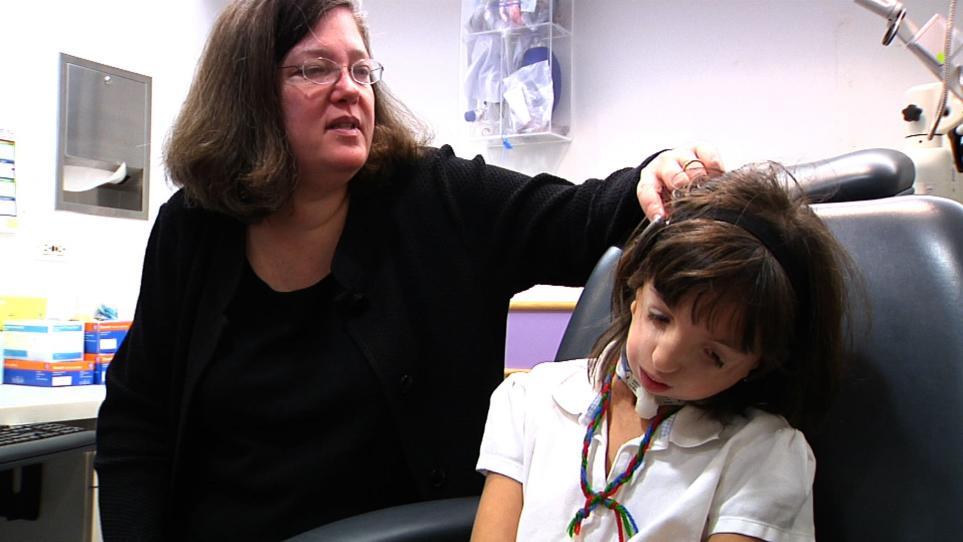
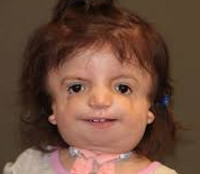
Внешний вид больного с синдромом Тричера Коллинза
Синонимы диагноза
Мандибулофациальный дизостоз, Синдром Тричера Коллинза-Франческетти, Челюстно-лицевой дизостоз.
Описание
Синдром Тричера Коллинза (англ. Treacher Collins syndrome, челюстно-лицевой дизостоз) — аутосомно-доминантное заболевание, характеризующееся черепно-лицевой деформацией. Описан английским офтальмологом Эдвардом Тричером Коллинзом в 1900 году.
Симптомы
Синдром Тричера Коллинза встречается у 1 из 50000 младенцев. Типичные клинические признаки: косоглазие, колобомы век, размер рта, подбородка и ушей существенно меньше нормы. В некоторых случаях — ослабление слуха.
Существуют различные степени этого заболевания — от почти незаметных признаков до крайне тяжелых форм. У большинства пациентов слаборазвитые лицевые кости, что приводит к «затонувшему» лицу, крупный нос и очень маленькие челюсти и подбородок (микрогнатия). У некоторых больных присутствует волчья пасть. В тяжелых случаях, микрогнатия может вытеснять язык пострадавших новорожденных достаточно, чтобы вызвать преграду ротоглотки и потенциально опасных для жизни заболеваний дыхательных путей. Нужно, чтобы надгортанник был удален хирургическим путем, чтобы помочь в дыхательных путях обструкции. Врожденный порок сердца является необычной особенностью.
Причины
Причиной заболевания является, чаще всего, нонсенс-мутация (возникновение стоп-кодона) в гене TCOF1, приводящая к гаплонедостаточности. Синдром наследуется по аутосомно-доминатному принципу и характеризуется высокой пенетрантностью. Экспрессивность может быть различной.
Лечение
Этиотропного лечения нет.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 2 апреля 2020;
проверки требуют 3 правки.
Синдром Тричера Коллинза (англ. Treacher Collins syndrome, TCS, челюстно-лицевой дизостоз, отомандибулярная дисплазия) — аутосомно-доминантное заболевание, характеризующееся черепно-лицевой деформацией. Описан английским офтальмологом Эдвардом Тричером Коллинзом в 1900 году[1].
Синдром Тричера Коллинза встречается у 1 из 50 000 младенцев[2]. Типичные клинические признаки: грубый дефект лицевой части черепа, косоглазие, колобомы век; размер рта, подбородка и ушей существенно меньше нормы. В некоторых случаях — ослабление слуха. У людей с синдромом Тричера Коллинза чаще всего обычный интеллект[3].
Этиология[править | править код]
Причиной заболевания является, чаще всего, нонсенс-мутация (возникновение стоп-кодона) в гене TCOF1, приводящая к гаплонедостаточности.
Ген TCOF1 расположен в локусе 5q32-33, на длинном (q) плече 5-й хромосомы, начинается от 149 737 202-й пары оснований и заканчивается на 149 779 871-й паре оснований[4][5].
Продукт гена TCOF1 — ядерный транспортный белок, который экспрессируется во многих тканях во время эмбрионального и постэмбрионального развития и принимает участие в транскрипции ДНК. При синдроме Тричера Коллинза развивается состояние, при котором половинного количества генного продукта недостаточно для нормального функционирования организма[6].
Синдром наследуется по аутосомно-доминантному принципу и характеризуется высокой пенетрантностью. Экспрессивность может быть от умеренной до выраженной, потому тяжесть дефекта отлична у разных пациентов — от почти незаметных признаков до крайне тяжёлых форм. У большинства пациентов слаборазвитые лицевые кости, что приводит к «затонувшему» лицу, крупный нос и очень маленькие челюсти и подбородок (микрогнатия). У некоторых больных присутствует волчья пасть. В тяжелых случаях микрогнатия может вытеснять язык пострадавших новорожденных достаточно, чтобы вызвать преграду ротоглотки и потенциально опасных для жизни заболеваний дыхательных путей. Врождённый порок сердца является необычной особенностью[7].
Лечение[править | править код]
В лечении пациентов, пострадавших от ТКС, применяется междисциплинарный подход, то есть требуются вмешательства различных специалистов. Основные проблемы у пациентов с ТКС — нарушения глотания и проходимости дыхательных путей. Некоторые пациенты нуждаются в трахеостомии. Гастростома может быть необходима для обеспечения адекватного потребления пищи и для защиты дыхательных путей[8]. Вопрос о хирургическом восстановлении структуры лица решается индивидуально и осуществляется по достижении определённого возраста[9].
Потеря слуха при синдроме Тричера Коллинза вызвана деформацией структур в наружном и среднем ухе. Потеря слуха, как правило, двусторонняя. Даже в тех случаях, когда ушные раковины и наружные слуховые проходы не затронуты синдромом, цепи слуховых косточек часто повреждены[10].
Попытки хирургическим путём восстановить наружный слуховой проход для улучшения слуха у детей с ТКС не дали положительных результатов[11]. Предпочтительной оказалась слуховая реабилитация со слуховыми аппаратами костной проводимости[en] (BAHA) или обычными слуховыми аппаратами[12].
В культуре[править | править код]
- «Чудо» — художественный фильм-драма 2017-го года с главным героем с синдромом ТК
Примечания[править | править код]
- ↑ Treacher Collin E, «Cases with symmetrical congenital notches in the outer part of each lid and defective development of the malar bones», 1900, Trans Ophthalmol Soc UK, 20, p. 190—192
- ↑ Chiara Conte, Maria Rosaria D’Apice, Fabrizio Rinaldi, Stefano Gambardella, Federica Sangiuolo and Giuseppe Novelli. Novel mutations of TCOF1 gene in European patients with Treacher Collins syndrome (англ.) // BMC Med Genet. : journal. — 2011. — 27 September (vol. 12). — doi:10.1186/1471-2350-12-125. — PMID 21951868.
- ↑ Treacher Collins syndrome (англ.). Genetics Home Reference (June 2012). Дата обращения 22 июля 2020.
- ↑ Dixon M.J., Dixon J., Raskova D., et al. Genetic and physical mapping of the Treacher Collins syndrome locus: refinement of the localization to chromosome 5q32-33.2 (англ.) // Human Molecular Genetics (англ.)русск. : journal. — Oxford University Press, 1993. — Vol. 1, no. 4. — P. 249—253. — doi:10.1093/hmg/1.4.249. — PMID 1303194.
- ↑ Dixon M.J., Dixon J., Houseal T., et al. Narrowing the position of the Treacher Collins syndrome locus to a small interval between three new microsatellite markers at 5q32-33.1 (англ.) // American Journal of Human Genetics (англ.)русск. : journal. — 1993. — Vol. 52, no. 5. — P. 907—914. — PMID 8488840.
- ↑ Синдром Тричер Коллинза-Франческетти (мандибулофациальный дизостоз, TCOF) //Центр молекулярной генетики Медико-генетического научного центра РАМН
- ↑ Электронный научный журнал «Медицина и образование в Сибири»
- ↑ Goel L., Bennur S.K., Jambhale S. Treacher Collins syndrome-a challenge for anaesthesiologists (англ.) // Indian Journal of Anaesthesia (англ.)русск. : journal. — 2009. — August (vol. 53, no. 4). — P. 496—500. — PMID 20640217.
- ↑ Evans, Adele Karen; Rahbar, Reza; Rogers, Gary F.; Mulliken, John B.; Volk, Mark S. Robin sequence: A retrospective review of 115 patients (англ.) // International Journal of Pediatric Otorhinolaryngology : journal. — 2006. — 31 May (vol. 70, no. 6). — P. 973—980. — doi:10.1016/j.ijporl.2005.10.016. — PMID 16443284.
- ↑ Argenta, Louis C.; Iacobucci, John J. Treacher Collins Syndrome: Present concepts of the disorder and their surgical correction (англ.) // World Journal of Surgery (англ.)русск. : journal. — 1989. — 30 June (vol. 13, no. 4). — P. 401—409. — doi:10.1007/BF01660753. — PMID 2773500.
- ↑ Marres, HA; Cremers, CW; Marres, E.H. Treacher-Collins syndrome. Management of major and minor anomalies of the ear (англ.) // Revue de laryngologie — otologie — rhinologie : journal. — 1995. — Vol. 116, no. 2. — P. 105—108. — PMID 7569369.
- ↑ Marres, H.A. Hearing loss in the Treacher-Collins syndrome (неопр.) // Advances in oto-rhino-laryngology. — 2002. — Т. 61. — С. 209—215. — doi:10.1159/000066811. — PMID 12408086.
Ссылки[править | править код]
- «Новое лицо Джулианы» — документальный фильм о девочке, родившейся с синдромом Тричера Коллинза тяжёлой формы
Источник

Синдром Тричера Коллинза – это генетическая (иногда наследственная) болезнь, сопровождающаяся деформациями костей и мягких тканей лица. К симптомам относятся грубые дефекты строения лица: антимонголоидный разрез глаз, вырезки ткани век (колобомы), уменьшенные размеры челюсти и скул, гипоплазия и аномалии структур уха, расщелина или арковидная форма неба, увеличенные размеры ротовой щели и языка, слаборазвитые кости лица. Диагноз устанавливается по данным клинического осмотра, биогенетического теста и семейного анамнеза. Лечение симптоматическое, направлено на улучшение слуха, устранение жизнеугрожающих деформаций и косметических дефектов хирургическим способом.
Общие сведения
У синдрома Тричера Коллинза есть несколько синонимов: челюстно-лицевой дизостоз, синдром Тричера Коллинза-Франческетти, мандибулофациальный дизостоз. Впервые патологию описал офтальмолог из Великобритании Эдвард Тричер Коллинз в 1900 году, поэтому наиболее распространено название, соответствующее его имени. Обширный обзор заболевания был сделан в 1949 году европейскими исследователями Э. Франческетти и Д. Клейном. В настоящее время понятие «синдром Тричера Коллинза» более распространено в Великобритании и США, а термин «синдром Франческетти-Клейна» чаще используется в странах Европы. Эпидемиология болезни составляет 1:50 000. Среди мальчиков и девочек заболеваемость одинакова.

Синдром Тричера-Коллинза
Причины
Развитие синдрома в 78-93% случаев обусловлено мутациями гена TCOF1, расположенного на пятой хромосоме в регионе 5q32. Данный ген кодирует производство ядерного фосфопротеина Treacle. У 7-9% пациентов причиной заболевания является дефект гена POLR1C, локализованного на шестой хромосоме, или гена POLR1D, находящегося на тринадцатой хромосоме. Они ответственны за синтез I и III РНК-полимеразы.
При мутациях в гене TCOF1 тип наследования синдрома аутосомно-доминантный с показателем пенетрантности 90%. Это означает, что при мутации в одной хромосоме из пары вероятность проявления болезни очень высока. У больного родителя риск рождения ребенка с синдромом Тричера Коллинза составляет 50%. Возможна наследственная передача дефекта и спорадические генетические изменения (новые мутации). Экспрессивность мутации переменная – в пределах одной семьи вероятно как ослабление, так и усиление симптомов заболевания у последующих поколений. При дефектах генов POLR1C и POLR1D наследование происходит по аутосомно-рецессивному типу. В парах, где родитель имеет синдром, вероятность рождения больного малыша составляет 25%.
Патогенез
Пятая хромосома ответственна за правильное формирование скелета в период внутриутробного развития. Локализованный в ней ген TCOF1 кодирует структуру и синтез ядерного транспортного белка Treacle. Данный протеин экспрессируется в большинстве тканей организма в эмбриональном и постэмбриональном периоде, участвует в переносе генетической информации с ДНК на РНК.
В основе синдрома чаще всего лежит нонсенс-мутация, приводящая к образованию преждевременного кодона терминации и развитию гаплонедостаточности – дефицита белка, необходимого для нормального формирования лицевой части черепа. Здоровый ген обеспечивает организм белком Treacle наполовину, но такого количества недостаточно для правильного развития лицевых структур. При изменениях в генах POLR1D и POLR1C процесс транскрипции ДНК нарушается из-за недостаточности фермента-катализатора ДНК-зависимой РНК-полимеразы. Клинические проявления синдрома такие же, как и при первичной недостаточности Treacle-протеина.
Симптомы
У больных наблюдаются аномалии в строении лица. Распространенным признаком, встречающимся в 80% случаев, является двусторонняя симметричная гипоплазия скуловых костей, инфраорбитального края и нижней челюсти. Внешне это проявляется своеобразным уплощенным бесформенным лицом, на котором выделяется нос, а остальные части «утоплены» в мягких тканях. Деформация челюсти обуславливает нарушение прикуса, формирование ортогнатии (постоянно приоткрытого рта). 89% больных имеют ограниченную возможность открывания рта и антимонголоидный тип разреза глаз с заметным опущением внешнего уголка. Данные особенности частично обусловлены патологическим строением височно-нижнечелюстного сустава.
У 69% пациентов определяется колобома радужки и нижних век в промежутке между средней и внешней третью, чаще она имеет треугольную форму. Ресницы на внешнем крае нижнего века отсутствуют. Небо арковидной формы, иногда сформирована расщелина (у 28% больных). Аномалии наружного уха представлены недоразвитием или полным отсутствием ушной раковины (микротией, анотией), атрезией наружного слухового прохода и деформацией слуховых косточек. Зачастую пациенты имеют кондуктивную тугоухость. В редких случаях диагностируется энхондрома, предкозелковые фистулы, аномальное строение сердца и позвоночника.
Осложнения
Микрогнатия и стеноз верхних дыхательных путей уже в первые годы жизни могут спровоцировать проблемы при приеме пищи и трудности дыхания вплоть до удушья. Своевременная диагностика заболевания позволяет спрогнозировать эти осложнения и предпринять меры по их предупреждению. Как правило, пациенты не имеют врожденных интеллектуальных расстройств, но при отсутствии коррекции нарушений слуха становится невозможным правильное формирование речи и обучение в обычных условиях. Дети начинают отставать в умственном развитии от сверстников, имеют задержку психического развития различной степени выраженности. В связи с наличием дефектов внешности и негативным отношением окружающих больные всех возрастов относятся к группе риска по возникновению депрессии, ипохондрии, тревожности и иных невротических расстройств.
Диагностика
Диагноз может быть установлен во время беременности или сразу после рождения. Обследование показано женщинам из группы риска и детям с врожденными лицевыми деформациями. В процессе диагностики принимают участие врачи-генетики и педиатры. Синдром Тричера-Коллинза необходимо дифференцировать с другими генетическими заболеваниями, при которых существует деформация лицевой части черепа, например, с синдромом Нагера и синдромом Гольденхара. Используются следующие методы:
- Осмотр, сбор анамнеза. Определяются характерные черепно-лицевые аномалии: недоразвитость костей скул и челюсти, деформация и гипоплазия ушных раковин, антимонголоидный тип глазных щелей, нарушения слуха и дефект верхнего неба. Иногда подтвержденный диагноз синдрома имеется у одного из родителей.
- Биогенетический тест. Антенатальное исследование включает молекулярный анализ образца ворсин хориона на 10-11 неделе беременности, фетоскопию и анализ крови из сосудов плаценты на 18-20 неделе. После родов выполняется забор крови из вены ребенка. В обоих случаях исследуется ген TCOF1. Заболевание подтверждается при наличии в нем мутации любого типа.
- Дородовое УЗИ. С 20-24 недели беременности ультразвуковое исследование плода способно выявить типичные изменения лица. Наиболее четко заметна двусторонняя аномалия ушей, гипоплазия скул и челюсти.
Дополнительно назначаются обследования, позволяющие своевременно обнаружить жизнеугрожающие состояния, оценить степень деформации костей черепа. Определяется эффективность кормления ребенка, уровень насыщения гемоглобина кислородом, ритмичность и глубина дыхания. Для диагностики сохранности слуха на 5-6 день жизни проводится аудиологическое тестирование. Инструментальная диагностика включает рентгенографию черепа, КТ и МРТ головного мозга.
Лечение синдрома
Специфической терапии не существует. Лечение нацелено на устранение симптомов и последствий заболевания, предполагает проведение хирургических операций и реабилитационных мероприятий. Объем процедур и сроки их выполнения устанавливаются индивидуально с учетом наличия угрозы для жизни больного, противопоказаний и рисков, связанных с оперативным вмешательством. Общая схема лечения включает:
- Восстановление глотания и дыхания. При развитии респираторного дистресс-синдрома осуществляется трахеостомия, дистракция подвижной челюсти, неинвазивная вентиляция легких. При невозможности потребления пищи устанавливается гастростома.
- Восстановление слуха. Деформация наружного и среднего уха устраняется хирургическим путем, но потеря слуха чаще обусловлена повреждением слуховых мелких косточек, поэтому оперативные вмешательства с целью устранения тугоухости неэффективны. Предпочтительна реабилитация слуховыми аппаратами.
- Устранение внешних дефектов. Деформации корректируются методами пластической и нижнечелюстно-лицевой хирургии. Применяется липоскульптурирование, хирургическая дистракция костей, установка трансплантатов и хирургическое восстановление неба.
Прогноз и профилактика
Комплексное лечение и реабилитация значительно улучшают качество жизни больных. При легкой и умеренной выраженности синдрома прогноз благоприятный. Профилактика затруднена, поскольку заболевание является генетическим, а мутации способны возникать спонтанно. Супружеским парам, в которых один родитель болен, необходимо медико-генетическое консультирование и перинатальная диагностика синдрома на ранних сроках беременности. Для снижения риска вынашивания больного ребенка рекомендуется процедура экстракорпорального оплодотворения с предварительным отбором генетически здоровых эмбрионов.
Источник
Рубрика МКБ-10: Q75.4
МКБ-10 / Q00-Q99 КЛАСС XVII Врожденные аномалии пороки развития, деформации и хромосомные нарушения / Q65-Q79 Врожденные аномалии пороки развития и деформации костно-мышечной системы / Q75 Другие врожденные аномалии (пороки развития) костей черепа и лица
Определение и общие сведения[править]
Синдром Тричера-Коллинза
Синонимы: челюстно-лицевой дизостоз Франческетти-Клейна, челюстно-лицевой дизостоз без аномалий конечностей
Синдром Тричера-Коллинза является врожденным расстройством черепно-лицевого развития, характеризуется двусторонней симметричной ухо-нижнечелюстной дисплазии без аномалий конечностей, а также связан с несколькими дефектами головы и шеи.
Наследуется по аутосомно-доминантному или аутосомно — рецессивному типу.
Ежегодная заболеваемость при рождении оценивается в 1/50000 родившихся живыми.
Этиология и патогенез[править]
Синдром вызывается мутациями гена TCOF1 (5q32), кодирующий фосфопротеин Treacle ядра клетки или генов POLR1C (6p21.1) или POLR1D (13q12.2), кодирующих I и III субъединицу РНК-полимеразы.
Передача аутосомно-доминантная с 90% пенетрантностью и переменной экспрессивностью, даже среди пациентов в пределах одной семьи. Мутации гена POLR1C наследуются аутосомно — рецессивным образом. Генетическое консультирование осложняется переменной экспрессией заболевания.
Клинические проявления[править]
У детей отмечается характерный лицевой дисморфизм с двусторонней симметричной гипоплазией скуловых костей, инфраорбитального края (80% случаев) и нижней челюсти (78%) (ретрогнатия, ретрогения), что приводит к аномалии прикуса, также наблюдается апертогнатия (так называемый «открытый прикус»). Преобладающая гипоплазия мягких тканей отмечается в скуловой кости, нижнем орбитальном крае и щеках. К особенностям также относятся сложные нарушения височно-нижнечелюстного сустава, что приводит к ограниченной возможности открытия рта различной степени тяжести, антимонголоидному разрезу глаз (89%) и колобоме нижних век между внешней и средней третью (69%), сопровождающейся отсутствием ресниц на внешней трети нижнего века. Небо имеет готическую форму и иногда наблюдается расщелина неба (28%). Часто отмечается аномалия наружного уха, например, микротия или анотия, атрезия наружного слухового прохода и аномалии развития слуховых косточек (60%), что вызывает к кондуктивную тугоухость. Умственные способности, как правило, нормальные. Из-за узких верхних дыхательных путей и ограниченного открывания рта в дошкольном возрасте могут возникать трудности с дыханием и питанием. К менее распространенным признакам относится энхондрома и/или предкозелковые фистулы, аномалии строения позвоночника и сердца, а также двусторонние комиссуральные расщелины.
Челюстно-лицевой дизостоз: Диагностика[править]
Диагноз ставят на основании клинических данных и дополнительных исследований и подтверждают с помощью молекулярных тестов.
Дифференциальный диагноз[править]
В ходе дифференциальной диагностики следует исключить синдромы Нагера, Миллера и Гольденхара в их билатеральной и легкой асимметричной форме.
Челюстно-лицевой дизостоз: Лечение[править]
В случаях с послеродовым респираторным дистрессом — трахеостомия, неинвазивная вентиляция легких или дистракция нижней челюсти. Челюстно-лицевая и пластическая хирургия могут скорректировать гипоплазию мягких тканей, костные гипоплазии, колобому века и расщелину нёба. Лечение ограниченного открывания рта очень трудно поддаются коррекции. Специалист по ЛОР хирургии требуется для лечения патологии среднего и наружного уха.
Для устранения аномалий среднего уха (функциональная хирургия) и наружного уха (реконструкция ушных раковин) требуется участие специалиста в области ЛОР-хирургии.
При надлежащем лечении прогноз для легких форм заболевания является благоприятным.
Профилактика[править]
Прочее[править]
Акродизостоз
Синонимы: акродисплазия, синдром Арклеса-Грэхэма, синдром Марото-Маламута
Определение и общие сведения
Акродизостоз является редкой первичной костной дисплазией, характеризуется выраженной брахидактилией, периферическим дизостозом с лицевым дизостозом, носовой гипоплазией и задержкой развития.
Менее 80 случаев акродизостоза было зарегистрировано в литературе до настоящего времени.
Этиология и патогенез
Акродизостоз вызван гетерозиготными мутациями гена PRKAR1A (17q24.2) либо гена PDE4D (5q11.2-q12.1). Мутации PRKAR1A по типу «усиления функции» приводят к потере функции протеинкиназы А (за счет снижения сродства белковых субъединиц цАМФ, тем самым препятствуя диссоциации с каталитической субъединицей). Функциональный дефект PDE4D не был пока охарактеризован, но, как ожидается, также по типу «усиления функции», что приводит к потере функции протеинкиназы А, по крайней мере, в тканях скелета.
Клинические проявления
Типичные клинические признаки акродизостоза включают выраженный периферический дизостоз (низкорослость и брахидактилии, затрагивающие кости пястны, плюсны и фаланги), дизостоз лица (широкое лицо, широко расставленные глаза и максиллоназальную гипоплазию), задержку развития. Часто также наблюдается быстрое скелетное созревание, снижение расстояния между позвонками и ожирение. Некоторые особенности акродизостоза аналогичны тем, которые присутствуют у пациентов с наследственной остеодистрофией Олбрайта, такие как низкий рост, ожирение и брахидактилия (только 4-й и 5-й пястных и плюсневых костей).
Пренатальное начало, множественная гормональная резистентность, чаще всего к паратиреоидному (ПТГ) и тиреотропному (ТТГ) гормонам, сообщается в примерно половине случаев акродизостоза. В то время как у пациентов с мутацией PRKAR1A (акродизостоз типа 1), всегда отмечается выраженная гормональная резистентность, у больных с мутациями PDE4D (акродизостоз типа 2) гормональная резистентность присутствует редко, а если есть, в относительно мягкой форме. Различные степени отставания интеллектуального развития и/или поведенческих расстройств также наблюдаются у пациентов акродизостозом.
Диагностика
Диагноз основывается на клинических, биохимических и рентгенологических (конусообразные эпифиза) исследованиях. Подтверждается результатами генетического скрининга PRKAR1A или PDE4D генов. Базальные уровни цАМФ в моче нормализуются креатинурией, отражение биологической активности ПТГ в почечных проксимальных канальцах, значительно увеличены у пациентов с мутацией PRKAR1A.
Дифференциальная диагностика
Дифференциальная диагностика включает в себя брахидактилию типа Е, псевдогипопаратиреоидизм типа 1a или псевдопсевдогипопаратиреоидизм.
Генетическая консультация
Большинство случаев происходят спорадически, но аутосомно-доминантное наследование было обнаружено в некоторых семьях — в этих случаях генетическое консультирование возможно.
Лечение
Пациенты должны быть обследованы на гормональную резистентность, в частности, к ПТГ и ТТГ, и назначается терапия согласно тем же критериям, дозам, как и в любом другом варианте гипопаратиреоза и гипотиреоза. Показана диета для предотвращения ожирения и поддерживающая когнитивная терапия.
Прогноз
Прогноз неизвестен из-за отсутствия долгосрочных данных о пациентах. Функциональные нарушения могут снижать качество жизни пациента.
Источники (ссылки)[править]
https://www.orpha.net
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
