Синдром коронарный сердца у ребенка
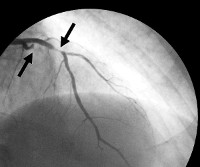
Коронарная недостаточность – это патология сердца, вызванная недостаточным снабжением (или полным его прекращением) питательными веществами и кислородом его средней мышцы – миокарда. Она может иметь острую и хроническую форму. Первый вариант может стать следствием инфаркта и привести к внезапной смерти, второй провоцируется атеросклерозом коронарных артерий, их стенозом (постепенное сужение), заканчивающимся окклюзией (полным закрытием).
Но если за то же время в желудочки поступает недостаточный объём биологической жидкости, значит, присутствует гиподиастолическая декомпенсация. У детей одна из разновидностей этого недуга возникает по ряду причин, среди которых наиболее часто встречаются:
- аномалии (пороки) врождённого характера;
- гипоплазия (недоразвитие) левого желудочка (он уменьшен в размерах);
- недостаточность (относительная) коронарного кровотока;
- травмы или заболевания сосудов, снабжающих ткани сердца кровью (венечные сосуды).
Врождёнными пороками, развившимися ещё в утробе, могут быть:
- ДМПЖ и ДМПП (дефекты межжелудочковой и межпредсердной перегородки);
- стеноз или коарктация аорты;
- ОАП (открытый аортальный проток);
- сужение легочной артерии;
- транспозиция (неправильное расположение) главных сосудов (ТКС).
Такие аномалии являются следствием:
- воздействия токсинов на организм будущей мамы в период вынашивания,
- врождённых заболеваний самого малыша.
Это заболевание условно делят на три периода (фазы), для каждого из которых характерны определённые признаки:
Для первых двух-трёх дней продромального периода характерны симптомы, схожие с признаками ОРВИ. Только потом начинают проявляться расстройства неврологического характера:
- чередование сомнолентности и возбуждения;
- двигательное беспокойство;
- непроизвольное подёргивание мышц (гиперкинез);
- шунто-диффузионная дыхательная недостаточность;
- нарушение перистальтики кишечника;
- бледность, синюшный оттенок губ и ногтей;
- поверхностное учащённое дыхание.
При физикальном обследовании наблюдается:
- жёсткое дыхание;
- признаки дыхательной недостаточности (эмфиземы легких);
- замедленное мочеобразование (олигурия);
- вздутие живота;
- пульс слабый при учащённом сердцебиении;
- сердечные тона глухие.
Период разгара делится на две степени в зависимости от тяжести заболевания. Для первой характерно сокращение времени диастолы (расслабления сердечной мышцы). При этом уменьшения оттока крови не наблюдается. При 2 степени возникает гипосистолия, которая сопровождается:
- артериальной гипотензией (значительным понижением АД);
- учащением пульса при замедленном дыхании;
- отёком лёгких;
- увеличением печени;
- коматозным состоянием.
Если не предпринять адекватные меры, в течение восьми-двенадцати часов из-за сокращения количества доставленного к сердечной мышце кислорода начинает развиваться гипоксия миокарда. Результатом этого заболевания становится отмирание его тканей и общая остановка сердца.
Важную роль в распознавании недуга играет дифференциальная диагностика. Коронарную недостаточность дифференцируют со следующими самостоятельными заболеваниями:
- острым перикардитом или миокардитом,
- фиброэластозом,
- сосудистой недостаточностью,
- врождёнными пороками сердца,
- мерцательной аритмией,
- децентрализацией кровообращения.
Несмотря на значительные достижения, связанные с инструментальным диагностированием заболеваний, включая и коронарную недостаточность, физикальные методы не уступают своих позиций в важности распознавания недугов. Они включают:
- визуальный осмотр пациента;
- пальпацию (ощупывание определённых мест);
- перкуссию (простукивание участков тела);
- аускультацию (прослушивание ухом или с помощью фонендоскопа).
Именно с них начинается диагностическое обследование и устанавливается предварительный диагноз. На основании выводов, сделанных доктором при физическом осмотре, выбираются необходимые инструментальные и лабораторные исследования. Для установления точного диагноза используются такие инструментальные методы обследования:
- электрокардиограмма,
- рентгенография,
- ЭХО-кардиография,
- коронография,
- поликардиография.
Осложнения
При своевременном правильном лечении малыш восстанавливается за короткий промежуток времени. Отсутствие адекватной терапии может привести к его смерти.
При возникновении малейших симптомов надвигающегося приступа коронарной недостаточности задача родителей – максимально быстро доставить малыша в лечебное учреждение.
Терапия недуга обычно состоит из трёх этапов:
- реанимационные мероприятия (только при гипосистолической недостаточности;
- интенсивная терапия (снятие психомоторного возбуждения и купирование тахикардии);
- лечение заболевания, спровоцировавшего болезнь.
Профилактика
Поскольку это заболевание у детей носит врождённый характер, рекомендовать какие-либо профилактические меры не представляется возможным.
Источник
Наиболее частой причиной развития инфаркта миокарда у детей являются врожденные аномалии и приобретенная патология коронарных артерий (острые и хронические коронариты). Коронариты наблюдаются при различных инфекционных заболеваниях, ревматических и неревматических кардитах, инфекционном эндокардите, системной красной волчанке, системных васкулитах, в том числе болезни Кавасаки. Болезнь Кавасаки у детей встречается чаще, чем диагностируется. Поражение сердца при болезни Кавасаки может происходить по типу миокардита (в острой стадии), коронарита с развитием множественных, иногда гигантских аневризм, стенозов и окклюзий коронарных артерий, что способно привести к развитию острого коронарного синдрома, вплоть до инфаркта миокарда. В статье рассмотрен клинический случай отдаленного катамнеза (12 лет) инфаркта миокарда у ребенка с болезнью Кавасаки, которому было проведено кардиохирургическое лечение: резекция аневризмы и маммарокоронарное шунтирование с хорошим результатом. Своевременная диагностика данного заболевания и его осложнений (острого коронарного синдрома и инфаркта миокарда) улучшает прогноз, повышает качество жизни пациентов, снижает риск летального исхода и инвалидизации.
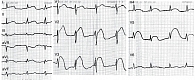
Рис. 1. ЭКГ пациента М. с болезнью Кавасаки, 2 года 10 месяцев
Рис. 2. ЭКГ пациента М. с болезнью Кавасаки, 3 года 9 месяцев
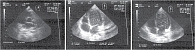
Рис. 3. ЭхоКГ пациента М. с болезнью Кавасаки, 3 года 9 месяцев
Введение
Распространенной причиной развития инфаркта миокарда (ИМ) у детей являются врожденные аномалии и приобретенная патология коронарных артерий [1, 2]. К последним относятся острые и хронические коронариты. Их диагностика сопряжена с определенными сложностями, поэтому истинная распространенность остается неизвестной. В большинстве случаев диагноз устанавливают при аутопсии.
Коронариты встречаются при различных инфекционных заболеваниях, ревматических и неревматических кардитах, инфекционном эндокардите, системной красной волчанке, системных (первичных) васкулитах (гигантоклеточный (височный) артериит, артериит Такаясу, узелковый полиартериит (классический), болезнь Кавасаки, гранулематоз Вегенера, синдром Черджа – Стросса, микроскопический полиангиит, пурпура Шенлейна – Геноха и др.) [3, 4], опухолях сердца (вторичные васкулиты). Клиническая картина коронарита однотипна независимо от этиологического фактора и характеризуется острой коронарной недостаточностью, вплоть до развития ИМ [5–7].
Болезнь Кавасаки (слизисто-кожно-лимфоузловой синдром) – системный васкулит с преимущественным поражением коронарных артерий. Обычно встречается в раннем детском возрасте. Поражение сердца может происходить по типу миокардита (в острой стадии), коронарита с развитием множественных, иногда гигантских аневризм (на 6–8-й неделе), стенозов и окклюзий коронарных артерий, что в ряде случаев приводит к развитию острого коронарного синдрома и ИМ [8–10], даже в отдаленные сроки от начала заболевания.
Клинический случай
Ребенок М., три года семь месяцев, поступил в отделение кардиоревматологии Республиканской детской клинической больницы (РДКБ) г. Симферополя 29 мая 2006 г. с жалобами на слабость, одышку при физической нагрузке.
Из анамнеза жизни и болезни известно, что ребенок болен на протяжении года. В июне 2005 г. впервые отмечались эпизоды подъема температуры до фебрильных цифр, плохо поддававшиеся антипиретической терапии и резистентные к антибиотикам, высыпания на теле, которые расценивались как аллергическая реакция, артралгии. Был госпитализирован в центральную районную больницу с диагнозом: «острая респираторная вирусная инфекция, тяжелое течение, гипертермический синдром. Атопический дерматит. Острый пиелонефрит. Экссудативный перикардит». Результаты общего анализа крови показали увеличенную скорость оседания эритроцитов (СОЭ) – до 64 мм/ч, лейкоцитоз – до 14,4 × 1012/л с палочкоядерным сдвигом до 17%, высокую серологическую активность (С-реактивный белок (СРБ) +++), антистрептолизин-О (АСЛ-О) – отрицательный. В общем анализе мочи – лейкоцитурия.
При эхокардиографии (ЭхоКГ) выявлены признаки перикардита.
Проведены антибактериальная терапия, терапия глюкокортикостероидами, на фоне которой отмечалась положительная динамика. После этого ребенок был выписан под наблюдение врачей поликлиники по месту жительства с рекомендацией повторного осмотра через месяц и консультации в РДКБ. Однако родители ребенка на протяжении всего года к врачам не обращались.
При поступлении в РДКБ выполнено обследование. Общий анализ крови показал выраженный лейкоцитоз – до 30,2 × 1012/л, палочкоядерный сдвиг до 17%, СРБ++++, увеличение СОЭ – до 61 мм/ч, циркулирующие иммунные комплексы – 283 Ед, АСЛ-О – отрицательный, повышенный уровень трансаминаз. Выполнена SIPS-пункция: по результатам миелограммы, острый лейкоз отсутствовал. При компьютерной томографии органической патологии не выявлено. Рентгенологическое исследование органов грудной полости показало расширение сердца в поперечнике, кардиоторакальный индекс – 78%.
При ретроспективном анализе серии электрокардиограмм (ЭКГ) в динамике (начиная с июня 2005 г.) стало понятно, что врачи поликлиники по месту жительства явно недооценили полученные результаты. Отмечались отрицательная динамика ЭКГ – усиление провала зубца R в отведениях V1–V4, элевация ST выше изоэлектрической линии с отрицательным зубцом T в грудных отведениях. На ЭКГ от 1 августа 2005 г. зарегистрирован синусовый ритм с частотой сердечных сокращений 94–120 в минуту. Электрическая ось сердца не отклонена. Зафиксированы изменения в виде дугообразного подъема над изолинией сегмента RS–T в отведениях V2–V3 (резко выраженная элевация от +9 до +15 мм), в отведениях I, AVL, V4–V5 – умеренно выраженная элевация. Комплекс QRS представлен в отведениях I – qR, AVL – qr, V4–V5 – Rs, V2–V3 – rs (рис. 1).
На последующих ЭКГ (с 12 августа 2005 г. по июнь 2006 г.) отсутствовала динамика графических изменений в виде комплекса QS в отведениях V1–V5 с глубоким инвертированным зубцом Т в отведениях V1–V6, умеренно выраженной элевацией сегмента ST. В отведениях I, AVL зарегистрирован комплекс qR. Данные изменения характерны для перенесенного трансмурального ИМ передней стенки левого желудочка (ЛЖ) и передне-перегородочной области. Застывшая кривая ЭКГ свидетельствовала об аневризме ЛЖ (рис. 2).
Кроме того, отрицательную динамику продемонстрировала ЭхоКГ: нарастала дилатация ЛЖ, прогрессивно снижалась сократительная способность миокарда (конечный диастолический объем (КДО) – 83 мл, конечный диастолический индекс (КДИ) – 126 мл/м2, фракция выброса (ФВ) – 28%), сократимость ЛЖ резко снижена, дискинезия передне-верхушечной зоны с образованием аневризмы. Патология левой коронарной артерии: расширенный ствол с дилатацией до 7 мм в месте бифуркации (рис. 3).
Ребенок был направлен в Научно-практический медицинский центр детской кардиологии и кардиохирургии Министерства здравоохранения Украины (г. Киев) с диагнозом: «болезнь Кавасаки. Множественные аневризмы коронарных артерий. Постинфарктный (2005 г.) кардиосклероз. Аневризма передне-верхушечной зоны левого желудочка». В центре ребенку провели хирургическое вмешательство: аневризма ЛЖ (по передней, боковой и задней стенке) вскрыта разрезом, произведена резекция аневризмы 6 × 1,5 см. Выполнены эндовентрикулопластика, маммарокоронарное шунтирование (наложен шунт между LIMA – LAD).
В послеоперационном периоде ребенок получал противорецидивное лечение. Через год после операции самочувствие хорошее, жалоб нет. ЭхоКГ: расширенная полость ЛЖ – КДО – 73 мл, конечный систолический объем – 43 мл, КДИ – 96 мл/м2, ФВ – 59%, правая коронарная артерия – до 6 мм. Сохранялась акинезия верхушечных (переднего, бокового) сегментов. Гипокинезия перегородочных сегментов.
В отдаленном послеоперационном периоде (2015 г.) больному провели спиральную компьютерную томографию с внутривенным контрастированием: истончение миокарда и его аневризматическое расширение на верхушке (30 × 14 × 10 мм), а также снижение сократительной способности миокарда на том же уровне. При коронарографии выявлены два аневризматических расширения правой коронарной артерии – 17 × 10 мм и 11 × 6 мм. Функция маммарокоронарного шунта удовлетворительная.
В настоящее время мальчику 16 лет (катамнез – 12 лет), состояние удовлетворительное, находится под наблюдением детских кардиологов.
Заключение
Болезнь Кавасаки у детей встречается чаще, чем диагностируется. Настороженность практических врачей в отношении данной патологии, своевременная диагностика не только заболевания, но и его осложнений в виде острого коронарного синдрома и инфаркта миокарда улучшают прогноз, повышают качество жизни больных, снижают риск летального исхода и инвалидизации.
Источник

Кардиальный синдром Х – это патологическое состояние, возникающее в результате недостаточного снабжения миокарда кислородом при неизмененных (интактных) коронарных артериях. Типичными симптомами выступают проявления стенокардии напряжения: боль в груди, усиливающаяся при физической нагрузке и эмоциональном стрессе, одышка, тахикардия. Диагностика производится на основании данных опроса, электрокардиографии, коронарографии, фармакологических нагрузочных тестов, сцинтиграфии миокарда. Программа лечения предусматривает использование бета-блокаторов, нитратов, блокаторов кальциевых каналов и ряда иных средств.
Общие сведения
Кардиальный синдром Х (КСХ, микроваскулярная стенокардия) впервые был описан американским исследователем Г. Кемпом в 1973-м году как ишемия миокарда без признаков поражения коронарных сосудов. В настоящее время патология выявляется примерно в 20-30% случаев коронарографии, выполняемой для выяснения причин кардиалгии. Среди заболевших преобладают лица среднего возраста, у женщин КСХ выявляется в 2-3 раза чаще, нежели у мужчин, особенно в возрастной группе 40-45 лет. Предполагается, что распространенность болезни намного выше, поскольку значительная часть случаев не диагностируется.

Кардиальный синдром Х
Причины
Этиология КСХ считается сложной и окончательно не изученной. Предполагается несколько основных механизмов развития патологического состояния, возможно их сочетание у одного больного. В основе большинства теорий лежит кардиальный генез заболевания (развитие по причине изменений в миокарде или его сосудистом русле). Имеются отдельные гипотезы о появлении симптомокомплекса в результате внесердечных нарушений – поражения вегетативной нервной системы, аномалий ноцицептивной чувствительности. Наиболее распространенными причинами КСХ считают:
- Структурные изменения артериол. Коронарные сосуды мелкого калибра не визуализируются при коронарографии, поэтому их аномалии очень сложно выявить. Однако сужение их просвета уменьшает перфузию миокарда, из-за чего может развиваться стенокардия.
- Дисфункция эндотелия. В результате нарушения работы клеток, выстилающих микроциркуляторное русло, снижается скорость доставки кислорода и энергетических соединений к кардиомиоцитам, что вызывает патологические изменения.
- Усиленная симпатическая активация. Под влиянием симпатической системы сужаются преартериолы, уменьшается поступление крови к тканям сердца. Такой механизм особенно актуален при наличии у больного тревожности, эмоциональной нестабильности, депрессии.
- Метаболические и ионные нарушения. Ряд веществ, ионы калия, кальция и натрия при аномальных концентрациях затрудняют процессы транспорта кислорода в миокарде, что приводит к его дефициту и стенокардии. Примером могут быть боли в сердце при гиперкалиемии, высоком уровне инсулина и иных состояниях. Аналогичный механизм предположительно отмечается на фоне снижения уровня эстрогена при климаксе.
- Расстройство болевой чувствительности. У части больных КСХ заболевания сердечно-сосудистой системы отсутствуют, но может быть снижен болевой порог на уровне нервов или таламуса. Это потенцирует появление субъективных симптомов – кардиалгии, усиливающейся на фоне нагрузок или переживаний, при нормальной перфузии и насыщении миокарда кислородом.
В отдельных случаях причиной КСХ являются начальные формы атеросклероза коронарных артерий, при которых бывает сложно выявить наличие бляшек в сосудах. Точное установление причин микроваскулярной стенокардии имеет большое значение для определения оптимальной программы лечения, осуществляется путем тщательной многокомпонентной диагностики.
Патогенез
Механизм формирования кардиального синдрома X зависит от причин его развития. При поражении микроциркуляторного русла миокарда (так называемой «истинной» микроваскулярной стенокардии) средняя оболочка артериол разрастается, в результате чего сужается просвет сосуда. Возникает ишемия сердца, не определяемая при проведении коронарографии, но выявляемая посредством иных диагностических исследований, например, сцинтиграфии. Аналогичные изменения возможны при симпатической активации – выделяющиеся медиаторы вызывают спазм сосудов, уменьшая объем поступающей крови.
При дисфункции эндотелия и метаболических нарушениях макроскопически артериолы не изменяются, но страдает транспорт кислорода и питательных веществ из крови в ткани. Одним из следствий кислородного голодания (как из-за снижения перфузии, так и по причине нарушения поступления кислорода) может быть развитие блокады ножек пучка Гиса. При КСХ изредка страдает левая ножка, что может спровоцировать дилатационную кардиомиопатию или мелкоочаговый кардиосклероз.
Симптомы
Клиническая картина КСХ сходна с ишемической болезнью сердца. Первым симптомом становятся давящие боли в левой половине грудной клетки, часто иррадиирующие в область левой лопатки, руки или нижней челюсти. Неприятные ощущения возникают или усиливаются при нагрузке, эмоциональных переживаниях. Провоцировать приступы боли может холод, или, напротив, перегрев тела. У значительной части больных симптомы не устраняются приемом нитратов (например, нитроглицерина). Это обстоятельство, наряду с увеличенной длительностью приступа относительно типичной стенокардии, нередко является причиной формирования ложной картины инфаркта миокарда.
Примерно у 30-40% больных кардиалгия возникает в спокойном состоянии, провоцирует чувство тревоги и страха. Пациент с этой формой кардиального синдрома может бояться скорой смерти из-за сердечной патологии, считать, что у него инфаркт или другая опасная болезнь. Как правило, эмоциональные переживания еще больше усиливают ишемию миокарда, приводят к увеличению выраженности болевого синдрома. Для многих больных характерна раздражительность. При таком течении заболевания нередко требуется помощь не только кардиолога, но и психолога или психиатра.
Помимо кардиалгии у пациентов с микроваскулярной стенокардией могут обнаруживаться жалобы на одышку, затрудненное дыхание, ощущение усиленного сердцебиения. Какие-либо симптомы недостаточности кровообращения (цианоз носогубного треугольника и дистальных отделов пальцев) зачастую не выявляются. Их наличие обычно свидетельствует о развитии осложнений или неверной диагностике состояния. Длительность заболевания без лечения может составлять годы, частота приступов индивидуальна и зависит от множества факторов – характера патологии, уровня физической активности больного, особенностей его метаболизма и гормонального фона.
Осложнения
Синдром протекает доброкачественно и даже при отсутствии лечения крайне редко провоцирует появление осложнений. По мнению исследователей, самым распространенным последствием патологии является ишемическая болезнь сердца «типичного» характера – то есть, с поражением коронарных артерий. Однако не все специалисты считают, что эти два состояния взаимосвязаны. Некоторые ученые связывают развитие ИБС на фоне КСХ с возрастными или метаболическими факторами. У части пациентов может возникать внутрисердечная блокада, способная провоцировать кардиомиопатию дилатационного типа. Отмечается ухудшение качества жизни больных из-за периодических приступов, негативно влияющих на активность и трудоспособность.
Диагностика
Для выявления кардиального синдрома и его дифференцировки от иных сердечно-сосудистых патологий применяют множество диагностических приемов и методов. В первую очередь необходимо выявить признаки ишемии миокарда и, в то же время, исключить поражение коронарного русла, характерное для обычной ИБС. Следующие шаги направлены на определение причин патологического состояния для разработки наиболее эффективной схемы лечения. Диагностика КСХ включает следующие этапы:
- Опрос и общий осмотр. Пациенты жалуются на приступообразные боли в области сердца давящего или колющего характера на фоне физической нагрузки или (реже) в состоянии покоя. Нередко обращает на себя внимание тревожность и раздражительность больного. При аускультации сердца может определяться тахикардия, изредка – нарушения ритма.
- Рентгенография венечных артерий. Коронарография является одним из ключевых исследований, позволяющим дифференцировать кардиальный синдром от других форм поражения сердца. Изменения в сосудистом русле (например, сужения, обусловленные атеросклерозом, спазмом или воспалительным процессом) обычно не определяются.
- Сцинтиграфия миокарда. Перфузионная сцинтиграфия дает возможность посредством введения радиофармпрепарата с теллуром-201 оценить качество кровоснабжения сердечной мышцы, обнаружить очаги ишемии. При КСХ перфузия понижена, выявляются отдельные участки с резким уменьшением объема поступающей крови.
- Электрокардиография. ЭКГ при кардиальном синдроме подтверждает типичные признаки ИБС – депрессию сегмента ST более 1,5 мм, однако такое нарушение является преходящим и может быть не обнаружено при регистрации стандартной электрокардиограммы. Диагностическую значимость имеет проведение исследования по Холлу – регистрация ЭКГ на протяжении 48 часов. Ишемическая депрессия ST чаще наблюдается утром или в дневное время, при эмоциональной или физической нагрузке.
- Фармакологические пробы. Характерным признаком КСХ, доказывающим внутрисердечную природу патологии, является эргометриновая проба. Положительный результат данного теста указывает на склонность тканей миокарда к ишемии. Аналогичный вывод делают при положительной дипиридамоловой пробе.
В качестве дополнительных методов диагностики осуществляют изучение крови коронарного синуса (выявляется увеличение уровня лактата), определяют количество инсулина в крови. Доказано, что при низкой восприимчивости тканей к данному гормону риск возникновения кардиального синдрома увеличивается в несколько раз. Производят определение уровня основных ионов крови (кальция, калия, натрия) и количество эстрогена у женщин. Дифференциальную диагностику проводят с коронарным атеросклерозом, вторичной микроваскулярной стенокардией (при васкулитах, амилоидозе), миокардитами и внесердечными состояниями – остеохондрозом грудного отдела, межреберными невритами и миозитами, плевритом.
Лечение кардиального синдрома Х
Специфическое лечение отсутствует, с помощью медикаментов можно только устранить основные патогенетические нарушения – улучшить перфузию миокарда, облегчить транспорт питательных веществ и кислорода из крови. Терапия обязательно должна быть комплексной, требует активного взаимодействия врача и пациента. Зачастую индивидуальная схема лечения определяется опытным путем, посредством назначения определенных препаратов и последующего наблюдения за динамикой болезни. Чаще всего применяются следующие группы лекарственных средств:
- Бета-адреноблокаторы. Являются наиболее популярными антиангинальными препаратами, включают атенолол, бисопролол и другие медикаменты. Снижают частоту сердечных сокращений, уменьшают потребность миокарда в кислороде, улучшают коронарную перфузию, ослабляя выраженность симптомов заболевания.
- Антагонисты кальция. Из этой группы при КСХ предпочтительны блокаторы медленных кальциевых каналов – нифедипин, верапамил. Они способствуют расширению сосудов, обеспечивая увеличение притока крови к сердечной мышце.
- Активаторы калиевых каналов. Перспективное средство для терапии кардиального синдрома – никорандил. Он эффективно устраняет гипоксические процессы в сердце, способствует восстановлению его кровоснабжения и обладает кардиопротективным действием.
- Нитраты. Сублингвальные антиангинальные препараты (например, нитроглицерин) эффективны лишь у половины больных с данной патологией. Более того, у 10-15% пациентов прием нитроглицерина для купирования приступа вызывает усиление болей и других симптомов. Поэтому такие лекарства должны назначаться крайне осторожно и строго индивидуально.
- Заместительная гормональная терапия. Является достаточно эффективным методом лечения КСХ у женщин, если он возник на фоне климакса. Восстановление уровня эстрогенов значительно снижает частоту и силу приступов, улучшая качество жизни больных.
В качестве вспомогательного лечения применяют антиагреганты (ацетилсалициловую кислоту), статины для уменьшения уровня липопротеидов крови, ингибиторы АПФ для кардиопротективного и гипотензивного эффекта. Большое внимание уделяют лечебной физкультуре – она повышает болевой порог и устойчивость больных к физическим нагрузкам. По некоторым данным, аллопуринол и метформин также можно применять при данной патологии, особенно если ее возможной причиной выступает дисфункция эндотелия. У лиц с повышенной тревожностью и эмоциональной нестабильностью оправдано использование седативных средств и антидепрессантов.
Прогноз и профилактика
Прогноз кардиального синдрома X в большинстве случаев благоприятный – несмотря на наличие приступов, заболевание не прогрессирует, осложнения развиваются крайне редко. Основным последствием, особенно при отсутствии лечебных мер, является снижение качества жизни больного. Адекватная терапия в сочетании с умеренной физической активностью способны заметно снизить как частоту, так и выраженность приступов, но они все равно могут периодически возникать на протяжении многих лет. Методы профилактики синдрома отсутствуют, лицам, имеющим такой диагноз необходимо регулярно проходить обследование у кардиолога для возможной коррекции схемы лечения.
Источник
