Сердце плода с синдромом дауна
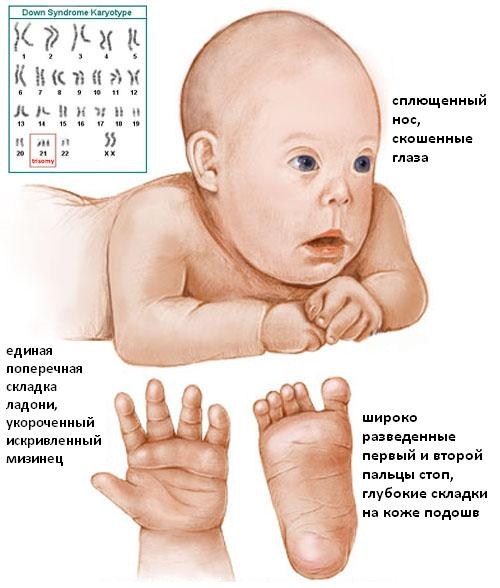
Хорошо известно, что врожденные аномалии сердца встречаются почти у половины детей с синдромом Дауна и оказывают большое влияние на младенческую выживаемость. С середины прошлого столетия проводилось множество исследований по выявлению частоты, специфичности и характера пороков сердца у этих детей. Так, в период 1970–1980-х гг. отмечалось повышение распространенности врожденных аномалий сердечнососудистой системы у пациентов с синдромом Дауна. Связано это было в основном с улучшением диагностики открытого артериального протока и дефекта межпредсердной перегородки (M. J. Khoury, J. D. Erickson, 1992). По данным зарубежных авторов, при синдроме Дауна наиболее часто встречаются дефект межжелудочковой перегородки, дефект межпредсердной перегородки, общий открытый атриовентрикулярный канал, тетрада Фалло и другие пороки, составляющие менее 1 %.
За годы научных наблюдений стало очевидным, что для выявления врожденного порока сердца у новорожденного с синдромом Дауна физическое обследование, включающее осмотр и аускультацию, является обязательным, но недостаточным. Так, McElhinney и др. установили, что информативность физического обследования для выявления сердечных аномалий у детей с синдромом Дауна не превышает 80 %. Оказалось, что 15 из 114 исследуемых детей при осмотре не имели признаков врожденных пороков сердца, но при ультразвуковом исследовании у них были диагностированы сердечные аномалии, а девяти из них в дальнейшем потребовалось оперативное лечение.
Материалы и методы
Нами проведено исследование частоты встречаемости и особенностей клинической картины врожденных пороков сердца и персистирующих фетальных коммуникаций у 522 детей с синдромом Дауна в возрасте от 0 до 8 лет, воспитывающихся в домашних условиях. Дети получали медико-психолого-педагогическую помощь в Центре ранней помощи Благотворительного фонда «Даунсайд Ап», где наблюдались с момента обращения (возраст при первом посещении варьировал от 0 до 7 лет) до 8 лет. При первичном обращении проводился сбор анамнеза, клиническое обследование, анализ медицинской документации. Все дети, даже в случае отсутствия клинически выраженных симптомов порока сердца, направлялись на электрокардиографическое и эхокардиографическое обследования и, при необходимости, на лечение в соответствующие профильные кардиологические стационары и диспансеры.
Результаты
У всех пациентов синдром Дауна был подтвержден хромосомным исследованием. Регулярная трисомия 21-й хромосомы была выявлена у 499 детей (499/522), что составило 90,4 %, транслокационная форма – у 24 (4,3 %), мозаицизм – у 28 (5,1 %), у одного ребенка трисомии 21-й и Х хромосом (кариотип 48,ХХХ,+21) – 0,2 %.
Получены результаты эхокардиографического исследования 428 детей (см. рис.). Врожденные пороки сердца диагностированы у 195 (195/428), что составило 45,6 %. В структуре этих аномалий у детей с синдромом Дауна чаще отмечался дефект межпредсердной перегородки (ДМПП), а именно в 30,2 % (59/195) случаев. Общий атриовентрикулярный канал (ОАВК) составил 24,1 % (47/195), дефект межжелудочковой перегородки (ДМЖП) – 23,1 % (45/195), сочетание дефектов межпредсердной и межжелудочковой перегородок (ДМПП+ДМЖП) – 10,8 %. Другие пороки, такие как тетрада Фалло, стеноз легочной артерии и др., в сумме составили 11,8 % (23/195). Персистенция гемодинамически значимого открытого артериального протока (ОАП), потребовавшего оперативного вмешательства, была выявлена в 2,8 % (12/428).
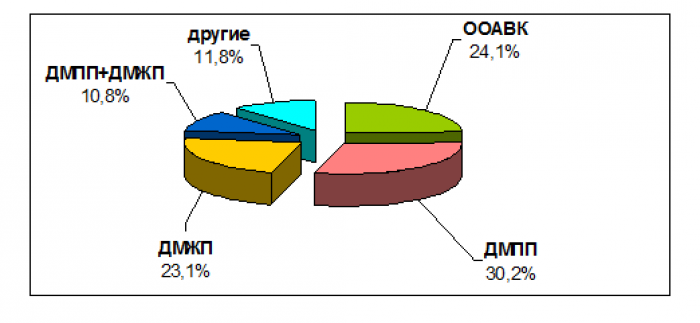 Структура сердечных аномалий у детей с синдромом Дауна
Структура сердечных аномалий у детей с синдромом Дауна
Почти все исследуемые нами дети родились доношенными. Срок родов составил 38,2 ± 1,3 недель. Однако при оценке антропометрических данных новорожденных с синдромом Дауна и врожденными пороками сердца оказалось, что их физическое развитие страдает еще внутриутробно. Задержка физического развития (ЗВУР) – масса тела при рождении ниже 10 перцентилей в соответствии со сроком гестации в сравнении с показателями физического развития Г. М. Дементьевой, Е. В. Короткой – отмечалась у 18,7% детей. У всех новорожденных с сердечными аномалиями наблюдалась асимметричная форма ЗВУР (Pounderal Index, PI>25). Вероятно, задержка физического развития формировалась под влиянием, в основном, не генетического фактора.
Известно, что у новорожденных с синдромом Дауна нередко отмечается морфофункциональная незрелость (по нашим данным, она встречается в 17,9 % случаев). У детей с морфофункциональной незрелостью часто недооцениваются размеры дефекта межпредсердной перегородки, который рассматривают как открытое овальное окно даже при гемодинамической его значимости, и артериального протока, в то время как имеет место недостаточность кровообращения. Застойная легочная гипертензия приводит к развитию пневмонии. Возникновение и затяжное течение пневмонии у детей с синдромом Дауна объясняется характерными для них иммунологическими нарушениями.
Хорошо известно, что манифестация сердечной недостаточности у детей раннего возраста, в отличие от детей старшего возраста, может протекать под маской других состояний. Помимо классических симптомов, таких как тахикардия (учащение сердцебиения), тахипноэ (увеличение частоты дыхания), цианоз кожи и слизистых, типичны вялое сосание, снижение темпов физического и психомоторного развития. В подобных случаях у педиатров возникают определенные затруднения в проведении дифференциальной диагностики при наличии у ребенка синдрома Дауна. У таких детей клинические симптомы недостаточности кровообращения могут расцениваться как проявления особенностей психомоторного развития, типичных для синдрома Дауна. Так, если возникают трудности вскармливания: ребенок вялый, неохотно берет грудь или соску, вяло сосет, не может высосать необходимый объем питания, вплоть до полного отказа от кормлений, такие проблемы часто объясняются мышечной гипотонией, общей вялостью, характерной для детей с синдромом Дауна, с последующим назначением общеукрепляющего массажа, что ухудшает состояние ребенка. В дальнейшем отмечается плохая прибавка в весе. Она направляет клиницистов на выявление патологии со стороны желудочно-кишечного тракта, гипогалактии у матери, исследования качества молока, его инфицированности. В борьбе с прогрессирующей гипотрофией младенца нередко переводят на искусственные смеси. Важно отметить, что гипотрофия может стать причиной отсрочки оперативного лечения порока сердца и/или неблагоприятно повлиять на его исход.
Таким образом, слабая нацеленность педиатров на выявление симптомов недостаточности кровообращения у ребенка с синдромом Дауна затрудняет ее своевременную диагностику, а следовательно, и адекватное лечение врожденного порока сердца.
Наглядным примером будет анализ истории болезни.
Андрей Б., от первой, физиологично протекавшей беременности. Роды в срок. Вес мальчика при рождении – 3000 г., рост – 51см, оценка по шкале АПГАР 88б. Состояние ребенка после рождения удовлетворительное. Отмечались признаки морфофункциональной незрелости, фенотипические признаки синдрома Дауна. С целью подтверждения хромосомной патологии была взята кровь для определения кариотипа. Выявлена регулярная трисомия 21-й хромосомы. С первых суток жизни отмечался систолический шум при аускультации грудной клетки. Для исключения аномалий развития сердца проведено ЭХОКГ и обнаружено открытое овальное окно размером 4 мм. Ребенок был выписан домой под наблюдение участкового педиатра и кардиолога по месту жительства. В дальнейшем мальчик стал вялым, неохотно брал грудь, отмечались частые срыгивания, редкий стул. За месяц ребенок прибавил в весе 210 г. При осмотре обращали на себя внимание признаки недостаточности кровообращения: одышка в покое, умеренная тахикардия. Мальчик был направлен в НЦССХ им. Бакулева, где диагностирован порок развития сердца – дефект межпредсердной перегородки размером 6 мм со значительным нарушением сердечной гемодинамики. Рентгенограмма грудной клетки показала расширение корней легких, КТИ = 57 %. По данным ЭКГ: отклонение электрической оси сердца вправо. В возрасте 4 месяцев проведено оперативное лечение дефекта межпредсердной перегородки.
Успехи в области кардиохирургии за последние десятилетия позволили повысить выживаемость младенцев с синдромом Дауна и патологией сердечнососудистой системы с 78 % в 1985 г до 90 % к 2004 г. (Claire Irving и др., 2008).
Hijii Т. и др. (1997) сообщили, что до 24-летнего возраста доживают 87,8 % пациентов с синдромом Дауна, перенесших оперативное лечение врожденного порока сердца.
При сравнении течения и исходов оперативного лечения полной формы атривентрикулярного канала у младенцев с синдромом Дауна и без синдрома, в работе, проведенной на базе НЦССХ им. Бакулева, Т. И. Задко отмечает, что у детей с синдромом Дауна быстрее развивается легочная гипертензия, важным механизмом в развитии которой, очевидно, является окислительный стресс. Генетически обусловленные особенности антиоксидантной системы, в том числе изначально низкий уровень глутатиона и более высокая антиоксидантная активность сыворотки у детей с синдромом Дауна (Н. П. Котлукова, О. И. Артеменко и др., 2008), свидетельствуют о более высоком окислительном стрессе при развитии легочной гипертензии при пороках сердца с легочной гиперволемией.
Из ранних осложнений хирургической коррекции атриовентрикулярного канала у детей с синдромом Дауна чаще встречаются инфекционно-септические осложнения, тогда как у детей без синдрома – острая сердечная недостаточность (Т. И. Задко, 2005). Это обстоятельство объясняется анатомическими особенностями порока и имеющимися иммунологическими нарушениями у младенцев с трисомией 21-й хромосомы.
Выводы
Полученные нами данные частоты сердечных аномалий не противоречат уже известным в литературе. Около половины детей с синдромом Дауна имеют патологию сердечнососудистой системы: 45,5 % – врожденные пороки сердца, 2,8 % – гемодинамически значимый открытый артериальный проток.
Анализ данных проведенных исследований, а также собственные полученные результаты делают очевидной необходимость раннего кардиологического обследования всех новорожденных с синдромом Дауна, включающего помимо осмотра и аускультации проведение эхокардиологического и электрокардиологического исследований. Внимательный подход и оценка клинических симптомов, а также знание генетически обусловленных особенностей детей с синдромом Дауна помогут своевременно диагностировать недостаточность кровообращения и начать адекватную терапию. Все дети с выявленными пороками сердца должны быть консультированы кардиохирургом для определения необходимости и сроков оперативного лечения.
Литература
- Задко Т. И. Синдром Дауна в сочетании с полной формой атриовентрикулярной коммуникации: актуальность, диагностика, сопутствующая патология, анатомия, особенности естественного течения, результаты хирургического лечения // Детские болезни сердца и сосудов. – 2005. – № 6. – С. 10–18.
- Роль окислительного стресса и антиоксидантной системы в патогенезе врожденных пороков сердца / Н. П. Котлукова, О. И. Артеменко, М. П. Давыдова, О. Н. Ильина, Л. А. Курбатова // Педиатрия. – 2009. – Т. 87, № 1. – С. 24–28.
- Cassidy S. B., Allanson J. E. Management of Genetic Syndromes. 2-nd ed. – P. 191–210. URL: https://www.wiley.com/en-us/Management+of+Genetic+Syndromes%2C+3rd+Edition-p-9780470191415
- Correlation between abnormal cardiac physical examination and echocardiographic findings in neonates with Down syndrome / D. B. McElhinney, M. Straka, E. Goldmuntz, E. H. Zackai // American Journal of Medical Genetics. – 2002. – Part A. – P. 238–241.
- Khory M. J., Erickson J. D. Improved ascertainment of cardiovascular malformation in infants with Down syndrome, Atlanta, 1968 through 1989 // Epidemiology. – 1992. – Vol. 136. – P. 1457–1464.
- Life expectancy and social adaptation in individuals with Down syndrome and without surgery for congenital heart disease / T. Hijii, J. Fukushige, H. Igarashi et al. // Clinical Pediatrics. – 1997. –Vol. 36. – P. 327–332.
- Twenty-year trends in prevalence and survival of Down syndrome / C. Irving, A. Basu, S. Richmond et al. // European Journal of Human Genetics. – 2008. – Vol. 16. – P. 1336–1340.
Источник
ñ ÔÏÖÅ ÓÌÙÛÁÌÁ ÏÔ ËÏÇÏ-ÔÏ ÉÚ ÐÏÄÒÕÇ ÐÒÏ ÚÎÁËÏÍÕÀ, Õ ËÏÔÏÒÏÊ ÐÏ ÁÎÁÌÉÚÕ Õ ÐÌÏÄÁ ÂÙÌ ÓÉÎÄÒÏÍ äÁÕÎÁ, ÎÏ ÏÎÁ ÂÙÌÁ ×ÅÒÕÀÝÁÑ, ÄÌÑ ÎÅ£ ÄÁÖÅ ×ÏÐÒÏÓ ÔÁËÏÊ ÎÅ ÓÔÏÑÌ — ÒÏÖÁÔØ ÉÌÉ ÎÅÔ. òÏÄÉÌÁ ÚÄÏÒÏ×ÏÇÏ ÒÅ£ÎËÁ. ÷ ÐÅÒ×ÕÀ ÂÅÒÅÍÅÎÎÏÓÔØ Ñ ËÕÐÉÌÁ × ÖÅÎÓËÏÊ ËÏÎÓÕÌØÔÁÃÉÉ ËÎÉÇÕ õÉÌØÑÍÁ É íÁÒÔÙ óÉÒÓ «÷ ÏÖÉÄÁÎÉÉ ÍÁÌÙÛÁ». üÔÏ ÏÄÎÉ ÉÚ ÓÁÍÙÈ Á×ÔÏÒÉÔÅÔÎÙÈ × óûá ÓÐÅÃÉÁÌÉÓÔÏ× × ÏÂÌÁÓÔÉ ÁËÕÛÅÒÓÔ×Á É ÄÅÔÓËÏÊ ÐÅÄÁÇÏÇÉËÉ, Á, ËÒÏÍÅ ÔÏÇÏ, ÏÎÉ ÓÁÍÉ ÒÏÄÉÔÅÌÉ 8-ÍÉ ÄÅÔÅÊ. óÅÄØÍÏÊ — Ó ÓÉÎÄÒÏÍÏÍ äÁÕÎÁ. åÓÌÉ ÉÎÔÅÒÅÓÎÏ, ÎÁÊÄÉ ÜÔÕ ËÎÉÇÕ É ÐÏÞÉÔÁÊÔÅ ÉÈ ÍÎÅÎÉÅ ÐÏ ÐÏ×ÏÄÕ ÄÅÔÅÊ-äÁÕÎÏ×, ÎÏ, ÓÒÁÚÕ ÓËÁÖÕ, ÏÎÏ ÏÔÌÉÞÁÅÔÓÑ ÏÔ ×ÁÛÅÇÏ. ðÒÏÞÉÔÁ× ×ÁÛÕ ÔÅÍÕ, ÏÔËÏÐÁÌÁ ËÎÉÇÕ × ÛËÁÆÕ. ðÒÏ ÁÎÁÌÉÚÙ ÏÎÉ ÐÉÛÕÔ, ÞÔÏ ÅÄÉÎÓÔ×ÅÎÎÙÊ (ÎÁ ÍÏÍÅÎÔ ÎÁÐÉÓÁÎÉÑ ËÎÉÇÉ!) ÁÂÓÏÌÀÔÎÏ ÎÁÄ£ÖÎÙÊ ÓÐÏÓÏ ÕÚÎÁÔØ, ÎÅÔ ÌÉ Õ ×ÁÛÅÇÏ ÒÅ£ÎËÁ ÈÒÏÍÏÓÏÍÎÏÊ ÁÎÁÍÁÌÉÉ, — ÁÍÎÉÏÃÅÎÔÅÚ. ôÁË ÞÔÏ, ÅÓÌÉ ×Ù ÐÅÒÅÄ ×ÙÂÏÒÏÍ, ÎÅ ÄÅÌÁÅÔÅ ×ÙÂÏÒÁ, ÎÅ ÓÄÅÌÁ× ×ÓÅÈ ÁÎÁÌÉÚÏ×. íÏÑ ×ÔÏÒÁÑ ÂÅÒÅÍÅÎÎÏÓÔØ ÂÙÌÁ ÎÅ ÚÁÐÌÁÎÉÒÏ×ÁÎÎÏÊ, ÓÔÁÒÛÅÍÕ ÔÏÌØËÏ-ÔÏÌØËÏ ÇÏÄ ÉÓÐÏÌÎÉÌÓÑ, ËÏÇÄÁ Ñ Ï ÎÅÊ ÕÚÎÁÌÁ. îÁ õúé ÎÁÛÌÉ ÏÔËÌÏÎÅÎÉÑ, ÇÉÎÅËÏÌÏÇ ÎÁÐÒÁ×ÉÌÁ Ë ÇÅÎÅÔÉËÕ. çÅÎÅÔÉË ÅÝ£ ÒÁÚ ÓÄÅÌÁÌ õúé, ÓËÁÚÁÌÁ, ÞÔÏ ÏÔËÌÏÎÅÎÉÑ ÔÁËÉÅ, ÞÔÏ, ÓËÏÒÅÅ ×ÓÅÇÏ, ÜÔÏ ÎÅ äÁÕÎ, Á ÛÅÊÎÏ-ËÉÓÔÏÚÎÁÑ ÇÉÇÒÏÍÁ Õ ÐÌÏÄÁ. îÁÐÒÁ×ÉÌÁ ÎÁ ÐÕÎËÃÉÀ. ñ ÄÌÑ ÓÅÂÑ ÒÅÛÉÌÁ, ÞÔÏ, × ÌÀÂÏÍ ÓÌÕÞÁÅ, ÎÅ ÓÍÏÇÕ ÕÂÉÔØ Ó×ÏÅÇÏ ÒÅ£ÎËÁ, ÄÁÖÅ ÂÏÌØÎÏÇÏ, ÐÏÜÔÏÍÕ — ÔÏÌØËÏ ÒÏÖÁÔØ. ñ ÎÅ ÄÕÍÁÌÁ Ï ÔÏÍ, ÞÔÏ ÂÕÄÅÔ ÐÌÏÈÏ ÒÅ£ÎËÕ: äÁÕÎÙ ÎÅ ÏÓÏÚÎÁÀÔ Ó×ÏÅÇÏ ÓÏÓÔÏÑÎÉÑ, ËÁË Ñ ÓÞÉÔÁÌÁ, Á ÅÓÌÉ ÜÔÏ ÇÉÇÒÏÍÁ, ÏÎÁ ÍÏÖÅÔ ÒÁÓÓÏÓÁÔØÓÑ (ÂÙÌÉ ÔÁËÉÅ ÓÌÕÞÁÉ, ÐÏ ÓÌÏ×ÁÍ ÇÅÎÅÔÉËÁ). ñ ÄÕÍÁÌÁ Ï ÓÅÂÅ É ÓÔÁÒÛÅÍ ÒÅ£ÎËÅ, ÞÔÏ ÍÏÑ ÖÉÚÎØ ÐÏÌÎÏÓÔØÀ ÂÕÄÅÔ ÏÒÉÅÎÔÉÒÏ×ÁÎÁ ÎÁ ÒÅ£ÎËÁ-äÁÕÎÁ, ÞÔÏ ËÁÞÅÓÔ×Ï ÖÉÚÎÉ ÓÔÁÒÛÅÇÏ ÏÄÎÏÚÎÁÞÎÏ ÓÎÉÚÉÔÓÑ. ðÅÒÅÄ ÉÌÉ ÐÏÓÌÅ ÐÕÎËÃÉÉ (ÕÖÅ ÎÅ ÐÏÍÎÀ), ÄÅÌÁÌÉ ÅÝ£ ÏÄÎÏ õúé. çÅÎÅÔÉË ÓËÁÚÁÌÁ, ÞÔÏ ÇÉÇÒÏÍÁ ×ÙÒÏÓÌÁ, ÞÔÏ ÓËÏÒÅÅ ×ÓÅÇÏ, ÐÌÏÄ ÕÍÒ£Ô ×ÎÕÔÒÉÕÔÒÏÂÎÏ. «ðÕÓÔØ ÔÁË, ÇÌÁ×ÎÏÅ, — Ñ ÅÇÏ ÎÅ ÕÂÉ×ÁÌÁ», — ÐÏÄÕÍÁÌÁ Ñ. òÅÚÕÌØÔÁÔÁ ÐÕÎËÃÉÉ ÎÁÄÏ ÂÙÌÏ ÖÄÁÔØ, ËÁÖÅÔÓÑ, ÎÅÓËÏÌØËÏ ÎÅÄÅÌØ. ðÏÚ×ÏÎÉÌÁ ËÏÇÄÁ ÏÎÉ ÐÒÏÛÌÉ, ÓËÁÚÁÌÉ: «òÅÚÕÌØÔÁÔ ÎÅ ×ÙÒÏÓ», ÚÁÐÉÓÁÌÁÓØ ÏÐÑÔØ Ë ÇÅÎÅÔÉËÕ. îÁÞÁÌÉÓØ ÐÅÒ×ÏÍÁÊÓËÉÅ ÐÒÁÚÄÎÉËÉ, ×Ï ×ÒÅÍÑ ËÏÔÏÒÙÈ Õ ÍÅÎÑ ÐÏÑ×ÉÌÉÓØ ÎÅÂÏÌØÛÉÅ ËÒÏ×ÑÎÉÓÔÙÅ ×ÙÄÅÌÅÎÉÑ. ëÏÎÓÕÌØÔÁÃÉÑ ÂÙÌÁ ÚÁËÒÙÔÁ, ÎÁ ×ÔÏÒÏÊ ÄÅÎØ ×ÙÄÅÌÅÎÉÊ ÐÏÅÈÁÌÁ × ÓÔÁÃÉÏÎÁÒ ÓÏ ×ÓÅÍÉ Ó×ÏÉÍÉ ÒÅÚÕÌØÔÁÔÁÍÉ õúé, ÇÏ×ÏÒÉÌÁ, ÞÔÏ ÒÅ£ÎÏË ÍÏÖÅÔ ÕÍÅÒÅÔØ, ÐÏ ÓÌÏ×ÁÍ ÇÅÎÅÔÉËÁ. äÅÖÕÒÎÙÊ ×ÒÁÞ ÓËÁÚÁÌ: «èÏÔÉÔÅ — ÌÏÖÉÔÅÓØ, × ÐÒÁÚÄÎÉËÉ, ÐÒÁ×ÄÁ, ÎÉËÁËÉÈ ÉÓÓÌÅÄÏ×ÁÎÉÊ ÎÅ ÂÕÄÅÍ ÄÅÌÁÔØ». ñ ÓÐÒÏÓÉÌÁ: «üÔÏ ÏÐÁÓÎÏ? üÔÏ ËÒÏ×ÏÔÅÞÅÎÉÅ?» «üÔÏ — ÎÅ ËÒÏ×ÏÔÅÞÅÎÉÅ», — ÏÔ×ÅÔÉÌ ×ÒÁÞ. «åÓÌÉ ÜÔÏ ÎÅ ËÒÏ×ÏÔÅÞÅÎÉÅ, ÞÔÏ Ñ ÂÕÄÕ ÐÒÏÓÔÏ ÔÁË × ÐÒÁÚÄÎÉËÉ ÌÅÖÁÔØ, ËÏÇÄÁ ÄÏÍÁ ÍÁÌÅÎØËÉÊ ÒÅ£ÎÏË?», — ÐÏÄÕÍÁÌÁ Ñ, ÎÁÐÉÓÁÌÁ ÏÔËÁÚ É ÕÅÈÁÌÁ ÄÏÍÏÊ. ÷ ÐÅÒ×ÙÊ ÄÅÎØ ÐÏÓÌÅ ÐÒÁÚÄÎÉËÏ× ÕÔÒÏÍ ÓßÅÚÄÉÌÁ ÓÏ ÓÔÁÒÛÉÍ ÎÁ ÚÁÒÁÎÅÅ ÎÁÚÎÁÞÅÎÎÙÊ ÐÒÉ£Í Ë óÅÎÑÇÉÎÏÊ, ÐÏÔÏÍ ÏÔÐÒÁ×ÉÌÁÓØ × ËÏÎÓÕÌØÔÁÃÉÀ. çÉÎÅËÏÌÏÇ ÓËÁÚÁÌÁ, ÞÔÏ ÌÕÞÛÅ ÌÅÞØ × ÓÔÁÃÉÏÎÁÒ. ÷ ÜÔÏÔ ÍÏÍÅÎÔ × ËÁÂÉÎÅÔ ÓÌÕÞÁÊÎÏ ÚÁÛÌÁ ÚÁ×ÅÄÕÀÝÁÑ ËÏÎÓÕÌØÔÁÃÉÅÊ. íÏÊ ×ÒÁÞ ÒÁÓÓËÁÚÁÌÁ ÅÊ ÐÒÏ ÍÏÀ ÓÉÔÕÁÃÉÀ, ÎÁ×ÅÒÎÏÅ, ÒÅÛÉ× ÚÁÒÕÞÉÔØÓÑ Å£ ÐÏÄÔ×ÅÒÖÄÅÎÉÅÍ, ÞÔÏ ÍÎÅ ÄÅÊÓÔ×ÉÔÅÌØÎÏ ÎÕÖÅÎ ÓÔÁÃÉÏÎÁÒ. õ ÔÏÊ, ×ÉÄÉÍÏ, ÕÖÅ ÂÙÌÉ ÐÒÅÔÅÎÚÉÉ Ë ÒÁÂÏÔÅ ÜÔÏÊ ÂÏÌØÎÉÃÙ: «ó ÐÅÒ×ÙÍÉ ÄÅÔØÍÉ ÏÎÉ ÎÏÓÑÔÓÑ, Á ÅÓÌÉ ×ÔÏÒÏÊ — ÍÏÖÎÏ ÔÁË ÏÔÎÏÓÉÔØÓÑ?!» ÷ÚÑÌÁ ÍÏ£ ÎÁÐÒÁ×ÌÅÎÉÅ × ÓÔÁÃÉÏÎÁÒ É ÎÁÐÉÓÁÌÁ ÎÁ ÎÅÍ: «âÏÌØÎÉÃÁ ÔÁËÁÑ-ÔÏ ÏÔËÁÚÁÌÁ × ÇÏÓÐÉÔÁÌÉÚÁÃÉÉ». ñ ÅÊ: «ëÁË ÏÔËÁÚÁÌÁ? ñ ÖÅ ÓÁÍÁ ÏÔËÁÚ ÎÁÐÉÓÁÌÁ! ëÁËÏÅ ËÏ ÍÎÅ ÏÔÎÏÛÅÎÉÅ ÂÕÄÅÔ, ËÏÇÄÁ Ñ Ó ÔÁËÉÍ ÎÁÐÒÁ×ÌÅÎÉÅÍ ÐÒÉÄÕ?» «åÓÌÉ ÞÔÏ, Ú×ÏÎÉÔÅ ÓÒÁÚÕ ÍÎÅ, » — ÏÔ×ÅÔÉÌÁ ÚÁ×ÅÄÕÀÝÁÑ É ÎÁÐÉÓÁÌÁ Ó×ÏÊ ÓÏÔÏ×ÙÊ. ëÏÇÄÁ, ÓÏÂÒÁ× ×ÅÝÉ, ×ÅÞÅÒÏÍ Ñ ÐÒÉÅÈÁÌÁ × ÓÔÁÃÉÏÎÁÒ, ÂÙÌ ÄÒÕÇÏÊ ÄÅÖÕÒÎÙÊ ×ÒÁÞ, ÎÉÞÅÇÏ ÐÒÏ ÎÁÐÒÁ×ÌÅÎÉÅ ÍÎÅ ÏÎÁ ÎÅ ÓËÁÚÁÌÁ, ÂÙÌÁ ÄÏÂÒÏÖÅÌÁÔÅÌØÎÁ, ÄÁÌÁ ÇÒÁÄÕÓÎÉË ÔÅÍÐÅÒÁÔÕÒÕ ÍÅÒÉÔØ. ðÏÍÅÒÉÌÁ — ÂÏÌØÛÅ 38, Á Ñ Å£ ÓÏ×ÓÅÍ ÎÅ ÏÝÕÝÁÌÁ, ×ÅÓØ ÄÅÎØ × ÄÅÌÁÈ ÂÙÌÁ, ÜÔÏ ÐÒÉ ÔÏÍ, ÞÔÏ Ñ ×ÓÅÇÄÁ ÞÕ×ÓÔ×ÕÀ ÄÁÖÅ ÍÁÌÅÎØËÕÀ ÔÅÍÐÅÒÁÔÕÒÕ. óÔÁÌÁ ÍÅÒÉÔØ ÍÁÔËÕ — ÍÁÔËÁ ÎÅ ÓÏÏÔ×ÅÔÓÔ×Ï×ÁÌÁ ÓÒÏËÕ. é ÔÕÔ Ñ ÏÓÏÚÎÁÌÁ, ÞÔÏ ÍÎÅ ÕÖÅ ÄÁ×ÎÏ ÎÉËÔÏ ÍÁÔËÕ ÎÅ ÍÅÒÉÌ! îÉ × ÓÔÁÃÉÏÎÁÒÅ, ÎÉ ÎÁ ÐÒÉ£ÍÅ ÕÔÒÏÍ, É ÎÁ ÐÒÅÄÙÄÕÝÅÍ ÐÒÉ£ÍÅ ÎÅ ÍÅÒÉÌÉ. ÷ÓÅ ×ÏËÒÕÇ ÇÉÇÒÏÍÙ, ÇÅÎÅÔÉÞÅÓËÉÈ ÁÎÁÌÉÚÏ× ËÒÕÔÉÌÏÓØ. íÅÎÑ ÓÒÁÚÕ ÐÏÄ ËÁÐÅÌØÎÉÃÙ. îÁ ÓÌÅÄÕÀÝÉÊ ÄÅÎØ ÓÄÅÌÁÌÉ õúé — ÒÅ£ÎÏË ÕÖÅ ÎÁÐÏÌÏ×ÉÎÕ ÒÁÚÌÏÖÉÌÓÑ. ðÏÓÔÁ×ÉÌÉ ×ÔÏÒÏÊ ËÁÔÅÔÏÒ, ÓÔÁÌÉ ÇÏÔÏ×ÉÔØ Ë ÏÐÅÒÁÃÉÉ, ×ÌÉ×ÁÔØ ÚÁÒÁÎÅÅ ÐÌÁÚÍÕ. ñ ÓÅÂÑ ÞÕ×ÓÔ×Ï×ÁÌÁ ÐÌÏÈÏ, ÈÏÔÅÌÁ, ÞÔÏÂÙ ×ÓÅ ËÏÎÞÉÌÏÓØ, ÐÒÉÞ£Í ÍÎÅ ÕÖÅ ÂÙÌÏ ×ÓÅ ÒÁ×ÎÏ ËÁË. úÎÁÌÁ, ÞÔÏ ÍÏÇÕ ÏÓÔÁÔØÓÑ ÂÅÚ ÍÁÔËÉ, ÐÒÏÓÎÕÔØÓÑ × ÒÅÁÎÉÍÁÃÉÉ ÉÌÉ ×ÏÏÂÝÅ ÎÅ ÐÒÏÓÎÕÔØÓÑ. îÏ × ÔÁËÏÍ ÓÏÓÔÏÑÎÉÉ ÍÅÎÑ ÒÁÄÏ×ÁÌÁ ÏÄÎÁ ÍÙÓÌØ: «ñ ÎÅ ÕÂÉÌÁ Ó×ÏÅÇÏ ÍÁÌÙÛÁ, ËÏÔÏÒÏÇÏ ×ÉÄÅÌÁ ÎÁ õúé, ÍÏÑ ÄÕÛÁ ÓÐÏËÏÊÎÁ, ÍÎÅ É ÕÍÅÒÅÔØ ÎÅ ÓÔÒÁÛÎÏ». îÏ ×ÒÁÞÉ Ó ÔÁËÉÍ ÍÏÉÍ ÎÁÐÒÁ×ÌÅÎÉÅÍ ÂÙÌÉ ËÒÁÊÎÅ ÚÁÉÎÔÅÒÅÓÏ×ÁÎÙ × ÂÌÁÇÏÐÏÌÕÞÎÏ ÉÓÈÏÄÅ ÓÉÔÕÁÃÉÉ, ÔÅÍ ÂÏÌÅÅ ÐÏ ÉÈ ÓÌÏ×ÁÍ, ÅÓÌÉ ÍÁÔËÉ ÌÉÛÁÅÔÓÑ 26-ÌÅÔÎÑÑ ÄÅ×ÕÛËÁ, ÜÔÏ ×ÙÚÙ×ÁÅÔ ×ÏÐÒÏÓÙ Ë ×ÒÁÞÁÍ Õ ÐÒÏËÕÒÁÔÕÒÙ,ÔÁË ÞÔÏ ÏÞÅÎØ ÓÔÁÒÁÌÉÓØ É ×ÓÅ ÐÒÏÛÌÏ ÈÏÒÏÛÏ. ôÅÐÅÒØ Ñ ÔÏÞÎÏ Õ×ÅÒÅÎÁ, ÞÔÏ âÏÇ ÄÁ£Ô ÉÓÐÙÔÁÎÉÅ ÐÏ ÓÉÌÁÍ, ÏÇÌÑÄÙ×ÁÑÓØ ÎÁ ÐÒÏÖÉÔÙÅ ÐÏÓÌÅ ÏÐÉÓÁÎÎÏÊ ÓÉÔÕÁÃÉÉ ÇÏÄÙ, Ñ ÐÏÎÉÍÁÀ, ÞÔÏ Ñ ÂÙ, ÎÁ×ÅÒÎÏÅ, ÎÅ ×ÙÎÅÓÌÁ ÉÓÐÙÔÁÎÉÅ ÒÏÄÉÔØ ÒÅ£ÎËÁ-äÁÕÎÁ, ÐÏÔÏÍÕ ÍÎÅ ÅÇÏ ÎÅ ÄÁÌÉ.
Источник
Признаки синдрома Дауна более десяти лет диагностируются врачами на раннем сроке беременности. Первичное скрининговое исследование включает в себя УЗИ и биохимический анализ крови. Процедура проводится не менее 3-х раз за беременность и сводит вероятность рождения ребенка с синдромом Дауна к низкому проценту.
Что это за заболевание у плода?

Под этим термином понимают нарушение генетического порядка в виде наличия лишней хромосомы в 21-й паре. Второе наименование этого заболевания – трисомия по двадцать первой паре хромосом. Согласно статистике, недуг у плода встречается примерно 1:800 случаям, причем между мальчиками и девочками заболевание распределяется одинаково. На возникновение патологии не влияет расовая и национальная принадлежность.
Причины возникновения хромосомного заболевания и характер его протекания пока до конца учеными медиками не изучены. Врачи предполагают, что при трисомии 21-й хромосомы клетки, полученные от родителей, не расходятся во время деления.
Считается, что риск рождения ребенка с отклонением выше в следующих случаях:
- Возраста матери на момент беременности — меньше 18 лет или больше 35 лет;
- Возраст отца — более 42 лет.
Остальные эндогенные причины, в том числе наследственного характера, пока не нашли достаточного подтверждения.
Дети с отклонением в 100% случаев имеют сопутствующие заболевания в виде пороков сердца, эндокринной системы, проблемы со зрением, слухом, иммунитетом. Они отстают в умственном и физическом развитии от сверстников.
Некоторые из сопутствующих пороков развития выявляют у детей на первом УЗИ-скрининге, например, дефект межжелудочковой перегородки сердца. На втором УЗИ признаки болезни могут проявиться в виде первичной пиелоэктазии (расширении почечных лоханок), кист сосудов головного мозга, проблемами со скелетом.
Риск рождения ребенка с отклонением
Если подтвердились результаты хромосомного заболевания у плода, то родителям, в особенности, матери, приходится решать, оставлять ребенка или прерывать беременность. Возможность сделать медикаментозное прерывание беременности есть только до 22 недель.
Нужно принять во внимание, что прогноз продолжительности жизни у такого малыша благоприятный, такие люди подчас доживают до 50 лет. Но дети с недугом это — серьезная нагрузка на будущих родителей, потому что они нуждаются в продолжительных коррекционных занятиях, специальных программах развития. Из-за наличия сопутствующих заболеваний дети должны 50–80% времени находиться под наблюдением врачей из-за риска развития обострения.
Комбинированный скрининг, который включает УЗИ и анализ на отклонение матерей, входящих в группу риска, делают в первый триместр на сроке беременности в 11–13 недель.
Перинатальный скрининг УЗИ второго триместра выявляет заболевание в 60–90% случаев. Трехмерное УЗИ в этом триместре повышает шансы в несколько раз.
Риски хромосомных заболеваний принято маркировать как высокие, средние и низкие. Высоким считается риск 1:200, низким 1:3001. Врачи в праве направить на дополнительное УЗИ при высоком и среднем риске.
Какие признаки у недуга?
Объективными маркерами, выявляемыми УЗИ диагностикой и указывающими на большой риск рождения ребенка с синдромом Дауна, являются:
- Толщина воротникового пространства (ТВП). Воротниковая область — кожная складка на задней стороне шеи малыша. В ней находится некоторое количество жидкости, но в случае трисомии по 21-й хромосоме объем жидкости превышен. При проведении обследования в период с 10 по 14 неделю беременности ширина складки составляет в норме 0,8–2,8 мм. Для точной диагностики УЗИ крайне важен срок беременности, потому что ТВП растет с возрастом ребенка. На мониторе УЗИ складка видна как белая линия, а жидкость черного цвета.
- Состояние носовой кости. Дети с синдромом Дауна имеют укороченные кости носа. Негативный симптом, если в 12 недель на УЗИ носовая косточка ребенка не визуализируется. В этот период норма величины кости носа лежит в диапазоне от 2–4,2 мм. При обнаружении патологии носовой косточки в 70% случаев диагноз подтверждается.
Изучают косвенные признаки. При обнаружении в 1-м триместре отклонений от нормы пространства ТВП на УЗИ обследуют остальные органы плода, скелет. Сопровождающие признаки заболевания проявляются:
- В укороченных размерах костей голеней;
- Увеличенном междуглазье;
- В изменении структуры мозга;
- В наличии только одной пупочной артерии (в норме их две);
- В увеличенном размере мочевого пузыря;
- В учащенном сердцебиении (тахикардии);
- Во множественных пороках сердца.
На мониторе сканера измеряют длину подвздошных костей и угол между ними. Обследуют мозг плода на гипоплазию мозжечка (недоразвитость органа и его функциональных зон). При этом на фото УЗИ мозжечок выглядит уменьшенным в размерах по сравнению с лобной долей мозга. Также при болезни наблюдают уменьшение размеров лобной доли по сравнению с нормой.
Когда обследуют мозг плода ультразвуком, то анализ на заболевание подтверждается сочетанием уменьшенного лобно-таламического расстояния и поперечного сечения мозжечка. Это занимает меньше времени, чем сканировать полностью мозг.
Один только размер ТВП не может служить достаточным основанием для окончательного диагноза недуга при беременности. Генетик обязан учесть результаты биохимического анализа крови и заключение УЗИ вместе.
УЗИ обычно проводится в двухмерном черно-белом изображении, при этом многие органы смотрятся укрупненно и не до конца визуализируются. Поэтому метод трехмерного УЗИ, проводимого для дополнительной диагностики генетических патологий, покажет поверхностные дефекты, такие как, например, ширина расстояния между глазами плода.
Для получения достоверной информации УЗИ в первом триместре должно обязательно проводиться в отведенный для него период, а именно — не ранее наступления 11 акушерской недели и не позднее 13 недель 6 дней!
Как обнаружить признаки синдрома Дауна?
Методы, позволяющие выявлять болезнь при беременности,подразделяются на не инвазивные и оперативные.
К первым относятся ультразвуковое обследование на сканере УЗИ и биохимический анализ крови на важные белки Альфа-фето-протеин (АФП) и человеческий хорионический гонадотропин (β-ХГЧ). Значительное отклонение от нормы показателя АФП указывает на возможные патологии, в том числе генетического характера, такие как синдром Дауна.
Ко второй группе причисляют следующие инвазивные способы:
| Вид оперативного обследования | Период | Материал диагностики |
|---|---|---|
| Биопсия хориона | 10–14 недель | Исследуется кусочек хориона (начальная стадия плаценты) |
| Плацентобиопсия | 14–20 недель | Изучают клетки плаценты |
| Амниоцентез | 15–18 недель | Анализ околоплодных вод, взятых методом пункции плодного пузыря |
| Амниоцентез | С 20-й недели | Забор пуповинной крови |
УЗИ и биохимический анализ на болезнь крови матери считаются безопасными методами, они не предполагают вмешательства внутрь организма матери или малыша. Анализ на синдром Дауна на УЗИ сканере проводится трансвагинально, через влагалище или поверхностным способом – трансабдоминально.
Неинвазивные методы используют чтобы выявлять подозрения на хромосомную патологию, а для подтверждения диагноза используют инвазивные, иначе говоря, оперативные методы перинатальной диагностики. Они со 100 процентной точностью выявляют хромосомное заболевание в период беременности.
Инвазивные процедуры в период внутриутробного развития плода проводить рискованно, потому что они предполагают внедрение в плодное яйцо или брюшную полость матери и забор частички кожи или крови ребенка. Собранный материал отправляют на генетическую экспертизу. Важно понимать, что оперативные вмешательства во время беременности несут в себе риск из-за возможности проникновения инфекций и бактерий.
Заключение
Дети с отклонением в 21 веке успешнее социализируются, чем ранее, однако многое зависит от усилий родителей и тяжести сопутствующих болезней. Анализ на заболевание проводят обязательно в первом триместре с 11-й по конец 13-й недели специалистом, при необходимости результат подтверждают инвазивным способом и только после этого говорят о 100% достоверном результате.
Источник
