Метаболический синдром и нарушения ритма сердца
Жижов Р.Э., Соловьев О.В., Кононов С.К., Онучина Е.Л.
В течение двух последних десятилетий значительно возрос интерес к изучению взаимосвязи метаболических нарушений и ожирения с ростом сердечно-сосудистых заболеваний. По данным Фремингемского исследования было установлено, что избыточный вес является достоверным независимым прогностическим фактором сердечно-сосудистых заболеваний у мужчин и женщин [1].
Рассмотрение проблемы метаболического синдрома (МС) началось еще в 1966 г., когда J. Camus предположил возможность анализа взаимосвязи между развитием гиперлипидемии, сахарного диабета 2-го типа (СД 2 типа) и подагры [2]. В 1988 г. G. Reaven описал симптомокомплекс, включавший гиперинсулинемию, нарушение толерантности к глюкозе (НТГ), гипертриглицеридемию, низкий уровень липопротеидов высокой плотности и артериальную гипертензию, под названием синдром X [3].
Позже был выявлен целый ряд состояний, которые ассоциируются с синдромом инсулинорезистентности: гипертрофия левого желудочка с нарушением диастолической дисфункции, повышение внутрисосудистой свертываемости крови и др. В настоящее время наиболее употребляемым термином является «метаболический синдром». Учитывая ведущий патогенетический механизм его развития, нередко в качестве синонима используют термин «синдром инсулинорезистентности». Понятие «метаболический синдром» (МС) было предложено в качестве способа выделения группы людей, имеющих повышенный риск развития сердечно-сосудистых заболеваний (ССЗ) и СД 2 типа, а также для принятия решения о тактике ведения такого пациента, благодаря которой можно добиться исчезновения или, по крайней мере, уменьшения выраженности основных проявлений МС [4]. При этом распространенность ожирения и ассоциированного с ним МС неуклонно растет и в настоящее время носит характер пандемии. Согласно результатам ряда проспективных исследований, у пациентов с МС и нормальной толерантностью к углеводам риск развития сердечно-сосудистых заболеваний и смертности от них повышается в 2-4 раза, а риск развития сахарного диабета в 5-9 раз [5-7]. Таким образом, изучение инсулинорезистентности тканей заставляет включать в зону ее патологического влияния все большее количество сердечно-сосудистых заболеваний. В этой связи, желудочковые нарушения ритма сердца могут стать одним из таких заболеваний.
Желудочковые нарушения ритма сердца (ЖНР) – одна из наиболее распространенных и одновременно недостаточно изученных проблем современной кариологии. Согласно данным различных авторов частота встречаемости идиопатических ЖНР колеблется от 30 до 70%. Существует достаточно большое количество классификаций ЖНР, из которых наиболее часто в клинической практике применяются по B. Lown и M. Wolf в модификации М. Ryan (1975), учитывающие количество и частоты желудочковых эктопий, а также по Т.Bigger (1984), в зависимости от наличия органического поражения сердца [8]. Сформировавшееся мнение, что ЖНР у совершенно здоровых людей являются прогностически благоприятными и относятся к группе неопасных для жизни и здоровья, является не таким уж и очевидным. В частности, опубликованное в 1992 году проспективное исследование Framingeham Heart Study показало, что у мужчин с ЖНР высоких градаций, хотя и без признаков заболевания сердца, в последующем отмечено двукратное увеличение частоты возникновения инфарктов миокарда и внезапной сердечной смерти [9]. А эпидемиологическое исследование MRFIT указывает на повышение риска внезапной сердечной смерти у лиц, на 2-х минутной электрокардиограмме (ЭКГ) которых регистрируются ЖНР [10]. Кроме того A. Kuhn и соавт. приводят случаи развития аритмогенной дисплазии правого желудочка (АДПЖ) через 15 лет от начала появления у больных желудочковой экстрасистолии без видимой патологии миокарда [11].
Метаболический синдром и ЖНР ассоциированы с повышенным риском развития сердечно-сосудистых заболеваний и смертности от них. Однако вопрос взаимоотношения ЖНР и МС не затрагивается большинством исследователей. Проблема желудочковых аритмий у пациентов без ишемической болезни сердца (ИБС), но с наличием метаболического синдрома и других факторов риска практически не изучена. Также не определено значение терапии МС у пациентов с ЖНР, ее влияние на эффективность антиаритмического лечения. Одним из решений усиления эффективности антиаритмической терапии ЖНР является сопутствующая терапия МС, включающая как медикаментозные, так и немедикаментозные методы лечения. Известные механизмы воздействия на МС могут иметь точки приложения и при терапии ЖНР.
Материалы и методы. В исследование включено 60 человек с желудочковыми нарушениями ритма и метаболическим синдромом. Критериями включения в исследование были ЖНР не ниже II градации (по B. Lown, M. Wolf в модификации М. Ryan, 1975) и наличие критериев МС (диагностические критерии Всероссийского научного общества кардиологов по МС) [16].
В число основных ассоциируемых заболеваний входили:
— артериальная гипертензия (АГ) – 56 (93%);
— ИБС (стенокардия напряжения) – 10 (16,7%);
— хроническая сердечная недостаточность I ФК – 42 (70%);
— хроническая сердечная недостаточность II ФК – 18 (30%);
— нарушение толерантности к углеводам (НТУ) – 24 (40%);
— ожирение – 27 (45%).
В исследование не включали лиц с:
— перманентной фибрилляции предсердий,
— атриовентрикулярной блокады 2,3 степени,
— наличием дополнительных пучков проведения,
— острый коронарным синдромом,
— гемодинамически значимыми врожденными или приобретенными пороки сердца,
— инфарктом миокарда в анамнезе,
— хронической сердечной недостаточностью III-IV ФК,
— сахарным диабетом,
— нарушением функции щитовидной железы,
— суб- и декомпенсированным синдромом слабости синусного узла.
Всем пациентам после обследования на исходном фоне (эхокардиоскопия, холтеровское мониторирование ЭКГ, тредмилл-тест) подбиралась эффективная антиаритмическая терапия. Согласно рандомизированным исследованиям в качестве анитаритмической терапии использовались бета-адреноблокаторы, соталол, амиодарон или их комбинации [12-14].
Антиаритмическая терапия считалась эффективной, если общее количество одиночных желудочковых экстрасистол уменьшалось в 4 раза и более, а количество желудочковых эктопий высоких градаций (IVA и выше по B. Lown, M. Wolf в модификации М. Ryan, 1975) не менее, чем в 10 раз или таковые отсутствовали [15]. Все пациенты, участвующие в исследовании и имевшие показания для катетерной аблации ЖНР, категорически от неё отказались. В соответствии с рекомендациями по МС Всероссийского научного общества кардиологов (2009) после проведенного лабораторного обследования применялась антигипертензивная, гиполипидемическая терапия, беседы по коррекции образа жизни, назначался метформин (стремились к суточной дозе 2000 мг) [16].
Важное значение придавалось как снижению веса, так и приему метформина в терапевтической дозе. Несмотря на это, часть пациентов не принимала метформин на этапе наблюдения в связи с плохой переносимостью, либо недостаточной приверженностью к терапии.
В связи с этим, в дальнейшем при анализе результатов, общая группа группа пациентов с ЖНР и МС была разделена на 2 подгруппы в зависимости от получаемой терапии:
— 1-я подгруппа с ЖНР и МС, получавшая наряду с антиаритмической терапией, метформин в терапевтической дозе в течение 3 месяцев (n=42, 22 мужчины и 20 женщин, средний возраст 61,45±10,19),
— 2-я подгруппа с ЖНР и МС, не получавшие метформин в терапевтической дозе в течение 3 месяцев в связи с недостаточной приверженностью к терапии (n=18, 3 мужчин и 15 женщин, средний возраст 65,83±8,1).
Группы были сопоставимы по ассоциированным заболеваниям и сопутствующей терапии (табл. 1).
Таблица 1. Распределение пациентов (абс. %) в зависимости от получаемой исходно терапии
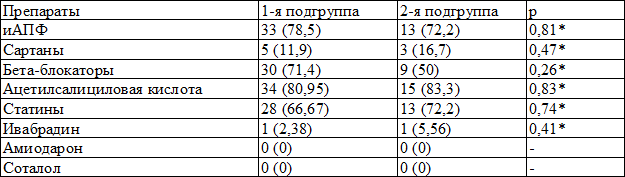
Примечание: иАПФ – ингибиторы ангиотензинпревращающего фермента, * — χ²
Всем пациентам, наряду с клиническим осмотром и определением антропоментрических параметров, проводилось лабораторное обследование, при котором определялось содержание общего холестерина (ОХ, ммоль/л), триглицеридов (ТГ, ммоль/л), холестерина липопротеидов высокой плотности (ЛПВП, ммоль/л) стандартным ферментативным методом с последующим расчетом липопротеинов низкой плотности по формуле Friedewald, расчитывался индекс атерогенности (ИА). Уровень гликемии определяли глюкозооксидазным методом на аппарате КФК-3-01 (Россия), инсулина – иммунохемилюминесцентным методом на аппарате Immulite 2000 (США). Рассчитывали индекс инсулинорезистентности HOMA-2 с помощью компьютерной модели HOMA-2, отражающей логарифмическую зависимость функции бета-клетки поджелудочной железы и чувствительности к инсулину периферических тканей. Пациенты были сопоставимы по лабораторным и клиническим характеристикам (табл. 2).
Таблица 2. Исходные клинические и лабораторные показатели (M±m)

Примечание: САД – систолическое артериальное давление, ДАД – диастолическое артериальное давление, ИМТ – индекс массы тела
Для оценки структурно-геометрических и функциональных показателей миокарда проводили эхокардиоскопию (ЭХОКС) на аппарате ViVID 3 Pro (США). Пациенты были сопоставимы по показателям ЭХОКС (табл. 3).
Таблица 3. Исходные показатели ЭХОКС в группах сравнения (M±m)
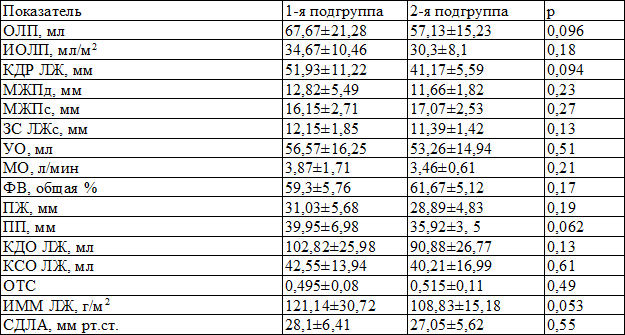
Примечания: ОЛП – объём левого предсердия, иОЛП – индекс объёма левого предсердия, КДРЛЖ – конечно-диастолический размер левого желудочка, МЖПд – межжелудочковая перегородка в диастолу, МЖПс – межжелудочковая перегородка в систолу, ЗСЛЖс – задняя стенка левого желудочка в систолу, УО – ударный объём, МО – минутный объём, ФВ – фракция выброса, ПЖ – правый желудочек, ПП – правое предсердие, КДОЛЖ конечно-диастолический объём левого желудочка, КСОЛЖ – конечно-систолический объём левого желудочка, ОТС – относительная толщина стенок, иММЛЖ – индекс массы миокарда левого желудочка, СДЛА – систолическое давление в легочной артерии
Градация желудочковых эктопий оценивалась с помощью холтеровского мониторирования ЭКГ системы Kenzo 301 (Япония), диагноз ИБС и толерантность к физической нагрузке (ТФН) определялись при проведении тредмилл-теста Schiller (Швейцария) Здесь также не было выявлено достоверно значимых различий исходно (табл. 4).
Таблица 4. Исходные показатели инструментального обследования и показатели ТФН (Me [25;75], M±m)
![Таблица 4. Исходные показатели инструментального обследования и показатели ТФН (Me [25;75], M±m) Таблица 4. Исходные показатели инструментального обследования и показатели ТФН (Me [25;75], M±m)](https://vrach-aspirant.ru/images/articles/2013/3.1/13135/t4.png)
Примечания: ЖЭС один. – одиночные желудочковые эктопии по ХМ-ЭКГ, ЖЭС куплеты – парные желудочковые эктопии по ХМ-ЭКГ, ТФН – толерантность к физической нагрузке выполненная на тредмилл-тесте, • — критерий Манна-Уитни
Динамическое наблюдение проводили в течение 3 месяцев, после чего было выполнено повторное обследование. Выбранная длительность наблюдения, с нашей точки зрения, была достаточной для оценки эффекта антиаритмической терапии, эффективности терапии МС и оценки клинических и лабораторных показателей.
Показатели, имеющие нормальное или близкое к нормальному распределение, представлены в виде (M±m), где М – выборочная средняя величина, m — выборочное стандартное отклонение; при отличии выборочного распределения от нормального – в виде медианы и интерквартильного (процентильного) интервала ( Ме [25;75]). При анализе динамики изменений проводился расчет в виде Δ%. Основным критерием в оценке значимости различий количественных показателей между обеими группами был критерий Стьюдента: 2-й тип критерия для равных дисперсий, 3-й тип для двухвыборочного теста с неравными дисперсиями. Для выявления существующих различий в группах, отличных от нормального распределения и при порядковых признаках использовали непараметрические критерии Манна-Уитни. Критический уровень значимости принимали равным 0,05.
Результаты и обсуждение. Через 3 месяца наблюдения установлено, что пациенты, получавшие метформин в рекомендуемой дозировке, а также соблюдающие рекомендации по немедикаментозному контролю (подгруппа 1), имели достоверно значимое улучшение в клинических, лабораторных и инструментальных показателях. Данные показатели отражены в табл. 5.
Таблица 5. Клинические, лабораторные и инструментальные показатели через 3 месяца наблюдения (Δ%, M±m, Me [25;75])
![Таблица 5. Клинические, лабораторные и инструментальные показатели через 3 месяца наблюдения (Δ%, M±m, Me [25;75]) Таблица 5. Клинические, лабораторные и инструментальные показатели через 3 месяца наблюдения (Δ%, M±m, Me [25;75])](https://vrach-aspirant.ru/images/articles/2013/3.1/13135/t5.png)
Примечания: ИМТ – индекс массы тела, ЖЭС один. – одиночные желудочковые эктопии по ХМ-ЭКГ, ЖЭС куплеты – парные желудочковые эктопии по ХМ-ЭКГ, ТФН – толерантность к физической нагрузке выполненная на тредмилл-тесте, • — критерий Манна-Уитни
Показатели табл. 5 свидетельствуют, что у пациентов подгруппы 1 наблюдается значимая положительная динамика в клинических показателях (окружность талии, масса тела, ИМТ) и толерантности к физической нагрузке. На фоне улучшения клинических показателей также отмечается статистически достоверное улучшение показателей липидного обмена (ЛПВП, ИА) и индекса инсулинорезистентности. Кроме того пациенты подгруппы 1 имели достоверно меньшее количество одиночных желудочковых эктопий, что можно расценивать как большую эффективность антиаритмической терапии.
Обе подгруппы пациентов через 3 месяца наблюдения были сопоставимы по сопутствующей терапии. Единственным различием в принимаемых препаратов был метформин, который подгруппа 1 принимала в средней дозе 1960±78 мг. Пациенты подгруппы 2 не принимали метформин на этапе наблюдения в связи с плохой переносимостью, либо недостаточной приверженностью к терапии.
В основе патогенеза МС лежит инсулинорезистентность[17]. При выраженной инсулинорезистентности на миокард воздействуют множественные факторы, в том числе свободные жирные кислоты, инсулиноподобный фактор роста. Наблюдается значимое влияние на развитие патологических изменений на уровне кардиомиоцита, связанное с низкой эффективностью синтеза АТФ. Они приводят к ремоделированию миокарда и формированию его электрической нестабильности. Все это в конечном итоге может приводить к развитию различных нарушений ритма сердца, в т.ч. и ЖНР. С учетом того, что инсулинорезистентность может быть одним из ключевых моментов в развитии ЖНР у пациентов с МС, все терапевтические мероприятия должны быть направлены на лечение компонентов МС и прежде всего инсулинорезистентности. В данном исследовании пациенты получали комплексную терапию МС, включая немедикаментозные методы, антигипертензивные и гиполипидемические препараты, а также метформин. В результате комплексного воздействия на ключевые звенья патогенеза МС, происходило улучшение клинических и лабораторных показателей, что в конечном счете позволяло повысить эффективность антиаритмической терапии ЖНР.
Заключение. Сопутствующая терапия метаболического синдрома у пациентов с желудочковыми нарушения ритма сердца приводит к достоверному улучшению клинических (окружность талии, масса тела и ИМТ) и лабораторных показателей (ЛПВП, индекс атерогенности), толерантности к физической нагрузке, эффективности антиаритмической терапии.
Источник
Что это такое
Аритмия – нарушение регулярности и последовательности сокращений сердца. Все, что не является синусовым ритмом, называется этим термином и включает в себя разнообразные патологии образования импульса и его проведения. Но из обывателей мало кто это знает, и считается, что если пациент сказал врачу: «У меня аритмия!», – то он все понял и сразу решит проблему, выписав одно определенное лекарство.
Увы, все не так просто.
Существует не одна классификация аритмий, но поскольку моя задача – познакомить читателей с разнообразием и помочь самостоятельно в нем разобраться, а не провести лекцию для кардиологов, то я разделю их на 2 группы:
- нарушение образования импульса – сюда мы отнесем экстрасистолии и тахикардии;
- патология проведения это же сигнала – блокады и брадиаритмии.
Как происходит нормальное сокращение сердца? В норме верховодит синусовый узел – электростанция, генерирующая импульсы и передающая их дальше через межузловые пути к атриовентрикулярному узлу, от которого сигнал идет по пучку Гиса, на его правую и левую ветвь, к волокнам Пуркинье и к миокарду желудочков.
Причины аритмий
Выделяют три группы причин:
- кардиальные – когда имеется сердечно-сосудистая патология: ишемическая болезнь, гипертония, порок сердца, миокардит, перикардит, кардиомиопатия и так далее;
- экстракардиальные – к ним относятся заболевания других органов и систем (хронический бронхит, патологии щитовидной железы, желудочно-кишечного тракта), прием лекарственных препаратов (антиаритмики, симпатомиметики, антидепрессанты, диуретики и др.) или токсическое воздействие (курение, алкоголь, наркотики), а также электролитные нарушения (гипо- или гиперкалиемия, гипомагниемия и т. д.);
- идиопатические – когда причину аритмии выявить не удалось.
Механизм возникновения нарушений сердечного ритма
Сердце обладает следующими способностями:
- автоматизм – кардиомиоциты могут спонтанно генерировать импульс (благодаря этому их называют «пейсмейкерами»);
- возбудимость – клетки воспринимают сигнал и реагируют на него;
- проводимость – импульс может распространяться по проводящей системе сердца;
- сократимость – способность сокращаться в ответ на раздражитель.
Таким образом, миокард самостоятельно генерирует электрические токи, которые проводятся по внутрисердечным путям, возбуждают мышцу и вызывают его сокращение.
Как было отмечено ранее, аритмии возникают вследствие нарушения образования импульса либо проведения. Основные механизмы представлены на рисунке ниже.
Изменение автоматизма в синусовом узле является причиной тахикардий, брадикардий (при слабости синусового узла) и других аритмий. Если повышается возбудимость нижележащих звеньев проводящей системы, например атриовентрикулярного соединения, то он берет на себя роль водителя ритма, и возникает эктопический ускоренный ритм.
Триггерная активность – это образование импульсов кардиомиоцитами, в норме не обладающими пейсмекерной (сигналообразующей) функцией. Этот механизм лежит в основе экстрасистолий и тахикардий так же, как и другой, re-entry (в его случае сигнал вызывает одно сокращение, но при определенных условиях он может возбуждать миокард неоднократно из-за циркуляции тока по кругу).
Блокада возникает, когда импульс сталкивается с тканью, неспособной прореагировать на сигнал, например с постинфарктным рубцом, занявшим место поврежденной проводящей системы сердца.
Признаки и симптомы: какие жалобы у пациентов
Палитра клинических проявлений разнообразна и красочна: от нормального самочувствия до потери сознания и аритмогенного шока.
В зависимости от вида аритмии, психоэмоционального статуса и сопутствующих заболеваний пациенты предъявляют следующие жалобы:
- замирание сердца;
- удары сердца о грудную клетку;
- учащенное сердцебиение;
- головокружение, потемнение в глазах;
- одышка, чувство нехватки воздуха;
- слабость, утомляемость;
- потеря сознания и так далее.
Эти симптомы сопровождаются чувством страха и не всегда являются специфичными. Подобную картину заболевания описывают также соматически (телесно) здоровые люди, страдающие паническими атаками, неврозами или фобиями. В этих ситуациях речь идет о психосоматике, и требуется работа с психотерапевтом, а не лечение у кардиолога.
Случай из практики: аритмия у женщины
В моей практике был интересный случай: обратилась женщина средних лет с жалобами на эпизоды потери сознания. Они происходили во время физической нагрузки (подъем по лестнице, езда на велосипеде), которая сопровождалась выраженной одышкой, и перед тем, как упасть, она ощущала сердцебиение. До обращения к кардиологу больная прошла обследование у невролога, но никаких отклонений не было выявлено.
При проведении эхокардиографии сердца визуализировано: вторичная гипертрофическая кардиомиопатия, развившаяся в результате субклапанного стеноза аорты. Утолщенный миокард левого желудочка – фактор риска развития жизнеопасных тахикардий и внезапной сердечной смерти. Во время суточного мониторирования ЭКГ были зафиксированы пробежки желудочковой аритмии различной продолжительности.
Пациентка направлена на оперативное лечение – коррекцию порока сердца и абляцию (прижигание) зоны аритмии.
Особенности у мужчин
Особенностью у нарушений ритма у мужчин является «синдром праздничного сердца». Это состояние, при котором после кратковременного употребления больших доз алкоголя (обычно во время застолий) возникает аритмия. Чаще случается фибрилляция предсердий (мерцалка) или желудочковые нарушения ритма.
Клинически данный синдром проявляется ощущением сердцебиения, чувством слабости, одышкой, дискомфортом в грудной клетке, которые могут привести к аритмогенной смерти. Механизмы влияния спиртного на сердце заключается как в прямом токсическом действии, так и в повышении активности симпатической нервной системы и электролитном дисбалансе. При хроническом алкоголизме развивается кардиомиопатия, основными проявлениями которой являются сердечная недостаточность и нарушения ритма сердца.
Если вовремя отказаться от употребления спиртного, есть шанс восстановить насосную функцию сердца, но где тот предел, когда еще не поздно, ученым выяснить не удалось. Отношение к выпивке в нашей стране очень легкомысленное, в народе считается, что алкоголь «чистит сосуды» и его употребление связано с пользой для здоровья. Да, у систематически выпивающих людей редко случаются инфаркты — они умирают от внезапных аритмий, не доживая до тромбоза.
Классификация аритмий
Поскольку статья общеобразовательная, не буду перегружать вас научными терминами, патофизиологией и прочими характеристиками, а в общих чертах объясню, на какие основные группы делятся аритмии.
По источнику (топографически) они бывают наджелудочковыми (все, что возникает выше атриовентрикулярного узла) и желудочковыми. По частоте ритма выделяют тахикардии (с ЧСС более 90-100 в минуту) и брадикардии (замедление ритма до 50-60 ударов и меньше). Тахикардии в свою очередь подразделяются на наджелудочковые и желудочковые, пароксизмальные и непароксизмальные.
В основе брадикардий лежит нарушение проводимости импульса – блокада, которая может быть синоатриальной, атриовентрикулярной, межпредсердной и внутрижелудочковой. Это наиболее часто встречаемые аритмии, и подобная классификация дает представление о том, как нужно их лечить.
Таблица 1. Классификация аритмий.
По локализации:
|
По частоте сердцебиений:
|
Тахикардии:
|
Блокады:
|
Отдельно выделю экстрасистолию – «королеву» среди аритмий. Подавляющее число пациентов обращаются ко мне именно с этой проблемой. Экстрасистолы – внеочередные сокращения сердца. Они встречаются у всех – как у здоровых, так и у лиц с различными заболеваниями – и нередко отнимают покой и сон у пациентов из-за тягостных ощущений, которые они испытывают во время перебоев ритма.
С этим типом нарушения ритма связан интересный парадокс: у здоровых лиц они не представляют опасности для жизни, несмотря на яркие проявления симптомов. У людей же с серьезными органическими заболеваниями экстрасистолы могут протекать бессимптомно и быть случайной находкой на электрокардиограмме или суточном мониторировании ЭКГ.
Проявления на кардиограмме
Рассмотрим признаки аритмии на электрокардиограмме на примере экстрасистолии, тахикардии и блокады проведения импульса.
Если у пациента есть экстрасистолия, например предсердная, его ЭКГ будет выглядеть следующим образом: на фоне синусового правильного ритма, где между желудочковыми комплексами одинаковые интервалы, появляется внеочередное сокращение, после которого следует пауза различной продолжительности в зависимости от вида экстрасистолы.
Тахикардию разберем на двух примерах: пароксизмальная АВ-узловая и желудочковая. При первом типе аритмии на ЭКГ зафиксирован эпизод ритма с высокой частотой, при этом она сохраняется постоянной на протяжении всего пароксизма. Комплексы на кардиограмме узкие и не будут видны зубцы Р, характерные для синусового ритма.
При желудочковой тахикардии регистрируются расширенные деформированные комплексы, напоминающие блокады ножек пучка Гиса, ЧСС – более 120 ударов в минуту.
В случае развития блокады, например АВ-блокады 1 степени, на ЭКГ мы видим удлинение интервала PQ более, чем на 0,2 сек, что отражает нарушение проведения импульса от предсердий к желудочкам. При АВ-блокаде 2 степени Мобитц 2 возникает внезапное выпадение комплекса, при этом интервал PQ либо удлиненный, либо нормальный.
Лечение нарушений сердечного ритма
«Есть аритмия – должен быть назначен антиаритмик» – логически рассуждает каждый, но это не так.
Аритмия может быть СИМПТОМОМ болезни и не обязательной сердечной! Тиреотоксикоз – состояние, обусловленное избыточным синтезом тиреоидных гормонов. Он осложняется фибрилляцией предсердий, и именно мерцательная аритмия является первым признаком нарушения функции щитовидной железы.
У женщин при климаксе возникают экстрасистолы, и они не требуют лечения антиаритмиками, так как причина устранима другим путем – назначением гормональных препаратов.
У больных с ишемической болезнью сердца одним из симптомов патологии считаются различные нарушения ритма – от экстрасистолии до желудочковой тахикардии – и первый пункт в их лечении – это устранение ишемии миокарда путем операции: стентирование коронарных артерий либо аорто-коронарное шунтирование.
У пациентов с перенесенным инфарктом миокарда субстратом аритмии является участок на границе рубца и здоровой ткани сердца. Этим людям рекомендуется абляция очага нарушения ритма либо гомогенизация этой области.
Большую группу пациентов составляют люди с мерцательной аритмией – нарушением возбудимости, при котором в предсердном миокарде возникают множественные импульсы, вызывающие сокращения мышцы несинхронно с работой желудочков. Помимо антиаритмических препаратов таким людям показаны антикоагулянты и терапия основного заболевания (например, ингибиторы АПФ при артериальной гипертензии), а также хирургическую деструкцию аритмогенных зон.
Пароксизм тахикардии (желудочковой, мерцательной аритмии, ортодромной с участием ДПП и т. д.) может осложниться аритмогенным шоком с падением артериального давления и отсутствием периферического пульса (на руке). Методом выбора в данной ситуации является экстренная электроимпульсная терапия с помощью дефибриллятора. Электрический разряд прерывает волну ре-ентри и восстанавливается синусовый ритм.
Антиаритмические препараты систематизированы в 4 группы и назначаются только врачом. Несмотря на то, что они созданы для лечения нарушений ритма, эти лекарства могут приводить к возникновению аритмий, поэтому применение требует осторожности и контроля кардиолога. Антиаритмики 1 класса противопоказаны пациентам с перенесенным инфарктом миокарда, хронической сердечной недостаточностью и гипертрофией левого желудочка более 14 мм.
Что касается блокад, то тактика их ведения зависит от уровня поражения и степени. АВ-блокада 3 степени, остановки синусового узла с асистолией желудочков являются абсолютными показаниями к имплантации постоянного кардиостимулятора. АВ-блокада высокой степени может сопутствовать инфаркту миокарда нижней стенки левого желудочка. Ранняя реваскуляризация приводит к восстановлению работы атриовентрикулярного узла.
Советы врача: как избавиться от аритмии
Золотое правило «легче предупредить, чем лечить» остается актуальным и в случае с аритмией. Занятия физическими упражнениями, здоровое сбалансированное питание, контроль артериального давления и отказ от вредных привычек всегда стоят во главе угла. Профилактика – наше все!
Неправильный ритм жизни, короткий сон, злоупотребление алкоголем, кофеинсодержащими напитками, психостимуляторами, стресс тоже вредят здоровью и могут провоцировать нарушения ритма и проводимости, поэтому нормализация режима труда и отдыха – далеко не последний компонент терапии аритмий. Пациентам с неврозами необходимо дать рекомендацию обратиться за помощью к психотерапевту.
Прежде чем лечить аритмию, нужно выяснить ее этиологию. Бессмысленно устранять симптом, если мы не знаем первопричину. У меня на приеме была молодая беременная женщина с жалобами на учащенное сердцебиение. У нее отсутствовали заболевания сердечно-сосудистой системы, и для уточнения диагноза я назначила ей общий анализ крови и сывороточное железо.
В итоге диагностирована железодефицитная анемия с гемоглобином 80 мг/л, которая и послужила причиной тахикардии у женщины. Назначение этиотропной терапии – препарата железа – купировало через некоторое время все симптомы. Бета-блокаторы для урежения пульса не решили бы проблему, а только усугубили ее.
В чем опасность и каковы прогнозы
Для определения прогноза пациента используется классификация, созданная Дж. Биггером. В зависимости от типа аритмии, наличия кардиоваскулярного заболевания оценивается риск внезапной сердечной смерти, и исходя из этого нарушение ритма считается доброкачественным или злокачественным. Чем серьезнее и опаснее проблема, тем интенсивнее ее необходимо устранять, а у пациентов с предсердной экстрасистолией и без патологии сердца аритмию искусственно убирать не стоит.
В процессе лечения оценивается возможный риск и польза от приема антиаритмических препаратов. Если есть риск развития нежелательных последствий (проаритмогенный эффект в первую очередь), то назначение нерационально и опасно.
Помимо терапии аритмии, обязательный пункт – лечение заболевания, последствием которого она стала. Частой причиной фибрилляции предсердий служит артериальная гипертония, и без контроля систолического и диастолического давления изменения в сердце продолжают развиваться, а пароксизмы мерцательной аритмии возникают чаще. Также при усугублении хронической обструктивной болезни легких, бронхиальной астмы наблюдается формирование легочного сердца и ухудшение течения аритмии.
Проведение катетерной абляции (модификации АВ-узла при пароксизмальной АВ-узловой тахикардии) в малом проценте случаев осложняется развитием полной поперечной блокады с дальнейшей необходимостью имплантации электрокардиостимулятора. Также операция может усугубиться гемоперикардом, перфорацией камер сердца, но это весьма редкие ситуации. Абляция остается главным способом устранить пароксизмальную тахикардию раз и навсегда.
У пациентов с синдромом WPW и редкими, малосимптомными приступами возможно динамическое наблюдение у врача. При этом существуют не медицинские, а социальные показания к разрушению ДПП (той же абляции). Данный пункт касается летчиков, космонавтов, профессиональных спортсменов и др. Если же пароксизмы протекают с выраженной симптоматикой, нарушающей повседневную жизнедеятельность, то катетерная деструкция является вариантом выбора в любом случае.
Источник
