Врожденный финского типа синдром финского типа
Врожденный нефротический синдром финского типа — клиника, диагностикаВрожденный нефротический синдром финского типа — заболевание наследуется по аутосомно-рецессивному типу и является основной причиной высокой протеинурии у детей первого месяца жизни. Хотя наибольшая распространенность этого заболевания отмечается в Финляндии (1,2 случая на 10 000 беременностей), описано много случаев заболевания у детей других национальностей. При этом заболевании протеинурия возникает еще внутриутробно, что проявляется повышенным уровнем а-фетопротеина в околоплодных водах. Уже на первой неделе жизни часто возникают отеки. Истощение, тяжелые инфекции и тромбозы обусловливают тяжесть заболевания и высокую смертность, ранее больные погибали на первом году жизни. Сегодня при интенсивном лечении больные могут дожить до того момента, когда им можно провести трансплантацию почки. Выживаемость как трансплантата, так и больных очень высокая. Локус, мутация в котором обусловливает данное заболевание, был найден с помощью позиционного клонирования на длинном плече 19-й хромосомы (19q13.1) и в финских, и в других семьях. При определении нуклеотидной последовательности этого локуса был найден ранее неизвестный ген NPHS1, который избирательно экспрессируется в подоцитах. Продукт этого гена получил название нефрин. Он относится к молекулам адгезии из суперсемейства иммуноглобулинов. Нефрин локализован в области щелевых диафрагм — видоизмененных плотных контактов между отростками ножек подоцитов. У больных с мутацией гена NPHS1 нет отростков ножек подоцитов и щелевых диафрагм. Это позволяет думать, что именно нефрин является важнейшим компонентом щелевых диафрагм, предотвращающих выход белка из сосудов клубочка. Среди всех мутаций гена NPHS1 у финнов преобладают две: Fin-major и Fin-minor. Они присутствуют более чем у 90% больных. Мутация Fin-major вызвана делецией двух пар нуклеотидов во 2-м экзоне, который кодирует терминирующий кодон, она встречается примерно у 80% больных финнов. Мутация Fin-minor — нонсенс-мутация в 26-м экзоне, она встречается примерно у 17% больных финнов. У больных других национальностей встречаются различные мутации по типу делеций, вставок, нонсенс- и миссенс-мутаций, а также мутации, нарушающие сплайсинг. Врожденный нефротический синдром финского типа — основная, но не единственная причина нефротического синдрома на первом месяце жизни.
— Также рекомендуем «Синдром Дени-Дрэша — клиника, диагностика» Оглавление темы «Наследственные болезни почек»:
|
Источник
Терминология. Под врожденным нефротическим синдромом понимается НС, развившийся у ребенка до 3-месячного возраста. Врожденный HC может быть первичным, генетически детерминированным и вторичным при врожденной цитомегалии, токсоплазмозе, сифилисе, туберкулезе, тромбозе почечных вен, СПИДе. Особое место среди врожденного HC занимает первичный наследственный, так называемый врожденный нефротический синдром финского типа. Это аутосомно-рецессивно наследуемая патология, проявляющаяся с первых дней жизни ребенка тяжелым нефротическим синдромом с большой протеинурией и резкой гипопротеи-немией. При «естественном» течении летальный исход наступает до 1 года, причем к нему приводят либо развитие почечной недостаточности, либо септические осложнения.
История и эпидемиология. Впервые заболевание описано в 1966 г. R. Norio. При анализе церковно-приходских книг в юго-западном регионе Финляндии, где наиболее часто встречалось это заболевание, был обнаружен родоначальник патологии — финн, который проживал в этом регионе во второй половине XVI в. До проведения антенатальной диагностики заболевание встречалось с частотой 1:8200 рождений. Аналогичные случаи регистрируются в северо-западном районе России, в Ленинградской области. He всегда удается подтвердить этническую (финскую) принадлежность семьи. Этот вариант патологии неоднократно описывался в различных странах мира у лиц нефинской национальности.
Клиническая характеристика. Течение беременности тяжелое, роды, как правило, преждевременные, масса плаценты составляет более 1/4-1/2 массы новорожденного. Чаще ребенок рождается уже с выраженными отеками, но они могут появиться несколько позднее — к концу первого месяца жизни. Протеинурия достигает 10 г за сутки. Резко выражена гипоальбуминемия, имеет место повышение липидов сыворотки крови. При уменьшении отечного синдрома после введения диуретиков обращают на себя внимание резкая дистрофия ребенка, множественные стигмы дизэмбриогенеза. Резко снижены показатели иммунной защиты, что является основой развития гнойных осложнений. Возможны тромбоэмболии. АД снижено или в пределах нормы. В амниотической жидкости и сыворотке крови беременных в высоком титре содержится альфа-фетопротеин. Обнаружение этого феномена позволило проводить своевременную антенатальную диагностику.
Морфология и патогенез. При гистологическом исследовании почек обнаруживаются микрокистоз проксимальных канальцев в кортикомедуллярной зоне, мультигломерулярность и другие признаки незрелости почечной ткани, пролиферация мезангиальных клеток, фиброзные изменения.
Врожденный нефротический синдром финского типа относится к гломерулярным болезням, причем продукт гена — нефрин — локализован на подоцитах. Недостаточность нефри-на вызывает протеинурию еще в антенатальном периоде развития ребенка.
Генетика. Врожденный HC финского типа наследуется аутосомно-рецессивным путем. М. Kestila и соавт. при исследовании 17 семей с указанной патологией не обнаружили дефекта ни в одном из генов альфа-1-, альфа-2-, альфа-3- и альфа-4-цепи коллагена IV типа, а также основных генов цепей ламинина и гепа-рансульфат-протеогликана, кодирующих основные компоненты БМ клубочков. Получены убедительные данные, что мутантный ген локализован на 19ql3, этот ген — NPHSI — кодирует трансмембранный протеин — нефрин, присущий подоцитам.
Современными исследованиями выяснено, что в различных регионах мира, где выявлялся врожденный НС, близкий по сути финскому, имеется около 40 мутаций гена NPHSI. Однако в Финляндии у больных и носителей обнаружены только 2 идентичные мутации этого гена. В семьях, где имеется врожденный НС, в процессе медико-генетического консультирования беременные женщины обязательно обследуются на наличие у них в крови альфа-фетопротеина. При его обнаружении рекомендуется прерывание беременности.
Диагностика. Рождение в семье ребенка с врожденным HC требует прежде всего выяснения этнических корней. Обязательно исключение вторичного НС, связанного с внутриутробными инфекциями. Врожденный HC финского типа следует дифференцировать от семейного НС, который описан в различных странах мира у людей различной национальности (см. ниже). О финском типе HC говорят тяжелая беременность, наличие очень крупной плаценты, обнаружение при морфобиоптическом исследовании микрокистоза проксимальных канальцев.
Лечение. Несмотря на то что в Финляндии проводится активное выявление семей, где возможно развитие врожденного HC финского типа, все же и в настоящее время рождаются дети с этой тяжелой патологией. Ни симптоматическая терапия, ни стероиды и иммуносупрессоры не вызывают улучшения у больных с врожденным HC финского типа.
Рекомендуется высокобелковая и высококалорийная диета наряду со строжайшим водноэлектролитным сбалансированным режимом до 10—12 мес жизни ребенка. К этому возрасту удается довести его массу тела до 10 кг, ликвидировать дистрофию и отечный синдром. После нефрэктомии проводят почечную трансплантацию. Десятилетнее наблюдение за группой, включавшей около 40 детей, убедительно свидетельствует о хорошей реабилитации таких больных.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 2 декабря 2019;
проверки требует 1 правка.
История заселения Финляндии. Красным цветом обозначена зона формирования финского этноса (южная часть провинции Саво), красной штриховкой — зона ранней финской колонизации (XVI век), за пределами красной линии — зона поздней колонизации (с середины XVII века)
Финские наследственные заболевания (фин. Suomalainen tautiperintö, англ. Finnish heritage diseases) — название ряда наследственных патологий, распространённых преимущественно среди этнических финнов[1]. Термин «финские наследственные заболевания» впервые появился в медицинской литературе в 1994 году и с тех пор приобрёл достаточно широкое распространение[1][2]. Он может быть применён по отношению примерно к 40 наследственным патологиям[3]. Следует отметить, что ни одно из этих заболеваний не ограничено исключительно финскими популяциями, однако они обнаруживают высокую частоту встречаемости именно среди них. Эти патологии чаще встречаются на севере и востоке страны. Можно отметить, что высокие частоты отдельных заболеваний концентрируются в изолированных регионах страны, и практически отсутствуют среди населения больших городов[1]. Они не затрагивают другие народы, живущие в Финляндии — шведов, саамов или карелов[1].
Открытию и изучению финских наследственных заболеваний благоприятствовали следующие условия[1]:
- сохранение традиционной структуры популяций в пределах ограниченных географических регионов страны
- высокий уровень медицинского обслуживания
- точные записи истории семьи в церковно-приходских книгах на протяжении десяти последних поколений.
В среднем 1 из 5 финнов является носителем генетического дефекта, связанного хотя бы с одним из финских наследственных заболеваний. Большинство из этих заболеваний носят аутосомно-рецессивный характер, то есть в случае, если и отец, и мать являются носителями одной и той же мутации, вероятность рождения больного ребёнка составляет 1/4. В настоящее время описаны и картированы большинство мутаций, приводящих к финским наследственным патологиям, что позволяет применять генетическое тестирование, пренатальную диагностику и генетическое консультирование. Распространение в финских популяциях определённых генетических болезней также вызывает дискуссии на тему евгеники и биоэтики[4].
Причины возникновения[править | править код]
Подавляющая часть современных финнов происходит от небольшой популяции, сформировавшейся в результате миграций уральских племён в промежутке от 4 000 до 2 000 лет тому назад[5]. Геногеографические исследования показывают низкое генетическое разнообразие финнов по сравнению с другими европейскими народами, а также подтверждают наличие эффекта основателя и эффекта бутылочного горлышка[5]. Численность первоначальной популяции оценивается разными исследователями в 3 000 — 24 000 человек[5]. К XIV веку численность финнов составляла около 150 тысяч человек, в основном населявших юг современной провинции Саво. С XVI века начинается финская колонизация юго-западных, а затем и северных регионов. Для этой колонизации также был характерен локальный эффект основателя, так как заселение отдельных регионов страны производилось небольшими группами, в дальнейшем почти не имевшими последующего притока населения[1].
Список финских наследственных заболеваний[править | править код]
К редким наследственным заболеваниям, встречающимися в Финляндии гораздо чаще в сравнении с другими популяциями, относятся врождённый нефротический синдром финского типа, аспартилгликозаминурия, ранний детский цероидлипофусциноз, врождённая гиперплазия коры надпочечников, врождённая дистрофия стромы роговицы, Синдром Ашера III типа, карликовость Мелбри и другие[1][3].
Примечания[править | править код]
- ↑ 1 2 3 4 5 6 7 Peltonen L, Jalanko A, Varilo T. Molecular genetics of the Finnish disease heritage (англ.) // Human Molecular Genetics. — 1999. — Vol. 8, no. 10. — P. 1913—1923.
- ↑ Perheentupa J. The Finnish disease heritage: a personal look (англ.) // Acta Paediatrica. — 1995.
- ↑ 1 2 Reijo Norjo. Finnish Disease Heritage I: characteristics, causes, background (англ.) // Hum Genet. — 2003. — Vol. 112. — P. 441—456.
- ↑ Seppo Poutanen. The first genetic screening in Finland: its execution, evaluation, and some possible implications for liberal government // Genetic governance: Health, risk, and ethics in the biotech era / Robin Bunton and Alan Petersen. — Routledge, 2005. — 215 с. — ISBN 0415354072.
- ↑ 1 2 3 Sajantila A, Salem AH, Savolainen P, Bauer K, Gierig C, Pääbo S. Paternal and maternal DNA lineages reveal a bottleneck in the founding of the Finnish population (англ.) // Proceedings of the National Academy of Sciences of the United States of America. — 1996. — Vol. 93, no. 21. — P. 12035—12039.
Ссылки[править | править код]
- Finnish Disease Database
Источник
Нефротический синдром (НС) — клинико-лабораторный cимптомокомплекс, клинически характеризующийся периферическими или генерализованными отеками вплоть до асцита и анасарки, а лабораторно — протеинурией более 2,5 г/сут или более 50 мг/кг/сут, гипопротеинемией, гипоальбуминемией (ниже 40 г/л), диспротеинемией, гиперлипидемией и липидурией.
Одним из наиболее частых наследственных типов НС является врожденный (семейный) нефротический синдром финского типа. Наибольшее распространение НС отмечается в Финляндии (заболеваемость среди новорожденных составляет 1:8200 родившихся), где доказан эффект основателя. В других странах, в том числе и РФ, это заболевание встречается гораздо реже.
Нефротический синдром финского типа (НСФТ) – аутосомно-рецессивное заболевание, проявляющееся полным клинико-лабораторным симптомокомплексом нефротического синдрома и выявляется с рождения до 3 месяцев Гистологически при этом типе НС выявляют четкообразные цепочечные расширения проксимальных отделов нефрона (псевдокистоз), гломерулярные, тубулярные и интерстициальные изменения, степень выраженности которых нарастает по мере прогрессирования заболевания, а также большое количество фетальных гломерул и гломерул с увеличенным диаметром. Причиной заболевания являются мутации гена NPHS1 [OMIM 602716].
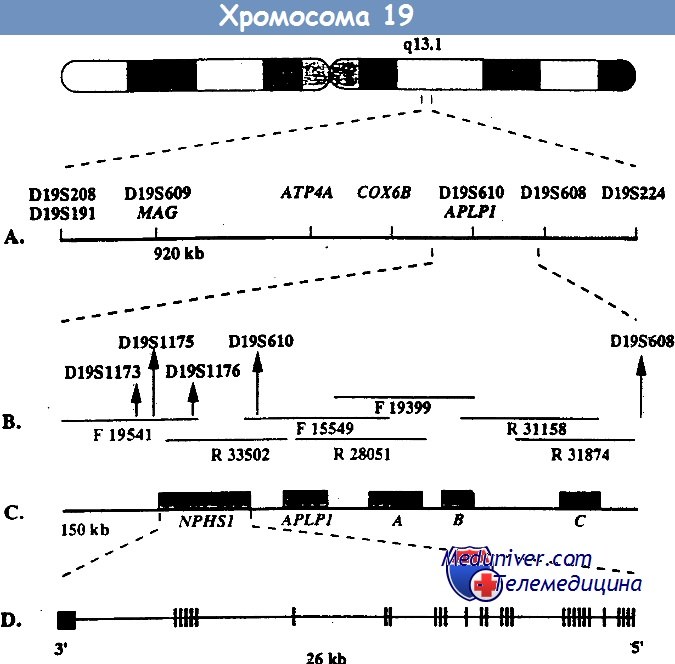
Ген NPHS1 расположен на длинном плече хромосомы 19 (19q13), содержит 29 экзонов. Генный продукт – белок нефрин имеет массу 185 КД. Ему отводится роль структурно-функциональной основы в щелевой мембране. Предполагается, что молекулы нефрина от смежных подоцитов соедининяются через их Ig-like внеклеточные области и формируют структуру, подобную «застежке – молнии», благодаря которой происходит селективная фильтрация в щелевой диафрагме.
В Финляндии 95% с нефротического синдрома Финского типа обусловлены только двумя мутациями: мажорной (делеция 2 п.н. в экзоне 2 (с.121delCТ, fin major), приводящей к сдвигу рамки считывания и минорной (стоп кодон в 1109-ой позиции аминокислотной последовательности в экзоне 26, с.3325 C>T или R1109X, fin minor). Остальные мутации представляют собой редкие миссенс-мутации и делеции. На сегодня нет данных о частоте и спектре мутаций в гене NPHS1у российских больных.
Лечение НС финского типа разрабатывается. Применение глюкокортикоидов и иммунодепрессантов не эффективно и нередко утяжеляет течение заболевания. В Финляндии предложена программа лечения НС финского типа, включающая активную борьбу с инфекцией, усиленное насыщение ребенка белком, а при достижении массы тела ребенка 10 кг — трансплантацию почки. Используется также рекомбинантный гормон роста.
Прогноз для жизни, если не произведена трансплантация почки, неблагоприятный. Срок наблюдения за детьми после успешной трансплантации почки составляет более 5 лет.
NPHS2 вторая по частоте форма врожденного кортикостероидо-резистентного (с отсутствием ответа на стероидную терапию) нефротического синдрома, обуславливающая от 45% до 55% семейных форм и от 8% до 20% спорадических случаев заболевания.
Развитие данного заболевания обусловлено мутациями в гене NPHS2 расположеном на длинном плече 1 хромосомы ( 1q25-q31) и кодирующем белок подоцин. На данный момент описано более 120 патологических мутаций, приводящих к изменениям структуры белка. Замечено, что среди населения Франции и Германии наиболее часто встречается мутация R138Q, а в итальянской и турецкой популяциях — мутация P20L.
Кроме отсутствия ответа на терапию кортикостероидами у NPHS2 формы нет специфических клинических признаков. При биопсии почек так же обнаруживают только неспецифичные гистологические изменения, такие как фокально-сегментарный гломерулосклероз, минимальные изменения и диффузную мезангиальную пролиферацию. Описаны больные как с поздней манифестацией заболевания, так и с врожденным и инфантильным НС.
В ООО «Центр Молекулярной Генетики» методом прямого автоматического секвенирования проводится анализ кодирующей последовательности генов NPHS1 и NPHS2.
При проведении пренатальной (дородовой) ДНК-диагностики в отношении конкретного заболевания, имеет смысл на уже имеющемся плодном материале провести диагностику частых анеуплоидий (синдромы Дауна, Эдвардса, Шерешевского-Тернера и др), пункт 4.54.1. Актуальность данного исследования обусловлена высокой суммарной частотой анеуплоидий — около 1 на 300 новорожденных, и отсутствием необходимости повторного забора плодного материала.
Публикации по теме раздела
Нефротический синдром
Источник
Болезнь финского наследия является генетическим заболеванием или расстройства , которое значительно чаще встречается у людей , чьи предки были этнические финны , выходцами из Финляндии и Швеции ( Meänmaa ) и России ( Карелии и Ингрии ). 36 редких заболеваний рассматриваются как заболевания финским наследия. Болезни не ограничиваются финнами; они являются генетическими заболеваниями с гораздо более широким распространением в мире, но из — за основатель эффекты и генетической изоляцию они более распространены в финнах.
В Финляндии эти заболевания чаще встречаются на востоке и на севере, в соответствии с их более высокой ассоциацией с этническими финнами , чем с этническими шведами . Финское наследие болезни не распространяется на другие этнические группы в регионе, на саамах и карелы , кроме финских карел . Это связанно с более узким местом населения среди предков современных финнов, по оценкам, произошли около 4000 лет назад, по- видимому , когда население практикующего сельского хозяйства и животноводство прибыли в Финляндии.
В Финляндии один из пяти людей несет в себе генный дефект , связанный с по меньшей мере одной финской болезнью наследия, и примерно один из 500 детей , рожденных пострадавшие. Большинство генных дефектов являются аутосомно — рецессивные , так что если и мать и отец несут один и тот же дефект, то вероятность , что их ребенок будет иметь соответствующий заболевание 1 в 4. Молекулярная генетика многих из этих заболеваний были определены, что позволяет генетическое тестирование , дородовое тестирование и консультирование. Это вызывает вопросы биоэтики и евгеники .
Типы болезней финского наследия
Есть 36 выявленных заболеваний Финские наследия:
- Амилоидоз, финский тип
- Летальный артрогрипоз с болезнью клеток переднего рога
- аспартилглюкозаминурия
- Синдром Аутоиммунный polyendocrinopathy, тип I , с или без реверсивного метафиза дисплазии
- Хрящ-волосы гипоплазии
- Цероида липофусциноз, нейронный , 1
- Цероида липофусциноз, нейронные, 3
- Цероида липофусциноз, нейронный , 5
- Цероида липофусциноз нейронные, 8, Северный эпилепсия вариант (Синонимы: Северная эпилепсия, эпилепсия, прогрессивный, с задержкой психического развития)
- хороидермия
- синдром Cohen
- Роговица Plana 2
- Понос 1, секреторный хлорид, врожденный
- Тектонические дисплазии
- Эпилепсия, прогрессивный миоклонические 1A ( Unverricht-Лундборг )
- Глицин энцефалопатия (Nonketotic hyperglycinemia)
- грацильное синдром
- Свернутый спиралью атрофия сосудистой оболочки и сетчатки
- Синдром Hydrolethalus 1
- Инфантильное начало спиноцеребеллярная атаксия ( митохондриальная ДНК истощение синдром 7)
- Лактазная недостаточность , врожденная
- Летальные врожденные контрактуры синдром 1
- Lysinuric непереносимости белка
- синдром Меккеля
- Мегалобластная анемия -1, финский и норвежский тип
- Mulibrey нанизм
- Мышечная дистрофия -dystroglycanopathy (врожденная с головным мозгом и глазом аномалиями), типа А, 3
- Нефротический синдром, тип 1 (Финский врожденное нефроз)
- Овариального гонад 1
- Поликистозный lipomembranous osteodysplasia с склерозирующей лейкоэнцефалопатией [ фи ] (Нас-Хакол болезнь)
- Прогрессивное энцефалопатия с отеком, Hypsarrhythmia и атрофии зрительного нерва
- синдром RAPADILINO
- Ретиношизис 1, Х-хромосомой, ювенильный
- Sialuria, финский тип (болезнь Салла)
- Большеберцовая мышечная дистрофия, поздние
- Синдром Ашера , тип 3A
Из них три редкие причины карликовости : хрящ-волосы гипоплазия , диастрофическая дисплазия и Mulibrey нанизм .
Четыре генетически различных подтипов нейронов цероид липофусциноза находятся в финском наследие: CLN1 , CLN3 , CLN5 и CLN8 . Названия состояний , связанные с этими подтипами включают инфантильный нейронный цероид липофусциноз , болезнь Янского-Bielschowsky и северную эпилепсию синдром . В 2001 году CLN5 и CLN8 было зарегистрировано почти исключительно в Финляндии.
Меккеля синдром типа 1 ( MKS1 ), летальное состояние, как известно в 48 финских семьях.
Другие генетические заболевания
Европейская организация по редким заболеваниям (EURORDIS) оценивает , что есть между 5000 и 7000 различными редкими заболеваниями, влияющим между 6% и 8% населением Европейского Союза . Большинство генетических заболеваний , зарегистрированных в Финляндии не является частью финского наследия болезни и их распространенность в Финляндии не выше , чем во всем мире.
Некоторые генетические заболевания непропорционально редки в финнов. К ним относятся муковисцидоз и фенилкетонурия . В Финляндии около 1 в 80 людей являются носителями мутации кистозного фиброза, по сравнению со средним значением 1 в 25 других местах в Европе.
Генетическая история
На основе молекулярных данных, узкое население среди предков современных финнов, по оценкам, произошли около 4000 лет назад. Это узкое место в результате исключительно низкое разнообразие в Y — хромосоме , по оценкам, отражает выживание всего два исконных мужских линий. Распределение Y хромосомы гаплотипов в Финляндии согласуется с двумя отдельными основывая поселения, в восточной и западной Финляндии. Узким населения наблюдается только в Y — хромосоме. Генетическое разнообразие в аутосомных хромосомах и в митохондриальной ДНК (материнский унаследованной) как высоко среди финнов , как среди других европейских этнических групп.
Финское наследие заболевание было связано с этим 4000-летним узким местом. Географическое распределение и семейные родословные , связанные с некоторыми финскими мутациями болезни наследия связаны обогащением в этих мутациях в нескольких локальных эффекты основателей , некоторые связан с периодом «позднего урегулирования» в 16 — м века (см Истории Финляндии ).
Этимология
Хотя концепция старше, английский термин «финское наследие болезни» впервые появляется в медицинской литературе в 1990 — х годах. Одна из самых ранних применений в переведенной названии 1994 медицинской статьи, вскоре последовали другие.
Смотрите также
- Лена Палотье
- Девять заболеваний
- Популяционная генетика
- BCG вспышка заболевания в Финляндии в 2000-е годы
- Медицинская генетика ашкеназов
- Финская ассоциация по интеллектуальной и порокам развития (FAIDD)
- Финно-угорское самоубийство гипотеза
Рекомендации
Источник
