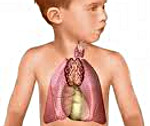
Вилочковая железа и синдром внезапной смерти
Несмотря на то, что в течение достаточно продолжительного времени внимание медицинских работников педиатрической службы было обращено на профилактику так называемого «синдрома внезапной смерти» маленьких детей, частота таких случаев не уменьшается. Этот факт объясняет пристальный интерес, как к патогенетическим, так и к танатогенетическим особенностям данного синдрома. Авторы работы поставили перед собой задачу изучить в случаях этого синдрома особенности строения отдельных органов детского организма , относящихся к системам, выполняющим адаптационную функцию, в частности, — надпочечников, рассматриваемых в настоящее время в качестве «главной железы стресса», и тимуса — центрального органа иммунной системы.
Для этого были исследованы 40 случаев смерти детей в возрасте до трех лет, наступившей на дому, внезапно (по оценке родителей и других окружающих взрослых). Эти случаи произошли на территории города Хабаровска и его ближайших пригородов за период 1994 по 1998 годы. Каких-либо признаков насильственной смерти при исследовании этих случаев выявлено не было. По мнению родителей, накануне трагических событий у детей не отмечалось признаков заболевания.
Для анализа авторами работы были взяты результаты исследований данных сорока случаев, произведенных в Хабаровском краевом бюро судебно-медицинской экспертизы и в паталогоанатомическом отделении Хабаровского Краевого детского хирургического центра.
Так как патогистологическое исследование этих случаев выявило значительное патологические отклонения в строении надпочечников умерших детей, появилась возможность разделить их на группы в зависимости от степени выраженности этих отклонений. Таким образом, из числа случаев были выделены две группы.
Первая группа включила 18 случаев (45 %) с умеренно выраженной гипоплазией надпочечников. Патогистологически в этих случаях были выявлены следующие изменения: истончение клубочковой или пучковой зоны или обоих слоев. Одновременно в пределах коры или вне её располагались очаги разрастания клеток, подобных клеткам коркового слоя в виде аденом. Такая пролиферация гормонально активных клеток очевидно указывает на длительную функциональную недостаточность в организме того гормонального компонента, за продукцию которого ответственны данные пролиферирующие клетки.
Во вторую группу вошли 17 случаев (42,5 %) с более грубыми нарушениями в строении надпочечников. В этих случаях наряду с изменениями, свойственными вышеописанной группе, имели место отклонения диспластического характера в виде замещения резко гипоплазированного мозгового вещества характерными провизорными структурами, свойственными надпочечникам плодов 28-32 недели гестации. Подобные изменения свидетельствуют о грубых нарушениях в процессе созревания структурно-функциональных характеристик надпочечников, т.е. о дисхронии в развитии надпочечников.
Сравнение различных признаков в пределах данных групп дало следущие результаты:
Таблица 1.
Иллюстрация связи надпочечниковой дисплазии разной степени выраженности с полом, возрастом, уровнем обмена
Группа 1 | Группа 2 | Среди всех | |
Мальчиков | 40% | 61,50% | 51,70% |
Нозраст до 1 месяца | 33,30% | 46,20% | 41,40% |
гипотрофия (от 1600 до 2900 г) | 53,30% | 50% | 51,70% |
Смерть при более выраженных изменениях надпочечников чаще отмечается в раннем возрасте, чаще у мальчиков. Около половины детей, умерших внезапно, имели явления гипотрофии.
Таблица 2.
Иллюстрация связи надпочечниковой дисплазии с нарушениями иммунной системы и тяжелыми формами инфекционного поражения
Признак | Группа 1 | Группа 2 |
Тимомегалия более 40 г | 66,60% | 52,90% |
Иммунный ответ эмбрионального типа | 22,20% | 64,30% |
Преждевременная жи- ровая трансформация тимуса. | 22,20% | 28,60% |
Жировая инфильтрация печени | — | 28,60% |
Кровоизлияния в надпочечники | 72,20% | 82,40% |
Патогистологические особенности тимомегалии заключаются в явлениях гиперплазии лимфоидной составляющей и гипоплазии ретикулоэпителиальной составляющей долек тимуса. Тем не менее, очевидные при тимомегалии нарушения в иммунном ответе протекают более благоприятно, чем в случаях, не сопровождающихся увеличением тимуса, но с явлениями иммунного ответа эмбрионального типа, то есть с минимальными иммунными изменениями, некрозом немногочисленных мелких тимических телец и выраженной инфильтрацией эозинофилами.
Таблица 3.
Частота сочетания надпочечниковой дисплазии с диспластическими нарушениями других органов
Признак | Группа 1 | Группа 2 |
Нарушения строения головного мозга | 44,40% | 42,80% |
Нарушение строения почек | 38,90% | 36,70% |
Нарушение строения островкового аппарата поджелудочной железы | 33,30% | 35,70% |
Значительная часть случаев дисплази и надпочечнико в сопровождается диспластическими нарушениями других органов.
Кроме описанных изменений при исследовании надпочечников были выявлены множественные очаговые кровоизлияния в мозговом и корковом слоях в 77,1 % всех случаев, а еще в 8,6% всех случаев были выявлены изменения воспалительного характера с явлениями вирусного метаморфоза клеток. Таким образом, в 85,7% случаев изменения в надпочечниках носили характер танатогенетический.
Как свидетельство выраженных иммунных нарушений в рассматриваемых случаях, надо оценивать результаты исследований, указывающих на наличие признаков воспаления в двух и более органах в 77,5% от изученных случаев, что является патоморфологическим признаком тяжелого течения инфекции в генерализованной форме. О тяжести инфекционной болезни в наших случаях говорят также признаки полиэтиологичности процесса в половине случаев, причем в сочетания входили такие возбудители, как цитомегаловирус, токсоплазма , менингококк, а в каждом третьем случае — из них — дрожжеподобные грибы. Другими признаками тяжелых форм инфекционных болезней были случаи жировой инфильтрации печени.
На основании всех приведенных данных можно утверждать, что «внезапная смерть» маленьких детей наступает не на фоне их здоровья, а на фоне отсутствия явных клинических проявлений заболевания, что само по себе должно рассматриваться как один из характерных признаков описанного врожденного патологического процесса.
Выводы:
- Во всех рассмотренных случаях «внезапной смерти» маленьких детей были выявлены морфологические признаки тяжелых заболеваний, развившихся на основе врожденных диспластических изменений различных органов, наиболее часто — надпочечников и вилочковой железы;
в 85,7 % случаев изменения в надпочечниках носили танатогенетический характер. - При судебно-медицинской экспертизе во всех случаях, требующих учета степени реактивности и адаптационных возможностей организма человека, важным источником медико-биологической информации является квалифицированное патогистологическое исследование, которое следует проводить с достаточно полным забором трупного материала.
Источник
Физиология вилочковой железы (тимуса)
Вилочковую железу (тимус) издавна причисляют к эндокринным органам, хотя из многочисленных наблюдений вытекало, что это скорее объект гормональных влияний, а не источник специфических гормонов. Однако в последние годы из вилочковой железы выделен ряд активных веществ, обладающих действием преимущественно на иммунные процессы в организме.
У человека тимус располагается за грудиной, достигая снизу дуги аорты. Он состоит из двух тесно прилегающих друг к другу долей, покрытых соединительнотканной капсулой, от которой отходят перегородки, разделяющие орган на отдельные дольки. В каждой из них различают корковый и мозговой слой. К моменту рождения масса тимуса составляет 10-15 г. В дальнейшем она увеличивается, достигая максимума к началу полового созревания (30-40 г), а затем уменьшается (возрастная инволюция тимуса). В ряде случаев при внезапной смерти на вскрытии обнаруживался тимус больших размеров. Сочетание этого с рыхлым («лимфатическим») телосложением уже давно дало повод говорить о существовании особого тимико-лимфатического статуса, якобы обусловливающего чрезвычайно высокую восприимчивость организма к неблагоприятным воздействиям. В настоящее время тимико-лимфатическому статусу не придают столь большого значения и даже высказывают сомнения в самом его существовании. Действительно, в случаях насильственной смерти размеры тимуса обычно столь же велики, что и при предполагаемом тимико-лимфатическом статусе. С другой стороны, явная гиперплазия тимуса, имеющая место, например, при злокачественной миастении, как правило, не приводит к внезапной смерти. Физиологическая инволюция железы заключается в постепенном исчезновении из нее характерных клеточных элементов с замещением их адипоцитами и фиброзной тканью. Наблюдается также острая инволюция вилочковой железы, связанная обычно со стрессом.
Корковое вещество тимуса представлено малыми лимфоцитами и небольшим числом ретикулоэндотелиальных клеток. Отношение этих элементов составляет примерно 100:1. В мозговом веществе присутствуют так называемые тельца Гассаля — скопления эпителиальных клеток, окружающие лимфоциты и эозинофилы. Однако первых в мозговом слое примерно в 20 раз меньше, чем вторых. Последние обладают ворсинками и содержат ШИК-положительный материал, напоминающий коллоид щитовидной железы. Электронно-микроскопические исследования выявляют в этих клетках шероховатый эндоплазматический ретикулум, хорошо развитый пластинчатый комплекс (аппарат Гольджи) и гранулы, содержимое которых может обладать гормональной активностью. Относительно структуры стенок сосудов в вилочковой железе (т. е. наличия гистогематического барьера в этом органе) нет единого мнения. Артерии проходят лишь в корковом веществе тимуса, тогда как вены — в мозговом. Митозы обнаруживаются практически только в лимфоцитах коркового слоя вилочковой железы.
На основании особенностей строения этого органа полагают, что он служит важным источником лимфоцитов в организме, но, в отличие от других подобных структур, не принимает непосредственного участия в иммунных реакциях. Присутствующие в тимусе кистозные образования, клетки стенок которых обладают секреторными признаками, могут отражать эндокринную функцию этого органа.
В фило- и онтогенезе прослеживается четкая связь между появлением и развитием тимуса, с одной стороны, и возникновением иммунологической реактивности организма — с другой. Поэтому основную роль тимуса усматривают в регуляции иммунологических процессов. С этой функцией тесно связана и лимфопоэтическая деятельность этого органа. В вилочковой железе происходит дифференцировка различных субпопуляций Т-лимфоцитов, оказывающих хелперное, супрессорное и киллерное действие. В последние годы показано, что иммунорегуляторная и лимфопоэтическая функции тимуса осуществляются за счет секреции гуморальных факторов. Секреторной активностью обладают, по-видимому, эпителиальные клетки мозгового вещества. Роль тимуса в организме отчетливо видна на примере патологических состояний, развивающихся при недостаточности его функций или при его отсутствии.
В таблице приведены некоторые гипотетические зависимости клинических синдромов от деятельности вилочковой железы, но отсутствуют указания на ряд других доказанных ее функций. Однако и в таком виде она дает представление о многообразии и важности физиологической активности тимуса.
Функции вилочковой железы и синдромы, обусловленные их нарушением
Функции
Синдромы
Развитие иммунокомпетентности
Восстановление иммунокомпетентности
Поддержание иммунокомпетентности
Регуляция периферической лимфоидной системы
Продукция фактора, стимулирующего костный мозг
Продукция гипогликемизирующего фактора
Продукция фактора проницаемости
Продукция фактора, ингибирующего нервно-мышечную передачу
Синдром иммунной недостаточности
Аутоиммунные заболевания
Неоплазии
Лимфоидная пролиферация
Тимома, агаммаглобулинемия с эритроцитарной аплазией
Гипогликемия при лейкозе
Гиперчувствительность замедленного типа
Злокачественная миастения
Неонатальная тимэктомия животных (особенно грызунов) приводит к развитию у них так называемого синдрома истощения (wasting-синдром) — отставание в росте, деплеция лимфоидной ткани, гипогаммаглобулинемия, дистрофические изменения кожи с выпадением шерсти, атрофия подкожной жировой клетчатки и, наконец, ранняя гибель… Помимо сугубо иммунологических причин возникновения этого синдрома, в его генезе может играть роль нарушение взаимодействия каких-то факторов тимуса с соматотропной функцией гипофиза… Близкие изменения развиваются и у выведенных методом узкородственного скрещивания мутантных линий грызунов с врожденным отсутствием вилочковой железы (мутант-ная атимия). У таких животных могут полностью отсутствовать Т-лимфоциты, не проявляется клеточно-опосредованный иммунитет, и они погибают гораздо раньше обычных особей данного вида. Врожденная гипоплазия и аплазия тимуса у человека характеризуются генерализованной лимфоидной деплецией и гипертрофией периферических лимфоидных структур. Имеет место угнетение синтеза иммуноглобулинов и клеточного иммунитета. Обычно дети с такой патологией не доживают до 1 года. Лечение больных препаратом нормального тимуса (тимозин) улучшает их состояние, что сопровождается увеличением количества Т-лимфоцитов в крови.
Источник

Эту историю рассказал Роберт Сапольски в одной из своих лекций.
Вы, наверное, слышали о синдроме внезапной смерти младенцев (sudden infant death syndrome, SIDS). Это загадочный феномен, когда абсолютно здоровый младенец просто умирает во сне, без видимых причин. Синдром обнаруживается в конце 19 века, хотя тогда его так никто не называл.
Интересно, что само обнаружение синдрома произошло благодаря достижениям цивилизации — тому, что ребенок был настолько здоров, что объяснить смерть становилось затруднительно. Ранее всегда было просто найти такое объяснение. Но есть и еще один фактор, почему синдром становится известным. Смерть забирает здоровых детей, но здоровы они потому, что происходят из небедных семей. В бедных семьях, по-прежнему, если кому-то и понадобится вдруг найти объяснение смерти младенца – их полно, всяких разных. Абсолютно здоровых бедных детей почти не бывает, и поэтому среди них SIDS не диагностируется. Это всё уже заслуживало бы полноценной истории, но дальше становится еще интереснее.
В поисках причин смерти детей вскрывают и вскоре обнаруживается, что у них у всех есть общий знаменатель: увеличенная вилочковая железа (тимус). Далее, рассуждения строились следующим образом: такая гипертрофированная железа сдавливала трахею во время сна, что приводило к удушью и смерти.
Так или иначе, с синдромом стало понятно, и болезнь обрела свое название: Status thymicolymphaticus. Особенного метода лечения не было, и родителям давали рекомендации по предотвращению удушья ребенка во сне. Любопытно, что одна из сегодняшних рекомендаций против синдрома – не класть ребенка на живот, чтобы он не задохнулся. Интересно, не оттуда ли растут ноги этого совета?
Но вот настал 20 век, и вскоре было открыта радиаоктивность. Мы помним, что медицина ринулась применять её свойства в самых необычных ситуациях. Для лечения Status thymicolymphaticus, в том числе: если у вас здоровый младенец, то ему следует для профилактики уменьшить размер железы радиоактивным облучением, чтоб он не умер внезапно во сне.
Позже выяснилось, что радиация наносила удар и по щитовидной железе, которая находится рядом. Это удар очень часто приводил к раку. По некоторым оценкам, профилактика SIDS привела к 10 тысячам смертей от рака щитовидной железы.
Цивилизация подкидывает еще карту: появились автомобили, и их жертвы. Это привело к странным данным: дело в том, что и вскрытия детей, погибших в автокатастрофах, тоже показывали увеличенную вилочковую железу. Почему у почти всех детей, погибших в автоавариях, такая большая вилочковая железа?
На протяжение сотен лет медицина развивалась, и для этого требовалось изучать человека, а, значит, изучать анатомию. Требовались трупы для анатомических исследований и обучения, и спрос на них рос с каждым годом. С другой стороны, никто никогда не хотел, чтобы его тело после смерти вскрывали и изучали. Поэтому медикам приходилось идти на всевозможные исхищрения, чтобы тела доставать. Это всегда был и есть нелегальный и жестокий бизнес, как сегодня, так и пятьсот лет назад. Сюжет с выкапыванием тела был, например, в книге про Тома Сойера, где события разворачиваются приблизительно в 1845 году (на картинке в начале).
Поэтому тела, которые попадали на столы анатомов, были практически всегда бедных людей. И всегда — непропорционально соотношению бедных и богатых в обществе, потому что богатые принимали все и всяческие меры против участи оказаться в анатомическом театре. И, как мы сейчас понимаем, тело бедного человека отличается от тела богатого человека по многим характеристикам. в худшую, разумеется, сторону.
Одно из таких многочисленных различий – размер вилочковой железы. Бедность, и плохие условия жизни, в самом широком смысле этого слова, приводят к патологическому уменьшению этой железы, иногда даже более чем в два раза. Железа участвует в работе иммунной системы, и размер имеет большое значение для борьбы с болезнями. Несчетное количество вскрытых тел за сотни лет утвердили анатомов в том, каков нормальный размер вилочковой железы. Но они всегда видели лишь уменьшенную версию, поэтому ее нормальный размер казался огромным.
Только в 1930-х годах один американский врач сопоставил все эти факты и ужаснулся. В 1940-х годах он написал об этом в учебнике и категорически предостерегал от облучения. Это был Уолдо Нельсон, которого называют «отцом педиатрии», автор классического Учебника по педиатрии Нельсона. Потребовалось, правда, с десяток лет, пока это прекратилось окончательно. Еще можно встретить людей, которым в детстве, в 1950 годы облучили вилочковую железу.
У этой истории может быть много разных уроков, на любой вкус. Мне лично кажется главным вывод о том, что надо постоянно задавать вопросы, на которых основано твое понимание чего угодно, потому что скорее всего, хоть где-то, ты обязательно ошибаешься. Это нормально ошибаться, но все же ошибки надо исправлять. Мы думаем, что сегодня-то мы уже невероятно мудры, научены опытом и не принимаем одно за другое, а все наши решения сверкают на солнце от гениальности. И скорее всего, мы ошибаемся.
Сам Сапольски предложил еще один дельный совет: никогда не рождайтесь в бедной семье, это плохо для здоровья и всего остального.
Другие Маленькие истории.
Источник

Тимомегалия — гиперплазия тимуса и его гипофункция, сопровождающие ряд заболеваний детского возраста. Незначительная тимомегалия протекает бессимптомно; выраженное увеличение тимуса может проявляться синдром сдавления жизненно важных органов, синдромом лимфопролиферации, иммунными и эндокрино-обменными нарушениями. Диагностика тимомегалии требует участия детского иммунолога, проведения УЗИ вилочковой железы, рентгенографии грудной клетки, исследования показателей Т-звена иммунной системы и гормонального статуса. Детям с тимомегалией рекомендуются общеоздоровительные мероприятия, прием поливитаминов, биостимуляторов; по показаниям — глюкокортикостероидов.
Общие сведения
Тимомегалия – превышение массы и объема вилочковой железы у детей предельных возрастных норм с сохранением нормальной гистологической структуры органа. Тимомегалия обнаруживается примерно у 13-34% детей раннего возраста и 3-12% детей старше 3-х лет. После 5-6 лет количество детей с тимомегалией существенно уменьшается. У мальчиков тимомегалия диагностируется в 1,5-2 раза чаще, чем у девочек. Дети, страдающие тимомегалией, составляют в педиатрии группу риска по развитию аллергических, эндокринных, аутоиммунных и онкологических заболеваний, синдрома внезапной детской смерти, потому нуждаются в особом уходе и дополнительном наблюдении со стороны педиатра и детского аллерголога-иммунолога.
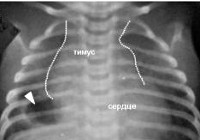
Тимомегалия
Причины тимомегалии
Вилочковая железа или тимус представляет собой центральный орган иммунной системы и железу внутренней секреции. В тимусе происходит трансформация клеток-предшественников (претимоцитов) в Т-лимфоциты, участвующие в регуляции клеточного и гуморального иммунитета. Кроме этого, вилочковая железа секретирует свыше 20 биологически активных веществ, среди которых гормоны и гормоноподобные вещества, регулирующие обмен веществ, гемопоэз, уровень кальция и сахара в крови, фосфора в скелетных мышцах, рост и половое созревание. Максимальную массу тимус имеет к моменту рождения ребенка (4,4% массы тела); его рост продолжается до 15 лет, после чего орган подвергается постепенной возрастной инволюции – замещению железистой ткани жировой и соединительной.
К развитию тимомегалии могут приводить различные эндогенные и экзогенные факторы, а также их сочетание. Доказана генетическая детерминированность тимомегалии и ее связь с HLA-антигенами B15, B18, В27. Определенную роль в формировании тимомегалии у ребенка играет отягощенный акушерский анамнез матери (аборты и выкидыши в анамнезе, токсикозы беременности, резус-конфликт, поздняя беременность и др.); вредное влияние на плод лекарств, алкоголя, рентгеновского облучения; патология периода новорожденности и раннего возраста (асфиксия, недоношенность, родовые травмы, синдром дыхательных расстройств, конъюгационная желтуха, сепсис новорожденных) и др. Тимомегалия является характерным проявлением лимфатико-гипопластического диатеза.
Классификация тимомегалии
Исследователи выделяют врожденную (первичную) и приобретенную (вторичную) тимомегалию. При врожденной тимомегалии вилочковая железа сформирована правильно, однако увеличена в размерах, что сопровождается снижением ее секреторной функции, гиперплазией лимфоидной ткани и дисфункцией нейро-эндокринной системы.
Приобретенная тимомегалия развивается вследствие первичного поражения других эндокринных желез: гипокортицизма, обусловленного аддисоновой болезнью, травмами, воспалительным или опухолевым поражением коры надпочечников; гипоталамического синдрома при окклюзионной гидроцефалии, васкулитах, опухолях головного мозга и пр.
Кроме этого, увеличение вилочковой железы может носить функциональный характер (например, при ОРВИ, пневмонии и др. заболеваниях); в этих случаях после выздоровления размеры тимуса и иммуногормональные показатели приходят в норму. Органическая тимомегалия связана с непосредственным поражением вилочковой железы.
Симптомы тимомегалии
Незначительное увеличение вилочковой железы может протекать без каких-либо выраженных клинических проявлений. Иногда для обозначения небольшой гиперплазии используется понятие «синдром увеличенной вилочковой железы» (СУВЖ), а термином «тимомегалия» обозначается значительное увеличение органа, сопровождающееся развернутой клинической симптоматикой.
Дети с тимомегалией отличаются характерными фенотипическими чертами: округлыми мягкими формами тела, крупными чертами лица и увеличенными поперечными размерами тела (широким лицом, плечами, грудной клеткой, ладонями и стопами), бледной, слабо пигментированной кожей, светлыми волосами и глазами, слабо развитой мускулатурой, повышенным аппетитом. Чаще чем в популяции у них отмечается нарушение темпов и последовательности прорезывания зубов, позднее начало ходьбы, задержка речевого развития и дислалия.
Из сопутствующих заболеваний при тимомегалии могут встречаться паховые и пупочные грыжи, ВПС (септальные дефекты), перинатальная энцефалопатия, рахит, врожденный вывих бедра, синдактилия, крипторхизм, фимоз, гипоплазия матки и влагалища и др. Дети с тимомегалией склонны к артериальной гипотонии, аритмиям, повышенной потливости, необъяснимому длительному субфебрилитету. Клинически значимая тимомегалии может сопровождаться сдавлением жизненно важных органов (трахеи, сосудистого пучка, ВПВ, блуждающего нерва), развитием синдромов иммунодефицита и лимфопролиферации, эндокрино-обменных нарушений.
При компрессии увеличенным тимусом жизненно важных органов может развиваться синдром верхней полой вены: набухание шейных вен, расширение венозной сети на верхней части туловища, одышка, цианоз. В случае сдавления трахеи возникает кашель, одышка, шумное храпящее дыхание, возбужденное состояние. Раздражение блуждающего нерва сопровождается брадикардией, дисфонией, срыгиваниями или рвотой, коллапсами.
Тимомегалия обычно сочетается с гиперплазией лимфоидной ткани (лимфаденопатией, увеличением аденоидов и миндалин, спленомегалией). В раннем и дошкольном возрасте дети с тимомегалией относятся к группе часто болеющих; у них отмечаются частые эпизоды ОРВИ с сильным коклюшеподобным кашлем и ложным крупом, отиты, пневмонии, выраженные поствакцинальные реакции. Эндокринные сдвиги проявляются ожирением, гипокортицизмом, гипопаратиреозом, сахарным диабетом, дисфункцией щитовидной железы, гиперпигментацией кожных покровов.
Диагностика тимомегалии
Обследование детей с тимомегалией проводится педиатром, детским иммунологом, детским эндокринологом и включает несколько этапов (клинико-анамнестический, инструментальный и лабораторный). При оценке объективного статуса ребенка с тимомегалией обращается внимание на перинатальный анамнез, конституционные данные, перенесенные заболевания.
Основная роль в выявлении тимомегалии принадлежит инструментальному обследованию – рентгенографии грудной клетки, УЗИ вилочковой железы, УЗИ органов брюшной полости и надпочечников. Рентгенодиагностика позволяет определить степень тимомегалии на основании исчисления кардио-тимико-торакального индекса (КТТИ) и вазокардиального индекса (ВКИ). В норме на рентгенограммах в прямой проекции тень вилочковой железы располагается за тенью сердца и сосудистого пучка. При тимомегалии I степени тень тимуса занимает 1/2 половину грудной клетки, II степени — 1/2 — 3/4 грудной клетки, III степени — более 3/4 грудной клетки. УЗИ тимуса позволяет оценить объем и массу органа и составить более четкое представление о степени тимомегалии.
Лабораторные показатели при тимомегалии характеризуются снижением субпопуляции Т-лимфоцитов (CD3, CD4, CD8); резким уменьшением количества зрелых В-клеток, низким уровнем IgG и IgА, повышенным — IgM и IgE; снижением концентрации АКТГ, кортизола, повышением уровня СТГ и ТТГ, некоторым увеличением концентрации паратиреоидного гормона.
Лечение тимомегалии
Вопросы ведения детей с тимомегалией и необходимости проведения корригирующей терапии разработаны недостаточно. Общепринято считать, что при незначительном увеличении тимуса специальных лечебных мероприятий не требуется. Рекомендуется грудное вскармливание, рациональное питание, ограничение стрессов и контактов с инфекционными больными.
Объем медикаментозной терапии определяет иммунолог, наблюдающий ребенка с тимомегалией. Часто болеющим детям каждые 3-4 месяца показан прием адаптогенов и биостимуляторов (женьшеня, пантокрина, элеутерококка, лимонника китайского). С целью иммунокоррекции используется экстракт тимуса крупного рогатого скота. Дважды в год до достижения 5-6-летнего возраста ребенку назначаются курсы индукторов синтеза глюкокортикоидов (аммония глицирризината, этимизола).
При тяжелых заболеваниях, стрессах, а также перед оперативными вмешательствами детям с тимомегалией назначаются глюкокортикоиды (преднизолон, гидрокортизон). В случае развития синдрома тимусо-надпочечниковой недостаточности (апатии, сильной слабости, брадикардии, рвоты, диспепсии, артериальной гипотонии, признаков почечной недостаточности) показано введение преднизолона, инфузионных растворов, сердечных гликозидов, препаратов калия.
При тимомегалии I-II степени профилактическая вакцинация не противопоказана, но проводится на фоне гипосенсибилизирующей терапии и гипоаллергенной диеты. Детям с тимомегалией III степени при благоприятной эпидобстановке дается отвод от прививок на 6 месяцев (за исключением вакцинации против полиомиелита).
Прогноз и профилактика тимомегалии
Обычно тимомегалия у детей сохраняется до 3-6 лет, после чего размеры вилочковой железы приходят норму. Тем не менее, дети с тимомегалией более подвержены инфекционно-воспалительным и аллергическим заболеваниям, риску внезапной смерти от гипофункции коры надпочечников, сдавления увеличенным тимусом органов средостения.
Дети с тимомегалией должны состоять на диспансерном учете у педиатра, детского аллерголога-иммунолога, эндокринолога; проходить ежегодное лабораторно-инструментальное обследование. К возможным мерам по предупреждению тимомегалии можно отнести исключение перинатальных вредностей. Детям с увеличенной вилочковой железой следует избегать стрессов, контактов с инфекционными больными, своевременно проходить профилактические курсы лечения.
Источник
