Узи признаки синдрома портальной гипертензии
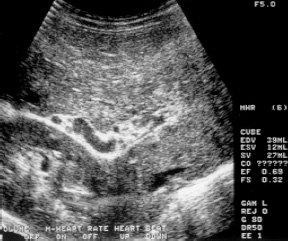
Кровь, питающая ряд органов брюшной полости, отводится по единому венозному руслу. Эта вена называется (учитывая ее расположение) воротной или портальной веной печени; она имеет множество ответвлений и является наиболее крупной веной в организме человека, достигая в диаметре 8-12 мм. Как и в любом ином магистральном кровеносном сосуде, в воротной вене должно постоянно поддерживаться определенное кровяное давление – здесь оно в норме составляет от 5-7 до 10-12 мм рт. ст. Хроническое превышение этого уровня приводит к общим нарушениям гемо- и гидродинамики брюшной полости, дегенеративным изменениям в тканях и другим тяжелым последствиям, которые в совокупности образуют синдром портальной гипертензии.
По определению, синдром не является самостоятельным заболеванием; это устойчивое, повторяющееся сочетание взаимосвязанных клинических симптомов, которое может формироваться в силу разных причин, но обладает собственными специфическими закономерностями развития и протекания. Это в полной мере касается и синдрома портальной гипертензии.
Причины
Выделяют две основные группы причин развития портальной гипертензии: внепеченочные и внутрипеченочные. На этих же критериях (конкретная локализация блока воротной вены) построены общепринятые ее классификации, обычно включающие под- или предпеченочную форму, внутрипеченочную (с несколькими подтипами), надпеченочную и смешанную.
Согласно доступной медицинской статистике, наиболее распространенной (85-90%) является внутрипеченочная локализация нарушений портально-венозного оттока. В этиологическом плане внутрипеченочная портальная гипертензия чаще всего обусловлена циррозом печени или иным процессом дегенеративного замещения паренхиматозных клеток соединительной тканью.
Предпеченочная форма составляет 10-12% в общем объеме портальной гипертензии и, как правило, развивается вследствие механического давления (например, злокачественной опухолью), врожденных или приобретенных аномалий анатомического строения вены, воспалительного процесса в миокарде, обструктивного тромбоза Бадда-Киари и пр.
Частота надпеченочной (постпеченочной) формы не превышает 3-4%; причинами обычно становятся прорастание опухоли, тромбоз, эндофлебит печеночных вен.
В целом, к перечню этиопатогенетических факторов портальной гипертензии следует добавить все разновидности гепатитов, онкозаболевания, патологию билиарной (желчевыводящей) и сердечнососудистой систем, последствия травм и некоторых хирургических вмешательств, отравления (медикаментами, грибами, соединениями меди и пр.), ожоги. Кроме того, портальная гипертензия нередко развивается на фоне жизнеугрожающих состояний в ходе реанимационных мероприятий.
Симптоматика
Классическая триада симптомов включает варикозное расширение вен пищевода и верхних отделов желудка (в 85% случаев), спленомегалию (селезенка в той или иной степени увеличена практически всегда) и асцит (массивное скопление жидкости в брюшной полости).
Ранние проявления синдрома портальной гипертензии могут быть неспецифическими: признаки диспепсии (абдоминальные боли и тяжесть в животе, тошнота, различные проблемы с дефекацией, метеоризм и т.д.). Кроме того, по мере нарастания выраженности нарушений кровоснабжения печени снижается ее способность к выполнению дезинтоксикационных функций, что отражается и на функционировании мозга, – развивается т.н. печеночная энцефалопатия с присущей ей психоневрологической симптоматикой. При тяжелой печеночной недостаточности наблюдается желтуха. Прямую угрозу жизни несут (и нередко приводят к летальному исходу) внутренние кровотечения из растянутых и истонченных венозных стенок.
Выраженность, стадийность и скорость появления симптомов в значительной мере различаются при разных типах портальной гипертензии. Так, «водянка живота» (асцит) в одних случаях развивается постепенно, в других остро, и т.д.
Диагностика
Диагноз устанавливается путем сопоставления жалоб, анамнестических данных, результатов клинического осмотра и инструментального обследования. В частности, необходимой и обязательной является ФГДС (фиброгастродуоденоскопия), в ходе которой визуализируются вены пищевода и желудка, оценивается их статус и собирается другая клинически значимая информация. Назначают УЗИ в дуплекс-режиме, рентгенографию, по необходимости – дополнительные методы исследования селезенки и гепатобилиарной системы (сканирование печени, спленоманометрия, спленопортография, КТ, МРТ и т.д.).
Лечение
Синдром портальной гипертензии, в целом, весьма проблематичен в терапевтическом плане. Амбулаторное консервативное лечение и курсы поддерживающей терапии могут занимать несколько лет; назначаются «прицельные» гипотензивные средства для снижения давления в воротной, нижней полой и печеночных венах, вазо- и гепатопротекторы. Однако с усугублением ситуации амбулаторное лечение становится все менее эффективным, и пациента приходится госпитализировать, – сроки стационарного лечения варьируют от двух недель до месяца и более.
Масштабы и цели хирургического вмешательства, – если оно целесообразно и необходимо, – определяются особенностями конкретного случая: в различных ситуациях основной задачей может быть восстановление венозной проходимости, коррекция путей отвода крови, удаление из брюшной полости избыточной жидкости при асците, склерозирование расширенных и кровоточащих вен пищевода, и т.д. Однако относительными или абсолютными противопоказаниями к операции могут становиться сопутствующие хронические заболевания, беременность, пожилой возраст, тяжелое общее состояние пациента (обусловленное, например, выраженной печеночной недостаточностью).
Отдаленный прогноз при некоторых формах синдрома портальной гипертензии (внутрипеченочная, надпеченочная) неблагоприятен, особенно при пищеводно-желудочных геморрагиях у больных циррозом печени. В других случаях оперативное вмешательство может значительно улучшить ситуацию. Однако единственным радикальным лечением в настоящее время остается трансплантация печени.
Источник
Видео. Лекция Оксаны Балтарович по патологии печени
Типы эхоструктуры печени
Типы эхоструктуры печени — центролобулярный, нормальный, фиброзно-жировой.
| Центролобулярная печень отечна, поэтому снижена эхогенность паренхимы. Кажется, что мелких воротных вен очень много, и их стенки ярко сияют — симптом «звездного неба». На самом деле, их количество не увеличилось, просто изображение более контрастное. Диафрагма хорошо просматривается — очень яркая линия. | При фиброзно-жировой дистрофии нормальную ткань печени замещает жировая и фиброзная. Печень становится гиперэхогенной. Пропадает контраст между паренхимой и стенками мелких воротных вен — их плохо видно или совсем не видно. Печень плотная, поэтому диафрагма просматривается плохо. |
|
|
Важно!!! Центролобулярную картину печени можно увидеть и у здоровых людей. Обычно это худощавые молодые люди и подростки. Если биохимические показатели крови (АЛТ, АСТ, ГГТ, биллирубин) в норме, то можно с уверенностью сказать, что пациент здоров.
Фульминантный (молниеносный) гепатит на УЗИ
Фульминантный (молниеносный) гепатит — это редкое, но тяжелое заболевание, которое легко пропустить. Молниеносный гепатит на УЗИ:
- печень неоднородна,
- зоны пониженной эхогенности с яркими стенками воротных вен (картина «звездного неба») чередуются с гиперэхогенными участками.
Картина «звездного неба» указывает на острый отек или некроз, а гиперэхогенные участки — это нормальная ткань печени.
Фиброзно-жировое перерождение печени на УЗИ
При фиброзно-жировой дистрофии нормальную ткань печени замещает жировая и фиброзная. Фиброзно-жировая дистрофия печени на УЗИ:
- печень гиперэхогенна,
- не видно стенок воротных вен,
- дорзальное затухание сигнала — не видно часть диафрагмы (выраженная жировая дистрофия),
- эхоструктура печени однородная при диффузной жировой инфильтрации или неоднородной — при очаговой.
При очаговой жировой инфильтрации участки сохраненной печени на фоне жировой инфильтрации можно ошибочно принять за образование. Сохранная паренхима встречается подкапсульно, вокруг крупных стволов воротных вен, а так же вокруг правой и левой продольной борозды печени. Чтобы не ошибиться, надо оценить внутреннюю структуру печени и убедиться, что НЕТ смещения сосудистых структур.
Цирроз печени на УЗИ
При циррозе происходит фиброзно-жировое перерождение печени. УЗИ признаки цирроза печени:
- печень неоднородна, как будто «изъедена молью», на фоне фиброза выделяются гипоэхогенные зоны регенерации, которые могут быть крупными и совсем крошечными (стрелка);
- «сморщенная» печень имеет бугристую поверхность;
- можно увидеть смещение сосудистых структур;
- часто увеличена хвостатая доля, отношение хвостатой доли к правой доле печени (ХД/ПД) — это специфический маркер для цирроза печени → ХД/ПД > 0.65 — вероятность цирроза 96%, а ХД/ПД > 0.73 — вероятность цирроза 99% (подробно смотри Размеры печени на УЗИ).
Важно!!! При циррозе паренхима печени становится тугой и не эластичной, поэтому растет давление в воротной вене. Если на УЗИ вы видите цирроз печени, нужно внимательно поискать признаки портальной гипертензии.
Признаки портальной гипертензии на УЗИ
- асцит;
- дилятация ствола воротной (норма до 13-14 мм), селезеночной и верхней брыжеечной вен (норма до 10 мм);
- появление коллатералей;
- увеличение селезенки; патологический доплер сосудов печени.
Где искать коллатерали при портальной гипертензии
Сначала поищем ищем пищеводно-желудочные анастомозы (стрелка), селезеночно-желудочный, спленоренальный анастомозы, реканализированную пупочную вену, идущую от пупочного сегмента воротной вены прямо к пупку.
Для портальной гипертензии характерны специфические изменения доплера сосудов. Сначала уменьшается скорость кровотока и исчезают дыхательные колебания в основном стволе воротной вены — кривая становится плоской. Затем ток крови может поменять направление.
При портальной гипертензии печеночные вены теряют нормальную пульсативность. Поток крови из 3-х фазного (систолический, диастолический, предсердный толчок) становится плоским и равномерным — это портализация печеночных вен. При портальной гипертензии печеночная артерия может расширяться.
С помощью УЗИ мы можем обнаружить очаговое образование в печени. Однако, только УЗИ недостаточно для проведения дифференциальной диагностики и постановки точного диагноза. КТ и МРТ гораздо лучше подходят для этого.
Простые кисты в печени на УЗИ
Простая киста печени, как и любая другая киста в нашем теле, анэхогенна, имеет ровные края и превосходно передает УЗ-сигнал — усиление позади кисты (стрелки).
Старая гематома, эхинококковый абсцесс, билома (ограниченное скопление желчи) и серома (ограниченное скопление серозной жидкости) могут выглядеть как простая киста.
Кисты в печени могут оказаться расширенными желчными протоками
Существует 5 типов кист желчных протоков. При 4 и 5 типе на УЗИ определяются множественные кисты.
Важно!!! Если кистозное образование не очень круглое, возможно, это сосудистая структура — аневризма, артерио-портальная или портально-печеночная фистулы.
Кисты печени с неоднородной эхоструктурой на УЗИ
Что скрывается за кистозным образованием с неоднородной эхоструктурой:
- геморрагическая или инфицированная киста;
- гематома;
- абсцесс;
- билома (изолированное скопление желчи);
- серома;
- большая билиарная цистаденома;
- метастазы злокачественных опухолей с кистозной или некротической дегенерацией.
Кистозное образование с неоднородной эхоструктурой может оказаться доброкачественным или злокачественным образованием, а так же метастазом. Нет никаких специфических признаков, которые позволят определиться с диагнозом без дополнительных методов исследования.
Гипоэхогенные образования печени на УЗИ
Нет специфических узи-признаков для дифференциальной диагностики гипоэхогенных образований печени. В печени гипоэхогенным может быть:
- абсцесс;
- аденома;
- фокальная нодулярная гиперплазия;
- типичная или атипичная гемангиома;
- локальное жировое неперерождение;
- микроабсцессы;
- злокачественное образование;
- метастазы;
- лимфома.
Гиперэхогенные образования печени
При выявлении гиперэхогенного образования в печени нет специфических ультразвуковых признаков, которые позволят установить точный диагноз без дополнительных исследований. Гиперэхогенными могут быть:
- гемангиома;
- абсцесс;
- геморрагическая киста;
- локальный жир;
- аденома;
- фокальная нодулярная гиперплазия;
- злокачественная опухоль;
- метастаз;
- гепатоцеллюлярная карцинома;
- лимфома.
Гомогенные гиперэхогенные образования печени очень часто оказываются гемангиомами. Если у пациента без жалоб и злокачественных образований в анамнезе выявили один однородный гиперэхогенный очаг менее 3 см с четкими границами, то диагноз гемангиомы можно ставить по УЗИ без дополнительных методов исследования.
Важно!!! Некоторые образования могут выглядеть как гемангиома. Если пациент старше 40 лет и имеет болезненные симптомы надо провести дополнительные обследования для уточнения диагноза.
Множественные солидные (плотные) образования в печени на УЗИ
Важно!!! Если на УЗИ множественные солидные образования в печени, проводим дифференциальную диагностику прежде всего с МЕТАСТАЗАМИ, МЕТАСТАЗАМИ и МЕТАСТАЗАМИ. Чтобы понять, откуда они, следует тщательно изучить историю болезни.
Важно!!! Множественные солидные образования не всегда оказываются метастазами. Другая патология, которая может имитировать метастазы в печени.
Некоторые метастазы кальцифицируются. Обычно это расценивают как метастазы рака толстой кишки. Кальцифицированные метастазы так же можно видеть при раке яичника, молочной железы, желудка, поджелудочной железы, остеосаркоме, лейомиосаркоме, хондросаркоме, тератокарциноме.
Важно!!! Когда вы видите метастазы в печени, надо подумать о возможных осложнениях. Например, сегментарная обструкция желчных путей, некроз, кровоизлияния, суперинфекция. Вы должны тщательно перепроверить сосуды. Есть ли инвазия метастазов в воротные и печеночные вены?
Берегите себя, Ваш Диагностер!
Смотри еще:
УЗИ печени для начинающих (лекция на Диагностере)
Сегменты печени на УЗИ (лекция на Диагностере)
Доплер сосудов печени (лекция на Диагностере)
Размеры печени на УЗИ (лекция на Диагностере)
Источник
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Портальная гипертензия — одна из основных причин тяжелых пищеводно-желудочных кровотечений у детей, нередко приводящая к летальности. Кроме того, исходом портальной гипертензии у детей с болезнями печени может быть печеночная или почечная недостаточность. В связи с этим крайне важно своевременное распознавание самого синдрома и установление причин его развития.
Впервые термин «портальная гипертензия» ввел в 1928 г. английский хирург A. McJandoe. В основе ее развития лежит препятствие току крови по системе воротной вены. Обычно предполагается блокада механического характера, но встречаются случаи функционального, спастического происхождения блокады какого-либо отдела портальной системы. Различаются следующие типы портальной гипертензии: внутрипеченочная (цирроз печени, врожденный фиброз печени, выраженная жировая инфильтрация, внутрипеченочные опухоли); внепеченочная (тромбоз воротной и селезеночной вен, изолированный тромбоз селезеночной вены, порок развития воротной вены, сдавление вен опухолью или лимфатическими узлами); надпеченочная (синдром Budd-Chiari, сдавление печеночных вен опухолью); смешанная (когда порок развития воротной вены осложняется хроническим вирусным гепатитом, а затем и циррозом печени или аномалия развития воротной вены сочетается с фиброзированием печени).
Патогенез портальной гипертензии при различных типах блокады портальной системы различен. Самой частой причиной печеночной формы гипертензии является цирроз печени, когда на фоне воспаления происходит склерозирование с последующим фиброзированием портальных трактов, развитие узлов регенерации, нарушение структуры печеночных долек, сдавливание сосудистых структур, в том числе внутрипеченочных разветвлений воротной вены. Нарушение же организации долек ведет к изменению внутридолькового кровообращения и является причиной развития некрозов в центре дольки, фиброза и выраженной клеточной инфильтрации с пролиферацией купферовских клеток. Последние могут вдаваться в просвет синусоидов, суживать их, приводя к повышению давления в портальной системе. Затруднение тока крови по системе воротной вены и повышение портального давления приводят к увеличению и гиперплазии селезенки. Далее портальная гипертензия вызывает развитие коллатералей как природных, так и новых портокавальных связей: через венечную вену желудка к венозному сплетению пищевода и далее через непарную и полунепарную вены с системой верхней полой вены. Расширяются вены пищевода. В развитии портокавальных анастомозов участвуют vv.epigastricae, образуя «голову медузы», чаще наблюдаемую у взрослых пациентов. Синдром Cruveillier-Baumgarten наиболее характерен для детского возраста при врожденном фиброзе печени. При развитии портокавальных коллатералей через v.mesentericae inferior увеличиваются геморроидальные вены. В возникновении развивающегося при портальной гипертензии асцита играют роль стаз в портальной и лимфатической системе органов брюшной полости и нарушение инактивации кортикостероидов, в частности, альдостерона.
В отличие от механизма внутрипеченочной портальной гипертензии внепеченочный, на первый взгляд, представляется более простым. Практическое отсутствие ствола и разветвлений воротной вены при врожденном генезе развития, облитерированный или суженный ее просвет в результате тромбоза или экстравазального сдавления приводит к повышению сопротивления кровотоку, ведущего к стабильному увеличению портального давления до 300-500 мм водяного столба (N до 120-180 мм водяного столба) и развитию гипердинамического типа гемоциркуляции в сосудах бассейна воротной вены, с выраженным артериовенозным шунтированием в органах, увеличивая нагрузку на сосуды, с последующими их морфологическими изменениями. Их выраженность зависит от продолжительности и тяжести течения заболевания.
Развитие портальной гипертензии при надпочечной блокаде кровообращения чаще всего обусловлено рестриктивным перикардитом, сужением печеночных вен или нижней полой вены выше ее слияния с печеночными венами (болезнь Chiari), сужением нижней полой и/или печеночной вен в результате врожденной перегородки, тромба, опухоли, гипертрофированной хвостатой доли печени, что в конечном счете ведет к расстройству крово- и лимфообращения в органах и тканях нижележащих отделов.
Основными методами исследования больных с подозрением на портальную гипертензию кроме общепринятых физикальных являются ангиографические, эндоскопические и ультразвуковые в сочетании с допплерографией (в цветном и обычном режимах). Все перечисленные методы взаимодополняют друг друга. Об относительной конкурентности может идти речь между ангиографией и допплерографией. Однако, учитывая безвредность ультразвукового метода и относительную простоту его применения, нужно признать, что он должен использоваться первым у каждого ребенка с увеличенной селезенкой и другими признаками, позволяющими подозревать портальную гипертензию. А затем, ориентируясь на полученные результаты, решать вопрос о проведении рентгеноконтрастных исследований.
Наиболее частой формой портальной гипертензии у детей по сравнению с другими является внепеченочная блокада портального кровообращения, частота которой в дифференциальной диагностике портальной гипертензии достигает 50-88%. При этом у взрослых этот показатель находится в пределах 10% [1, 2]. Такая разница объясняется тем, что основная причина развития гипертензии — это первичное поражение вен портальной системы, которое в ряде случаев сопровождается фиброзированием паренхимы печени.
Эхографическое исследование органов брюшной полости у детей с подозрением на внепеченочнув форму портальной гипертензии практически в 100% случаев позволяет правильно предположить диагноз. Печень, как правило, нормального или уменьшенного размера. Последнее обусловлено значительным снижением портального кровотока при развитии фиброзирования паренхимы, наблюдаемом у 60-70% детей. При врожденном фиброзе от паренхимы регистрируются множественные мелкие сильные эхосигналы, рассеянные по всей площади среза органа (рис. 1). Воротная вена изменена, при этом может наблюдаться отсутствие просвета ее ствола или основных ветвей (рис. 2), наличие множественных тонких извитых сосудов с гиперэхогенными стенками, собранных вместе — ангиоматозная трансформация (рис. 3), наличие тромба, сужающего или закрывающего просвет сосуда, или локальное сужение просвета, что приводит к развитию коллатералей, видимых как анэхогенные узкие, извитые тубулярные структуры, идущие рядом с основным стволом (рис. 4). Такие изменения воротной вены приводят к значительному замедлению кровотока. Цветное допплеровское картирование облегчает качественную оценку состояния воротной вены, позволяя определить направление кровотока (гепатопетальный — к печени или гепатофугальный — от печени).
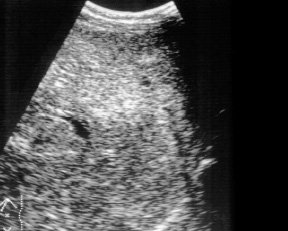
Рис. 1. Эхограмма печени при врожденном фиброзе.
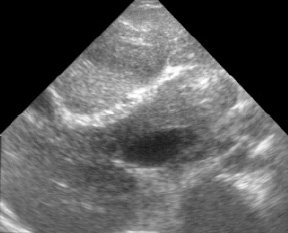
Рис. 2. Эхограмма воротной вены без просвета.

Рис. 3. Эхограмма воротной вены при ангиоматозной трансформации.
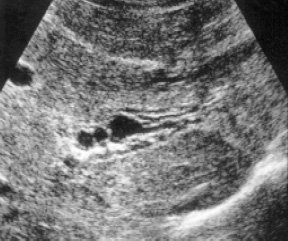
Рис. 4. Эхограмма правой ветви воротной вены с коллатералями, развившимися из-за тромбоза ствола.
Портальная гипертензия при ее внепеченочной форме постепенно приводит к ряду вторичных изменений. Селезенка увеличивается, наблюдается мелкоочаговое или диффузное мелкоочаговое уплотнение паренхимы, уплотнение стенок мелких сосудов, некоторые могут быть тромбированными (рис. 5). Селезеночная вена расширена, часто извита в области ворот. Скорость кровотока по ней, как правило, сохраняется, но значительно увеличивается показатель объемного кровотока. Селезеночная артерия несколько расширена, что приводит к увеличению индекса резистентности и свидетельствует об увеличении периферического сопротивления, косвенно подтверждая данные эхографии о состоянии паренхимы селезенки.
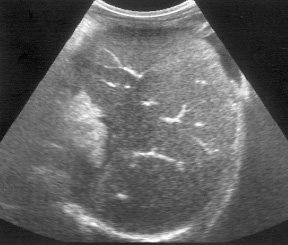
Рис. 5. Эхограмма селезенки, тромбоз мелких ветвей селезеночной вены.
Малый сальник у детей обычно не визуализируется при эхографическом обследовании, однако при портальной гипертензии он часто утолщается и становится видимым как эхогенное тканевое образование с нечеткими краями, расположенное между передней поверхностью поджелудочной железы и задней поверхностью желудка, или, eсли желудок не виден, то задней поверхностью печени (рис. 6).
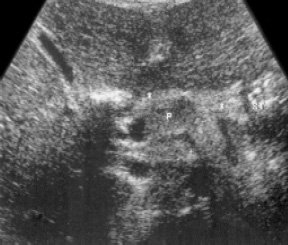
Рис. 6. Эхограмма утолщенного малого сальника.
Р — поджелудочная железа; ST — желудок.
В норме стенки желчного пузыря обычно не видны, но допускается их утолщение до 2 мм. При портальной гипертензии желчный пузырь, как правило, деформирован, с резко утолщенными стенками (рис. 7). В некоторых случаях в стенках могут быть видны варикозно расширенные сосуды, что особенно хорошо демонстрируется при использовании цветного допплеровского картирования в энергетическом режиме.
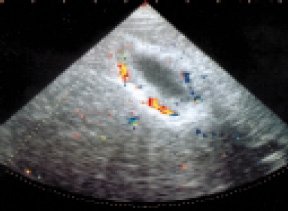
Рис. 7. Эхограмма желчного пузыря с резко утолщенными стенками, содержащими варикозно расширенные сосуды, и уменьшенным просветом (режим ЦДК).
При тяжелой форме портальной гипертензии развиваются венозные коллатерали, некоторые из которых могут быть видны: это венечные, желудочно-пищеводные, определяемые между левой долей печени и головкой, телом поджелудочной железы как анэхогенные округлые или тубулярные структуры (рис. 8). Варикозно расширенные вены пищевода могут быть определены при продольном сканировании в области аорты. В связи с различной направленностью кровотока из-за извитости сосудов при ЦДК демонстрируется его смешанный характер. При исследовании печени при фиброзе отмечается проходимая пупочная вена, имеющая иногда неровные стенки и направленная от области бифуркации воротной вены к поверхности печени в цефально-латеральном направлении (рис. 9).
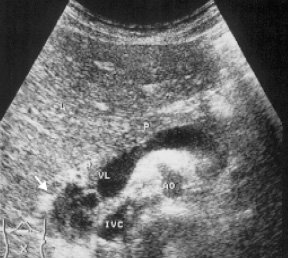
Рис. 8. Эхограмма области головки поджелудочной железы с сосудистыми коллатералями (стрелка).
L — печень; P — поджелудочная железа; VL — селезеночная вена; AO — аорта; IVC — нижняя полая вена.
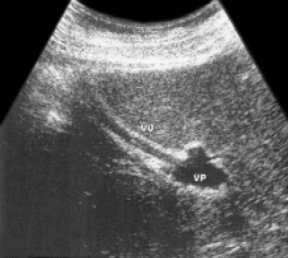
Рис. 9. Эхограмма расширенной пупочной вены.
VU — пупочная вена; VP — воротная вена.
При печеночной форме портальной гипертензии, основной причиной развития которой у детей является цирроз печени, наблюдаются практически все те же вторичные изменения. Воротная же вена значительно расширена, достигая в диаметре 20 мм, стенки ее утолщены. Скорость кровотока по вене снижена, но за счет увеличения диаметра возрастает и величина объемного кровотока. Так же увеличение этого показателя имеет место и в селезеночной вене. Изменения, происходящие в портальной системе, ведут к перераспределению объема крови — его увеличению в сосудах портальной системы и снижению в других жизненно важных органах (мозг, почки) [3]. При более выраженных нарушениях кровообращения по воротной вене происходит накопление жидкости в брюшной полости, которая при ее малом количестве прежде всего локализуется в латеральных каналах и малом тазу, а затем в околопеченочном и околоселезеночном пространствах.
Наиболее эффективным способом лечения внепеченочной портальной гипертензии и основного ее осложнения — рецидивов острых кровотечений из варикозных вен пищевода и желудка — является создание портокавальных анастомозов, позволяющих создать условия для декомпрессии портальной системы. Выбор сосудов для создания шунта определяется индивидуально, с учетом гемодинамических параметров и возраста пациента. В последние годы предпочтение отдается спленоренальным, мезокавальным по типу «бок в бок». Все данные о кровотоке в потенциально используемых сосудах могут быть получены при допплеровском исследовании. Наблюдение же за характером кровотока после проведенной операции и сопоставление получаемых данных с первичными дает возможность говорить об эффективности проведенного оперативного лечения как сразу после него, так и в позднем катамнезе. Одним из осложений после проведенной операции шунтирования является образование гематомы (4-5% наблюдений), которая на эхограмме представляется округлым эхосвободным образованием с довольно четкими границами. Динамическое исследование позволяет контролировать состояние гематомы и регрессию ее размеров.
Одним из способов лечения внутрипеченочной портальной гипертензии является удаление селезенки. К основным возможным послеоперационным осложнениям, диагностируемым при УЗИ, следует отнести кровотечение с образованием гематомы, развитие абсцесса, реактивные изменения в соседних органах, чаще всего поджелудочной железе.
При синдроме Badd-Chiari на эхограммах определяется сужение или отсутствие просвета нижней полой вены или одной из печеночных вен, в частности, гипертрофированной хвостатой долей (рис. 10). При хронизации процесса образуются визуализируемые при УЗИ венозные коллатерали, сосуд выше облитерации или сужения расширен, кровоток значительно ослаблен.
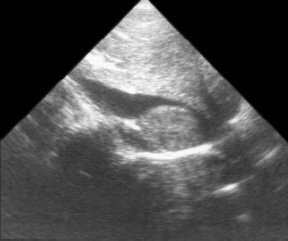
Рис. 10. Эхограмма нижней полой вены (продольный срез). Просвет вены сужен гипертрофированной хвостатой долей.
Таким образом, ультразвуковое исследование органов брюшной полости является методом выбора на раннем как амбулаторном, так и стационарном диагностическом этапах обследования детей с портальной гипертензией, включает обязательную допплеровскую оценку состояния кровотока, позволяет с высокой точностью подтвердить и определить причину портальной гипертензии, а сравнительный анализ данных, полученных в различные сроки терапевтического и хирургического лечения заболевания — оценить его эффективность.
Литература
- Пациора М.Д. Хирургия портальной гипертензии. М.: Медицина. 1974. С. 232.
- Van Vroonhen T., Molenaar J. Distal splenorenal shunt for decompression of portal hypertension in children with cystic fibrosis// Surg.Ginecol.Obst. 1979. V.149. P.559-566.
- Аббас Н.М. Состояние центральной и периферической гемодинамики у детей с хроническими заболеваниями печени: Дисс… канд. мед. наук. — М., 1996. С.160.

УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Источник
