Уремический синдром клиника диагностика лечение
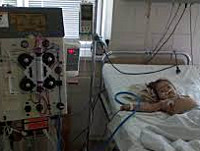
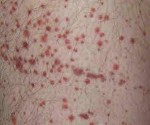
Гемолитико-уремический синдром — острое патологическое состояние, характеризующееся одновременным развитием микроангиопатической гемолитической анемии, тромбоцитопении и азотемии. Гемолитико-уремический синдром может проявляться кровавой диареей, абдоминальными болями, бледностью и иктеричностью кожи и склер, пастозностью лица, петехиями на коже, анурией, поражением ЦНС, печени, поджелудочной железы и сердца. Диагноз гемолитико-уремического синдрома основан на характерных клинических признаках, результатах общего и биохимического анализа крови и мочи, коагулограммы, бакпосева кала. Лечение гемолитико-уремического синдрома включает патогенетическую, симптоматическую и заместительную терапию.
Общие сведения
Гемолитико-уремический синдром (болезнь Гассера) – тяжелое полиэтиологическое расстройство, проявляющееся сочетанием неиммунной гемолитической анемии, тромбоцитопении и острой почечной недостаточности. Гемолитико-уремический синдром наблюдается преимущественно у детей грудного и младшего возраста (с 6 мес. до 4 лет), но также встречается у детей старшего возраста и редко у взрослых. Ежегодно в расчете на 100 тыс. детского населения регистрируются 2-3 случая гемолитико-уремического синдрома у детей до 5 лет и 1 случай у детей до 18 лет. Поскольку гемолитико-уремический синдром — одна из частых причин острой почечной недостаточности у детей, то от своевременности его диагностики и лечения зависит исход заболевания.

Гемолитико-уремический синдром
Классификация гемолитико-уремического синдрома
В зависимости от этиологии и клинических особенностей разделяют гемолитико-уремический синдром диареяассоциированный — Д+ (типичный) и не ассоциированный с диареей — Д- (спорадический или атипичный). Д+ гемолитико-уремический синдром чаще встречается у детей раннего и младшего возраста, является эндемическим (распространен в Поволжье, Московском регионе); недиарейный – более свойственен детям старшего возраста и взрослым.
По тяжести течения выделяют легкую и тяжелую формы гемолитико-уремического синдрома. Легкая форма гемолитико-уремического синдрома подразделяется на тип А (анемия, тромбоцитопения и азотемия) и тип Б (триада симптомов в сочетании с судорожным синдромом или артериальной гипертензией); тяжелая – на тип А (триада симптомов в сочетании с анурией длительностью более суток) и тип Б (триада симптомов в сочетании с анурией, артериальной гипертензией и судорожным синдромом).
Причины гемолитико-уремического синдрома
У детей частыми причинами гемолитико-уремического синдрома являются острая кишечная инфекция (90%) и инфекции верхних дыхательных путей (10 %).
Основное значение в развитии Д+ гемолитико-уремического синдрома имеет энтерогеморрагическая Е. coli, продуцирующая специфический шига-подобный веротоксин, способный избирательно повреждать эндотелиальные клетки сосудов почек и головного мозга. Наибольшее сродство веротоксина с эндотелием капилляров почек наблюдается у детей первых 3 лет жизни. Веротоксин вызывает эндотелиальный апоптоз и лейкоцитозависимое воспаление, а также запускает цепь патологических реакций, приводящих к гемолизу эритроцитов, агрегации и деструкции тромбоцитов, локальной активации процесса коагуляции и внутрисосудистого отложения фибрина, развитию ДВС-синдрома. Такими же свойствами обладает шигатоксин S. dysenteriae I типа. Развивающиеся микроциркуляторные нарушения (микроангиопатическая гемолитическая анемия, тромбоцитопения и микротромбозы) приводят к ишемическим изменениям в органах мишенях. При гемолитико-уремическом синдроме на фоне ОКИ наиболее часто поражаются капилляры клубочков почек, что может приводить к снижению скорости гломерулярной фильтрации, ишемии или некрозу клубочков, вторичной дисфункции или некрозу почечных канальцев, при массивном поражении – к ОПН.
Заражение энтерогеморрагической Е. coli может произойти при контакте с животными (кошками, крупным рогатым скотом) или инфицированным человеком; употреблении недостаточно термически обработанных мясных изделий, непастеризованных молочных продуктов, фруктовых соков, загрязненной воды. Для гемолитико-уремического синдрома характерна сезонность: на фоне ОКИ — преимущественно теплое время года (июнь-сентябрь), на фоне вирусных инфекций — зимне-весенний период.
Д- гемолитико-уремический синдром может быть постинфекционным, лекарственным, поствакцинальным, наследственным, связанным с системными заболеваниями соединительной ткани, идиопатическим. В 40% случаев развитие Д- гемолитико-уремического синдрома обусловлено респираторной инфекцией, возбудителем которой является S. pneumoniae, разрушающий мембраны эритроцитов, тромбоцитов и эндотелиоцитов с помощью фермента нейраминидазы. Вирусы ветряной оспы, ВИЧ, гриппа, Эпштейна-Барра, Коксаки также могут быть причиной гемолитико-уремического синдрома.
Установлена связь между развитием гемолитико-уремического синдрома у взрослых и употреблением некоторых медикаментов (циклоспорина А, митомицина С, эстроген — содержащих контрацептивов, противоопухолевых препаратов), трансплантацией костного мозга, злокачественными новообразованиями, системной красной волчанкой и антифосфолипидным синдромом, беременностью. Выявлены семейные случаи гемолитико-уремического синдрома с аутосомным типом наследования обусловленные дефектом системы комплемента, нарушением обмена простациклина, недостаточностью антитромботических факторов и др.
В основе гемолитико-уремического синдрома может лежать активация тромбоцитов иммунными комплексами (например, комплексом антиген – антитело после прививок живыми вакцинами против полиомиелита, против ветряной оспы, против кори, АКДС).
Симптомы гемолитико-уремического синдрома
В клинической картине гемолитико-уремического синдрома различают продромальный период, разгар заболевания и восстановительный период. Продолжительность продромального периода составляет от 2 до 7 суток. Для него характерно появление признаков поражения ЖКТ или дыхательных путей.
Гемолитико-уремический синдром на фоне ОКИ, вызванной энтеропатогенной Е. coli, имеет ярко выраженную симптоматику. Развиваются симптомы гастроэнтерита или колита (часто кровавая диарея), тошнота, рвота, абдоминальные боли, лихорадка. Постепенно общее состояния ребенка ухудшается, повышенная возбудимость сменяется вялостью.
В период разгара гемолитико-уремического синдрома превалируют проявления гемолитической анемии, тромбоцитопении и ОПН: бледность и иктеричность кожного покрова, склер и слизистых оболочек; пастозность век, голеней; кожный геморрагический синдром в виде петехий или экхимозов, иногда — носовые кровотечения, в тяжелых случаях — снижение диуреза (олигурия или анурия). Тяжесть и продолжительность дизурии зависит от степени и глубины повреждения почек.
Гемолитико-уремический синдром может проявляться полиорганной патологией: поражением ЦНС, печени, поджелудочной железы, сердца, артериальной гипертензией. В 50% случаев гемолитико-уремического синдрома наблюдаются неврологические нарушения: подергивания мышц, гиперрефлексия, децеребрационная ригидность, гемипарезы, судороги, ступор, кома (особенно выраженные у детей первых лет жизни). Выявляются гепатоспленомегалия, кардиомиопатия, тахикардия, аритмия.
В самых тяжелых случаях возможно легочное кровотечение, развитие отека легких, синдрома «ригидного легкого», сердечно-легочной недостаточности, отека головного мозга. Поражение ЖКТ может проявляться эзофагитом, энтероколитом, гепатитом, панкреатитом, а также некрозом, перфорацией, инвагинацией кишечника.
Продолжительность гемолитико-уремического синдрома обычно составляет 1-2 недели, затем наступает стабилизация и в 70% случаев — постепенное восстановление нарушенных функций: улучшение выделения мочи, повышение уровня тромбоцитов, нормализация уровня гемоглобина. При тяжелом течении наступает либо летальный исход вследствие экстраренальных поражений, либо формирование ХПН.
Диагностика гемолитико-уремического синдрома
Диагноз гемолитико-уремического синдрома основан на выявлении характерных клинических признаков, осложняющих течение ОКИ или ОРВИ: гемолитической анемии, тромбоцитопении, ДВС-синдрома, азотемии.
При гемолитико-уремическом синдроме в крови обнаруживаются анемия, анизоцитоз и полихроматофилия эритроцитов (наличие фрагментированных форм), присутствие свободного гемоглобина, снижение количества тромбоцитов, лейкоцитоз, умеренная непрямая гипербилирубинемия, возрастание уровня мочевины и креатинина, гипонатриемия, гиперкалиемия, ацидоз (в олигоанурической стадии ОПН), гипоальбуминемия.
Моча приобретает коричневато-ржавый цвет, в ней могут появиться фибриновые комки, отмечается гематурия, протеинурия, гемоглобинурия. У детей с ОКИ выполняют бактериологическое исследование кала на выявление штаммов энтеропатогенной Е. coli. При тяжелых неврологических нарушениях возможно проведение КТ головного мозга и люмбальной пункции для исключения кровотечения и менингита.
Дифференциальная диагностика гемолитико-уремического синдрома проводится с неотложными хирургическими состояниями (аппендицитом, кишечной непроходимостью, окклюзией мезентериальных сосудов, перфорацией кишечника, дивертикулом подвздошной кишки), ишемическим колитом, септицемией с ДВС-синдромом, вирусным или бактериальным гастроэнтеритом, тяжелой степенью дегидратации при кишечных токсикозах, тромботической тромбоцитопенией.
Лечение гемолитико-уремического синдрома
Лечение гемолитико-уремического синдрома определяется периодом развития заболевания и тяжестью поражения почечной ткани. Чем раньше ребенок с гемолитико-уремическим синдромом поступает в стационар, тем выше вероятность его успешного и полного излечения. Патогенетическая терапия включает нормализацию агрегатного состояния крови с использованием антиагрегантов, гепаринотерапии; улучшение микроциркуляции (трентал, эуфиллин); коррекцию антиоксидантного статуса (витамины А и Е).
При бактериальной этиологии гемолитико-уремического синдрома назначаются антибиотики широкого спектра действия; при инфекции, вызванной энтеропатогенной Е. coli, прием антибиотиков и препаратов, замедляющих моторику кишечника, не рекомендуется. При олигоанурии показана коррекция водно-электролитных расстройств, подавление реакций метаболического распада и инфекционного процесса. Для коррекции тяжелой анемии используется инфузия эритроцитарной массы.
В половине случаев типичного гемолитико-уремического синдрома необходимо раннее проведение заместительной терапии: обменного плазмафереза, перитонеального диализа или гемодиализа. Гемодиализ проводится ежедневно в течение всего олигоуремического периода. В случае развития терминальной стадии ХПН показана трансплантация почки.
Прогноз гемолитико-уремического синдрома
Гемолитико-уремический синдром имеет серьезный прогноз, летальность у маленьких детей во время острой фазы заболевания составляет 3-5%, у 12% развивается терминальная ХПН, у 25% происходит снижение клубочковой фильтрации. Плохой прогноз имеют атипичные наследственные, аутоиммунные и связанные с беременностью формы гемолитико-уремического синдрома.
Классическая форма гемолитико-уремического синдрома у детей раннего возраста с преимущественным поражением почечных клубочков протекает более благоприятно. В случае Д+ гемолитико-уремического синдрома наблюдается лучший исход по сравнению с недиарейным синдромом, сопровождающимся частыми рецидивами и высокой летальностью.
Источник

Уремия — это тяжелое клиническое проявление прогрессирующей почечной недостаточности, вызванное аутоинтоксикацией азотистыми и другими токсическими метаболитами. Проявляется нарастающей астенией, бледностью и субиктеричностью кожи, мучительным зудом, петехиальной сыпью, артериальной гипертензией, запахом аммиака изо рта, диспепсическими расстройствами, нарушением дыхания. Диагностируется с помощью биохимического исследования крови, пробы Реберга, УЗИ почек, экскреторной урографии, нефросцинтиграфии. Лечение предполагает комплексную терапию основного заболевания, коррекцию метаболических расстройств и отдельных симптомов, проведение ЗПТ, трансплантацию почки.
Общие сведения
Уремия (мочекровие) является ведущим клинико-биохимическим синдромом, развивающимся во 2-3 стадиях ОПН и при терминальной ХПН. Расстройство вызвано накоплением в крови пациентов токсичных продуктов обмена, которые в норме выводятся почками. Термин «уремия» для определения интоксикационного синдрома, возникающего у больных, страдающих почечной недостаточностью, был предложен в 1840 году французскими врачами П.А. Пьорри и Д. Л’Эритье.
Традиционно уремический синдром рассматривается как самостоятельное патологическое состояние в связи с полисистемностью поражений, тяжестью симптоматики, неблагоприятным витальным прогнозом, которые выходят за рамки прямых признаков ренальной патологии. Как и почечная недостаточность, мочекровие может быть острым и хроническим.

Уремия
Причины уремии
Аутоинтоксикация при мочекровии связана с прогрессированием острой или хронической почечной недостаточности. Соответственно причинами возникновения уремического синдрома являются те же ренальные и экстраренальные факторы, которые нарушили функционирование почек. Специалисты в сфере урологии и нефрологии выделяют следующие группы причин, вызывающих состояние уремии:
- Заболевания почек. Уменьшение количества активных нефронов со снижением почечной функциональности становится следствием гнойной, аутоиммунной, ишемической деструкции почечных тканей. Развитие уремии возможно при пиелонефрите, гломерулонефрите, наследственном нефрите, волчаночной нефропатии, пионефрозе, отторжении почечного трансплантата, тромбозе вен почек.
- Онкопатология. Азотная интоксикация наблюдается при разрушении раковым процессом ренальной паренхимы, повреждении гемато-уремического барьера у больных с аденокарциномой почки и другими злокачественными неоплазиями органа. Уремия также возникает вследствие почечной дисфункции при паранеопластической нефропатии, осложнившей экстраренальные опухоли.
- Обструкция мочевыводящих путей. Нарушение оттока мочи приводит к повышению давления в канальцах и гломерулах. Попаданию токсинов в кровь способствует разрушение клубочковых мембран. Обструкционный механизм уремии отмечается при мочекаменной болезни, мочеточниково-влагалищных свищах, сморщенном мочевом пузыре, аденоме простаты и др.
- Повреждение почек при отравлениях и интоксикациях. Почечная недостаточность с уремическим синдромом является этапом развития или исходом ряда токсических нефропатий. Уремия вследствие острой и хронической деструкции почек диагностируется при балканской эндемической нефропатии, лекарственном поражении почек, контраст-индуцированных дисфункциях.
- Экстраренальные причины. Недостаточностью почек осложняются острые состояния (кардиогенный шок, ДВС-синдром, кровотечения). Поражение почек выявляется при сахарном диабете, гипертонической болезни, туберкулезе, гестозах, других соматических, эндокринных, инфекционных болезнях. Дисметаболические нефропатии с исходом в уремию возникают при нарушениях обмена веществ.
Патогенез
Механизм развития уремического синдрома при ОПН, ХПН основан на комплексном повреждающем воздействии метаболитов, выведение которых нарушается при ренальной дисфункции. Ключевую роль в патогенезе уремии играет накопление продуктов белкового обмена, в первую очередь — мочевины, которая подвергается трансформации в кишечнике, выводится через кожу, слизистые оболочки, органы дыхания, раздражая их ткани. Токсическое воздействие на клетки разных органов и систем оказывают аммиак, метаболиты ароматических кислот (фенолы, индолы, скатолы), среднемолекулярные пептиды, ацетон, протеазы, ряд других соединений.
Повреждение клеточных мембран и нарушение работы ферментных систем при уремии усугубляет интоксикационный синдром и провоцирует полиорганную недостаточность. Низкая экскреция веществ с кислой реакцией, ингибирование процессов аммонио- и ацидогенеза, нарушение канальцевой реабсорбции завершается развитием ацидоза, электролитного дисбаланса, возникновением тяжелых мозговых, сердечно-сосудистых, дыхательных, гормональных расстройств.
Симптомы уремии
Клиническая картина уремического синдрома обычно формируется постепенно. Первыми признаками уремии являются изменения общего состояния: слабость, быстрая утомляемость, нарушения когнитивных функций, ухудшение аппетита, сонливость в дневное время с последующей ночной бессонницей, выраженная жажда, снижение температуры тела до 35,0-35,5° C. Кожа становится сухой, бледной с желтоватым оттенком, при длительной почечной недостаточности — серой. Появляется сильный зуд, петехиальная сыпь, расчесы.
Язык покрыт сероватым налетом, изо рта пациента слышен запах аммиака. У многих больных отмечается повышение артериального давления. На поздней стадии уремии происходит выделение токсических метаболитов через слизистые ЖКТ и дыхательной системы, что проявляется симптомами гастроэнтерита (тошнота, рвота, диарея), болью в горле, сухим кашлем. В тяжелых случаях наблюдается шумное глубокое дыхание, свидетельствующее о поражении дыхательного центра.
Осложнения
Длительное декомпенсированное течение уремии приводит к развитию острой энцефалопатии, при которой наблюдается спутанность сознания, наличие бреда и галлюцинаций, миоклонии, судороги. На фоне ионного дисбаланса выявляется аритмия, сердечная недостаточность. Угнетение иммунитета повышает риск возникновения и тяжесть течения инфекционных процессов. Для уремии характерно формирование плеврита и перикардита вследствие выделения кристаллов мочевины через серозные оболочки.
Расстройство может осложняться желудочно-кишечными, легочными, носовыми, маточными кровотечениями, причиной которых являются изъязвления слизистых, снижение количества тромбоцитов и белков свертывающей системы крови. При значительном снижении уровня кальция уремия усугубляется остеопорозом, остеомаляцией, гиперплазией паращитовидных желез. Наиболее опасное осложнение заболевания – уремическая кома, которая развивается при высокой концентрации аммиака в крови, выраженном метаболическом ацидозе и зачастую завершается летальным исходом.
Диагностика
Постановка диагноза уремии не представляет затруднений при наличии характерных клинических признаков и изменений биохимического состава крови. Подозревать нарушение фильтрационной и выделительной функции нефронов следует у пациентов, которые имеют заболевания мочевой системы в анамнезе. Для диагностики применяют ряд лабораторных и инструментальных методов исследования:
- Биохимический анализ крови. У всех больных отмечается многократное повышение уровня мочевины. Увеличивается концентрация креатинина, его количество кор релирует с тяжестью состояния. Для уремии типично уменьшение уровня альбуминов, диспротеинемия, изменение показателей электролитного обмена — снижение содержания натрия и кальция, повышение концентрации калия.
- Проба Реберга. Фильтрационная способность почек определяется с помощью формульного метода на основании данных об уровне креатинина в моче и плазме. При скорости клубочковой фильтрации от 60 мл/мин до 15 мл/мин у пациента диагностируют компенсированную стадию уремии. Показатель ниже 15,0 мл/мин считается прогностически неблагоприятным и свидетельствует о декомпенсации состояния.
- УЗИ почек. Ультразвуковое исследование позволяет быстро оценить состояние коркового и мозгового вещества органа, выявить абсцесс почки, почечнокаменную болезнь, злокачественные новообразования, склеротические изменения, которые могут служить непосредственной причиной уремии. Сонографию обычно дополняют проведением УЗДГ почечных сосудов для оценки ренального кровотока.
- Рентгенография. Рентгенологически можно визуализировать форму и контуры чашечно-лоханочной системы, мочеточников, мочевого пузыря, динамику заполнения мочевыводящих путей контрастом. Из-за нагрузки на почки при введении контрастного вещества у пациентов с выраженной уремией урографию применяют ограниченно. Экскреторную урографию сочетают с проведением нефросцинтиграфии.
Изменения в клиническом анализе крови при уремии неспецифичны, обычно наблюдается нормохромная анемия, повышение СОЭ, возможна тромбоцитопения, относительная лимфопения. В общем анализе мочи отмечается гипоизостенурия, цилиндрурия, эритроцитурия, при декомпенсированных состояниях рН мочи снижается до 4,5-5. В качестве дополнительных методов обследования мочевыделительной системы могут применяться КТ, МРТ.
Дифференциальная диагностика уремии проводится с гипохлоремической азотемией, гепаторенальным и панкреоренальным синдромами, печеночной энцефалопатией, эклампсией, атипичным гемолитико-анемическим синдромом, в терминальных стадиях — с диабетической комой и другими коматозными состояниями. Кроме врача-нефролога и уролога пациента могут консультировать гематолог, токсиколог, ревматолог, онколог, инфекционист, эндокринолог, анестезиолог-реаниматолог.
Лечение уремии
Выбор врачебной тактики определяется формой и причинами развития почечной недостаточности, особенностями клинической картины, тяжестью состояния пациента. Основными терапевтическими задачами являются максимальное сохранение функциональной способности почек, предупреждение и уменьшение интоксикационных нарушений, коррекция возникших расстройств.
Медикаментозные и хирургические методы ведения больных с уремией дополняют изменением диеты со снижением калорийности, ограничением белковых продуктов, соли, введением в рацион свежих овощей и фруктов, оказывающих ощелачивающий эффект. Для устранения проявлений мочекровия кроме терапии основного заболевания, на фоне которого развилась почечная недостаточность, могут быть использованы:
- Инфузионная терапия. Введение коллоидных, кристаллоидных растворов направлено на коррекцию водно-электролитного и кислотно-щелочного дисбаланса, уменьшение интоксикации. Грамотная дезинтоксикационная и регидратационная терапия позволяет уменьшить проявления полиорганной недостаточности, нормализовать работу сердца и головного мозга. Инфузии специальных составов при необходимости применяют для парентерального питания больных.
- Лекарственная коррекция отдельных симптомов. Чаще всего пациентам с уремией назначают противоанемическую терапию (эритропоэтины, препараты железа, фолиевой кислоты, витамин B12, переливание цельной крови, эритроцитарной массы), гипотензивные средства. При мучительном зуде для усиления дезинтоксикационного эффекта инфузий рекомендованы энтеросорбенты, осмотические слабительные. Для лечения сердечной недостаточности используют гликозиды.
- Заместительная почечная терапия. При недостаточной эффективности фармакотерапии, выраженной ОПН и прогрессирующей ХПН со значительными полиорганными нарушениями, угрозе развития уремической комы показана аппаратная детоксикация. В зависимости от возможностей лечебного учреждения и состояния пациента для удаления токсичных метаболитов разово или периодически проводят перитонеальный диализ, гемодиализ, гемофильтрацию, гемодиафильтрацию.
Хирургическое лечение уремии эффективно при острых интоксикационных состояниях, вызванных обструкцией мочевыводящих путей. Для обеспечения естественного пассажа мочи при обтурации камнем мочеточника выполняют уретеролитотомию, уретеролитоэкстракцию, контактную и дистанционную уретеролитотрипсию. При невозможности восстановления ренальной паренхимы у пациентов, страдающих хроническими нефрологическими заболеваниями, единственным радикальным методом лечения является трансплантация почки.
Прогноз и профилактика
Исход заболевания зависит от степени нарушения функции почек и наличия сопутствующих патологий. Прогноз при острой уремии относительно благоприятный, если скорость клубочковой фильтрации превышает 30 мл/мин. Благодаря использованию ЗПТ у 65-95% таких пациентов удается достичь положительного терапевтического результата. В хронических случаях больным требуется пожизненное проведение диализа либо трансплантация почки. Специфической профилактики не существует. Для предупреждения развития уремии необходима своевременная диагностика и комплексная терапия состояний, которые могут вызвать необратимое ухудшение выделительной функции почек.
Источник
