Судорожный синдром у детей при нейротоксикозе


Нейротоксикоз у детей – это патологическое состояние, которое возникает у ребенка раннего возраста при генерализации вирусных и/или бактериальных заболеваний и преимущественно проявляется нарушениями функций ЦНС. Клинически данное состояние характеризуется нарушением сознания ребенка, повышением температуры, гипертонусом мышц, увеличением ЧСС и ЧД. Диагностика нейротоксикоза у детей подразумевает сопоставление клинической картины, клинических анализов и результатов исследования ликвора. Лечение включает в себя этиотропные препараты, дезинтоксикацию и симптоматическую терапию, зависящую от клиники.
Общие сведения
Нейротоксикоз у детей (токсическая энцефалопатия, инфекционный токсикоз у детей) являет собой системную реакцию организма на инфекцию, при которой неврологические нарушения становятся ведущим фактором, а нарушения периферической гемодинамики отходят на второй план. Термин «нейротоксикоз» ввел Дж. Левеск в 1955 году, обратив внимание на форму токсикоза, которая не сопровождалась сильной дегидратацией. Как правило, встречается нейротоксикоз в педиатрии, у детей до 3-х лет и у тех, кто имеет неблагоприятный преморбидный фон – родовую травму новорожденных, интранатальную асфиксию, аномалии развития ЦНС или частые ОРВИ с осложненным течением, атопические заболевания, рахит и т. п. Предрасполагающую роль играют гестозы матери во время беременности. Риск развития нейротоксикоза увеличивается при комбинировании нескольких заболеваний, например – кишечной и респираторной вирусной инфекции.
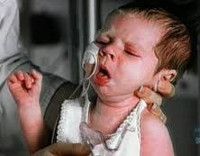
Нейротоксикоз у детей
Причины нейротоксикоза у детей
Нейротоксикоз у детей – это полиэтиологическое явление. Он может возникать на фоне большого количества заболеваний вирусного (ОРВИ, аденовирусная инфекция и т. д.) и бактериального (шигеллез, сальмонеллез, пищевая токсикоинфекция и др.) генеза или их сочетания. Также нейротоксикоз является первым симптом нейроинфекций (менингиты и энцефалиты).
Нейротоксикоз чаще всего развивается у детей раннего возраста благодаря их анатомо-физиологическим особенностям. Для ребенка характерен высокий уровень обмена веществ, который значительно выше такового у взрослых. Строение ЦНС и ее функционирование также отличается. У детей есть склонность к массивным воспалительным реакциям тканей головного мозга. Ткани гипоталамуса более чувствительные к гипоксии и поражаются быстрее, чем у взрослых. В возрасте до 3 лет ГЭБ функционально незрелый, из-за чего он пропускает токсины через себя. Это проявляется повышением внутричерепного давления и отеком головного мозга.
Патогенетически нейротоксикоз у детей обусловлен нарушением микроциркуляторного русла центральной и автономной нервной системы. Экзотоксины, которые выделяют бактерии в процессе жизнедеятельности, и эндотоксины, что попадают в кровь после их гибели, повреждают сосудистую стенку, повышают ее проницаемость для патогенных агентов и провоцируют гипоксию тканей. Вирусы вызывают аналогичный эффект, но другими путями. Они разрушают клетки организма, в результате чего в кровь попадают агрессивные протеолитические ферменты. Также вирусы способны самостоятельно вызывать деструкцию клеток эндотелия сосуда. Благодаря АФО ребенка такие изменения происходят диффузно по всей ЦНС. В развитии нейротоксикоза ведущую роль играет нарушение работы гипоталамуса, т. к. он является высшим вегетативным центром человека и отвечает за терморегуляцию, контролирует работу всех систем и эндокринных желез.
Классификация нейротоксикоза у детей
Различают 3 степени тяжести нейротоксикоза у детей:
- I (легкая) степень – беспокойство; незначительное повышение ЧД, умеренная тахикардия; срыгивание, кратковременные судороги, небольшое выбухание и/или пульсация большого родничка.
- II (средняя) степень – нарушение сознания; гипертермия; ЧД 60-80/мин., ЧСС 200/мин., колебания АД; бледность и акроцианоз. Олигоурия 1мл/кг/час и меньше. Выраженные общие мозговые и менингеальные симптомы.
- III (тяжелая) степень – сопор или кома; судороги, нарушающие работу дыхательной системы и сердца; t° тела 40°C и больше; мраморный оттенок кожи, петехии; падение АД, нитевидный пульс; анурия, рвота «кофейной гущей».
Также нейротоксикоз у детей классифицируется согласно вариантам его протекания и ведущим симптомам:
- Энцефалический вариант. Главные симптомы соответствуют клинике энцефалита – судороги, нарушение сознания, очаговые симптомы поражения ЦНС.
- Менингеальный вариант. Клиника имитирует менингит – рвота, головные боли, выбухание родничков, ригидность затылочной мускулатуры.
- Менингоэнцефалический вариант. Включает в себя симптомы предыдущих двух вариантов.
- Гипертермический вариант, или злокачественная гипертермия. Характеризуется повышением температуры тела до 39-40°С и резистентностью к антипиретикам.
- Гипервентиляционный вариант. Встречается редко. Ведущие симптомы этой формы – тахипное и «большое токсическое дыхание», которое реализуется за счет вспомогательной дыхательной мускулатуры.
Симптомы нейротоксикоза у детей
Нейротоксикоз у детей возникает остро, клинические проявления развиваются быстро. Токсическая энцефалопатия протекает в 3 периода: продромальный, развернутой клинической симптоматики и восстановления. Для каждого из них характерны свои симптомы.
Продромальный период кратковременный – от 2 до 6 часов. Проявляется ранними симптомами нарушения ЦНС: тошнота, рвота, которая не приносит облегчения и не зависит от приема пищи; нарастание головной боли; чрезмерное беспокойство и капризность; беспокойство, вздрагивания во время сна; сонливость днем; постепенное нарастание температуры тела до 38,5-39°С. Без медицинского вмешательства развивается нарушение сознания (от ступора до комы), дыхательной (повышение ЧД, одышка) и сердечно-сосудистой (повышение ЧСС) систем.
Развернутый нейротоксикоз у детей может иметь различные проявления, которые зависят от степени поражения ЦНС и микроциркуляторного русла. Длительность варьирует от 12 до 72 часов. При интенсивном нарушении кровообращения нейротоксикоз у детей развивается молниеносно. За несколько часов возникает декомпенсация работы сердечно-сосудистой системы, появляются геморрагии, развивается дыхательная недостаточность и отек легких. Нарушения ЦНС выражены в меньшей степени.
При непосредственном поражении ЦНС течение нейротоксикоза у детей более медленное. Нарастает интенсивность симптомов продромального периода, возникают судороги. Сознание ребенка нарушается постепенно – от сонливости до комы, продолжительность которой может составлять до 2 суток. Могут развиваться гипервентиляционный и гипертермический синдромы. Гипервентиляция проявляется увеличением ЧД до 80/мин. без структурных изменений легких или дыхательных путей. Гипертермия при нейротоксикозе достигает 40° С и не снимается обычными жаропонижающими средствами. Без экстренного медицинского вмешательства может возникнуть остановка сердца и дыхания, которые переходят в клиническую и биологическую смерть.
Период восстановления начинается после купирования острого состояния. Восстановление напрямую зависит от тяжести нейротоксикоза, адекватности и своевременности лечения. При легкой степени симптомы нарушения ЦНС исчезают за 12-24 часа. При тяжелых случаях неврологическая симптоматика может сохраняться на протяжении 2-4 суток.
Диагностика нейротоксикоза у детей
Диагноз «нейротоксикоз» у детей выставляется на основе характерных клинических проявлений. Основаниями для такого вывода служат различные нарушения ЦНС при инфекционных заболеваниях (в особенности при дисфункциях других органов и систем); развитие коматозного состояния и клиники отека головного мозга; гипертермия, резистентная к лечению; клинические проявления нарушения микроциркуляции; тенденция к снижению неврологических симптомов при восстановлении периферического кровообращения.
Общие клинические анализы малоинформативны. В ОАК присутствуют явления «сгущения» крови – повышение гематокрита, относительный эритроцитоз, лейкоцитоз, тромбоцитоз. Определение КОС выявляет снижение рН крови. Анализ электролитов сыворотки определяет повышение Na+; повышение или снижение К+.
При подозрении на нейротоксикоз проводится дифференциальная диагностика с нейроинфекциями, которые сопровождаются синкопе и судорожным синдромом. Для этого выполняется спинномозговая пункция с исследованием ликвора.
Лечение нейротоксикоза у детей
Терапия нейротоксикоза у детей проводится исключительно в условиях реанимационного отделения. Если ребенок на момент развития патологии находится дома – его немедленно госпитализируют. На догоспитальном этапе проводится лечение жизнеугрожающих проявлений: судорожного синдрома и гипертермии.
Этиотропное лечение включает назначение антибиотиков широкого спектра действия, после получения результатов антибиотикограммы – противомикробных препаратов, к которым чувствительна высеянная микрофлора. Допускается использование иммуностимуляторов. При проведении дезинтоксикационной терапии используются 0,9% раствор NaCl, 5% глюкоза, раствор Рингера-лактат. Важно соблюдать небольшой объем и низкую скорость введения растворов, т. к. инфузионная терапия может спровоцировать отек головного мозга.
Симптоматическая терапия направлена на конкретный синдром. Лечение гипертермического синдрома зависит от формы лихорадки. При «розовой» применяют физическое охлаждение, жаропонижающие внутрь (парацетамол, ибупрофен). При «бледной» — спазмолитические средства в/в («литическая смесь», дротаверин или папаверин). Судорожный синдром снимается в/м или в/в введением противосудорожных средств (диазепам), при их неэффективности применяют барбитураты (фенобарбитал). При гипервентиляционном синдроме используется кислородно-воздушная смесь с 40-60% концентрацией кислорода, при необходимости – ИВЛ. Вводятся антиагреганты (пентоксифиллин, дипиридамол). Отек головного мозга требует назначения глюкокортикостероидов (преднизолон, дексаметазон) и диуретиков (фуросемид, маннитол).
Прогноз
Прогноз при нейротокискозе зависит от степени тяжести и своевременности лечения. I и II степени при адекватном лечении имеют благоприятный прогноз. При тяжелой (III) степени прогноз для жизни при полноценной терапии благоприятный, для здоровья – сомнительный. При несвоевременном оказании квалифицированной помощи при I-II степени прогноз сомнительный, III степени – неблагоприятный. Без соответствующего лечения – неблагоприятный прогноз нейротоксикоза любой степени тяжести.
Профилактика
Профилактика нейротоксикоза у детей заключается в полноценном лечении основного заболевания по рекомендациям педиатра, соблюдении рациональной диеты и укреплении иммунитета. Лечение инфекционных заболеваний у детей с наличием неврологических нарушений в анамнезе должно проводиться под строгим наблюдением в условиях стационара.
Источник
Нейротоксикоз — токсическая энцефалопатия, при которой доминируют неврологические расстройства на фоне прогрессирующей недостаточности периферической гемодинамики.[1]
Наиболее типичный вариант течения периода генерализованной реакции. Чаще всего он возникает при сочетанных респираторно-вирусных инфекциях (грипп, аденовирусная, парагриппозная инфекция) и особенно тяжело протекает у детей до 3 лет. Большое влияние на тяжесть течения оказывает преморбидное[2] состояние больного. В анамнезе отмечаются различные неблагоприятные моменты — перенесённая асфиксия в родах, врождённые дефекты ЦНС, родовая травма, хронические интоксикации. Предрасполагают к возникновению токсикоза также и предшествующая вакцинация или заболевания, перенесённые ребёнком в течение последних 2-3 недель.[1]
Симптомы[править | править код]
В течение токсикоза выделяют: продромальный период, период разгара и период обратного развития. Разгар токсикоза по тяжести рассматривают с учётом глубины неврологических расстройств и степени недостаточности периферической гемодинамики.
Продромальный период — короткий, чаще на фоне ОРВИ или другого заболевания проявляются предшественники нейротоксического синдрома: рвота, иногда повторная, не связанная с приемом пищи и не облегчающая состояния больного. Усиливается головная боль, ребёнок становится возбуждённым, капризным, ночью сон его беспокоен, сопровождается вздрагиваниями, днём наблюдается сонливость. Постепенно температура достигает 39°С и выше. Если в этот период больному не оказана помощь, может развиться тяжёлый нейротоксикоз с различной степени расстройством сознания — от сомнолентности до комы. Нарастают сердечно-сосудистые, дыхательные и другие расстройства.[3]
Разгар токсикоза чрезвычайно многолик по своей клинической картине. Создаётся впечатление, что у каждого больного эта разновидность токсикоза протекает индивидуально. Однако при анализе конкретных вариантов удается выделить типичные поражения, встречающиеся у больных. Это прежде всего неврологические расстройства, недостаточность периферического кровотока, нарушение терморегуляции. Нередко они сочетаются с дыхательной недостаточностью, признаками поражения почек, желудочно-кишечного тракта. Характер этой патологии, степень её тяжести варьируют в значительных пределах и сочетаниях, что обусловливает полиморфизм клинической картины.
Течение нейротоксикоза зависит от соотношения между неврологическими и циркуляторными расстройствами. Если доминирует недостаточность периферического кровотока, то нейротоксикоз протекает быстро и нередко злокачественно. Стойкий спазм периферических сосудов и нарушение реологических свойств крови в течение нескольких часов приводят к декомпенсации кровообращения, появлению геморрагического синдрома, нарастанию дыхательной недостаточности по шунто-диффузионному типу, отеку легких. Неврологические изменения в этих случаях быстро ликвидируются, если удается нормализовать кровообращение. Если доминируют неврологические нарушения, то нейротоксикоз имеет не столь бурное течение. Ухудшение неврологического статуса нарастает постепенно — от сомнолентности до комы, которая может сохраняться в течение нескольких суток. В последующем могут длительно оставаться незначительные неврологические изменения. Это состояние требует дифференциальной диагностики с нейроинфекциями.
Более лёгкими вариантами нейротоксикоза являются так называемые гипертермический и гипервентиляционный синдромы, которые чаще всего свидетельствуют о поражении центров дыхания и терморегуляции.
Гипертермия у некоторых больных является ведущим синдромом, изменения ЦНС ограничиваются ирритативной фазой с централизацией кровообращения (расстройство кровообращения I степени тяжести). В этих случаях гипертермия легко поддается жаропонижающей терапии. По-видимому, такая клиническая картина может соответствовать началу любого инфекционного заболевания. Злокачественная гипертермия (39,5- 40 °С), не поддающаяся жаропонижающей терапии, указывает на набухание или отёк мозга. Больной обычно в коме, наблюдается децеребрационная ригидность, расстройства кровообращения II—III степени. Такую гипертермию скорее следует отнести к токсической гипоксической энцефалопатии.
Гипервентиляционный синдром редко является превалирующим в клинической картине, чаще он сочетается с другими, более тяжелыми нарушениями. При отсутствии физикальных изменений в лёгких наблюдаются тахипноэ и «большое токсическое дыхание» с участием вспомогательной мускулатуры.
По нашему мнению, не логично выделять как гипертермический, так и гипервентиляционный варианты токсикоза. Их следует считать синдромами, так как они не являются ведущими, чаще наблюдаются в сочетании с другими, ещё более грозными синдромами (мозговом, сердечно-сосудистым, почечным, печеночным и др.).
Характерных для данного варианта токсикоза лабораторных проявлений нет. Результаты обследования соответствуют различным степеням нарушения периферического кровотока и выявляют прогрессирующий метаболический ацидоз и различные стадии ДВС. На начальных этапах нередко имеется гипернатриемия, генез которой сложен. В её происхождении имеет значение как вододефицитное обезвоживание, так и выраженный гиперальдостеронизм. На этом фоне очень быстро патологическое значение приобретает дизгидрия. Синдром перераспределения воды и электролитов сопровождается интерстициальным отеком и по мере прогрессирования токсикоза — внутриклеточным отеком. В происхождении последнего основную роль играют клеточный энергодефицит и трансминерализацня. Трансминерализация лабораторно проявляется гипонатриемией. Уровень калия плазмы зависит от функционального состояния почек и наличия в терапии диуретиков и кортикостероидов. При трансминерализации, особенно на фоне нарушения калийурической функции почек, выражена гиперкалиемия. При других условиях чаще возникает гипокалиемия. Помимо недостаточности функции почек для характера метаболических расстройств имеют значение степень и вид дыхательной недостаточности.
Диагностика[править | править код]
Диагноз нейротоксикоза различной этиологии ставят прежде всего по совокупности клинических данных. Он должен основываться на наличии выраженные неврологических расстройств, присутствии признаков недостаточности периферического кровотока в сочетании с клиническими проявлениями полисистемного поражения. Так как при токсической энцефалопатии преобладает различная степень поражения ЦНС, то дифференциальный диагноз необходимо проводить с инфекционными заболеваниями, сопровождающимися комой и судорогами. Помимо характера и глубины поражения, при оценке комы на фоне нейроинфекции для дифференциального диагноза решающее значение приобретают результаты люмбальной пункции.[3]
Опорными пунктами для постановки диагноза нейротоксикоза являются:
1. Различная степень неврологических расстройств при острых инфекционных заболеваниях в сочетании с признаками полисистемного поражения (легкие, печень, почки, миокард).
2. При появлении комы наличие клинико-лабораторных признаков отека-набухания мозга.
3. Обязательное присутствие клинико-лабораторных признаков недостаточности периферического кровообращения.
4. Стойкая, плохо поддающаяся терапии гипертермия.
5. Обратное развитие неврологической симптоматики тесно связано с ликвидацией расстройств периферической гемодинамики.
Лечение[править | править код]
В терапии нейротоксикоза следует выделить 3 этапа.
В задачи первого реанимационного этапа входят мероприятия по нормализации периферического кровотока, профилактике и лечению отека мозга, борьбе с гипертермией и судорогами, терапия синдромов, угрожающих жизни больного. В зависимости от тяжести тканевой гипоксии этот комплекс дополняют стабилизация клеточных мембран и ликвидация клеточного энергодефицита.
Конкретная реализация этой программы зависит от степени тяжести токсикоза.
При токсикозе III степени первичные реанимационные мероприятия начинают с венесекции и фармакологической стабилизации центральной гемодинамики. Оптимальным в этих случаях является раннее назначение предшественников адреналина или симпатомиметиков. Препараты вводят после внутривенного применения преднизолона. Эти мероприятия нередко приходится проводить на фоне геморрагического синдрома, обусловленного ДВС. Диагностику ДВС и выбор необходимого лечения осуществляют после проведения «однопробирочного» теста. При наличии тяжёлых дыхательных расстройств, неэффективности оксигенотерапии и трудности стабилизации центральной гемодинамики больного переводят на искусственную вентиляцию легких. Интубацию трахеи, перевод на искусственную вентиляцию лёгких желательно осуществлять без применения миорелаксантов. Эти манипуляции проводят после введения седуксена или оксибутирата натрия. Последующая инфузионная терапия по своему объёму не должна превышать объём почасового диуреза, для его контроля необходима катетеризация мочевого пузыря. При отсутствии диуреза объём назначаемой внутривенно жидкости должен быть равен 1,5 мл/кг-ч массы тела больного. В общем количестве вводимой жидкости обязательно следует учитывать объём растворов, назначаемых с сосудосуживающими препаратами. Основной инфузионной средой является 10 % раствор глюкозы с панангином (1 мл/кг на весь период первичных реанимационных мероприятий).
При токсикозе II степени также начинают с получения доступа к венозному руслу. Последовательность мероприятий определяют в зависимости от выраженности судорожного синдрома, стойкости и длительности гипертермии, степени расстройств периферического кровотока. Эффективным первичным мероприятием является нейровегетативная блокада, которая может быть получена использованием смеси дроперидола или аминазина в сочетании с пипольфеном и новокаином. Наряду с этим для окончательной ликвидации судорог прибегают к дополнительному введению 6 % раствора сульфата магния, оксибутирата натрия или седуксена. При сохраняющейся гипертермии назначают антипиретические средства (анальгин, амидопирин) и используют методы физического охлаждения.
Ключом к патогенетической терапии токсикоза II степени тяжести являются первичные мероприятия по ликвидации централизации кровообращения. Отсутствие эффекта от нейроплегических препаратов, наличие пастозности подкожной клетчатки, продолжительность гипертермии более 6-8 ч косвенно свидетельствуют о ведущей роли в генезе сосудистых расстройств интерстициального отека. Последний в виде муфты охватывает сосуды, вызывая вторичный «спазм». В этих случаях эффективной будет та программа, которая предусматривает ограничение объёма инфузионной терапии, назначение диуретиков, кортикостероидов, антипротеазных препаратов и проведение мероприятий по улучшению реологии крови. Наряду с перечисленным комплексом проводят лечение, направленное на стабилизацию цитомембран (витамин Е, эссенциале).
Интенсивной терапии требует токсикоз I степени, и токсикозы II и III степени — после того, как для них решены задачи реанимационного этапа. У больных последней группы при отсутствии положительной динамики в неврологических расстройствах интенсивную терапию начинают с лечебно-диагностической люмбальной пункции.
При токсикозе I степени интенсивную терапию следует начинать с введения сосудорасширяющих препаратов в сочетании с нейролептиками. Больному назначают каждые 6-8 ч папаверин с дибазолом либо эуфиллин с никотиновой кислотой в комплексе с пипольфеном. При стойкой гипертермии и отсутствии эффекта от перечисленных препаратов добавляют антипиретические средства. Периферический сосудистый спазм в этих случаях снимают одно- или двукратным назначением ганглиолитиков.
Количество жидкости, назначаемое больному внутривенно и для питья, не должно превышать возрастных суточных потребностей в воде. Внутривенно назначают не более 1/2-2/3 этого количества. По составу инфузиониая терапия включает реополиглюкин и гемодез (по 10 мл/кг), а всю оставшуюся часть назначают в виде 10 % раствора глюкозы с препаратами калия, кальция, инсулина. Этих электролитов, так же как и витаминов, в глюкозу добавляют соответственно возрастным суточным потребностям. Включение гидрокарбоната натрия в состав инфузионной терапии необходимо при отсутствии эффекта от сосудорасширяющих препаратов и при наличии гипервентиляционного синдрома.
Все внутривенные инфузии проводят под контролем динамики массы тела и диуреза. В период инфузионной терапии ребёнок с нейротоксикозом не должен увеличивать массу тела, а диурез у него не должен быть менее возрастного суточного, в противном случае показано регулярное назначение 2-3 раза в сутки лазикса. Это необходимый компонент в борьбе с отеком мозга.
Профилактика ДВС на этом этапе лечения зависит от степени токсикоза. При I степени токсикоза, помимо назначения реополиглюкина, применяют дезагреганты.
На втором этапе терапии токсикоза II—III степени продолжают применять гепарин с учётом индивидуальной чувствительности.
В интенсивной терапии нейротоксикоза принципиальное значение имеет адекватная оксигенация. На этом этапе оптимально применение методов самостоятельного дыхания под постоянным положительным давлением, не выше 0,294-0,392 кПа. Такой выбор давления позволяет предупредить венозную и ликворную гипертензию.
Всем больным на этом этапе назначают преднизолон и препараты, стабилизирующие клеточные мембраны. Антибиотикотерапия проводится по общим принципам, а при продолжающемся лечении токсикоза II—III степени один из препаратов обязательно вводят внутривенно.
Восстановительный этап лечения совпадает с полной нормализацией периферического кровообращения. Последующая терапия зависит от того, какой орган-мишень пострадал больше всего в период, предшествующий генерализации. Лечение должно быть направлено на восстановление функции этого пострадавшего органа. Больному прекращают постепенно инфузионную терапию. Отменяют кортикостероиды и антипротеазные препараты, сохраняют антибактериальную и стимулирующую терапию.
Примечания[править | править код]
- ↑ 1 2 Пяткин К.Д. Микробиология. — М. Мир Б. г., 1990.
- ↑ Совокупность факторов (врождённых и приобретённых, биологических и психологических), принимающих участие в возникновении, формировании и течении заболевания (психического, соматического)
- ↑ 1 2 Поздеев О.К. Медицинская микробиология. — М. Геотар-мед, 2001.
Источник
