Синдромом хатчинсона гилфорда детская прогерия что это

Синдром преждевременного старения – редчайшая аномалия генетической природы. Частота встречаемости патологии – 1:4000000. В мире зарегистрировано только около 80 изученных случаев, что усложняет поиск эффективных методов лечения. Синдром прогерия (от древнегреческих слов «сверх» и «старик») имеет неустановленное происхождение. Морфологические формы болезни – детская и взрослая, характеризуются рядом отличий.
Причины аномалии
Синдром быстрого старения имеет генетическое происхождение, но механизм развития патологии у взрослых и детей различный.
Факторы развития болезни в детском возрасте
Подобная аномалия, развивающаяся в раннем периоде (по достижении возраста одного-двух лет) имеет название синдром Хатчинсона-Гилфорда по имени врачей, впервые описавших независимо друг от друга с интервалом в 10 лет детское заболевание. Труды специалистов датируются девяностыми годами девятнадцатого века. За более чем 100 лет медики не сделали прорыва в изучении и лечении патологии.
Причина болезни у детей – стойкое изменение генома, затрагивающее носитель наследственности, кодирующий ламин А. Фибриллярный белок – структурная единица, выстилающая слой оболочки ядра клетки. Вследствие мутации клетки теряют способность к нормальному делению, что вызывает ряд нарушений и приводит к преждевременному износу органов.
Предполагается возможность аутосомно-рецессивного наследования. Теория такой передачи основана на случаях развития аномалии у детей, рожденных от родителей, состоящих в близкородственных связях.

Причины развития аномалии у взрослых
Если аутосомно-рецессивная передача признака при болезни у детей только предполагается, патология взрослых, доказано, имеет именно этот тип наследования.
Условия развития болезни – сбой обменных процессов, происходящих в соединительной ткани. Клетки этой ткани активно делятся, а поскольку они продуцируют предшественники коллагена, этот фибриллярный белок разрастается. Продуцирование мукополисахаридов снижается. Такие изменения приводят к нарушению клеточного обмена, что провоцирует патологические процессы.
Аномалия у взрослых вызвана стойким изменением в гене WRN, участвующем в механизмах восстановления, исправления химических повреждений и разрывов в молекулах дезоксирибонуклеиновой кислоты, выполняющем функцию расщепления двойной спирали ДНК на одноцепочные молекулы.
Существует предположение о том, что к возникновению дефекта гена может привести радиационное воздействие на организм матери, однако такая гипотеза не имеет чёткого обоснования, предполагается также случайность мутации.
К возможным факторам развития относят экологическую обстановку, образ жизни.
Симптоматика
Как разнятся причины и факторы развития болезни у взрослых и детей, так и во многом различаются проявления синдрома у разных возрастных категорий.
У детей
Синдром Гетчинсона (Хатчинсона)-Гилфорда может проявиться в возрасте до года, но чаще обнаруживается у детей от одного до трёх лет.
Внешние проявления аномалии таковы:
- Непропорциональные размеры частей черепа. Лицевая часть значительно уменьшена, мозговой отдел патологически увеличен.
- Деформация зубов в связи с их ростом в 2 ряда: молочные, в соответствии с возрастом, ещё не выпали, постоянные при синдроме старения у детей появляются раньше времени.
- Недоразвитая нижняя челюсть.
- Низкий рост, карликовость.
- Кожа тонкая, сухая, морщинистая, особенно это касается лица, шеи и конечностей.
- Выступающие сквозь тонкую прозрачную кожу вены.
- Ранняя потеря ресниц, бровей, облысение волосистой части головы, седина.
- Характерные черты лица: заострённый клювоподобный нос, выступающие лобные бугры.
Кроме внешних признаков, болезнь проявляется поражением органов, их ранним износом, общим истощением организма. Внутренние проявления, выражающиеся в недомоганиях и определяемые путём дополнительных обследований:
- ранний атеросклероз;
- нарушения мозгового кровообращения;
- инсульты;
- инфаркты;
- разрастание миокарда с появлением рубцовых изменений;
- утрата костной тканью минералов и солей, как следствие,частые переломы костей;
- контрактура суставов – сложность в сгибании и разгибании;
- остеопорозы;
- атрофия мышц;
- снижение остроты зрения, вызываемое катарактой;
- недоразвитие половых органов;
- отклонения в липидном обмене.
Организм ребёнка претерпевает изменения, характерные для людей пожилого возраста, при этом в интеллектуальном и психоэмоциональном развитии такие дети не уступают здоровым сверстникам.
Продолжительность жизни обычно не превышает 14 лет, однако известен случай, когда пациент с диагностированным синдромом дожил до 27. Летальные исходы наступают чаще всего на фоне инфарктов, инсультов.
У взрослых
Синдром раннего старения у взрослых носит название болезнь Вернера по имени немецкого врача, описавшего в начале двадцатого века симптомокомплекс, присущий пациентам. Первые признаки аномалии отмечаются в период полового созревания, при этом патология быстро прогрессирует. На фото, сделанных с интервалом в один год, невозможно узнать человека, и внешние изменения – лишь малая часть преждевременных преобразований.

Существенное отличие заболевания взрослых от детской прогерии – то, что болезнь затрагивает умственное развитие, интеллектуальные способности резко снижаются.
К внешним проявлениям патологии относятся:
- Снижение веса, замедление (остановка) процессов роста.
- Поседение волос.
- Выпадение ресниц, бровей, предшествующее облысению головы. Истончение волос.
- Бледность и истончение кожных покровов.
- Сужение ротового отверстия.
- Смещение вперёд глазного яблока.
- Появление морщин, пигментных пятен на кожных покровах.
- Просвечивание сосудов сквозь кожу.
- Атрофия подкожной клетчатки приводит к утончению верхних и нижних конечностей.
- Высокий и хриплый голос.
- Деформация ногтевой пластины («часовые стёкла»).
К внутренним признакам болезни относят разнообразные поражения органов, приводящие к множественным дисфункциям. Наиболее выражены следующие симптомы синдрома:
- Истончение подкожно-жировой клетчатки, в результате чего она замещается волокнами соединительной ткани.
- Ухудшение зрения, обусловленное помутнением хрусталика.
- Потеря слуха – от частичной до полной.
- Снижение когнитивных способностей: проблемы с концентрацией внимания, памятью.
- Утолщение миокарда.
- Атеросклероз сосудов.
- Снижение иммунитета вследствие недостаточного продуцирования антител.
- Нарушения в работе репродуктивной системы: ранний климакс у женщин, гипогонадизм у мужчин, приводящий к половой дисфункции.
- Тугоподвижность суставов, остеопорозы, остеоартрозы, гнойно-некротические процессы в костях и прилежащих мягких тканях.
- Нарушения в работе сальных и потовых желез.
- Сахарный диабет.
- Злокачественные новообразования костной, мышечной, хрящевой, жировой тканей, кожных покровов, аденокарциномы.
Взрослые пациенты с диагностированным синдромом при своевременном лечении могут дожить до сорока лет, но редко переступают этот возрастной порог.
Необходимая диагностика
Поскольку синдром характеризуется чётко выраженной внешней картиной, диагностика предполагает проведение осмотра и сбор данных анамнеза пациента и его родственников, чего бывает достаточно для постановки диагноза.
Для определения сопутствующих заболеваний, обусловленных развитием основной патологии, используются следующие методы:
- Анализы крови – могут показать повышенное содержание холестерина при атеросклерозе, высокую концентрацию сахара при диабете.
- Ультразвуковое исследование показывает аномалии сердечно-сосудистой системы.
- Рентгенологическое исследование визуализирует проблемы костной ткани.
- Компьютерная и магнитно-резонансная томография показывают нарушения мозгового кровообращения, патологии костной системы, визуализируют опухоли.
Современные методы лечения
До недавнего времени считалось, что прогерия неизлечима. Проводилась симптоматическая терапия, призванная улучшить качество жизни человека и несколько продлить продолжительность жизни.
Недавние исследования, проведённые в США, и опробование нового препарата дают возможность предполагать, что учёные всё же изобретут средства, которые позволят вылечить заболевание.
В детскую больницу Бостона были приглашены пациенты юного возраста с диагностированной аномалией. Под постоянным контролем медиков и регулярным мониторингом состояния всех систем организма дети принимали новый препарат на основе ингибитора фарнезилтрансферазы.
Результаты обследований показали стабилизацию состояния сердечно-сосудистой и костной систем, улучшение самочувствия пациентов. Ожидается, что из категории смертельных заболевание перейдёт в разряд трудноизлечимых. В данный момент клинические испытания продолжаются, учёные пытаются усовершенствовать лекарственное средство.
Пока такого препарата, который бы мог эффективно справиться с патологией, не изобрели. Пациенты с диагностированным синдромом рассчитывают на замедленное старение, что позволит не только улучшить качество жизни, но и увеличить ее продолжительность. Обеспечить это врачи могут посредством симптоматического лечения, основными направлениями которого являются:
- Терапия атеросклеротических изменений – используются статины.
- Профилактика инфарктов и инсультов – применяется ацетилсалициловая кислота.
- Устранение сахарного диабета – проводится посредством гипогликемических средств.
- Лечение новообразований – хирургические методы, сопутствующая терапия.
- Коррекция отставания в физическом развитии – гормональные препараты.
- Заживление трофических язв – производят, используя средства, заживляющие и стимулирующие кровообращение.
Кроме медикаментозной терапии, пациентам назначают массаж, бальнеотерапию, рефлексотерапию, различные физиопроцедуры для активизации обменных процессов, нормализации кровообращения, повышения мышечного тонуса и так далее.
Синдром преждевременного старения на сегодняшний день поддаётся лишь симптоматической терапии, в то время как специфического лечения для него не существует.
Загрузка…
Источник
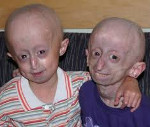
Прогерия – редкое генетическое заболевание, характеризующееся преждевременным старением организма, соответствующими изменениями внутренних органов. Проявляется гиперпигментацией, истончением и утратой эластичности кожи, поседением и выпадением волос, увеличением размеров черепа, уменьшением его лицевой части, экзофтальмом, развитием атеросклероза сосудов, инфаркта и фиброза миокарда, остеопороза, сахарного диабета, формированием злокачественных опухолей. Диагностика основана на сборе клинических данных, лабораторном исследовании ДНК. Лечение направлено на устранение симптомов заболевания: профилактику и терапию атеросклероза, инфаркта миокарда, диабета, остеопороза, рака.
Общие сведения
Термин «прогерия» в переводе с древнегреческого языка означает «преждевременное старение». Детская форма прогерии называется синдромом Хатчинсона-Гилфорда согласно фамилиям исследователей, которые впервые независимо друг от друга описали данную патологию: британский врач Дж. Хатчинсон – в 1889 году, его соотечественник Х. Гилфорд – в 1897 году. Взрослая форма носит название «синдром Вернера», так как в 1904 году немецкий врач О. Вернер первым официально наблюдал симптомы старения у подростков 14-19 лет. Оба варианта болезни являются крайне редкими. Распространенность детской прогерии составляет 1 случай на 7-8 млн. человек, с момента начала исследований патологии выявлено около 150 больных детей. Взрослая прогерия встречается чаще, средние эпидемиологические показатели – 1 больной на 100 тыс. населения.

Прогерия
Причины прогерии
В основе заболевания лежит генетическая мутация. Причиной детского типа прогерии является дефект гена LMNA, который кодирует особый белок ламин A, выстраивающий оболочку ядра клетки. Как правило, мутация происходит спорадически – во время созревания половых клеток у родителей или при зачатии. Однако исследователи выявили несколько случаев патологии у родных братьев и сестер, часть из которых входила в семьи с близкородственными браками. Это свидетельствует о возможности наследования мутации по аутосомно-рецессивному типу (родители являются носителями дефектного гена, но не болеют и способны к деторождению).
Прогерия взрослых – наследственное заболевание. Оно развивается при наличии дефекта в гене RECQL2, который ответственен за производство белка WRN, поддерживающего стабильность генома, целостность и структуру ДНК. Передача мутации происходит аутосомно-рецессивным способом, болезнь проявляется у людей, получивших два дефектных гена в одной аллели (от матери и от отца).
Патогенез
При детском варианте прогерии генетический дефект приводит к нарушению синтеза структурно правильного белка ламина А, образующего внутренний каркас ядерной оболочки. В результате мутации налаживается производство укороченного белка-предшественника преламина А, а строение созревшего конечного белка отличается от нормального. Молекулы белка встраиваются в ядерную мембрану, изменяют ее форму и повышают хрупкость. Ядро не может сохранять свою целостность, клетка гибнет раньше времени.
При болезни Вернера возникает недостаточность WRN-белка, определяется генетически детерминированная нестабильность хромосом. Их структура очень часто изменяется спонтанно или под воздействием некоторых факторов. В итоге ухудшается способность клеток к делению, пролиферативный потенциал становится в 3-5 раз меньше, чем должен быть в норме. В 10 раз увеличивается частота спонтанных мутаций, аномально укорачиваются теломеры – концевые участки хромосом, защищающие гены от повреждений.
Симптомы прогерии
Прогерия Хатчинсона дебютирует после периода нормального развития в возрасте от 6 месяцев до 2 лет. Изменяется внешность детей: замедляется рост, увеличиваются размеры черепа, но лицевая часть остается маленькой, нижняя челюсть – недоразвитой. Формируется клювовидный тонкий нос и экзофтальм (выпячивание глаз). Тотально выпадают волосы – на голове и теле, ресницы и брови. При алопеции разрушаются волосяные фолликулы, поэтому дальнейший рост волос становится невозможным. На волосистой части головы выбухают вены. Дерма и подкожная клетчатка подвергаются атрофическим изменениям: кожа истончается, иссушается, покрывается морщинами. Развивается липодистрофия – заметное снижение количества подкожного жира. Относительно сохранным он остается на щеках и лобке.
На туловище образуются склеродермоподобные очаги – уплотнения в нижней части живота, на ягодицах и бедрах. На открытых участках кожи появляются пигментные пятна. Ногти недоразвитые, ломкие, утолщенные, округло выпуклые – имеют форму «часовых стекол». К 2 годам развивается фиброз органов и околосуставных тканей. Пассивные движения в локтевых и коленных суставах ограничены (контрактуры), формируется характерное положение костей ног – «поза всадника». Скелет подвергается гипоплазии, дисплазии и дегенеративным изменениям. Молочные и постоянные зубы прорезываются с опозданием, частично отсутствуют, скученные, искривленные, подвержены кариесу. К 5-6 годам диагностируется атеросклероз сосудов, сердечные шумы, гипертрофия левого желудочка, помутнение хрусталика, резистентность к инсулину. Половые органы остаются недоразвитыми. Уровень умственного развития обычно выше, чем у сверстников.
Клинические проявления синдрома Вернера обнаруживаются с 14 до 18 лет. Подросток начинает отставать в росте, его волосы седеют и выпадают. К 20 годам пациенты лысеют. Кожа лица и конечностей бледнеет, истончается, натягивается. Под ней видна сеть кровеносных сосудов. Мышечная и жировая ткани атрофируются, руки и ноги становятся непропорционально тонкими, кожа над суставными выступами изъязвляется. К 30 годам появляется катаракта, голос слабеет и хрипнет, на ногах образуются язвы, на подошвах – мозоли, сосудистые звездочки, кератоз. Внешний вид пациентов специфичен: низкий рост, лунообразное лицо, выступающий подбородок, суженное ротовое отверстие, псевдоэкзофтальм.
Сальные и потовые железы атрофируются. Костно-суставные изменения включают метастатическую кальцификацию, явления генерализованного остеопороза, эрозивных остеоартритов, ограниченную подвижность и деформацию пальцев рук, сгибательные контрактуры, боли в конечностях, артрит и остеомиелит. Отмечаются атеросклеротические изменения сосудов, медленно прогрессирует катаракта, снижаются интеллектуальные способности. После 30 лет проявляются эндокринные заболевания – сахарный диабет, гипогонадизм, тиреопатии. У 5-10% больных обнаруживаются злокачественные опухоли различных органов, костей и кожи. Причиной смерти становится онкопатология или тяжелое сердечно-сосудистое заболевание.
Диагностика
Диагноз прогерии устанавливается на основании клинико-анамнестических данных. В зависимости от имеющейся симптоматики в диагностике могут принимать участие эндокринологи, неврологи, дерматологи, терапевты, врачи-генетики. Детскую и взрослую прогерию необходимо дифференцировать с системной склеродермией, пойкилодермией, синдромом Ротмунда-Томсона, синдромом Видемана-Раутенштрауха. К основным методам обследования больных относятся:
- Опрос. В ходе беседы врачи уточняют время появления симптомов, их выраженность, степень физической и социальной дезадаптации, наличие периода обычного развития (6-24 месяца при детской форме, 14-20 лет – при взрослой). Собирают данные семейного и генеалогического анамнеза, выявляя генетическую патологию или ее отсутствие в роду.
- Осмотр. Специалисты оценивают неврологический статус, пассивную и активную подвижность суставов, костные деформации, состояние кожи и подкожной клетчатки, сохранность зрения, интеллектуальных функций. Пациенты могут быть направлены на инструментальные исследования: рентгенографию костей, УЗИ и МР-томографии органов, ЭКГ, офтальмоскопию.
- Биогенетическое исследование. Выполняется анализ генетического материала методом секвенирования ДНК. Исследуются участки генов, дефекты в которых приводят к развитию прогерии. У пациентов с детской и взрослой формой болезни обнаруживаются мутации в гомозиготном и компаунд-гетерозиготном состоянии.
Лечение прогерии
Специфические методы терапии прогерии не разработаны. Медицинская помощь пациентам заключается в облегчении симптомов болезни. Проводится лечение атеросклероза, остеопороза, остеомиелита, катаракты, диабета, патологий сердца и онкологических заболеваний. Известен случай, когда состояние больного заметно улучшилось на несколько лет после операции трансплантации сердца.
Научные исследования ведутся в области генной инженерии – совершаются попытки выделить мутационный ген из ДНК и заменить его здоровым. Параллельно разрабатывается метод этиотропной терапии. Ученые из Швеции нашли способ нейтрализации дефектных молекул ламина A, которые проникают в мембрану клеточных ядер и способствуют гибели клетки. Положительные результаты получены на экспериментах с мышечной тканью крыс, на людях препарат пока не опробован. В США с 2012 года ведется изучение эффективности применения ингибитора фарнезилтрансферазы (лекарственного средства, разработанного для лечения рака). После терапии дети из экспериментальной группы чувствовали себя лучше, повысилась жесткость и эластичность артерий, плотность костей, снизились случаи транзиторных ишемических атак, сердечных патологий, утраты зрения и слуха. Продолжительность жизни увеличилась на 1,6-6 лет.
Прогноз и профилактика
В среднем больные детской прогерией доживают до 13 лет, зарегистрированы случаи смерти в 7 и 27 лет. Продолжительность жизни при взрослом типе заболевания составляет 30-40 лет. Причиной летального исхода становятся атеросклеротические осложнения и злокачественные новообразования. Профилактические меры отсутствуют. Предупредить рождение больного ребенка можно при наследственном характере болезни – при синдроме Вернера, в отдельных случаях синдрома Хатчинсона, когда патология выявлена в семье, будущие родители отнесены к группе высокого риска. Таким парам назначается медико-генетическое консультирование.
Источник
