Синдром тернера и заместительная терапия

ДАД — диастолическое артериальное давление
ЖАС — жесткость артериальной стенки
ИМТ — индекс массы тела
КМР — кардиометаболический риск
КПОК — комбинированные пероральные контрацептивы
ЛПВП — липопротеиды высокой плотности
ЛПНП — липопротеиды низкой плотности
МГТ — менопаузальная гормональная терапия
МПКТ — минеральная плотность костной ткани
ОТ — окружность талии
ПАС — прирост амплитуды сигнала
ПВ — пульсовая волна
САД — систолическое артериальное давление
ССО — сердечно-сосудистые осложнения
ССС — сердечно-сосудистая система
СФ — сдвиг фаз
СШТ — синдром Шерешевского—Тернера
ТГ — триглицериды
ФР — фактор риска
ФЭ — функция эндотелия
ХС — холестерин
AIp — индекс аугментации
AIp75 — нормализованный для пульса 75 уд/мин индекс аугментации
RI — индекс отражения
SI — индекс жесткости
Синдром Шерешевского—Тернера (СШТ) — одна из наиболее частых аномалий половых хромосом, которая встречается у 1 из 2000 новорожденных девочек [1—3]. СШТ является результатом частичной или полной моносомии по X-хромосоме. При СШТ встречаются самые разные пороки развития органов и систем, в первую очередь сердечно-сосудистой, нарушаются физиологические процессы, что приводит к уменьшению ожидаемой продолжительности жизни больных [4].
Отклонения в анатомии грудной аорты и ее ветвей, клапанные пороки выявляются у 65—70% больных с СШТ [5]. Помимо пороков развития сердечно-сосудистой системы (ССС), отмечается повышение риска развития приобретенных сердечно-сосудистой заболеваний (ССЗ), таких как артериальная гипертония (АГ), тромбоэмболические осложнения, острый инфаркт миокарда и мозговой инсульт, одной из частых причин смерти больных с СШТ является разрыв аорты [6].
Развитию тяжелых сердечно-сосудистой осложнений (ССО) способствуют типичные для СШТ нарушения метаболизма, такие как предрасположенность к сахарному диабету, ожирению, дислипидемии [7]. В связи с высокой распространенностью гипогонадизма более 90% женщин с СШТ показана так называемая менопаузальная гормональная терапия (МГТ). Стратификация риска развития ССО у больных с СШТ на современном этапе затруднена, так как очевидно, что простой перенос тактики, применяемой в общей популяции, на пациенток с СШТ некорректен. Нет также однозначного мнения относительно назначения МГТ больным гипогонадизмом. Отсутствие единой научно обоснованной позиции не позволяет унифицировать стратегию ведения больных с СШТ [8, 9]. Таким образом, оценка распространенности факторов риска (ФР) развития ССО и возможного влияния МГТ на риск развития ССО при СШТ представляется актуальной проблемой здравоохранения.
Работа проведена В ФГБУ «Эндокринологический научный центр» Минздрава России на базе отделения эндокринной гинекологии. За 2010—2012 гг. в рамках проспективного исследования обследована 41 пациентка с СШТ в возрасте от 14 до 35 лет, средний возраст составил 25,1±6,5 года. У всех больных диагноз подтвержден результатами кариотипирования.
Проведено открытое проспективное обсервационное сравнительное исследование с оценкой влияния МГТ или комбинированных пероральных контрацептивов (КПОК) на частоту возникновения ФР развития ССО у больных с СШТ. Критериями включения в исследования служили возраст от 14 до 35 лет, установленный диагноз СШТ. Наличие другой патологии эндокринной системы не являлось фактором исключения, а рассматривалось как дополнительный параметр исследования. Критерием исключения служило хирургическое лечение по поводу коарктации аорты или другого порока сердца. Протокол клинического исследования одобрен локальным этическим комитетом ФГБУ ЭНЦ Минздрава России. Исследование проводили в соответствии с положениями, изложенными в Хельсинкской декларации Всемирной медицинской ассоциации и принципами надлежащей клинической практики (GCP).
В зависимости от статуса по проведению МГТ/ КПОК больные разделены на 4 группы: 1-я — 7 пациенток, не получающих МГТ (средний возраст 25,4±3,2 года); 2-я группа — 12 пациенток, получающих в рамках МГТ 1 мг эстрадиола (средний возраст 23,7±4,4 года); 3-я группа — 14 женщин, получающих в рамках МГТ 2 мг эстрадиола (средний возраст 26,2±5,3 года); 4-я группа — 8 пациенток, получающих КПОК (средний возраст 28,4±3,6 года).
Пациентки 2-й группы получали дидрогестерон + эстрадиол (фемостон 1/10), пациентки 3-й группы — один из двух препаратов: фемостон 2/10, либо левоноргестрел + эстрадиол, пациентки 4-й группы — этинилэстрадиол + дезогестрел.
Все пациентки проходили динамическое обследование, в ходе которого регистрировались все нежелательные явления. На рисунке представлено распределение обследованных больных по кариотипу.
 Распределения 41 больной по кариотипу.
Распределения 41 больной по кариотипу.
Кроме того, в рамках ретроспективной части исследования проведен анализ амбулаторных карт 100 больных с СШТ, которым проведены обследование и лечение в отделении эндокринной гинекологии ЭНЦ МЗ РФ с 2000 по 2010 г. Отбирали карты больных, у которых была доступна информация, соответствующая следующим минимальным требованиям: кариотип, результаты эхокардиографии (ЭхоКГ), проведение и вид КПОК/МГТ. Возраст больных с СШТ ретроспективной когорты составил от 15 до 46 лет (32±8,7 года).
В лаборатории ФГБУ ЭНЦ проводили гормональный и биохимический анализы крови, а также оценку свертывающей системы крови. Ультразвуковое исследование органов малого таза, молочных желез и щитовидной железы выполняли на ультразвуковых аппаратах Hewlett Packard Image Point (США), Agilent Son’s 4500 (CША) с использованием линейного трансабдоминального и вагинального датчиков с частотой 3,5 МГц по общепринятой методике. Минеральную плотность костной ткани (МПКТ) определяли на денситометре фирмы «Lunar» (США) методом двухэнергетической рентгеновской абсорбциометрии. Оценивали МПКТ поясничных позвонков (совокупная МПКТ в регионе LII—LIV) и проксимальном отделе бедренной кости (в области Wards). Результаты исследования выражали в абсолютном содержании (в граммах) костной ткани и сравнивали с референсной базой данных, представленной фирмой-производителем. Полученные значения МПКТ выражали в граммах на 1 см². В целях оценки полученных показателей использовали Z-критерий и Т-критерий для данного хронологического возраста и пола. Значение Z— и Т-критерия менее 2,5 расценивали как остеопороз, а при в диапазоне от –1,0 до –2,5 — как остеопения.
Электрокардиограмму регистрировали с помощью 12-канального электрокардиографа Philips Page Writer Xli (Голандия).
Исследование структур и функции сердца, которое основано на регистрации отраженных импульсных сигналов ультразвука, генерируемых эхокардиографическим датчиком частотой 3,5 МГц, проводили на ультразвуковом аппарате Philips iE-33, дуплексное исследование сосудов шеи — на приборе LOGIQ-9. Данный метод объединяет возможности В-режима (визуальная интерпретация физического состояния сосудов и прилежащих к ним тканей) и допплероскопии (исследование качественных и количественных характеристик кровотока)*.
Статистическую обработку полученных данных проводили с использованием пакета прикладных программ Statistica 6. Качественные признаки сравнивали между собой с помощью критерия χ2 и точного критерия Фишера. Для каждого количественного признака выполняли оценку нормальности распределения с помощью критерия Шапиро—Уилка. Для изучения межгрупповых различий нормально распределенных признаков оценивали дисперсии распределений признаков в двух сравниваемых группах по критерию Левена. Непараметрические признаки описаны в виде медианы и интерквартильного размаха — Mе (25-й процентиль; 75-й процентиль). Для оценки межгрупповых различий использовали критерий U Манна—Уитни. Для анализа зависимостей между выборками найдены коэффициенты ранговой корреляции Спирмена.
Оценка параметров риска развития ССЗ и /или СД (кардиометаболического риска — КМР). При анализе распространенности ФР развития ССО у больных проспективной и ретроспективной когорт получены следующие результаты (табл. 1). Согласно приведенным данным у больных обеих когорт выявлена умеренная атерогенная дислипидемия, что проявлялось в повышении уровня общего ХС до 5,2 и 5,4 ммоль/л соответственно в проспективной и ретроспективной когортах больных.
 Таблица 1. Параметры КМР в проспективной и в ретроспективной когортах больных (n=104)* Примечание. * — при сравнении значения всех параметров между когортами p>0,05. ИМТ — индекс массы тела; ОТ — окружность талии; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; ХС — холестерин; ЛПНП — липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ТГ — триглицериды.
Таблица 1. Параметры КМР в проспективной и в ретроспективной когортах больных (n=104)* Примечание. * — при сравнении значения всех параметров между когортами p>0,05. ИМТ — индекс массы тела; ОТ — окружность талии; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; ХС — холестерин; ЛПНП — липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ТГ — триглицериды.
Для оценки влияния МГТ на параметры КМР мы сравнили их значения в группах больных в зависимости от типа получаемой МГТ. Результаты представлены в табл. 2.
 Таблица 2. Параметры КМР в группах больных проспективной когорты в зависимости от статуса МГТ (n=41) Примечание. Различия статистически значимы при сравнении с уровнем в 1-й группе (* — p<0,05; ** — p<0,01).
Таблица 2. Параметры КМР в группах больных проспективной когорты в зависимости от статуса МГТ (n=41) Примечание. Различия статистически значимы при сравнении с уровнем в 1-й группе (* — p<0,05; ** — p<0,01).
На фоне МГТ или КПОК отмечалось статистически значимое снижение ДАД. В группе больных, не получавших МГТ или КПОК, констатирована диастолическая АГ (ДАД 92±6,3 мм рт.ст.), в группе больных, получавших МГТ с дозой эстрадиола 1 мг/сут, ДАД составляло 83,6±5,1 мм рт.ст., в группе МГТ с дозой эстрадиола 2 мг/сут — 80,8±4,8 мм рт.ст., и наконец, в группе КПОК — 88,2±7,4 мм рт.ст. (p<0,05 при сравнении значений во 2-й и 3-й группах со значениями в 1-й группе), во всех этих группах ДАД оставалось в пределах нормы.
Кроме того, выявлено статистически значимое повышение уровня ЛПВП — 0,6±0,09 ммоль/л в 1-й группе против 1,5±0,2, 1,7±0,35 и 1,3±0,27 во 2, 3 и 4-й группах соответственно. Выявлена сильная положительная корреляция между дозой эстрогена в МГТ и уровнем ЛПВП (r=0,74).
Таким образом, МГТ в зависимости от дозы (по содержанию эстрадиола) повышает уровень протективных в отношении риска развития атеросклероза ЛПВП, не влияя на уровень общего ХС. МГТ и КПОК способствуют снижению уровня ДАД на 13% (p<0,01) у больных с СШТ.
Оценка состояния сосудистой стенки у больных с СШТ. Эту оценку проводили с помощью аппарата Ангиоскан. Оценивали следующие параметры контурного анализа ПВ: индекс жесткости (SI), который отражает жесткость аорты; индекс отражения (RI) — параметр, характеризующий тонус мелких резистивных артерий; индекс аугментации, служащий индикатором состояния ССС (AIp), нормализованный для пульса 75 уд/мин индекс аугментации (AIp75), в окклюзионной пробе определяли прирост амплитуды сигнала (ПАС) и сдвиг фаз (СФ). Параметры оценки состояния сосудистой стенки с помощью аппарата Ангиоскан приведены в табл. 3. Значение практически всех параметров контурного анализа в группах больных, получавших МГТ или КПОК, оказалось ниже, чем в группе больных, не получавших гормональной терапии.
 Таблица 1. Параметры КМР в проспективной и в ретроспективной когортах больных (n=104)* Примечание. * — при сравнении значения всех параметров между когортами p>0,05. ИМТ — индекс массы тела; ОТ — окружность талии; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; ХС — холестерин; ЛПНП — липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ТГ — триглицериды.
Таблица 1. Параметры КМР в проспективной и в ретроспективной когортах больных (n=104)* Примечание. * — при сравнении значения всех параметров между когортами p>0,05. ИМТ — индекс массы тела; ОТ — окружность талии; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; ХС — холестерин; ЛПНП — липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ТГ — триглицериды.
Кроме того, выполняли окклюзионную пробу, во время которой пережимали артерии на руке испытуемого на несколько минут. В ответ на окклюзию после освобождения конечности регистрировали выраженность дилатации сосудов. Полученные данные характеризовали Ф.Э. Результаты окклюзионной пробы представлены в табл. 4. В группах МГТ с дозой эстрадиола 1 или 2 мг отмечалось приблизительно одинаковое статистически значимое повышение амплитуды сигнала по сравнению с 1-й и 4-й группами. СФ оказался сниженным в группах больных, не получавших МГТ и получавших КПОК, однако у больных 4-й группы этот параметр оказался статистически значимо выше, чем в 1-й.
 Таблица 1. Параметры КМР в проспективной и в ретроспективной когортах больных (n=104)* Примечание. * — при сравнении значения всех параметров между когортами p>0,05. ИМТ — индекс массы тела; ОТ — окружность талии; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; ХС — холестерин; ЛПНП — липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ТГ — триглицериды.
Таблица 1. Параметры КМР в проспективной и в ретроспективной когортах больных (n=104)* Примечание. * — при сравнении значения всех параметров между когортами p>0,05. ИМТ — индекс массы тела; ОТ — окружность талии; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; ХС — холестерин; ЛПНП — липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ТГ — триглицериды.
При анализе параметров контурного анализа ПВ у больных, не получавших МГТ, наблюдались отчетливые признаки нарушения структуры функционирования артериальной системы, выявляемые в 100% случаев. Повышение SI свидетельствовало о снижении эластичности аорты. МГТ в зависимости от дозы у 77% больных приводила к снижению SI. Он оказался повышенным в 1-й и 4-й группах.
В окклюзионной пробе оценивали Ф.Э. Выявлено ее нарушение у больных в 1-й и 4-й группах, что проявилось в уменьшенном расширении артериол в ответ на прирост кровотока, а также в уменьшении СФ. МГТ способствовала зависимой от дозы нормализации перечисленных показателей, и это свидетельствует, что применение МГТ способствует улучшению ФЭ.
Целью нашей работы явились изучение распространенности врожденных аномалий сердца и распространенности ФР развития ССО у больных с СШТ, а также оценка влияния на эти параметры разных режимов МГТ.
Мы провели оценку распространенности общепринятых ФР развития атеросклеротических заболеваний у больных с СШТ. В обеих когортах больных значения таких параметров, как ИМТ, ОТ, САД, не выходили за пределы нормы, при этом статистически значимо не различались между группами больных; в то же время у больных обеих когорт выявлялось умеренное повышение уровня общего ХС в основном за счет ЛПНП, хотя уровень ЛПВП оказался в пределах нормы, выявлялось повышение уровня Т.Г. Гиперхолестеринемия — один из основных независимых ФР прогрессирования атеросклероза. Таким образом, в нашем исследовании подтверждено наличие атерогенной дислипидемии у молодых больных с СШТ из российской популяции. Наши данный согласуются с результатами, полученным у больных, проживающих в других регионах.
Международные и отечественные рекомендации постулируют необходимость МГТ, начиная с 12 лет, с постепенным увеличением содержания эстрогенного компонента [1, 11]. Мы провели оценку влияния режима МГТ на наличие и выраженность различных ФР развития ССО у больных с СШТ. На фоне МГТ или КПОК отмечалось статистически значимое снижение ДАД по сравнению с больными 1-й группы. АГ страдают приблизительно 50% больных с СШТ [12, 13]. В нашем исследовании больным не выполнялось суточного мониторирования АД и, возможно, поэтому у большинства больных превышение пороговых нормальных уровней АД не зарегистрировано. Тем не менее даже при измерении АД методом Короткова у больных 1-й группы (не получавших МГТ) оказалось возможным констатировать диастолическую А.Г. Вне зависимости от дозы эстрогенного компонента МГТ приводила к статистически значимому снижению ДАД, чего не наблюдалось на фоне КПОК.
Кроме того, МГТ в зависимости от дозы приводила к статистически значимому повышению уровня ЛПВП. Если средний уровень ЛПВП у больных проспективной когорты не отличался от нормы, то при анализе по группам выраженность атерогенной дислипидемии оказалась максимальной в группе больных, не получавших МГТ. Таким образом, МГТ с учетом антиатерогенных свойств ЛПВП способна предотвратить развитие атеросклероза и улучшить прогноз у больных с СШТ.
В работе С. Gravholt и соавт. [14] МГТ сопровождалась уменьшением толерантности к углеводам, однако, как и в нашем исследовании, приводила к снижению ДАД. J. Ostberg и соавт. [15] показали зависимое от дозы влияние МГТ на параметры метаболизма у больных с СШТ: с увеличением дозы эстрадиола (максимально 4 мг) уровень ЛПВП увеличивался, а концентрация глюкозы умеренно снижалась. Эти результаты согласуются с полученными нами данными.
При оценке параметров контурного анализа ПВ у больных, не получавших МГТ, наблюдались отчетливые признаки нарушения структуры функционирования артериальной системы. Повышение SI свидетельствует о снижении эластичности аорты. У больных 1-й группы (без МГТ) и 4-й группы (КПОК) отмечались статистически значимо (p<0,05) большие значения этого показателя, чем у больных 2-й и 3-й групп (получавших МГТ). Это наряду со снижением SI свидетельствует о повышении эластичности артерий на фоне МГТ.
RI оказался повышенным в 1-й и 4-й группах, при этом в указанных группах статистически значимо (p<0,05) отличался от более низких и нормальных уровней в группах больных, получавших МГТ в дозе 1 мг (2-я группа) или 2 мг (3-я группа) эстрогена. Таким образом, для больных с СШТ характерно повышение тонуса периферических артерий и артериол, МГТ способствует снижению их тонуса.
При окклюзионной пробе выявлено нарушение ФЭ у больных в 1-й и 4-й группах, что проявилось в уменьшенном расширении артериол в ответ на увеличение кровотока, а также в уменьшении С.Ф. При этом МГТ способствовала нормализации данных показателей (статистически значимое отличие от параметров в 1-й и 2-й группах, причем изменения зависели от дозы), что согласуется с данными зарубежных исследователей. В исследовании М. Elsheikh и соавт. [16] проведение МГТ у больных с СШТ сопровождалось снижением AIp, характеризующего жесткость аорты. С учетом того, что в этом исследовании изменений параметров липидного состава крови или АД под действием МГТ не наблюдалось, можно сделать вывод о снижении жесткости артериальной стенки (ЖАС) под действием МГТ через другие механизмы, в частности улучшение Ф.Э. Данное предположение подтверждается полученными нами данными.
Уменьшение ЖАС, склонности артериол к спазму и улучшение ФЭ у больных с СШТ, получавших МГТ, соответствует полученным нами результатам и данным литературы о снижении ряда ФР, поражающих стенку артерий, под действием МГТ. По нашим данным, МГТ приводит к снижению уровня ДАД и повышению уровня протективных ЛПВП.
Таким образом, МГТ, благоприятно влияя на ФЭ сосудов и снижая выраженность атерогенной дислипидемии, потенциально способствует уменьшению риска развития ССО у больных с СШТ.
Работа выполнена при поддержке гранта РНФ № 17−75−30035.
Авторы заявляют об отсутствии конфликта интересов.
Источник
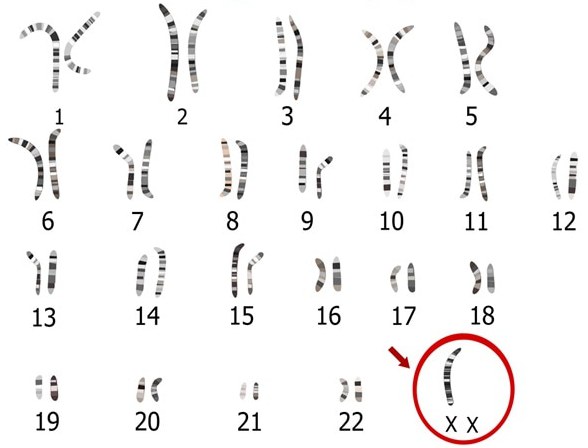
Синдром Шерешевского-Тернера (также синдром Ульриха-Тернера) — генетическое заболевание, вызванное полным или частичным отсутствием одной Х-хромосомы у женщин. Как и другие хромосомные аномалии, характеризуется тяжелыми последствиями для больных. Кариотип при синдроме Тернера обозначается как 45,X0.
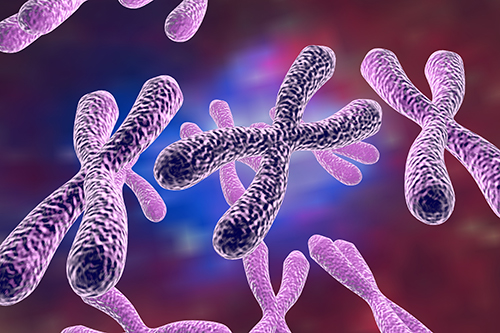
Генетика
Если говорить кратко, синдром Тернера развивается в случае полной или частичной моносомии Х-хромосомы у женщины. Примерно в 20% случаев болезнь связана с мозаицизмом Х-хромосомы — состоянием, при котором в некоторых клетках женского организма находятся две нормальные Х-хромосомы, одна из которых не активна, а в других клетках одна из половых хромосом существенно повреждена или полностью отсутствует. Иногда встречается переход части Х-хромосомы на аутосому (транслокация).
В некоторых случаях синдром связан с появлением, так называемых кольцевых хромосом или изохромосом. Кольцевые хромосомы возникают, когда концы хромосомы прерываются, а их длинные и короткие плечи соединяются вместе, образуя кольцо. Изохромосомы возникают, когда утраченное длинное или короткое плечо хромосомы заменяется идентичной копией другого плеча.
Отмечены случаи, когда у больных некоторые клетки имеют только одну копию Х-хромосомы, в то время как в других клетках присутствует Х-хромосома и некоторый материал Y-хромосомы. Количество материала на Y-хромосоме недостаточно, чтобы заставить организм развиваться по мужскому типу, но его наличие связано с повышенным риском развития формы рака, известной как гонадобластома.
Более 90% беременностей в случае наличия у плода синдрома Шерешевского-Тернера заканчиваются выкидышем или мертворождением, около 15% спонтанных абортов связано с этой патологией. Однако стоит заметить, что это единственная моносомия в человеческом организме, которая в некоторых случаях совместима с жизнью: моносомия по любой аутосоме (неполовой хромосоме) или У-хромосоме неизбежно приводит к смерти плода на ранних строках беременности. Надлежащий медицинский уход позволяет облегчить симптомы болезни детям, родившимся с синдромом Ульриха-Тернера.
Симптомы заболевания сильно отличаются у разных пациентов. Для большинства больных характерен низкий рост из-за патологий развития скелета, короткая шея, недоразвитие вторичных половых признаков, патологии органов зрения и сердечно-сосудистой системы, бесплодие. Несмотря на этот перечень симптомов, синдром Тернера является далеко не самой страшной генетической патологией — интеллект у больных, как правило, сохранен, и при правильно назначенном курсе лечения женщины с такой генетической аномалией могут вести нормальный образ жизни.
Синдром Ульриха-Тернера можно выявить до рождения с помощью современных методов диагностики, о которых речь пойдет ниже. В отличие от других генетических болезней, синдром не наследуется внутри семей и проявляется спонтанно (спорадически).
Причины
Причины синдрома Шерешевского-Тернера пока недостаточно хорошо изучены. Неизвестно точно, какие факторы влияют на вероятность рождения ребенка с этим нарушением. Была выдвинута гипотеза о том, что на риск развития синдрома влияет облучение матери повышенными дозами ионизирующего излучения (более 1 мЗв за год). Масштабные исследования, связанные с выявлением причин синдрома Тернера и других хромосомных аномалий проводились в 70-х годах прошлого века. Исследования проходили в индийском штате Керала, где радиационный фон существенно выше нормы из-за присутствия в почве тория и продуктов его распада, и в китайской провинции Гуангдонг, где годовая эквивалентная доза составляет 6,4 мЗв. Результаты показали, что повышенные дозы ионизирующего излучения увеличивают риск рождения детей с синдромом Дауна и синдромом кошачьего крика. Однако не было зафиксировано повышения частоты возникновения синдрома Тернера. На сегодняшний день во многих источниках можно встретить информацию о том, что ионизирующее излучение влияет на риск развития патологии, но не существует никаких статистических данных, которые бы это подтверждали.
Не выявлено также связи между возрастом матери и вероятностью рождения ребенка с этой патологией.
Симптомы
Для больных с данным заболеванием характерны: низкий рост, патологии развития скелета и вторичных половых признаков. Болезнь может поражать и другие системы органов. Наличие синдрома Шерешевского-Тернера еще не означает, что у одного пациента будут наблюдаться все возможные признаки заболевания. Синдром характеризуется широким спектром симптомов и специфических внешних черт. Наличие определенных симптомов, их тяжесть и время проявления строго индивидуальны.
Большинство детей с синдромом Тернера рождаются несколько раньше срока и с массой тела ниже нормы. У новорожденных часто наблюдается отекание рук и ног. У многих больных в подростковом возрасте появляется избыточная масса тела или ожирение, рост замедляется, проявляется недоразвитие молочных желез и матки, аменорея, деформация грудной клетки. Иногда встречаются такие патологии, как подковообразная почка, гипоплазия левых отделов сердца, сужение аорты, во взрослом возрасте — артериальная гипертензия.
Интеллект у больных обычно нормальный, но могут наблюдаться сложности связанные с концентрацией внимания и запоминанием нового материала. У некоторых детей с синдромом Тернера в детском и подростковом возрасте встречается СДВГ — синдром дефицита внимания и гиперактивность.
У больных повышены риски гипотиреоза из-за аутоиммунного тиреоидита. Некоторые женщины с синдромом Тернера страдаю непереносимостью глютена (целиакией).
К возможным симптомам заболевания также относятся: высокое небо, низкая линия роста волос, недоразвитие нижней челюсти. Встречаются патологии органов зрении и мочевыделительной системы.
Пренатальная диагностика
Ни для кого не секрет, что современные методы диагностики позволяют выявить большинство генетических отклонений плода задолго до рождения. Одну из таких процедур, неинвазивное пренатальное тестирование (скрининг внеклеточной ДНК плода, находящейся в крови матери), можно производить с конца первого триместра беременности.
Преимуществом этой процедуры является то, что она совершенно не опасна для матери и плода. Помимо синдрома Тернера, скрининг внеклеточной ДНК позволяет выявить такие анеуплоидии как синдром Патау (трисомия по 13-й хромосоме), синдром Эдвардса (трисомия по 18-й хромосоме), синдром Дауна (трисомия по 21-й хромосоме), трисомия по Х-хромосоме, синдром Клайнфельтера, синдром Мартина-Белл.
С помощью ультразвукового исследования можно выявить аномалии развития почек и сердца — они относятся к возможным симптомам заболевания.
Синдром можно выявить при помощи амниоцентеза или биопсии хориона. Обе эти процедуры инвазивны и имеют противопоказания. К их достоинствам относится высокая точность полученного результата.
Диагностика в детском и подростковом возрасте
Наличие синдрома Шерешевского-Тернера не всегда выходит обнаружить до родов. Многие женщины, у которых беременность протекает нормально, не считают нужным прибегать к пренатальной диагностике генетических аномалий плода, некоторые отказываются от нее из-за противопоказаний или страха перед побочными эффектами. Тогда рождение ребенка с хромосомной аномалией становиться для них неожиданностью.
В некоторых случаях синдром Тернера у детей можно диагностировать сразу после рождения, в то же время легкие формы болезни часто остаются незамеченными специалистами и родителями ребенка вплоть до начала подросткового периода. Бывает так, что первые три-четыре года жизни ребенок развивается нормально. После этого рост резко замедляется, становится заметным отставание от сверстников в физическом развитии. В начальной школе появляются трудности в обучении из-за невозможности сконцентрироваться. Детям с синдромом Тернера особенно сложно даются науки, требующие высокой концентрации внимания и пространственного мышления.
К концу пубертатного периода девочки с этой генетической аномалией намного ниже своих родителей (средний рост женщин с синдромом Ульриха-Тернера 145 см), заметны аномалии скелета и другие симптомы патологии. Чтобы убедиться в наличии заболевания у ребенка, следует обратиться к специалисту, который предложит произвести кариотипирование — диагностическую процедуру, позволяющую выявить хромосомные аномалии в геноме. Эта процедура абсолютно безопасна, безболезненна и не имеет противопоказаний. В ходе кариотипирования исследователь берет на анализ несколько кубиков венозной крови и исследует митотический цикл выделенных оттуда лейкоцитов.
Лечение
На данный момент не существует никаких процедур или препаратов, позволивших осуществлять лечение синдрома Тернера. Возможно, в будущем генная терапия позволит восстанавливать утраченную Х-хромосому в ходе эмбриогенеза, но пока такие процедуры остаются за гранью возможного. Лечение синдрома Шерешевского-Тернера остается симптоматическим. Для коррекции низкорослости назначаются гормональные препараты, содержащие соматотропин, которые принимают до и во время пубертатного периода. Чем раньше начинается соматотропная терапия, тем более эффективной она будет.
Заместительная эстрогенная терапия уже более семидесяти лет применяется для нормального развития у больных вторичных половых признаков, назначается она в возрасте 12-14 лет. Чтобы поддерживать нормальный баланс гормонов в организме, большинству женщин требуется прием эстрогена и прогестерона до начала менопаузы.
Эстроген имеет также ключевое значение для поддержания целостности костей и нормального функционирования тканей организма. У женщин с синдромом Шерешевского-Тернера без введения эстрогена повышается риск остеопороза и сердечных заболеваний.
При гипотиреозе пациенткам назначается введение тиреоидных гормонов.
В случае наличия у пациенток сахарного диабета, им необходимо постоянно контролировать уровень инсулина в крови и придерживаться диеты.
Если у женщины с синдромом Ульрика-Тернера присутствует подковообразная почка или пороки мочевыделительной системы, необходима консультация нефролога и уролога.
Прогноз
Прогноз, как и при любой генетической патологии, зависит от тяжести симптомов. Многие женщины, прошедшие гормональную терапию, живут полноценной жизнью. Они имеют нормальный уровень интеллекта и способности к обучению.
Почти все больные с синдромом Тернера не способны иметь детей. Медицине известны случаи, когда такие женщины могли забеременеть самостоятельно, однако это большая редкость. Эту проблему большинство пациенток решают с помощью искусственного оплодотворения.
Следует помнить, что женщины с синдромом Тернера имеют повышенный риск развития осложнений во время беременности. Им требуется постоянное наблюдение у гинеколога и терапевта.
Конечно же, непростая судьба у тех, кому был поставлен диагноз «синдром Тернера». Фото молодой женщины, страдающей этим заболеванием, представлено ниже.

Распространенность
Синдром Ульриха-Тернера нельзя назвать редким заболеванием. Его частота колеблется от 1:2000 до 1:5000 у новорожденных девочек, а учитывая тот факт, что большинство беременностей с этим синдромом заканчивается выкидышем или спонтанным абортом, можно сказать, что частота возникновения болезни гораздо выше.
Не выявлены расовые или этнические факторы, которые влияли бы на частоту появления на свет детей с синдромом Тернера.
История открытия
Первыми данное заболевание описали независимо друг от друга российский эндокринолог Николай Шерешевский в 1925 году и американский эндокринолог Генри Тернер в 1938 году. Они изучили основные симптомы патологии, однако не предполагали, что открытое ими заболевание связано с хромосомной аномалией. Немецкий ученый Ульрих также внес вклад в изучение заболевания. В 1930 году им был описан клинический случай, когда у 8-летней пациентки отсутствовали вторичные половые признаки, отмечался низкий рост, микрогнатия (недоразвитие верхней челюсти). В европейской литературе эту хромосомную аномалию часто называют синдромом Ульриха-Тернера или просто синдромом Ульриха.
Первая публикация о женщине с кариотипом синдрома Шерешевского-Тернера принадлежала британскому физиологу Чарльзу Форду. Именно он определил, что причина синдрома — моносомия по Х-хромосоме.
Медицинский курьез
Существуют еще два заболевания, которые иногда сокращенно называют синдромами Тернера. Открыли и описали эти патологии однофамильцы американского эндокринолога Генри Тернера, отсюда и путаница с названиями. Это синдромы Мея-Тернера и Персонейджа-Тернера. Оба эти заболевания никак не связаны с моносомией по Х-хромосоме, описанной выше, и даже не являются наследственными болезнями.
Первое описание синдрома Мея-Тернера появилось в 1957 году. Патология проявляется нарушением оттока венозной крови от левой нижней конечности и органов таза, в результате чего больные страдают от постоянных болей в левой ноге и области таза. На поздних стадиях болезни на венографии виден тромбоз глубоких вен. Синдром сложно диагностируется, особенно на ранних стадиях, так как поначалу протекает бессимптомно. Синдром Мея-Тернера обычно начинается в подростковом возрасте, у мужчин встречается чаще, чем у женщин.

В качестве основной диагностической процедуры применяется УЗИ подвздошных вен таза. В случае наличия заболевания, левая общая подвздошная вена в диаметре значительно больше нормальной. Для подтверждения диагноза применяется магнитно-резонансная ангиография подвздошных вен с контрастом. На поздних стадиях болезни лечение проводится хирургически. Часто назначается прием медицинских препаратов, призванных восстановить нормальный кровоток.
Синдром Персонейджа-Тернера в клинической практике встречается редко и его причины до сих пор точно не установлены. Первый сигнал о наличии заболевания — резкая беспричинная боль в плече или руке, реже — в обеих руках одновременно. Многие люди, у которых впервые проявилась эта патология, не считают нужным обращаться за помощью к специалисту, надеясь, что симптомы исчезнут сами.

Боль может не проходить несколько дней, иногда несколько недель. Боль усиливается при движениях и ослабевает, если конечность находится в покое. Многие пациенты перестают разрабатывать руку, из-за чего со временем развивается мышечная дистрофия. У большинства людей заболевание со временем проходит без какого-либо вмешательства. Иногда требуется прием сильных анальгетиков. Причины синдрома Персонейджа-Тернера представляют большой интерес для медиков, но пока не изучены. Распространенность заболевания также не известна.
Источник
