Синдром слабости синусового узла википедия
| Проводящая система сердца | |
|---|---|
| лат. Systema conducens cordis | |
| Элементы проводящей системы сердца | |
Расположение элементов проводящей системы сердца 10. Правая ножка пучка Гиса | |
| |
| Медиафайлы на Викискладе |
Проводящая система сердца (ПСС) — комплекс анатомических образований сердца (узлов, пучков и волокон), состоящих из атипичных мышечных волокон (сердечные проводящие мышечные волокна) и обеспечивающих координированную работу разных отделов сердца (предсердий и желудочков), направленную на обеспечение нормальной сердечной деятельности.
Анатомия[править | править код]
ПСС состоит из двух взаимосвязанных частей: синоатриальной (синусно-предсердной) и атриовентрикулярной (предсердно-желудочковой).
К синоатриальной относят синоатриальный узел (узел Кис-Флака), три пучка межузлового быстрого проведения, связывающие синоатриальный узел с атриовентрикулярным и межпредсердный пучок быстрого проведения, связывающий синоатриальный узел с левым предсердием.
Атриовентрикулярная часть состоит из атриовентрикулярного узла (узел Ашоффа–Тавара), пучка Гиса (включает в себя общий ствол и три ветви: левая передняя, левая задняя и правая) и проводящих волокон Пуркинье.[B: 1]
Кровоснабжение[править | править код]
Иннервация[править | править код]
ПСС морфологически отличается как от мышечной, так и от нервной ткани, но находится в тесной связи и с миокардом, и с внутрисердечной нервной системой.[B: 2]
Эмбриология[править | править код]
Развитие сердца начинается с третей недели внутриутробного развития. К середине 4 недели происходит разделение сердца на 2 камеры и формирование проводящей системы: начинается с образования синоатриального узла, с почти одновременным развитием остальной части проводящей системы.
Гистология[править | править код]
Атипичные мышечные волокна сердца — это специализированные проводящие кардиомиоциты, богато иннервированные, с небольшим количеством миофибрилл и обилием саркоплазмы.[B: 1]
Синусовый узел[править | править код]
Синусовый узел или синоатриальный узел (САУ) (лат. nódus sinuatriális), открытый в 1907 году Артуром Кейтом[en] и Мартином Флаком[en][2], расположен субэндокардиально в стенке правого предсердия латеральнее устья верхней полой вены, между отверстием верхней полой вены и правым ушком предсердия; отдаёт ветви к миокарду предсердий.[B: 1][B: 2]
Микрофотография синусового узла. Мышечные волокна в узле напоминают миоциты сердца, однако они тоньше, имеют волнистую форму и менее интенсивно окрашиваются гематоксилин-эозином. На фотографии к узлу прилегает нервное волокно: синусовый узел взаимодействует с ответвлениями блуждающего нерва.
Длина САУ ≈ 15 мм, ширина его ≈ 5 мм и толщина ≈ 2 мм. У 65% людей артерия узла берёт своё начало из правой венечной артерии, у остальных — из огибающей ветви левой венечной артерии. САУ богато иннервирован симпатическими и правым парасимпатическим нервами сердца, которые вызывают, соответственно, положительный и отрицательный хронотропные эффекты.[B: 2].
Клетки, составляющие синусовый узел, гистологически отличаются от клеток рабочего миокарда. Хорошим ориентиром служит выраженная a.nodalis (узловая артерия). Клетки синусового узла по размерам меньше клеток рабочего миокарда предсердия. Они группируются в виде пучков, при этом вся сеть клеток погружена в развитый матрикс. На границе синусового узла, обращенной к миокарду устья верхней полой вены, определяется переходная зона, которая может расцениваться как присутствие клеток рабочего миокарда предсердий в пределах синусового узла. Такие участки вклинения клеток предсердия в ткань узла чаще всего встречаются на границе узла и пограничного гребня (выступа стенки правого предсердия сердца, которым заканчиваются вверху гребенчатые мышцы).[B: 3]
Гистологически синусовый узел состоит из т.н. типичных клеток узла. Они располагаются беспорядочно, имеют веретенообразную форму, а иногда разветвления. Для этих клеток характерно слабое развитие сократительного аппарата, случайное распределение митохондрий. Саркоплазматический ретикулум развит хуже, чем в миокарде предсердий, а система T-трубочек отсутствует. Это отсутствие, правда, не является критерием, по которому выделяются «специализированные клетки»: часто система T-трубочек отсутствует и в рабочих кардиомиоцитах предсердия.
По краям синусового узла наблюдаются переходные клетки, отличающиеся от типичных лучшей ориентацией миофибрилл наряду с более высоким процентом межклеточных соединений — нексусов. Находимые ранее «вставочные светлые клетки», по последним данным, являются не более чем артефактом.
Согласно концепции, предложенной T.James и соавт. (1963-1985), связь синусового узла с АВ-узлом обеспечивается за счет наличия 3-х трактов: 1) короткий передний (пучок Бахмана), 2) средний (пучок Венкебаха) и 3) задний (пучок Тореля), более длинный. Обычно импульсы попадают в АВУ по короткому переднему и среднему трактам, на что расходуется 35-45 мсек. Скорость распространения возбуждения по предсердиям составляет 0,8—1,0 м/с. Описаны и другие проводящие тракты предсердий; к примеру, по данным B.Scherlag (1972), по нижнему межпредсердному тракту возбуждение проводится из передней части правого предсердия в нижнезаднюю часть левого предсердия. Считается, что в физиологических условиях эти пучки, а также пучок Тореля находятся в латентном состоянии.[B: 2]
Тем не менее, многими исследователями оспаривается существование каких-либо специализированных пучков между САУ и АВУ. Так, к примеру, в хорошо известной коллективной монографии[B: 3] сообщается следующее:
Полемика по вопросу об анатомическом субстрате для проведения импульсов между синусовым и атриовентрикулярным узлами ведётся уже сто лет, сколько насчитывает и сама история изучения проводящей системы. (…) По мнению Aschoff, Monckeberg и Koch, ткань между узлами является рабочим миокардом предсердий и не содержит гистологически различимых трактов. (…) На наш взгляд, в качестве трёх указанных выше специализированных путей James дал описание практически всего миокарда предсердной перегородки и пограничного гребня. (…) Насколько нам известно, никто до сих пор на основе морфологических наблюдений не доказал, что в межсердечной перегородке и пограничном гребне проходят узкие тракты, каким-либо образом сравнимые с атриовентрикулярным трактом и его ответвлениями.
Область атриовентрикулярного соединения[править | править код]
Предсердно-желудочковый узел (лат. nódus atrioventriculáris) лежит в толще передне-нижнего отдела основания правого предсердия и в межпредсердной перегородке. Длина его составляет 5-6 мм, ширина 2-3 мм. Кровоснабжается он одноименной артерией, которая в 80-90% случаев является ветвью правой коронарной артерии, а в остальных — ветвью левой огибающей артерии.[B: 2]
АВУ представляет собой ось проводящей ткани. Располагается на гребне входного и верхушечного трабекулярного компонентов мышечной части межжелудочковой перегородки. Архитектонику АВ-соединения удобнее рассматривать по восходящей — от желудочка к миокарду предсердий. Ветвящийся сегмент АВ-пучка расположен на гребне апикального трабекулярного компонента мышечной части межжелудочковой перегородки. Предсердный отрезок АВ-оси может быть разделен на компактную зону АВ-узла и переходную клеточную зону. Компактный участок узла по всей своей длине сохраняет тесную связь с фиброзным телом, которое образует его ложе. Он имеет два удлинения, проходящие вдоль фиброзного основания направо к трёхстворчатому клапану и налево — к митральному.
Переходная клеточная зона — это область, диффузно расположенная между сократительным миокардом и специализированными клетками компактной зоны АВ-узла. В большинстве случаев переходная зона более выражена сзади, между двумя удлинениями АВ-узла, но она также образует полуовальное покрытие тела узла.
С точки зрения гистологии, клетки предсердного компонента АВ-соединения мельче, чем клетки рабочего миокарда предсердий. Клетки переходной зоны имеют вытянутую форму и иногда разделены тяжами фиброзной ткани. В компактной зоне АВ-узла клетки расположены более тесно и часто организованы во взаимосвязанные пучки и завитки. Во многих случаях выявляется разделение компактной зоны на глубокий и поверхностный слои. Дополнительным покрытием служит слой переходных клеток, придающий узлу трехслойность. По мере перехода узла в проникающую часть пучка наблюдается увеличение размеров клеток, но в основном клеточная архитектоника сравнима с таковой в компактной зоне узла. Границу между АВ-узлом и проникающей частью одноименного пучка трудно определить под микроскопом, поэтому предпочтительней чисто анатомическое разделение в районе точки входа оси в фиброзное тело. Клетки, составляющие ветвящуюся часть пучка, по своим размерам напоминают клетки миокарда желудочков.
Коллагеновые волокна делят АВУ на кабельные структуры. Эти структуры создают анатомическую основу для продольной диссоциации проведения. Проведение возбуждения по АВУ возможно как в антероградном, так и в ретроградном направлениях. АВУ, как правило, оказывается функционально разделённым продольно на два проводящих канала (медленный α и быстрый β) — это создаёт условия для возникновения пароксизмальной узловой реципроктной тахикардии.
Продолжением АВУ является общий ствол пучка Гиса.
Пучок Гиса[править | править код]
Предсердно-желудочковый пучок (лат. fascículus atrioventriculális), или пучок Гиса, связывает миокард предсердий с миокардом желудочков. В мышечной части межжелудочковой перегородки этот пучок делится на правую и левую ножки (лат. crus déxtrum et crus sinístrum). Концевые разветвления волокон (волокна Пуркинье), на которые распадаются эти ножки, заканчиваются в миокарде желудочков.[B: 1]. Описан немецким кардиологом Вильгельмом Гисом[3].
Длина общего ствола пучка Гиса 8-18 мм в зависимости от размеров перепончатой части межжелудочковой перегородки, ширина около 2 мм. Ствол пучка Гиса состоит из двух сегментов — прободающего и ветвящегося. Прободающий сегмент проходит через фиброзный треугольник и доходит до мембранной части межжелудочковой перегородки. Ветвящийся сегмент начинается на уровне нижнего края фиброзной перегородки и делится на две ножки: правая направляется к правому желудочку, а левая — к левому, где распределяется на переднюю и заднюю ветви. Передняя ветвь левой ножки пучка Гиса разветвляется в передних отделах межжелудочковой перегородки, в передне-боковой стенке левого желудочка и в передней сосочковой мышце. Задняя ветвь обеспечивает проведение импульса по средним отделам межжелудочковой перегородки, по задне-верхушечным и нижним частям левого желудочка, а также по задней сосочковой мышце. Между ветвями левой ножки пучка Гиса существует сеть анастомозов, по которым импульс при блокаде одной из них попадает в блокированный области за 10-20 мсек. Скорость распространения возбуждения в общем стволе пучка Гиса составляет около 1,5 м/с, в разветвлениях ножек пучка Гиса и проксимальных отделах системы Пуркинье она достигает 3-4 м/с, а в терминальных отделах волокон Пуркинье снижается и в рабочем миокарде желудочков равняется примерно 1 м/с. [B: 2]
Прободающая часть ствола Гиса кровоснабжается из артерии АВУ; правая ножка и передняя ветвь левой ножки — от передней межжелудочковой венечной артерии; задняя ветвь левой ножки — от задней межжелудочковой венечной артерии.[B: 2]
Волокна Пуркинье[править | править код]
Бледные или набухшие клетки (так называемые клетки Пуркинье) редко встречаются в специализированной области атриовентрикулярного соединения у младенцев и детей младшего возраста.
Функциональное значение[править | править код]
Координируя сокращения предсердий и желудочков, ПСС обеспечивает ритмичную работу сердца, т.е нормальную сердечную деятельность. В частности, именно ПСС обеспечивает автоматизм сердца.
Функционально синусовый узел является водителем ритма первого порядка. В состоянии покоя в норме он генерирует 60-90 импульсов в минуту.[B: 2]
В АВ-соединении, главным образом в пограничных участках между АВУ и пучком Гиса, происходит значительная задержка волны возбуждения. Скорость проведения сердечного возбуждения замедляется до 0,02-0,05 м/с. Такая задержка возбуждения в АВУ обеспечивает возбуждение желудочков только после окончания полноценного сокращения предсердий. Таким образом, основными функциями АВУ являются: 1) антероградная задержка и фильтрация волн возбуждения от предсердий к желудочкам, обеспечивающие скоординированное сокращение предсердий и желудочков и 2) физиологическая защита желудочков от возбуждения в уязвимой фазе потенциала действия (с целью профилактики рециркуляторных желудочковых тахикардий). Клетки АВУ также способны брать на себя функции центра автоматизма второго порядка при угнетении функции САУ. Они обычно вырабатывают 40-60 импульсов в минуту. [B: 2]
Патологии:
- Синдром слабости синусового узла.
- Патологические добавочные проводящие пути между предсердиями и желудочками.
- Блокада проведения.
Добавочные пучки между предсердиями и желудочками являются анатомическим субстратом для классического варианта предвозбуждения желудочков (синдром Вольфа-Паркинсона-Уайта)[B: 3].
Литература[править | править код]
- Книги
- ↑ 1 2 3 4 Борзяк Э. И., Бочаров В. Я., Сапин М. Р. и др. Анатомия человека. В 2 томах / Под ред. акад. РАНМ, проф. М. Р. Сапина. — М.: Медицина, 1993. — Т. 2. — 560 с. — 40 000 экз. — ISBN 5-225-00879-8.
- ↑ 1 2 3 4 5 6 7 8 9 Анатомия и физиология проводящей системы сердца // Клиническая аритмология / Под ред. проф. А. В. Ардашева. — М.: МЕДПРАКТИКА-М, 2009. — С. 35—41. — 1220 с. — ISBN 978-5-98803-198-7.
- ↑ 1 2 3 Аритмии сердца. Механизмы. Диагностика. Лечение. В 3 томах / Пер. с англ./Под ред. В. Дж. Мандела. — М.: Медицина, 1996. — Т. 1. — 10 000 экз. — ISBN 0-397-50561-2.
- ↑ 1 2 Foundational Model of Anatomy
- ↑ Глязер Г. Исследователи человеческого тела. От Гиппократа до Павлова = Die Entdecker des Menschen. Von Hippokrates bis Pawlow / Пер. с нем. Ю. А. Федосюка. Под ред. Б. Д. Петрова. — М.: Государственное издательство медицинской литературы, 1956. — С. 200. — 7000 экз.
- ↑ Гаврилов Л. Ф. Гис Вильгельм (младший) // Большая Медицинская Энциклопедия / Главный редактор Б. В. Петровский. — М.
Источник
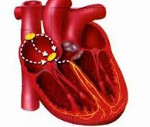
Синдром слабости синусового узла (СССУ, синдром дисфункции синусового узла) – нарушение ритма, вызванное ослаблением или прекращением функции автоматизма синусно-предсердного узла. При СССУ нарушается образование и проведение импульса из синусового узла в предсердия, что проявляется урежением сердечного ритма (брадикардией) и сопутствующими эктопическими аритмиями. У пациентов с синдромом слабости синусового узла возможно наступление внезапной остановки сердечной деятельности.
Общие сведения
Синдром слабости синусового узла (СССУ, синдром дисфункции синусового узла) – нарушение ритма, вызванное ослаблением или прекращением функции автоматизма синусно-предсердного узла. При СССУ нарушается образование и проведение импульса из синусового узла в предсердия, что проявляется урежением сердечного ритма (брадикардией) и сопутствующими эктопическими аритмиями. У пациентов с синдромом слабости синусового узла возможно наступление внезапной остановки сердечной деятельности.
Синдромом слабости синусового узла в основном страдают пожилые пациенты (старше 60-70 лет) обоего пола, хотя СССУ также встречается у детей и подростков. Распространенность данного вида аритмии в общей популяции составляет от 0,03 до 0,05%. Помимо истинной дисфункции синусового узла, связанной с его органическим поражением, встречаются вегетативные и медикаментозные нарушения функции автоматизма, устраняющиеся лекарственной денервацией сердца либо отменой препаратов, ведущих к подавлению образования и проведения импульса.
Синусовый (синусно-предсердный) узел является генератором импульсов и водителем сердечного ритма первого порядка. Он расположен в зоне устья верхней полой вены в правом предсердии. В норме в синусовом узле зарождаются электрические импульсы с частотой 60—80 в 1минуту. Синусовый узел состоит из ритмогенных пейсмекерных клеток, обеспечивающих функцию автоматизма. Деятельность синусно-предсердного узла регулирует вегетативная нервная система, что проявляется изменениями сердечного ритма сообразно гемодинамическим потребностям организма: учащением сердечных сокращений при физической нагрузке и замедлением в покое и период сна.
При развитии синдрома слабости синусового узла возникает периодическая или постоянная утрата синусно-предсердным узлом ведущей позиции в формировании сердечного ритма.

Синдром слабого синусового узла
Классификация СССУ
По особенностям клинического проявления выделяют следующие формы синдрома слабости синусового узла и варианты их течения:
1. Латентная форма – отсутствие клинических и ЭКГ-проявлений; дисфункция синусового узла определяется при электрофизиологическом исследования. Ограничений трудоспособности нет; имплантация электрокардиостимулятора не показана.
2. Компенсированная форма:
- брадисистолический вариант – слабо выраженные клинические проявления, жалобы на головокружение и слабость. Может быть профессиональное ограничение трудоспособности; имплантация электрокардиостимулятора не показана.
- брадитахисистолический вариант – к симптомам брадисистолического варианта добавляются пароксизмальные тахиаритмии. Имплантация электрокардиостимулятора показана в случаях декомпенсации синдрома слабости синусового узла под влиянием противоаритмической терапии.
3. Декомпенсированная форма:
- брадисистолический вариант – определяется стойко выраженная синусовая брадикардия; проявляется нарушением церебрального кровотока (головокружением, обморочными состояниями, преходящими парезами), сердечной недостаточностью, вызванной брадиаритмией. Значительное ограничение трудоспособности; показаниями к имплантации служат асистолия и время восстановления функции синусового узла (ВВФСУ) более 3 секунд.
- брадитахисистолический вариант (синдром Шорта) – к симптомам брадисистолического варианта декомпенсированной формы добавляются пароксизмальные тахиаритмии (суправентрикулярная тахикардия, мерцание и трепетание предсердий). Пациенты полностью нетрудоспособны; показания к имплантации электрокардиостимулятора те же, что и при брадисистолическом варианте.
4. Постоянная брадисистолическая форма мерцательной аритмии (на фоне ранее диагностированного синдрома слабости синусового узла):
- тахисистолический вариант – ограничение трудоспособности; показаний к имплантации электрокардиостимулятора нет.
- брадиситолический вариант — ограничение трудоспособности; показаниями к имплантации электрокардиостимулятора служат церебральная симптоматика и сердечная недостаточность.
Развитию брадисистолической формы мерцательной аритмии может предшествовать любая из форм дисфункции синусового узла. В зависимости от регистрации признаков слабости синусового узла при холтеровском ЭКГ-мониторировании выделяют латентное (признаки СССУ не выявляются), интермиттирующее (признаки СССУ выявляются при снижении симпатического и возрастании парасимпатического тонуса, например, в ночные часы) и манифестирующее течение (признаки СССУ выявляются при каждом суточном ЭКГ-мониторировании).
Синдром слабости синусового узла может протекать остро и хронически, с рецидивами. Острое течение синдрома слабости синусового узла часто наблюдается при инфаркте миокарда. Рецидивирующее течение СССУ может быть стабильным или медленно прогрессирующим. По этиологическим факторам различаются первичная и вторичная формы синдрома слабости синусового узла: первичная вызывается органическими поражениями синусно-предсердной зоны, вторичная — нарушением ее вегетативной регуляции.
Причины СССУ
К случаям первичного синдрома слабости синусового узла относится дисфункция, вызванная органическими поражениями синоатриальной зоны при:
- кардиальной патологии — ИБС, гипертонической болезни, кардиомиопатии, пороках сердца, миокардитах, хирургических травмах и трансплантации сердца;
- идиопатических дегенеративных и инфильтративных заболеваниях;
- гипотиреозе, дистрофии костно-мышечного аппарата, старческом амилоидозе, саркаидозе, склеродермическом сердце, злокачественных опухолях сердца, в стадии третичного сифилиса и др.
Ишемия, вызванная стенозом артерии, питающей синусовый узел и синоатриальную зону, воспаление и инфильтрация, кровоизлияние, дистрофия, локальный некроз, интерстициальный фиброз и склероз вызывают развитие на месте функциональных клеток синусно-предсердного узла соединительной ткани. Вторичный синдром слабости синусового узла обусловлен внешними (экзогенными) факторами, воздействующими на синусный узел. К экзогенным факторам относят гиперкалиемию, гиперкальциемию, лечение лекарственными препаратами, снижающими автоматизм синусового узла ( b-адреноблокаторами, клофелином, допегитом, резерпином, кордароном, верапамилом, сердечными гликозидами и др.).
Особо среди внешних факторов выделяют вегетативную дисфункцию синусового узла (ВДСУ). ВДСУ часто наблюдается в связи с гиперактивацией блуждающего нерва (рефлекторной или длительной), вызывающей урежение синусового ритма и удлинение рефрактерности синусового узла. Тонус блуждающего нерва может повышаться при физиологических процессах: во сне, во время мочеиспускания, дефекации, кашля, глотания, тошноты и рвоты, пробы Вальсавы. Патологическая активация блуждающего нерва может быть связана с заболеваниями глотки, мочеполового и пищеварительного трактов, имеющих обильную иннервацию, а также при гипотермии, гиперкалиемии, сепсисе, повышении внутричерепного давления.
ВДСУ чаще наблюдается у подростков и молодых людей в связи со значительной невротизацией. Стойкий синусовый брадикардический ритм также может отмечаться у тренированных спортсменов в связи с выраженным преобладанием вагусного тонуса, однако, такая брадикардия не является признаком синдрома слабости синусового узла, т. к. нарастание частоты сердечных сокращений происходит адекватно нагрузке. Вместе с тем, у спортсменов может развиваться истинная СССУ в сочетании с другими нарушениями ритма, обусловленные дистрофией миокарда.
Симптомы СССУ
Варианты клинического течения синдрома слабости синусового узла разнообразны. У части пациентов клиника СССУ длительный период времени может отсутствовать, у других отмечаются выраженные нарушения ритма, сопровождающиеся в тяжелых случаях головными болями, головокружением, приступами Морганьи-Адамса-Стокса. Возможно расстройство гемодинамики в результате уменьшения ударного и минутного объема выброса, сопровождающихся, в том числе, развитием кардиальной астмы, отека легких, коронарной недостаточностью (стенокардией, реже – инфарктом миокарда).
В клинике синдрома слабости синусового узла выделяют две основные группы симптомов: церебральные и кардиальные. Церебральная симптоматика при маловыраженных нарушениях ритма проявляется усталостью, раздражительностью, забывчивостью, эмоциональной лабильностью. У пожилых пациентов наблюдается снижение интеллекта и памяти. При прогрессировании СССУ и недостаточности мозгового кровообращения церебральная симптоматика нарастает. Развиваются предобморочные состояния и обмороки, которым предшествует появление шума в ушах, резкой слабости, ощущение замирания или остановки сердца. Обмороки кардиального генеза при синдроме Морганьи-Эдемс-Стокса протекают без предвестников и судорог (исключение – случаи длительной асистолии).
Кожные покровы бледнеют, холодеют, покрываются холодным потом, АД резко снижается. Провоцировать обмороки может кашель, резкий поворот головы, ношение тесного воротника. Обычно обмороки проходят самостоятельно, однако при затяжных обморочных состояниях может потребоваться оказание неотложной помощи. Выраженная брадикардия может вызывать дисциркуляторную энцефалопатию, характеризующуюся усилением головокружения, появлением мгновенных провалов в памяти, парезов, «проглатыванием» слов, раздражительностью, инсомнией, снижением памяти.
Кардиальные проявления синдрома слабости синусового узла начинаются с ощущений пациентом замедленного или нерегулярного пульса, болей за грудиной (в связи с недостатком коронарного кровотока). Присоединяющиеся аритмии сопровождаются сердцебиением, перебоями в работе сердца, одышкой, слабостью, развитием хронической сердечной недостаточности.
При прогрессировании СССУ нередко присоединяется вентрикулярная тахикардия или фибрилляция, повышающие вероятность развития внезапной сердечной смерти. Среди других органических проявлений синдрома слабости синусового узла могут отмечаться олигурия, обусловленная почечной гипоперфузией; нарушения со стороны желудочно-кишечного тракта, перемежающаяся хромота, мышечная слабость в связи с недостаточностью оксигенации внутренних органов и мышц.
Объективно выявляются синусовая брадикардия (особенно ночная), сохраняющаяся при физической нагрузке, синоаурикулярная блокада и эктопические ритмы (мерцание и трепетание предсердий, пароксизмальная тахикардия, суправентрикулярная, реже желудочкая экстрасистолия). После периода эктопических ритмов восстановление нормального синусового ритма замедлено и наступает после предшествующей длительной паузы.
Диагностика СССУ
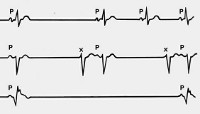
Наиболее характерным признаком синдрома слабости синусового узла служит брадикардия, встречающаяся в 75% случаев, поэтому предположить наличие СССУ следует у любого пациента с выраженным урежением сердечного ритма. Установление наличия брадикардии производится при помощи ЭКГ-регистрации ритма во время появления характерной симптоматики. В пользу синдрома слабости синусового узла могут свидетельствовать следующие электрокардиографические изменения: синусовая брадикардия, синоатриальная блокада, остановка деятельности синусового узла, депрессия синусового узла в постэкстрасистолический период, синдром тахи-брадикардии, внутрипредсердная миграция водителя ритма.
В диагностике преходящей брадикардии используется холтеровское суточное мониторирование ЭКГ на протяжении 24-72 часов. Мониторирование с большей вероятностью и частотой позволяет зафиксировать вышеозначенные феномены, проследить их связь с нагрузкой и реакцию на лекарственные препараты, выявить бессимптомное течение синдрома слабости синусового узла. Для диагностики СССУ применяется атропиновая проба: при синдроме слабости синусового узла после введения 1 мл 0,1% атропина частота синусового сердечного ритма не превышает 90 ударов в минуту.
Следующим этапом диагностики СССУ служит ЭФИ — электрофизиологическое исследование. Путем введения чрезпищеводного электрода (ЧПЭКГ) пациенту проводится стимуляция ритма до 110-120 в мин., и после прекращения стимуляции по ЭКГ оценивается скорость восстановления синусовым узлом ритма сокращений. При паузе, превышающей 1,5 см, можно предположить наличие синдрома слабости синусового узла.
При выявлении измененной функции синусового узла проводится дифференциальная диагностика между истинным СССУ, обусловленным органическим поражением водителя ритма, и вегетативной или медикаментозной дисфункцией синусового узла. Для выявления кардиопатологии проводится УЗИ сердца, МСКТ и МРТ сердца.
Лечение СССУ
Объем лечебных мероприятий при синдроме слабости синусового узла зависит от степени нарушения проводимости, остроты нарушения ритма, этиологии, выраженности клинической симптоматики. При отсутствии или минимальных проявлениях СССУ проводится терапия основного заболевания и динамическое наблюдение кардиолога. Медикаментозное лечение СССУ проводится при умеренных проявлениях бради- и тахиаритмий, однако, оно малоэффективно.
Основным методом лечения синдрома слабости синусового узла является постоянная электрокардиостимуляция. При выраженной клинике СССУ, вызванной брадикардией, удлинении ВВФСУ до 3-5 сек., наличии признаков хронической сердечной недостаточности показана имплантация электрокардиостимулятора, работающего в demand-режиме, т. е. вырабатывающего импульсы при падении частоты сердечных сокращений до критических показателей.
Абсолютными показаниями к электрокардиостимуляции служат:
- хотя бы однократное возникновение приступа Морганьи-Эдемс-Стокса;
- брадикардия < 40 уд. в мин., ВВФСУ более 3 сек.;
- головокружения, пресинкопальные состояния, коронарная недостаточность, высокая артериальная гипертензия;
- сочетание брадикардии с другими видами аритмий, требующих назначения противоаритмических препаратов, что невозможно при нарушении проводимости.
Прогноз при СССУ
Течение синдрома слабости синусового узла обычно имеет тенденцию к прогрессированию, поэтому в отсутствии лечения клиническая симптоматика усугубляется. Неблагоприятно на прогноз СССУ влияют имеющиеся органические заболевания сердца.
В значительной мере прогноз СССУ определяется проявлением дисфункции синусового узла. Наиболее неблагоприятным сочетанием является синусовая брадикардия и предсердные тахиаритмии; менее неблагоприятный прогноз – при сочетании с синусовыми паузами; удовлетворительный – наличие изолированной синусовой брадикардии. Такой прогноз обусловлен вероятностью развития тромбоэмболических осложнений при каждом из вариантов течения, являющихся причиной летальности у 30-50% пациентов с синдромом слабости синусового узла.
В целом СССУ увеличивает процент летальности в среднем на 4-5% ежегодно, причем развитие внезапной сердечной смерти может наступить в любой из периодов заболевания. Продолжительность жизни пациентов с СССУ при отсутствии лечения вариабельна и может составлять от нескольких недель до 10 и более лет.
Профилактика СССУ
Предупреждение развития синдрома слабости синусового узла включает своевременное выявление и терапию опасных этиологических состояний, осторожное назначение противоаритмических препаратов, влияющих на автоматизм и проводимость синусового узла. Для профилактики фибрилляции предсердий у пациентов с СССУ необходимо проведение электрокардиостимуляции.
Источник
