Синдром швахмана даймонда у детей

Синдром Швахмана-Даймонда – это генетическая патология, проявляющаяся секреторной недостаточностью поджелудочной железы, костномозговыми нарушениями и серьезными гематологическими изменениями. Первые симптомы (диарея, метеоризм, снижение аппетита, дистрофия, деформация скелета, анемия и т. п.) регистрируются на 5-6 месяце во время введения прикорма. Основные диагностические мероприятия: биохимический и общий анализ крови и кала, гормональные исследования, УЗИ, КТ и МРТ органов брюшной полости, рентгенография скелета. Лечение направлено на устранение клинических признаков и поддержание жизнедеятельности.
Общие сведения
Синдром Швахмана-Даймонда – редкое генетическое заболевание, для которого характерны нарушение работы поджелудочной железы и дисфункция костного мозга. Болезнь проявляется всесторонней задержкой развития (умственного, психического и физического), отмечена повышенная восприимчивость к инфекциям. Распространенность заболевания составляет 1:50 000 рожденных детей. Синдром несколько чаще встречается у мальчиков. Прогноз крайне неблагоприятный, так как большинство пациентов не доживают до 7 лет.
Впервые патология была описана Bodian и Sheldon в 1964 году у пациентов с врожденной гипоплазией поджелудочной железы, задержкой роста и панцитопенией. В том же году Швахмоном и Даймондом была детально изучена экзокринная панкреатическая недостаточность и дисфункция костного мозга при данном заболевании. Многообразие проявлений синдрома требует согласованного междисциплинарного подхода к лечению патологии с участием специалистов в области гастроэнтерологии, генетики, педиатрии.
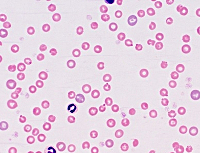
Синдром Швахмана-Даймонда
Причины синдрома Швахмана-Даймонда
Причиной развития синдрома Швахмана-Даймонда является генетическая аномалия. Патология вызвана мутацией одного из участков 7 хромосомы (ген SBDS), она наследуется по аутосомно-рецессивному типу, то есть оба родителя должны передать дефектный ген своему ребенку. Регистрируются и спорадические случаи синдрома Швахмана-Даймонда – в их этиологии важную роль отводят воздействию вирусов паротита и Коксаки на ткани эмбриона. Клинические признаки начинают появляться на 5-6 месяц после рождения.
Хотя точная функция гена SBDS не определена, его мутация вызывает задержку развития; жировое перерождение ткани поджелудочной железы; гипоплазию костного мозга, которая приводит к серьезным гематологическим изменениям.
Симптомы синдрома Швахмана-Даймонда
Клинические признаки синдрома Швахмана-Даймонда появляются после начала введения прикорма (5-6 месяцев). Первый симптом патологии – диарея, а точнее, стеаторея, для которой характерно значительное увеличение доли жира в каловых массах. На фоне нарушения стула снижается аппетит, появляется метеоризм. Эти признаки обусловлены недостаточностью секреторной функции поджелудочной железы. Помимо этого, выявляются и другие эндокринные нарушения, результатом которых является развитие субнанизма – низкорослости. Постепенно развивается дистрофия костной ткани, задерживается физическое и психическое развитие ребенка. У большинства пациентов регистрируется деформация костей, сопровождающаяся беспричинными переломами.
С первого дня жизни ребенка определяется измененная картина крови: снижается количество нейтрофилов (нейтропения), резко сокращается число эритроцитов (анемия) и тромбоцитов (тромбоцитопения), все это сочетается с геморрагическим синдромом (повышенная кровоточивость на фоне нарушения свертываемости). Пациенты подвержены развитию инфекционных заболеваний различных систем организма (органов дыхания, мочевыделительной системы, кожи и пр.).
При легкой форме симптомы, характерные для заболевания, не ярко выражены, при адекватной терапии такие пациенты доживают до 20 лет. При тяжелой форме клинические признаки рано появляются и быстро прогрессируют, любые терапевтические мероприятия не дают положительного эффекта, эти больные погибают очень рано.
Диагностика синдрома Швахмана-Даймонда
Диагностика синдрома Швахмана-Даймонда не представляет трудностей, заподозрить наличие патологии может педиатр при проведении профилактического осмотра и появлении характерных симптомов. Врач тщательно собирает анамнез, выявляет хронические заболевания, а также случаи возникновения синдрома у ближайших родственников. Так как первые признаки связаны с диспепсическими нарушениями, то патологию может заподозрить и гастроэнтеролог.
Чтобы поставить окончательный диагноз, необходимо провести инструментальные и лабораторные методы обследования: анализ кала и крови, гормональные исследования, КТ, МРТ, УЗИ органов брюшной полости, рентгенографию скелета.
Анализ каловых масс выявляет стеаторею, общий анализ крови — нейтропению, тромбоцитопению, анемию, иногда панцитопению – снижение количества всех клеток крови. Биохимический анализ крови показывает состояние обменных процессов, а также концентрацию и свойства ферментов.
КТ, МРТ, УЗИ органов брюшной полости выявляют изменение ткани поджелудочной железы, эти исследования проводят также для исключения других болезней пищеварительной системы. Рентгенография костей определяет степень деформации скелета. После подтверждения диагноза всем пациентам назначается консультация невролога и генетика.
Лечение синдрома Швахмана-Даймонда
Лечение синдрома Швахмана-Даймонда направлено на устранение неблагоприятных симптомов и поддержание жизненно важных функций. Всем пациентам прописывают строгую диету: ограничивают жиры, повышают содержание белков. Обязательна заместительная терапия, восполняющая недостающие ферменты поджелудочной железы. При появлении инфекционных заболеваний выписывают антибактериальные препараты. Также необходимо восстановить показатели картины крови; анемия успешно поддается терапии, другие изменения трудно корректируются. Если развивается тяжелая форма патологии и серьезные гематологические нарушения, проводят химио- и лучевую терапию, трансплантацию костного мозга.
Прогноз синдрома Швахмана-Даймонда крайне неблагоприятный. Согласно статистике, пациенты умирают в 7-10 лет, очень редко они доживают до 20 лет. Это связано с сильным снижением иммунитета и развитием серьезных инфекционных заболеваний. В редких случаях характер течения патологии меняется в сторону улучшения, как правило, постепенно уменьшается секреторная недостаточность, но при этом гематологические нарушения не восстанавливаются.
Источник
Синдром Швахмана – Даймонда
Синдром Швахмана – Даймонда или синдром Швахмана – Бодиана –
Даймонда (Shwachman-Diamond syndrome, Shwachman-Bodian-Diamond
syndrome, МКБ-10: Q45.3) — редкое генетическое заболевание, которое
проявляется недостаточностью функции поджелудочной железы, нарушением
кроветворения и аномалиями развития скелета [1]. Патогенез синдрома
связан с мутациями генов, участвующих в биогенезе внутриклеточных
органелл — рибосом. Частой причиной смерти больных являются
онкогематологические заболевания: миелодиспластический синдром (МДС),
острый миелобластный лейкоз (ОМЛ) и апластическая анемия (последняя
развивается у 20 % пациентов).
Первое описание синдрома дал английский врач Мартин Бодиан (Martin
Bodian) с коллегами в мае 1964 г. В их публикации приведены несколько
случаев гипоплазии поджелудочной железы у пациентов с панцитопенией и
задержкой роста [2]. В ноябре того же года американские гематологи Гарри
Швахман (Harry Shwachman) и Луис Даймонд (Louis Diamond) представили
аналогичные наблюдения сочетания экзокринной недостаточности
поджелудочной железы с дисфункцией костного мозга [3].
В 2001 г. канадские ученые идентифицировали патогенетически значимый
ген SBDS [4], после чего в 2003 г. были открыты типичные мутации [5].
Распространенность и тип наследования
Заболеваемость синдромом Швахмана – Даймонда составляет примерно 1
случай на 77 000 человек. Всего в научной литературе описано около 200
случаев заболевания. Среди больных преобладают мальчики: соотношение
мальчиков и девочек — 1,7 к 1. Синдром является второй по частоте после
муковисцидоза причиной недостаточности функции поджелудочной железы.
Заболевание наследуется по аутосомно-рецессивному механизму. Больной
ребенок получает по одному мутированному аллелю от каждого из
родителей, которые являются бессимптомными гетерозиготными носителями.
Вероятность развития синдрома у брата или сестры больного ребенка — 25
%, вероятность носительства у них — 50 %. Примерно 10 % мутаций SBDS
возникают у больных впервые, а не приобретаются по наследству.
Синдром Швахмана – Даймонда может заподозрить педиатр, терапевт,
гастроэнтеролог или гематолог. Наиболее типичные симптомы появляются в
младенческом возрасте — диарея с жирным стулом (стеаторея), снижение
показателей крови (цитопения), отставание в росте, потеря веса, сухость кожи
и экзема. Пациенты часто страдают инфекционными заболеваниями из-за
низкого уровня нейтрофилов (нейтропении). Нарушения развития скелета
проявляются деформациями грудной клетки, хондродисплазией,
клинодактилией. Возможны неврологические патологии: нарушение
визуальной координации движений, отставание в интеллектуальном
развитии, снижение способности концентрировать внимание.
В биохимических анализах крови отмечается снижение уровня
панкреатической изоамилазы и катионного трипсиногена. Анализ стула
показывает избыток жиров и снижение уровня эластазы.
Хотя единых критериев диагностики синдрома нет, имеются коллективные
рекомендации, полезные для клинической практики [9, 10]. По мнению
некоторых авторов, для постановки диагноза достаточно выявления
сочетания экзокринной недостаточности поджелудочной железы и дисплазии
кроветворения. Однако наиболее точно заболевание можно
идентифицировать с помощью генетических тестов (ПЦР или
секвенирования генов SBDS, DNAJC21, EFL1 и SRP54).
Синдром следует дифференцировать с муковисцидозом, анемией Фанкони,
синдромом Пирсона, анемией Даймонда – Блэкфана, целиакией, синдромом
Йохансона – Близзарда и наследственным дефицитом G6PC3.
На сегодняшний день заболевание остается неизлечимым. Пациенты нуждаются в постоянном медицинском наблюдении педиатров, гематологов, диетологов, ортопедов и проведении симптоматической терапии. В детском возрасте показан прием ферментов поджелудочной железы и жирорастворимых витаминов (витамины D, A, E и K). Это позволяет избежать тяжелых симптомов дефицита, белково-энергетической недостаточности и отставания в развитии. По неустановленным причинам у некоторых больных функция поджелудочной железы с течением времени нормализуется, что позволяет отойти от ферментной терапии.
У пациентов с выраженной цитопенией используются заместительные трансфузии тромбоконцентрата и эритроцитарной взвеси (с назначением по необходимости хелаторных препаратов), а также стимуляция гранулоцитопоэза препаратами рекомбинантного Г-КСФ. Для своевременной санации очагов инфекции (таких как кариес) проводятся регулярные осмотры стоматолога.
У больных часто обнаруживается клональный гемопоэз с повышенным риском развития МДС, ОМЛ и апластической анемии. В связи с этим рекомендуется контроль клинического анализа крови каждые 3–4 месяца, а также периодическое исследование миелограммы. При выявлении онкогематологической патологии решается вопрос о трансплантации гемопоэтических стволовых клеток (2-летняя выживаемость составляет около 58 %).
Проводится медико-генетическое консультирование членов семьи больного.
В 90–95 % случаев заболевание связано с мутациями гена SBDS,
расположенного в локусе 7q11.22, т. е. на длинном плече 7-й хромосомы. Ген
SBDS кодирует белок, локализующийся в ядрышках клеток и участвующий в
сборке большой субъединицы рибосом [6]. Также этот белок задействован в
таких важных внутриклеточных процессах, как амплификация центросом и
сборка веретена деления. Считается, что нарушение этих процессов вызывает
генетическую нестабильность в гемопоэтических клетках пациентов, что
обусловливает предрасположенность к развитию МДС и ОМЛ (около 1 % в
год) [7].
В целом детальные молекулярные механизмы заболевания изучены
недостаточно [8]. В редких случаях (менее 1 %) у больных выявляются
мутации в других генах, участвующих в биогенезе рибосом: EFL1, DNAJC21
и SRP54. Примерно в 10 % случаев конкретные мутации обнаружить не
удается.
- SBDS (258+2T>C, 183-184TA>CT)
- DNAJC21
- EFL1
- SRP54
- Nelson A. S., Myers K. C. Diagnosis, Treatment, and Molecular Pathology
of Shwachman-Diamond Syndrome. Hematol Oncol Clin North Am. 2018
Aug;32(4):687–700 - Bodian M., Sheldon W., Lightwood R. 1964. Congenital Hypoplasia of the
exocrine pancreas.Acta. Paediatr. 53: 282–293 - Shwachman H., Diamond L. K,, Oski F. A., Khaw K. T. (1964). «The
syndrome of pancreatic insufficiency and bone marrow dysfunction». J
Pediatr. 65: 645–663 - Goobie S., Popovic M., Morrison J. et al. Shwachman–Diamond syndrome
with exocrine pancreatic dysfunction and bone marrow failure maps to the
centromeric region of chromosome 7. Am. J. Hum. Genet. 2001; 68:
1048–1054 - Boocock G. R., Morrison J. A., Popovic M., Richards N., Ellis L., Durie P.
R., Rommens J. M., 2003. Mutations in SBDS are associated with
Shwachman-Diamond syndrome. Nat. Genet. 33 (1), 97e101 - Bezzerri V., Cipolli M. Shwachman-Diamond Syndrome: Molecular
Mechanisms and Current Perspectives. Mol Diagn Ther. 2019
Apr;23(2):281–290 - Dale D. C., Bolyard A. A., Schwinzer B. G. et al. The severe chronic
neutropenia international registry: 10-year follow-up report. Support Cancer
Ther 2006;3(4):220–231 - Warren A. J. Molecular basis of the human ribosomopathy Shwachman-
Diamond syndrome. Adv Biol Regul. 2018 Jan;67:109–127 - Ипатова М. Г., Куцев С. И., Шумилов П. В., Мухина Ю. Г., Финогенова
Н. А., Полякова С. И. Захарова, Е. Ю., Щербина А. Ю., Деордиева Е. А.,
Пучкова А. А., Рославцева Е. А., Комарова О. Н., Чубарова А. И.
Краткие рекомендации по ведению больных с синдромом
Швахмана–Даймонда. Педиатрия. 2016; 95 (6): 181–186 - Dror Y., Donadieu J., Koglmeier J., Dodge J., Toiviainen-Salo S., Makitie
O., Kerr E., Zeidler C., Shimamura A., Shah N., Cipolli M., Kuijpers T.,
Durie P., Rommens J., Siderius L., Liu J. M. Draft consensus guidelines for
diagnosis and treatment of Shwachman-Diamond syndrome. Ann N Y Acad
Sci. 2011 Dec;1242:40–55
Источник

Синдром Швахмана-Даймонда – это генетическое заболевание, которое выражается в недоразвитости поджелудочной железы и нарушении работы костного мозга. Патология встречается достаточно редко, одинаково часто диагностируется у мальчиков и девочек. Прогнозы заболевания неблагоприятные, поскольку большинство детей умирает в возрасте до 7 лет, только 5% больных доживают до своего двадцатилетия.
Причины
Главной причиной развития синдрома является мутация ДНК. Возникает болезнь в случае передачи гена SBDS с дефектной 7-й хромосомой от обоих родителей.
Формы
В медицине выделяют две формы синдрома Швахмана-Даймонда в зависимости от тяжести проявления симптомов у детей.
Для легкой характерно наличие некоторых симптомов, присущих заболеванию. При правильно выбранной своевременно начатой заместительной терапии пациент может дожить до 20 лет.
Тяжелая форма характеризуется максимальным проявлением всех симптомов с первых месяцев жизни малыша. Заболевание быстро прогрессирует, не поддается лечению. Пациенты умирают в раннем возрасте, несмотря на приложенные усилия со стороны медицинского персонала.
Симптомы
Все симптомы синдрома Швахмана-Даймонда можно разделить на несколько групп: экзокринные и эндокринные нарушения, проблемы с костным мозгом и скелетом. Первые симптомы выявляются на пятом-шестом месяце жизни ребенка.
Проблемы с работой поджелудочной железы вызывают резкое, необоснованное снижение веса, потерю аппетита и нарушение стула. Каловые массы имеют кашицеобразную структуру, оттенок серого цвета и крайне неприятный запах. Кроме того, опорожнение кишечника происходит достаточно часто.
Дефицит объема костного мозга провоцирует частые вирусные и инфекционные заболевания. Обычно поражаются органы дыхательной системы, что грозит развитием пневмонии, бронхита или астмы.
Проблемы с костным скелетом проявляются деформацией костей, искривлением позвоночника, нарушением двигательной активности.
Изменения со стороны эндокринной системы возникают в результате недостаточной или избыточной выработки гормонов щитовидной железой, надпочечниками и гипофизом. Это проявляется низким ростом больного, гипогонадизмом, гиперкортицизмом, отсталостью в умственном и физическом развитии.
Крайне редко встречаются дополнительные симптомы: аномалии количества и формы пальцев, пигментные пятна на слизистых оболочках, кожных покровах, глазах и косоглазие.
Осложнения
Синдром Швахмана-Даймонда может спровоцировать ряд осложнений. Часто наблюдается деформация костей – искривление грудной клетки, позвоночника и аномальное развитие ребер (слишком короткие). В некоторых случаях у больного диагностируется цирроз печени или жировой гепатоз. В результате ослабленного иммунитета ребенка часто поражают разного рода вирусы и инфекции.
Диагностика
Для диагностики синдрома необходима консультация педиатра, гастроэнтеролога, эндокринолога и генетика. При первичном осмотре врач анализирует жалобы, уточняет симптомы, устанавливает время их появления. Важно максимально точно описать все признаки и рассказать, какие были приняты меры для их устранения. Дополнительно уточняется наличие хронических и наследственных заболеваний, частота инфекционных и вирусных поражений организма. Врач обязательно собирает семейный анамнез, выясняя наличие синдрома у родственников.
Для оценки общего состояния здоровья пациента проводится осмотр: взвешивание, измерение роста, анализ соотношения показателей к возрастным нормам, измерение пульса, артериального давления, прослушивание сердцебиения, дыхания и пальпация живота.
Чтобы получить полную картину, врач назначает ряд лабораторных тестов и диагностических процедур.
- Общий анализ крови позволяет определить уровень тромбоцитов, лейкоцитов и эритроцитов. Часто при синдроме Швахмана-Даймонда наблюдается панцитопения – пониженное содержание всех кровяных клеток.
- Анализ кала дает возможность выявить стеаторею – высокое содержание жира в каловых массах.
- Биохимический анализ крови позволяет оценить ряд показателей, которые характеризуют состояние больного. В частности, это характер липидного, белкового, минерального и углеводного обмена.
- Общий анализ мочи проводится для определения количества белка, эритроцитов и лейкоцитов. Как правило, при заболевании все показатели значительно превышают норму.
- УЗИ органов брюшной полости необходимо для оценки состояния поджелудочной железы. Кроме того, такая процедура позволяет исключить другие патологии. С этой же целью проводится КТ или МРТ.
Лечение
В большинстве случаев выбранная терапия купирует симптомы и на короткое время облегчает состояние больного.
Лечение синдрома включает:
- соблюдение диеты, суть которой заключается в большом употреблении белковой пищи и ограничении жиров;
- заместительную терапию, которая устраняет дефицит ферментов поджелудочной железы;
- своевременное лечение инфекционных заболеваний антибактериальными препаратами.
Единственно верного и эффективного лечения синдрома Швахмана-Даймонда не существует.
Внимание!
Данная статья размещена исключительно в познавательных целях и не является научным материалом или профессиональным медицинским советом.
Записаться на прием к врачу
Источник
