Синдром гудпасчера по мкб 10
Содержание
- Описание
- Дополнительные факты
- Причины
- Симптомы
- Диагностика
- Лечение
- Прогноз
Названия
Название: Синдром Гудпасчера.

Синдром Гудпасчера
Описание
Синдром Гудпасчера. Аутоиммунная патология, характеризующаяся образованием аутоантител к базальным мембранам почечных клубочков и легочных альвеол. Клинически синдром Гудпасчера проявляется рецидивирующими легочными кровотечениями, прогрессирующим гломерулонефритом и почечной недостаточностью. Диагноз синдрома Гудпасчера подтверждается выявлением антител к базальной мембране клубочков (Anti GBM), данными биопсии почек и легких, рентгенологического исследования легких. Лечение синдрома Гудпасчера включает иммуносупрессивную терапию (глюкокортикостероиды, цитостатики), плазмаферез, по показаниям – гемодиализ, трансплантацию почек.
Дополнительные факты
Синдром Гудпасчера — иммуно-воспалительное поражение капилляров почек и легких, протекающее с развитием гломерулонефрита и геморрагического пневмонита. Впервые признаки данной патологии были описаны в 1919 г. Американским патофизиологом Э. У. Гудпасчером, за что болезнь и была названа его именем. В ревматологии синдром Гудпасчера относится к системным васкулитам и нередко обозначается как «геморрагический легочно-почечный синдром», «геморрагическая пневмония с гломерулонефритом», «идиопатический гемосидероз легких с нефритом». Частота развития синдрома Гудпасчера составляет 1 случай на 1 млн. Населения. Отмечается два возрастных пика заболеваемости – в 20-30 лет и 50-60 лет; болеют преимущественно мужчины. При отсутствии лечения синдрома Гудпасчера летальность среди пациентов достигает 75-90%.
Синдром Гудпасчера
Причины
Этиологические механизмы заболевания достоверно не определены. Клинические наблюдения указывают на связь развития синдрома Гудпасчера с перенесенной вирусной инфекцией (гриппом, вирусным гепатитом А и тд ), приемом лекарственных препаратов (карбимазола, пеницилламина), производственными вредностями (вдыханием паров органических растворителей, лаков, бензина), переохлаждением, курением. Отмечена генетическая предрасположенность к данному синдрому у лиц–носителей HLA-DRwl5, HLA-DR4 и HLA-DRB1 аллелей. Описаны семейные случаи синдрома Гудпасчера.
Под воздействием того или иного этиологического фактора, в результате изменения толерантности иммунной системы, в организме начинается выработка аутоантител к базальным мембранам легочных альвеол и почечных клубочков. Предполагается, что в роли аутоантигена выступает структурный компонент а-3 цепи коллагена IV типа, присутствующий в базальных мембранах легочных и почечных капилляров. Сформировавшиеся антитела (GВМ-антитела) в присутствии С3-комплемента связываются с антигенами; образовавшиеся иммунные комплексы откладываются вдоль базальных мембран, индуцируя иммуно-воспалительное поражение почечных клубочков (гломерулонефрит) и альвеол (альвеолит). В развитии аутоиммунного воспаления большая роль принадлежит активации клеточных элементов (Т-лимфоцитов, эндотелиоцитов, моноцитов, альвеолярных макрофагов, полиморфноядерных лейкоцитов), цитокинов (инсулиноподобного, тромбоцитарного факторов роста, факторов некроза опухоли, интерлейкина-1), свободных радикалов, протеолитических ферментов и других факторов, повреждающих почечную и легочную ткань.
Патоморфологическими субстратами синдрома Гудпасчера служат геморрагический некротизирующий альвеолит и нефрозонефрит. При гистологическом исследовании почечной ткани обнаруживается пролиферативно-мембранозный, пролиферативный или некротизирующий гломерулонефрит, склероз клубочков и фиброз почечной паренхимы. Морфологическое исследование легочной ткани выявляет капиллярит межальвеолярных перегородок, легочные инфильтраты, гемосидероз, пневмосклероз.
Симптомы
Выделяют три варианта клинического течения синдрома Гудпасчера: злокачественный, умеренный и медленный. Для злокачественного течения характерны рецидивирующая геморрагическая пневмония и стремительно прогрессирующий гломерулонефрит. При втором типе легочно-почечный синдром развивается медленнее и выражен умеренно. При третьем варианте синдрома Гудпасчера преобладают явления гломерулонефрита и ХПН; легочные проявления развиваются поздно.
Злокачественный вариант синдрома Гудпасчера дебютирует легочным кровотечением и острой почечной недостаточностью, требующими проведения интенсивной терапии (устранения водно-электролитных нарушений, возмещения кровопотери, ингаляций кислорода, ИВЛ, гемодиализа или перитонеального диализа). В других случаях заболевание может начинаться с общих симптомов: субфебрилитета, недомогания, похудания. Иногда появлению жалоб предшествует перенесенная ОРВИ. Из специфических симптомов обычно первыми развиваются признаки поражения легких — кашель, прогрессирующая одышка, цианоз, боль в грудной клетке, рецидивирующее кровохарканье или легочное кровотечение. Поражение легких при синдроме Гудпасчера нередко осложняется сердечной астмой и отеком легких.
Боль в грудной клетке. Кашель. Кровохарканье. Лейкоцитоз. Недомогание. Одышка. Увеличение СОЭ.
Диагностика
При осмотре пациентов с синдромом Гудпасчера обращает на себя внимание бледность кожных покровов, пастозность или отеки лица. В легких выслушиваются сухие и влажные хрипы, количество которых увеличивается в момент кровохарканья и после него. В общем анализе крови обнаруживается гипохромная анемия, анизоцитоз, пойкилоцитоз, лейкоцитоз, резкое увеличение СОЭ. Для общего анализа мочи характерна протеинурия, цилиндрурия, эритроцитурия; проба по Зимницкому выявляет изогипостенурию. В биохимическом анализе крови определяется нарастание уровня креатинина, мочевины, серомукоида; снижение концентрации железа. Для синдрома Гудпасчера типично обнаружение большого количества эритроцитов, сидерофагов и гемосидерина в общем анализе мокроты.
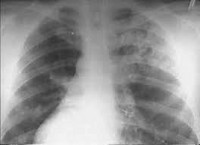
Наиболее чувствительным и специфичным методом диагностики синдрома Гудпасчера служит определение антител к базальной мембране клубочков (Anti-GBM) с помощью ИФА или РИА. На рентгенограммах легких выявляются множественные очаговые тени. Морфологическое подтверждение синдрома Гудпасчера основывается на данных биопсии легких и почек. Вспомогательное значение имеют результаты инструментальной диагностики: спирометрии, УЗИ почек, ЭКГ, ЭхоКГ.
В рамках проведения диагностических мероприятий необходимо исключить рак легких, туберкулез, бронхоэктазы, идиопатический гемосидероз легких, системную красную волчанку, узелковый периартериит, геморрагический васкулит, синдром Черджа-Стросс, гранулематоз Вегенера, микроскопический полиангиит, криоглобулинемию. Диагностика и лечение синдрома Гудпасчера должны проводиться совместными усилиями специалистов — ревматологов, пульмонологов, нефрологов.
Лечение
В остром периоде синдрома Гудпасчера показано назначение пульс-терапии метилпреднизолоном или комбинированной пульс-терапии (метилпреднизолон+циклофосфан) с последующим переводом на поддерживающую терапию после достижения клинико-лабораторной и рентгенологической ремиссии. С целью элиминации циркулирующих иммунных комплексов проводится плазмаферез. Симптоматическая терапия синдрома Гудпасчера включает переливания эритроцитарной массы и плазмы крови, назначение препаратов железа. При развитии терминальной почечной недостаточности применяются сеансы гемодиализа. Возможно выполнение нефрэктомии с последующей трансплантацией почки, однако это не исключает рецидива некротизирующего гломерулонефрита в трансплантате.
Прогноз
Течение синдрома Гудпасчера неуклонно прогрессирующее; прогноз – мало обнадеживающий. Гибель пациентов происходит, как правило, вследствие профузных легочных кровотечений, тяжелой почечной или дыхательной недостаточности. При злокачественном варианте летальный исход наступает в считанные недели. В остальных случаях средняя продолжительность жизни колеблется от нескольких месяцев до 1-3 лет. В литературе описаны единичные спонтанные ремиссии синдрома Гудпасчера.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 6 сентября 2018;
проверки требуют 8 правок.
Синдром Гудпасчера — системный капиллярит с преимущественным поражением альвеол лёгких и базальных мембран гломерулярного аппарата почек по типу геморрагических пневмонита и гломерулонефрита. Для СГ характерно бимодальное возрастное распределение заболеваемости с двумя пиками: первый в возрасте 20–30 с преобладанием у мужчин (страдают в три раза чаще[3][4]), характеризующийся более высокой частотой легочных кровотечений[5]. Второй пик характеризуется преобладанием женщин в возрасте 60–70 лет, страдающих почечнокаменной болезнью.[5]
Есть теория о наследственности болезни.[источник не указан 3088 дней]
Этиология и патогенез[править | править код]
Причина образования аутоантител против коллагена IV типа (к домену NC1 а3-цепи коллагена типа IV, необходимого для поддержания супраструктуры клубочков почек[3]) до сих пор неизвестна. Поскольку эпитопы (EA, EB[5][6]) коллагена, вызывающие образование антиколлагеновых антител, обычно находятся внутри молекулы гексамерного домена NC1, предполагается, что некоторые факторы окружающей среды демаскируют эпитопы[3][4], увеличивая связывание антител с a3 цепью до 15 раз[5]. Факторы возникновения заболевания неизвестны, однако отмечается связь с вирусной (в частности, вирус гриппа А[6]) и бактериальной инфекцией, переохлаждением, приёмом лекарственных препаратов (D-пенициллинамин[7], алемтузумаб[6], карбимазол), курением[6]. Первое описания болезни сделал американский врач и патофизиолог Э. У. Гудпасчер (E.W.Goodpasture) (1886–1960) во время эпидемии гриппа в 1919 году у 18-летнего юноши, у которого через месяц после перенесённого гриппа развились поражение почек в виде нефрита и пневмония, сопровождавшаяся кровохарканьем.
Клиника[править | править код]
Выделяют три варианта течения синдрома Гудпасчера:
- Злокачественный вариант характеризуется рецидивирующей геморрагической пневмонией и быстро прогрессирующим гломерулонефритом.
- С более медленным развитием изменений в почках и лёгких.
- С преобладанием прогрессирующего гломерулонефрита и быстрым развитием почечной недостаточности.
Начало острое с высокой лихорадкой, кровохарканьем или лёгочным кровотечением, одышкой. При аускультации отмечается рассеянные сухие и влажные хрипы в средних и нижних отделах лёгких.[8] При рентгенографии определяются рассеянные очаги уплотнения легочной ткани[3], либо множественные затемнения с нечеткими контурами[9], инфильтраты определяются в обоих лёгких, чаще в прикорневой и срединной зонах. Тяжёлый, прогрессирующий гломерулонефрит развивается почти одновременно, быстро приводя к почечной недостаточности. Повторные кровохарканье и потеря крови с мочой ведут, как правило, к анемии, усугубляющейся при почечной недостаточности. При лабораторном исследовании: анемия, увеличение количества лейкоцитов в крови и повышенная СОЭ. Характерным иммунологическим признаком болезни является наличие антител к базальным мембранам почки. Прогноз обычно неблагоприятен — смерть наступает в течение 12 месяцев от начала болезни при явлениях лёгочно-сердечной или почечной недостаточности.
Также имели место случаи с быстрым прогрессированием заболевания. Стадии от лихорадки до предсмертного состояния проходили в течение недели.
Изредка заболевание может начаться с поражения почек, а поржаение легких развивается лишь в конце, при этом поражение легких протекает без кровохарканья или оно скудное.[10]
Лечение[править | править код]
Для успешного лечения важна своевременная диагностика и ликвидация причинного фактора. Назначаются кортикостероиды в больших дозах (метилпреднизолон) в сочетании с цитостатическими препаратами (циклофосфамид). При сопутствующей анемии: препараты эритропоэтина, колониостимулирующие факторы, препараты железа. Успешно применяется плазмаферез и иммуноабсорбция.
- ↑ Disease Ontology release 2019-05-13 — 2019-05-13 — 2019.
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 3 4 Robbins and Cotran pathologic basis of disease.. — 8th ed.. — Philadelphia, PA: Saunders/Elsevier, 2010. — xiv, 1450 pages с. — ISBN 978-1-4160-3121-5, 1-4160-3121-9, 978-0-8089-2402-9, 0-8089-2402-8, 978-1-4377-0792-2, 1-4377-0792-0.
- ↑ 1 2 Billy G. Hudson, Karl Tryggvason, Munirathinam Sundaramoorthy, Eric G. Neilson. Alport’s Syndrome, Goodpasture’s Syndrome, and Type IV Collagen (англ.) // New England Journal of Medicine. — 2003-06-19. — Vol. 348, iss. 25. — P. 2543–2556. — ISSN 1533-4406 0028-4793, 1533-4406. — doi:10.1056/NEJMra022296.
- ↑ 1 2 3 4 Patrick Nachman, Ashley Henderson. Pathogenesis of Lung Vasculitis (англ.) // Seminars in Respiratory and Critical Care Medicine. — 2011-06. — Vol. 32, iss. 03. — P. 245–253. — ISSN 1098-9048 1069-3424, 1098-9048. — doi:10.1055/s-0031-1279822.
- ↑ 1 2 3 4 Antonio Greco, Maria Ida Rizzo, Armando De Virgilio, Andrea Gallo, Massimo Fusconi. Goodpasture’s syndrome: A clinical update (англ.) // Autoimmunity Reviews. — 2015-03. — Vol. 14, iss. 3. — P. 246–253. — doi:10.1016/j.autrev.2014.11.006.
- ↑ Болезни органов дыхания: Руководство для врачей В 4 томах. Частная пульмонология. / под ред. Палеева Н. Р.. — М.: Медицина, 1990. — Т. 4. — С. 49—50. — ISBN 5-225-01159-4.
- ↑ Кумар В, Аббас А. К. Основы патологии заболеваний по Роббинсу и Котрану. — Логосфера, 2016. — Т. 2. — С. 806—807, 1037—1038, 1045. — ISBN 978-5-98657-053-2.
- ↑ Шабалов Н. П. Детские болезни: учебник для вузов. — 6-е изд. — Питер, 2011. — Т. 1. — С. 497, 499. — ISBN 978-5-459-00609-4. — ISBN 978-5-459-00608-7.
- ↑ В. Е. Кочетов. К вопросу отдельных форм легочных геморрагических синдромов // Вестник экстренной медицины. — 2019. — Т. 12, вып. 2. — ISSN 2010-9881.
Источник
- Описание
- Причины
- Симптомы (признаки)
- Диагностика
- Лечение
Краткое описание
Синдром Гудпасчера — аутоиммунное заболевание, характеризующееся присутствием АТ к коллагену типа IV c a — 3 — цепью (Гудпасчера Аг). Указанный Аг входит в состав базальной мембраны почечных клубочков и альвеолярной мембраны, поэтому основными клиническими проявлениями синдрома Гудпасчера выступают лёгочное кровотечение и прогрессирующий гломерулонефрит. Статистические данные. Распространённость: 0,5 на 1 000 000. Возраст: 5–40 лет. Преобладающий пол — мужской (6:1).
Код по международной классификации болезней МКБ-10:
- M31.0 Гиперчувствительный ангиит
Причины
Этиология неизвестна. К факторам риска относят: курение, респираторную инфекцию, контакт с летучими углеводородами.
Генетические аспекты. Выявлена ассоциация с HLA DRw2.
Патоморфология • Почки •• Эпителиальноклеточные полулуния •• Сморщивание почечных клубочков •• Интерстициальный воспалительный экссудат • Лёгкие •• Внутриальвеолярные кровоизлияния •• Макрофаги, нагруженные гемосидерином •• Фиброз межальвеолярных перегородок.
Симптомы (признаки)
Клиническая картина • Поражение лёгких (опережает поражение почек на несколько недель или месяцев); варьирует от небольшой одышки до повторных лёгочных кровотечений с развитием дыхательной недостаточности • Быстропрогрессирующий гломерулонефрит с развитием почечной недостаточности • Артериальная гипертензия (20%) • Гриппоподобный синдром: лихорадка, миалгии, артралгии, слабость.
Диагностика
Лабораторные данные • ОАК •• гипохромная ЖДА • ОАМ •• микрогематурия •• протеинурия, не достигающая нефротического порога • АТ против Аг базальной мембраны клубочков почек (радиоиммунный метод или метод непрямой иммунофлюоресценции) • Перинуклеарные антинейтрофильные АТ.
Инструментальные данные • Биопсия почек — отложения иммуноглобулинов и комплемента в базальной мембране клубочков, экстракапиллярные полулуния в 50% клубочков • Рентгенография органов грудной клетки — летучие асимметричные облаковидные инфильтраты; деструкция лёгких не характерна.
Дифференциальная диагностика • Гранулематоз Вегенера протекает с деструкцией лёгочной ткани и поражением верхних дыхательных путей • Микроскопический полиангиит, помимо лёгочного и почечного синдромов, имеет и другие (множественный мононеврит, кожные изменения) • Тромбоз почечных вен и ТЭЛА (острое развитие, отсутствие иммунологической активности) • Быстропрогрессирующий гломерулонефрит, осложнённый отёком лёгких.
Лечение
ЛЕЧЕНИЕ
Общая тактика предполагает сочетание плазмафереза, активной иммунодепрессивной терапии и методов коррекции почечной функции. Диета соответствует диете при почечной недостаточности.
Лекарственное лечение • ГК •• Пульс — терапия метилпреднизолоном 30 мг/кг/сут в/в капельно в течение 20–30 мин 3 дня подряд •• Преднизолон после пульс — терапии в дозе 2 мг/кг внутрь до клинического эффекта с постепенным снижением дозы: до 1,75 мг/кг в течение 1 мес, 1,5 мг/кг в течение 3 мес, далее каждую дозу назначают по 6 мес (1,25–1,0–0,75–0,5–0,25 мг/кг), далее каждую дозу назначают по 12 мес (0,125–0,0625 мг/кг). Больным старше 60 лет дозу следует снизить на 25%.
• Цитотоксические иммунодепрессанты применяют в комбинации с ГК •• Циклофосфамид 2–3 мг/кг/сут •• Азатиоприн 1–2мг/кг/сут. Примечания: дозу препарата следует уменьшить на 50% при снижении СКФ до 10 мл/мин; необходим контроль за количеством лейкоцитов и тромбоцитов крови.
Немедикаментозная терапия • Плазмаферез ежедневно или через день в сочетании с иммунодепрессивной терапии в течение 1–2 нед • Гемодиализ — при развитии почечной недостаточности.
Хирургическое лечение • Трансплантация почки в терминальной стадии ХПН. Рецидива заболевания в трансплантате не наблюдают, если перед операцией в крови не обнаруживались АТ к базальной мембране клубочков.
Прогноз неблагоприятен, если на момент постановки диагноза (до начала лечения) уже имеются признаки почечной недостаточности.
Синоним. Синдром лёгочно — почечный наследственный.
МКБ-10 • M31.0 Гиперчувствительный ангиит
Источник
Рубрика МКБ-10: M31.0
МКБ-10 / M00-M99 КЛАСС XIII Болезни костно-мышечной системы и соединительной ткани / M30-M36 Системные поражения соединительной ткани / M31 Другие некротизирующие васкулопатии
Определение и общие сведения[править]
Гломерулонефрит, обусловленный антителами к гломерулярной базальной мембране
Синонимы: синдром Гудпасчера
Гломерулонефрит, обусловленный антителами к гломерулярной базальной мембране представляет собой быстро прогрессирующее и обычно молниеносное редкое аутоиммунное заболевание, характеризующееся наличием антител к гломерулярной базальной мембране и поражающее гломерулярные и/или легочные капилляры. Заболевание может проявляться как изолированный гломерулонефрит (анти-ГБМ нефрит) или как легочно-почечный синдром с тяжелым кровоизлиянием легких (синдром Гудпасчера).
Этиология и патогенез[править]
В настоящее время его причиной считают выработку цитотоксических антител к базальной мембране клубочков, обусловленную разными факторами (синдром Гудпасчера был описан как осложнение гриппа). Показано, что эти антитела связываются с альфа3-цепью коллагена типа IV. Болеют чаще мужчины в возрасте 10—50 лет. Женщины составляют менее 30% больных. Описаны семейные случаи заболевания.
Клинические проявления[править]
Более чем у 90% больных наблюдается кровохарканье. Одновременно с ним или несколько раньше развивается гломерулонефрит. Кроме того, у 57% больных наблюдается одышка, у 51% — повышенная утомляемость, у 41% — кашель, у 22% — лихорадка. У 20% больных заболеванию предшествует острое респираторное заболевание. При физикальном исследовании у 50% больных отмечается бледность, у 37% — влажные и сухие хрипы, у 25% — отеки. Кроме того, иногда наблюдаются незначительное повышение АД, кровоизлияния и экссудаты на сетчатке.
Гиперчувствительный ангиит: Диагностика[править]
Лабораторные исследования
Наиболее чувствительный и специфичный метод диагностики синдрома Гудпасчера — определение антител к базальной мембране клубочков с помощью РИА или твердофазного ИФА. У 98% больных наблюдается железодефицитная анемия, у 50% выявляется лейкоцитоз, у 88% — протеинурия, более чем у 70% — эритроциты, лейкоциты и зернистые цилиндры в моче. У 10% больных на ранней стадии заболевания изменения в моче отсутствуют. У большинства больных в сыворотке постепенно нарастает уровень креатинина.
Рентгенография грудной клетки
На ранних стадиях заболевания у 90% больных выявляются множественные очаговые тени, обусловленные скоплением крови в альвеолах. Если легочное кровотечение продолжается, тени увеличиваются, становятся более выраженными. Через несколько суток после остановки кровотечения рентгенологическая картина нормализуется. Из-за повторных кровотечений и отложения гемосидерина в легких развивается пневмосклероз.
Исследование функции внешнего дыхания
Исследование функции внешнего дыхания обычно выявляет рестриктивные нарушения. В отсутствие кровотечения диффузионная способность легких снижена. При продолжающемся кровотечении скопившаяся в альвеолах кровь связывает окись углерода, используемую в исследовании, в результате чего диффузионная способность легких оказывается завышенной.
Иммунологические исследования
Антитела к базальной мембране клубочков связываются с C-концевым участком альфа3-цепи коллагена типа IV. Иммунный ответ развивается при нарушении трехмерной структуры коллагена, вызванном инфекцией или интоксикацией. Связывание антител с базальной мембраной клубочков приводит к активации комплемента, миграции нейтрофилов и повреждению клубочков.
Гистологическое исследование
1. Легкие. Во время обострения в альвеолах обнаруживают кровь. При длительном течении заболевания в легких выявляются содержащие гемосидерин макрофаги, неповрежденные альвеолярные и эндотелиальные клетки и пневмосклероз. Васкулит не характерен. При электронной микроскопии определяются широкие щели между эндотелиальными клетками и повреждение базальной мембраны. При иммунофлюоресценции можно выявить линейные отложения IgG и комплемента в базальной мембране альвеол.
2. Почки. Наблюдается картина острого гломерулонефрита. При электронной микроскопии обнаруживается пролиферация и набухание клеток эндотелия, утолщение базальной мембраны клубочков и отложение фибрина в субэндотелиальном слое. При иммунофлюоресценции выявляются линейные отложения IgG в базальной мембране клубочков.
Диагностика
1. Предварительный диагноз ставят при сочетании легочного кровотечения, гломерулонефрита и железодефицитной анемии. В отсутствие одновременного поражения легких и почек диагностика затруднена.
2. Окончательный диагноз
а. Исследование биоптатов почек методом иммунофлюоресценции необходимо проводить при первых признаках поражения почек. Это позволяет поставить диагноз на ранней стадии заболевания, определить тяжесть и распространенность поражения.
б. Антитела к базальной мембране клубочков в сыворотке определяют с помощью РИА или твердофазного ИФА. Это чувствительные и надежные методы диагностики синдрома Гудпасчера, применяемые и для оценки эффективности лечения. Лечение начинают, не дожидаясь результатов данного исследования, поскольку до их получения может пройти несколько суток.
в. Биопсия легкого. Трансбронхиальная биопсия информативна только в том случае, когда получено достаточное количество материала для исследования. Для оценки эффективности лечения в динамике ее обычно не проводят, для этого используют чрескожную биопсию почки.
Дифференциальный диагноз[править]
Исключают идиопатический гемосидероз легких, отек легких, острый гломерулонефрит, пневмококковую и вирусную пневмонию, осложненную гломерулонефритом, узелковый периартериит, гранулематоз Вегенера, СКВ. Характерное для синдрома Гудпасчера поражение легких и почек может наблюдаться в отсутствие антител к базальной мембране клубочков. Возможно, оно обусловлено иными иммунными механизмами.
Гиперчувствительный ангиит: Лечение[править]
1. Общие мероприятия. Нередко требуется неотложная помощь — переливание компонентов крови, устранение водно-электролитных нарушений, ингаляция кислорода, интубация трахеи, ИВЛ, перитонеальный диализ и гемодиализ.
2. Иммуносупрессивная терапия. Проводят плазмаферез, одновременно с ним назначают преднизон, 1 мг/кг/сут внутрь, и циклофосфамид, 1—2 мг/кг/сут внутрь. Плазмаферез позволяет удалить антитела из сыворотки, а кортикостероиды и иммунодепрессанты подавляют продукцию этих антител. При ОПН (но не в терминальной стадии ХПН) кортикостероиды и циклофосфамид вводят в/в струйно. На фоне лечения легочное кровотечение быстро прекращается, при его рецидивах повторно проводят плазмаферез. Плазмаферез продолжают до полной стабилизации функции почек и исчезновения антител к базальной мембране клубочков. Через несколько суток или недель после начала лечения нормализуются рентгенологическая картина и показатели функции внешнего дыхания. ХПН может прогрессировать даже на фоне лечения. Монотерапия кортикостероидами эффективна при легочном кровотечении, но не влияет на течение гломерулонефрита.
Прогноз
В отсутствие лечения 75% больных умирают от ХПН, 25% — от легочного кровотечения. То же касается и неправильного режима лечения: применения иммунодепрессантов в низких дозах или коротким курсом. Однако раннее проведение плазмафереза и длительное лечение преднизоном и циклофосфамидом значительно улучшают состояние больных и несколько снижают летальность.
Профилактика[править]
Прочее[править]
Кожный лейкоцитокластический ангиит
Синонимы: гиперчувствительный ангиит, кожный лейкоцитокластический васкулит, кожный гиперчувствительный васкулит
Кожный лейкоцитокластический ангиит — это васкулит мелких сосудов, который проявляется пальпируемой пурпурой и уртикарной сыпью, которые наиболее часто поражают нижние конечности. При заболевании также могут наблюдаться системные симптомы, включая лихорадку, кашель, кровохарканье, синусит, артралгии, артрит, миалгии, боли в животе, диарею, гематоцезию, парестезию, слабость и гематурию.
Биопсия кожи выявляет экссудаты, богатые нейтрофилами, повреждение эндотелия, отложение фибрина и лейкоцитоклазию в посткапиллярных венулах мелких сосудов.
Кожный лейкоцитокластический ангиит может быть идиопатическим (до 50% случаев) или вторичным по отношению к инфекциям, лекарственной терапии (например противотуберкулезные препараты), коллагеновым сосудистым заболеваниям или новообразованиям.
Источники (ссылки)[править]
Дополнительная литература (рекомендуемая)[править]
1. Kalluri R. et al. Goodpasture’s syndrome, localization of the epitope for the autoantibodies to the carboxyl-terminal region of the alpha 3(IV) chain of basement membrane collagen. J. Biol. Chem. 266:24018, 1991.
2. McCormick J. R. et al. Goodpasture’s syndrome. Comp. Ther. 13:25, 1987.
Действующие вещества[править]
Источник
