Синдром франческетти код мкб 10

Синдром Тричера Коллинза – Франческетти
Синдром Тричера Коллинза – Франческетти (мандибуло-фациальный дизостоз, челюстно-лицевой дизостоз, синдром Томпсона, TCOF, МКБ 10 – Q75.4) — редкое аутосомно-доминантное заболевание, для которого характерно нарушение черепно-лицевого развития. Проявляется рядом врожденных челюстно-лицевых дефектов, в их числе арковидное нёбо или расщелина нёба, большая ротовая щель и отсутствие ресниц на нижнем веке, дефект слухового прохода, приводящий к кондуктивной тугоухости. Молекулярно-генетической причиной заболевания являются мутации гена TCOF1, реже — генов POLR1C или POLR1D. Лечение включает хирургические методы, слухопротезирование и регулярные занятия с сурдопедагогом.
Впервые болезнь описал в 1846 г. британский врач А. Томпсон (A. Thompson). В 1900 г. британский хирург Эдвард Тричер Коллинз (Edward Treacher Collins) представил на заседании офтальмологического общества в Лондоне двух пациентов с характерными для болезни симптомами [1]. Термин «мандибуло-фациальный дизостоз» предложил в 1944 г. швейцарский офтальмолог Адольф Франческетти (Adolphe Franceschetti).
В 1996 г. было установлено, что молекулярно-генетической причиной заболевания в большинстве случаев является мутация в гене TCOF1 [6].
Распространенность и тип наследования
Для пациентов с синдромом Тричера Коллинза – Франческетти характерен ряд врожденных челюстно-лицевых дефектов. Это антимонголоидный разрез глаз (раскосые глаза, направленные вниз), гипоплазия нижней челюсти, дефект нижних век, аномалии ушных раковин, дефект слухового прохода, приводящий к кондуктивной тугоухости, двусторонняя гипоплазия скуловых костей и орбит, арковидное нёбо или расщелина нёба, большая ротовая щель и отсутствие ресниц на нижнем веке [4]. Лицевые кости у большинства пациентов слаборазвитые. Это приводит к формированию «затонувшего» типа лица: крупный нос и очень маленькие челюсти и подбородок. У некоторых больных присутствует «волчья пасть». В ряде случаев отмечаются рост волос на щеках, дефект верхнего века и радужной оболочки глаз.
Диагноз может быть установлен как во время беременности, так и после рождения. Диагностика для пациентов с характерным внешним видом включает исследование слуха, компьютерную томографию височных костей, анализ мутаций генов TCOF1, POLR1C и POLR1D [5].
Лечение синдрома Тричера Коллинза – Франческетти включает в себя хирургические операции, направленные на устранение дефектов лица (с целью улучшения внешнего вида и качества жизни пациента), стоматологическое лечение (в том числе ортодонтическое, направленное на исправление прикуса). Пациентам имплантируют слуховые аппараты костного проведения звука. Детям с мандибуло-фациальным дизостозом необходимы регулярные занятия с сурдопедагогом и логопедом.
Прогноз для пациентов, как правило, благоприятный. Важно как можно раньше провести слухопротезирование, чтобы избежать отставания ребенка в речевом и общем развитии. Существенную роль играют также регулярные занятия с сурдопедагогом и психологическая поддержка родителей ребенка [3].
Молекулярно-генетической причиной заболевания в 78–93 % случаев является мутация в гене TCOF1, кодирующем ядерный транспортный фосфопротеин. Этот белок принимает участие в транскрипции ДНК. Ген TCOF1 представлен во многих тканях организма во время эмбрионального и постэмбрионального развития. Нонсенс-мутация в гене TCOF1, приводящая к возникновению преждевременного стоп-кодона, ведет к нарушению синтеза белка. В результате вырабатывается недостаточное для нормального функционирования организма количество ядерного транспортного фосфопротеина [2], что способствует нарушению черепно-лицевого развития.
В 8 % случаев мандибуло-фациальный дизостоз связан с мутациями в генах POLR1C или POLR1D, кодирующих субъединицы I и III РНК-полимеразы. При мутации генов POLR1C или POLR1D происходит нарушение процесса транскрипции ДНК из-за недостаточного количества фермента РНК-полимеразы, что также способствует нарушению черепно-лицевого развития.
- Treacher Collin E, Cases with symmetrical congenital notches in the outer part of each lid and defective development of the malar bones, 1900, Trans Ophthalmol Soc UK, 20, p. 190—192
- Chiara Conte, Maria Rosaria D’Apice, Fabrizio Rinaldi, Stefano Gambardella, Federica Sangiuolo and Giuseppe Novelli (2011 Sep 27). Novel mutations of TCOF1 gene in European patients with Treacher Collins syndrome. BMC Med Genet. 12
- Козлова С. И., Демикова Н. С. Наследственные синдромы и медико-генетическое консультирование. – М.: КМК, 2007 – 448 с.
- Кеннет Л. Джонс Наследственные синдромы по Девиду Смиту. Атлас-справочник. Москва, Практика, 2011
- Кадышев В. В., Бессонова Л. А., Зинченко Р. А. Распространенность синдрома Тричер Коллинз-Франческетти в Кировской области. Медицинская генетика, 2009 г. Том 8. №12 (90) , 2009
- Treacher Collins Syndrome Collaborative Group. Positional cloning of a gene involved in the pathogenesis of Treacher Collins syndrome. Nature Genet. 12: 130-136, 1996
- База данных Orphanet
Источник
Медицинский эксперт статьи

х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
При внутриутробных нарушениях процессов развития костей возникают серьезные черепно-лицевые деформации, и одной из разновидностей такой патологии является синдром Тричер Коллинза (TCS) или мандибулофасциальный, то есть челюстно-лицевой дизостоз.
Код заболевания по МКБ 10: класс XVII (врожденные аномалии, деформации и хромосомные нарушения), Q75.4 — mandibulofacial dysostosis.
Код по МКБ-10
Q75.4 Челюстно-лицевой дистоз
Эпидемиология
Распространенность синдрома Тричер Коллинза находится в диапазоне – один случай на 25- 50 тыс. новорожденных обоего пола (хотя британские медики отмечают, что патология выявляется у одного младенца из 10-15 тыс.).
 [1], [2], [3], [4], [5]
[1], [2], [3], [4], [5]
Причины синдрома Тричер Коллинза
Данный синдром получил имя выдающегося британского офтальмолога Эдварда Тричер Коллинза, описавшего основные черты патологии более ста лет назад. Однако европейские врачи чаще называют этот вид аномалии костей лица и челюстей болезнью или синдромом Франческетти – на основании обширных исследований швейцарского офтальмолога Адольфа Франческетти, который ввел термин «мандибулофасциальный дизостоз» в середине прошлого века. В медицинских кругах также используется название – синдром Франческетти-Коллинза.
Причины синдрома Тричер Коллинза – мутации гена TCOF1 (в локусе хромосомы 5q31.3-33.3), который кодирует ядрышковый фосфопротеин, отвечающий за формирование черепно-лицевой части эмбриона человека. В результате преждевременного уменьшения количества этого белка нарушаются биогенез и функции рРНК. По мнению генетиков исследовательской программы Human Genome, эти процессы приводят к сокращению пролиферации эмбриональных клеток нервного гребня – валика вдоль нервного желоба, который в ходе развития зародыша замыкается в нервную трубку.
Формирование тканей лицевой части черепа происходит благодаря трансформации и дифференциации клеток верхней (головной) части нервного гребня, которые мигрируют вдоль нервной трубки в область первой и второй жаберных дуг зародыша. И дефицит этих клеток вызывает черепно-лицевые деформации. Критический период возникновения аномалий – с 18 по 28 день после оплодотворения. По завершении миграции клеток нервного гребня (на четвертой неделе гестации) образуются практически все рыхлые мезенхимальные ткани в области лица, которые позже (с 5 по 8 недели) дифференцируются в скелетные и соединительные ткани всех частей лица, шеи, гортани, уха (в том числе внутреннего) и будущих зубов.
 [6], [7], [8], [9]
[6], [7], [8], [9]
Патогенез
Патогенез синдрома Тричер Коллинза часто имеет семейный характер, и аномалия наследуется по аутосомно-доминантному принципу, хотя бывают случаи аутосомно-рецессивной передачи дефекта (при мутациях других генов, в частности, POLR1C и POLR1D). Самым непредсказуемым в челюстно-лицевом дизостозе является то, что мутация наследуется детьми только в 40-48% случаев. То есть у 52-60% пациентов причины синдрома Тричер Коллинза не связаны с наличием аномалии в роду, и, как полагают, патология возникает в результате спорадических генных мутаций de novo. Вероятнее всего, новые мутации представляют собой последствия тератогенного воздействия на плод во время беременности.
В числе тератогенных причин данного синдрома специалисты называют большие дозы этанола (этилового спирта), радиацию, сигаретный дым, цитомегавирус и токсоплазму, а также гербициды на основе глифосата (Раундал, Глифор, Торнадо и др.). А в список ятрогенных факторов попали препараты от угрей и себореи с 13-цис-ретиноевой кислотой (Изотретиноин, Аккутан); противосудорожное лекарство Фенитоин (Дилантин, Эпанутин); психотропные средства Диазепам, Валиум, Реланиум, Седуксен.
 [10], [11], [12], [13], [14], [15], [16], [17], [18]
[10], [11], [12], [13], [14], [15], [16], [17], [18]
Симптомы синдрома Тричер Коллинза
По большей части, клинические признаки мандибулофасциального дизостоза и степень их выраженности зависят от особенностей проявления генных мутаций. И первые признаки данной аномалии в большинстве случаев видны у ребенка сразу же после его появления на свет: лицо при синдроме Тричер Коллинза имеет характерный вид. Причем морфологические аномалии обычно двусторонние и симметричные.
Наиболее очевидные симптомы синдрома Тричер Коллинза:
- недоразвитость (гипоплазия) лицевых костей черепа: скуловых, скуловых отростков лобной кости, боковых крыловидных пластинок, придаточных пазух носа, нижней челюсти и выступов костных эпифизов (мыщелков);
- недоразвитие костей нижней челюсти (микрогнатия) и более тупой чем обычно нижнечелюстной угол;
- нос имеет нормальный размер, однако, кажется большим из-за гипоплазии надбровных дуг и недоразвитости или отсутствия скуловых дуг в области висков;
- глазные щели нисходящие, то есть разрез глаз аномальный, с опущенными вниз наружными уголками;
- дефекты нижних век (колобома) и частичное отсутствие ресниц на них;
- ушные раковины неправильной формы с широким диапазоном отклонений, вплоть до их расположения в углу нижней челюсти, отсутствия мочек, слепых свищей между козелком уха и углом рта и др.;
- сужение или заращение (атрезия) наружного слухового каналов и аномалии косточек среднего уха;
- отсутствие или гипоплазия околоушных слюнных желез;
- фарингеальная гипоплазия (сужение глотки и дыхательных путей);
- несращение твердого нёба (волчья пасть), а также отсутствие, укорочение или неподвижность мягкого неба.
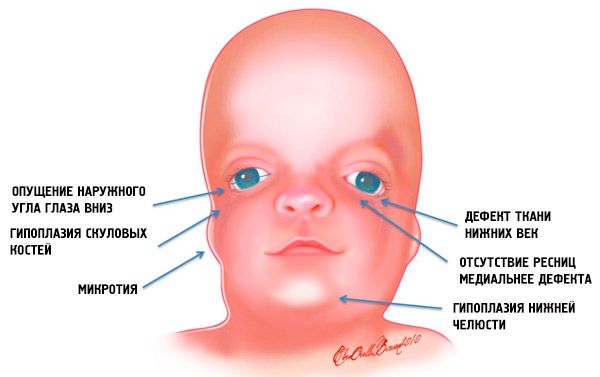
Такие анатомические аномалии во всех случая имеют осложнения. Это функциональные нарушения слуха в виде проводящей (кондуктивной) тугоухости или полной глухоты; нарушения зрения из-за неправильно формирования глазных яблок; дефекты нёба вызывают трудности с кормлением и глотанием. Имеются связанные с дефектами челюстей нарушения окклюзии зубов (неправильный прикус), что, в свою очередь, вызывает проблемы с жеванием и артикуляцией. Патологии мягкого неба объясняют гнусавость голоса.
Осложнения и последствия
Последствия челюстно-лицевых аномалий при синдроме Тричер Коллинза проявляются в том, что при рождении ребенка его интеллектуальные способности нормальные, но из-за дефектов слуха и других нарушений отмечается вторичная задержка умственного развития.
Кроме того, дети с такими дефектами остро чувствуют свою ущербность и страдают, что негативно сказывается на их нервной системе и психике.
 [19], [20], [21]
[19], [20], [21]
Диагностика синдрома Тричер Коллинза
Постнатальная диагностика синдрома Тричер Коллинза, по существу, проводится на основании клинических признаков. Челюстно-лицевой дизостоз легко определяется при полный экспрессивности синдрома, но когда присутствуют минимально выраженные симптомы патологии, с постановкой правильного диагноза могут возникнуть проблемы.
При этом особого внимания требует оценка всех связанных с аномалиями функций, особенно тех, что затрагивают дыхание (в связи с угрозой апноэ во сне). Также проводится оценка и мониторинг эффективности кормления и насыщения гемоглобина кислородом.
В дальнейшем — на 5-6 день после рождения — предстоит выяснить степень повреждений слуха с помощью аудиологического тестирования, которое должно проводиться еще в родильном доме.
Назначается обследование, в ходе которого инструментальная диагностика проводится рентгеноскопией черепно-лицевой дисморфологии; пантомографией (панорамным рентгеном костных структур лицевого черепа); полной черепной компьютерной томографией в различных проекциях; КТ или МРТ головного мозга для определения состояния внутреннего слухового прохода.
Самое раннее – пренатальное – диагностирование челюстно-лицевых аномалий при наличии синдрома Тричер Коллинза в семейном анамнезе возможно путем биопсии ворсин хориона на 10-11 неделе беременности (процедура угрожает выкидышем и занесением инфекции в матку).
Также берутся анализы крови членов семьи; на 16-17 неделе беременности берется анализ околоплодных вод (трансабдоминальный амниоцентез); на 18-20 неделях беременности проводится фетоскопия и берется кровь из плодовых сосудов плаценты.
Но чаще всего в дородовой диагностике данного синдрома у плода используется УЗИ (на 20-24 неделях беременности).
 [22], [23]
[22], [23]
Какие анализы необходимы?
Дифференциальная диагностика
Этими же методами специалисты пользуются, когда нужна дифференциальная диагностика, чтобы распознать неярко выраженный синдром Тричер Коллинза и отличить его от других врожденных аномалий черепно-лицевых костей, в частности: синдромов Апера, Крузона, Нагера, Петерс-Хевельса, Хеллермана-Штефа, а также с гемифациальной микросомии (синдрома Гольденхара), гипертелоризма, преждевременного заращения швов черепа (краниостеноза) или нарушения сращения лицевых костей (краниосиностоза).
 [24], [25], [26], [27]
[24], [25], [26], [27]
Лечение синдрома Тричер Коллинза
Как и во всех случаях, генетически обусловленных врожденных дефектов, лечение синдрома Тричер Коллинза в тяжелых формах носит исключительно паллиативный характер, поскольку терапевтических методов при таких патология просто не существует. Спектр и степень деформаций при данном синдроме обширны и, следовательно, характер и интенсивность врачебного вмешательства также имеет множество вариантов.
Для коррекции и улучшения слуха используются слуховые аппараты, для улучшения речи – занятия с логопедом.
Хирургические вмешательства требуются в раннем возрасте в тяжелых случаях сужения дыхательных путей (проводят трахеостомию) и гортани (выполняется гастростоммия для кормления) Также может потребоваться оперативная коррекция нёба.
Операции по удлинению нижней челюсти выполняются в возрасте 2-3 лет или позже. Реконструкция мягких тканей включает в себя коррекцию колобомы нижнего века и пластику ушных раковин.
Профилактика
Профилактика синдрома Тричер Коллинза состоит в посещении будущими родителями генетической консультации, а при семейном анамнезе синдрома возникает вопрос о возможности самой беременности – во избежание рождения ребенка с черепно-лицевыми аномалиями.
 [28], [29], [30], [31]
[28], [29], [30], [31]
Прогноз
Каким может быть прогноз при данной патологии? Это зависит от степени деформаций и интенсивности симптоматики. Синдром Тричер Коллинза – это пожизненный диагноз.
 [32], [33], [34], [35]
[32], [33], [34], [35]
Источник

Синдром Тричера Коллинза – это генетическая (иногда наследственная) болезнь, сопровождающаяся деформациями костей и мягких тканей лица. К симптомам относятся грубые дефекты строения лица: антимонголоидный разрез глаз, вырезки ткани век (колобомы), уменьшенные размеры челюсти и скул, гипоплазия и аномалии структур уха, расщелина или арковидная форма неба, увеличенные размеры ротовой щели и языка, слаборазвитые кости лица. Диагноз устанавливается по данным клинического осмотра, биогенетического теста и семейного анамнеза. Лечение симптоматическое, направлено на улучшение слуха, устранение жизнеугрожающих деформаций и косметических дефектов хирургическим способом.
Общие сведения
У синдрома Тричера Коллинза есть несколько синонимов: челюстно-лицевой дизостоз, синдром Тричера Коллинза-Франческетти, мандибулофациальный дизостоз. Впервые патологию описал офтальмолог из Великобритании Эдвард Тричер Коллинз в 1900 году, поэтому наиболее распространено название, соответствующее его имени. Обширный обзор заболевания был сделан в 1949 году европейскими исследователями Э. Франческетти и Д. Клейном. В настоящее время понятие «синдром Тричера Коллинза» более распространено в Великобритании и США, а термин «синдром Франческетти-Клейна» чаще используется в странах Европы. Эпидемиология болезни составляет 1:50 000. Среди мальчиков и девочек заболеваемость одинакова.
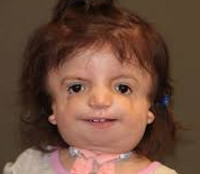
Синдром Тричера-Коллинза
Причины
Развитие синдрома в 78-93% случаев обусловлено мутациями гена TCOF1, расположенного на пятой хромосоме в регионе 5q32. Данный ген кодирует производство ядерного фосфопротеина Treacle. У 7-9% пациентов причиной заболевания является дефект гена POLR1C, локализованного на шестой хромосоме, или гена POLR1D, находящегося на тринадцатой хромосоме. Они ответственны за синтез I и III РНК-полимеразы.
При мутациях в гене TCOF1 тип наследования синдрома аутосомно-доминантный с показателем пенетрантности 90%. Это означает, что при мутации в одной хромосоме из пары вероятность проявления болезни очень высока. У больного родителя риск рождения ребенка с синдромом Тричера Коллинза составляет 50%. Возможна наследственная передача дефекта и спорадические генетические изменения (новые мутации). Экспрессивность мутации переменная – в пределах одной семьи вероятно как ослабление, так и усиление симптомов заболевания у последующих поколений. При дефектах генов POLR1C и POLR1D наследование происходит по аутосомно-рецессивному типу. В парах, где родитель имеет синдром, вероятность рождения больного малыша составляет 25%.
Патогенез
Пятая хромосома ответственна за правильное формирование скелета в период внутриутробного развития. Локализованный в ней ген TCOF1 кодирует структуру и синтез ядерного транспортного белка Treacle. Данный протеин экспрессируется в большинстве тканей организма в эмбриональном и постэмбриональном периоде, участвует в переносе генетической информации с ДНК на РНК.
В основе синдрома чаще всего лежит нонсенс-мутация, приводящая к образованию преждевременного кодона терминации и развитию гаплонедостаточности – дефицита белка, необходимого для нормального формирования лицевой части черепа. Здоровый ген обеспечивает организм белком Treacle наполовину, но такого количества недостаточно для правильного развития лицевых структур. При изменениях в генах POLR1D и POLR1C процесс транскрипции ДНК нарушается из-за недостаточности фермента-катализатора ДНК-зависимой РНК-полимеразы. Клинические проявления синдрома такие же, как и при первичной недостаточности Treacle-протеина.
Симптомы
У больных наблюдаются аномалии в строении лица. Распространенным признаком, встречающимся в 80% случаев, является двусторонняя симметричная гипоплазия скуловых костей, инфраорбитального края и нижней челюсти. Внешне это проявляется своеобразным уплощенным бесформенным лицом, на котором выделяется нос, а остальные части «утоплены» в мягких тканях. Деформация челюсти обуславливает нарушение прикуса, формирование ортогнатии (постоянно приоткрытого рта). 89% больных имеют ограниченную возможность открывания рта и антимонголоидный тип разреза глаз с заметным опущением внешнего уголка. Данные особенности частично обусловлены патологическим строением височно-нижнечелюстного сустава.
У 69% пациентов определяется колобома радужки и нижних век в промежутке между средней и внешней третью, чаще она имеет треугольную форму. Ресницы на внешнем крае нижнего века отсутствуют. Небо арковидной формы, иногда сформирована расщелина (у 28% больных). Аномалии наружного уха представлены недоразвитием или полным отсутствием ушной раковины (микротией, анотией), атрезией наружного слухового прохода и деформацией слуховых косточек. Зачастую пациенты имеют кондуктивную тугоухость. В редких случаях диагностируется энхондрома, предкозелковые фистулы, аномальное строение сердца и позвоночника.
Осложнения
Микрогнатия и стеноз верхних дыхательных путей уже в первые годы жизни могут спровоцировать проблемы при приеме пищи и трудности дыхания вплоть до удушья. Своевременная диагностика заболевания позволяет спрогнозировать эти осложнения и предпринять меры по их предупреждению. Как правило, пациенты не имеют врожденных интеллектуальных расстройств, но при отсутствии коррекции нарушений слуха становится невозможным правильное формирование речи и обучение в обычных условиях. Дети начинают отставать в умственном развитии от сверстников, имеют задержку психического развития различной степени выраженности. В связи с наличием дефектов внешности и негативным отношением окружающих больные всех возрастов относятся к группе риска по возникновению депрессии, ипохондрии, тревожности и иных невротических расстройств.
Диагностика
Диагноз может быть установлен во время беременности или сразу после рождения. Обследование показано женщинам из группы риска и детям с врожденными лицевыми деформациями. В процессе диагностики принимают участие врачи-генетики и педиатры. Синдром Тричера-Коллинза необходимо дифференцировать с другими генетическими заболеваниями, при которых существует деформация лицевой части черепа, например, с синдромом Нагера и синдромом Гольденхара. Используются следующие методы:
- Осмотр, сбор анамнеза. Определяются характерные черепно-лицевые аномалии: недоразвитость костей скул и челюсти, деформация и гипоплазия ушных раковин, антимонголоидный тип глазных щелей, нарушения слуха и дефект верхнего неба. Иногда подтвержденный диагноз синдрома имеется у одного из родителей.
- Биогенетический тест. Антенатальное исследование включает молекулярный анализ образца ворсин хориона на 10-11 неделе беременности, фетоскопию и анализ крови из сосудов плаценты на 18-20 неделе. После родов выполняется забор крови из вены ребенка. В обоих случаях исследуется ген TCOF1. Заболевание подтверждается при наличии в нем мутации любого типа.
- Дородовое УЗИ. С 20-24 недели беременности ультразвуковое исследование плода способно выявить типичные изменения лица. Наиболее четко заметна двусторонняя аномалия ушей, гипоплазия скул и челюсти.
Дополнительно назначаются обследования, позволяющие своевременно обнаружить жизнеугрожающие состояния, оценить степень деформации костей черепа. Определяется эффективность кормления ребенка, уровень насыщения гемоглобина кислородом, ритмичность и глубина дыхания. Для диагностики сохранности слуха на 5-6 день жизни проводится аудиологическое тестирование. Инструментальная диагностика включает рентгенографию черепа, КТ и МРТ головного мозга.
Лечение синдрома
Специфической терапии не существует. Лечение нацелено на устранение симптомов и последствий заболевания, предполагает проведение хирургических операций и реабилитационных мероприятий. Объем процедур и сроки их выполнения устанавливаются индивидуально с учетом наличия угрозы для жизни больного, противопоказаний и рисков, связанных с оперативным вмешательством. Общая схема лечения включает:
- Восстановление глотания и дыхания. При развитии респираторного дистресс-синдрома осуществляется трахеостомия, дистракция подвижной челюсти, неинвазивная вентиляция легких. При невозможности потребления пищи устанавливается гастростома.
- Восстановление слуха. Деформация наружного и среднего уха устраняется хирургическим путем, но потеря слуха чаще обусловлена повреждением слуховых мелких косточек, поэтому оперативные вмешательства с целью устранения тугоухости неэффективны. Предпочтительна реабилитация слуховыми аппаратами.
- Устранение внешних дефектов. Деформации корректируются методами пластической и нижнечелюстно-лицевой хирургии. Применяется липоскульптурирование, хирургическая дистракция костей, установка трансплантатов и хирургическое восстановление неба.
Прогноз и профилактика
Комплексное лечение и реабилитация значительно улучшают качество жизни больных. При легкой и умеренной выраженности синдрома прогноз благоприятный. Профилактика затруднена, поскольку заболевание является генетическим, а мутации способны возникать спонтанно. Супружеским парам, в которых один родитель болен, необходимо медико-генетическое консультирование и перинатальная диагностика синдрома на ранних сроках беременности. Для снижения риска вынашивания больного ребенка рекомендуется процедура экстракорпорального оплодотворения с предварительным отбором генетически здоровых эмбрионов.
Источник
