Синдром фрайзера и денис драш
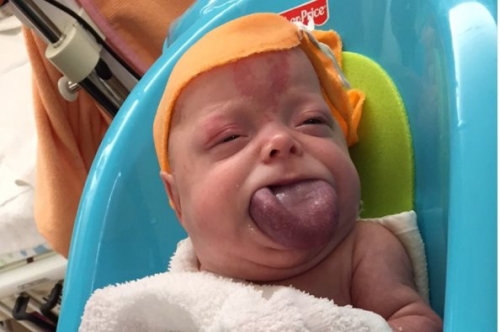
Синдром Дениса-Драша является редким состоянием, которое поражает почки и гениталии. Синдром Дениса-Драша характеризуется развитием заболеваний почек, которые развиваются в течение первых нескольких месяцев жизни. Пострадавшие лица развивают такое состояние, которое называется диффузным гломерулосклерозом, при котором рубцовая ткань начинает распространяться по всем клубочкам почек, которые в свою очередь являются крошечными кровеносными сосудами, фильтрующими отходы из крови. У людей с синдромом Дениса-Драша часто развивается почечная недостаточность уже в детском возрасте. Люди с синдромом Дениса-Драша также имеют 90-процентный шанс развития редкой формы рака почки, известной как опухоль Вильмса. Более того, пострадавшие лица могут развивать множественные опухоли в одной или в обеих почках.
Хотя лица мужского пола с синдромом Дениса-Драша имеют типичный набор мужских хромосом (46, XY), у них часто встречаются дисгенезии гонад, при которой наружные половые органы выглядят немного не так как должны или они выглядят явно женскими или вполне женскими. Яички часто не выходят в нужное место. В результате, лица мужского пола с синдромом Дениса-Драша, как правило, не в состоянии иметь биологических детей (бесплодность). А вот в отличие от пострадавших мужского пола, лица женского пола обычно имеют нормальные половые органы и имеют только проблемы с почками.
Синдром Дениса-Драша. Причины
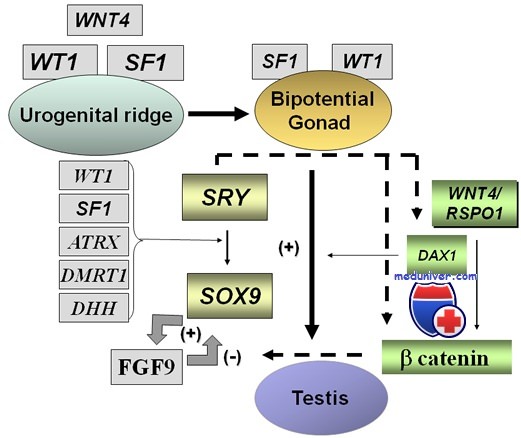
Мутации в гене WT1 вызывают развитие синдрома Дениса-Драша. Ген WT1 кодирует белок, который регулирует активность других генов путем присоединения (связывания) с конкретными участками ДНК. На основе этого действия, белок WT1 называется фактором транскрипции. Белок WT1 играет важную роль в развитии почек и половых желез (яичников у женщин и яичек у мужчин) до рождения.
WT1 генные мутации, которые вызывают синдром Дениса-Драша, приводят к производству ненормального белка, который не может связываться с ДНК. В результате, активность определенных генов является нерегулируемой, что только будет ухудшать развитие почек и половых органов. Аномальное развитие этих органов приведет к развитию диффузного гломерулосклероза и дисгенезии гонад, что очень характерно для синдрома Дениса-Драша. Также, аномальная активность гена, которая вызывает потерю нормальной функции белка WT1, увеличивает риск развития опухоли Вильмса.

Почка пациента с синдромом Дениса-Драша. Опухоль Вильмса выталкивает нормальную почечную паренхиму в сторону.

Хорошо разграниченная опухоль.

Опухоль Вильмса у пациента с синдромом Дениса-Драша.
Подробнее о мутациях и их роли.
Более 96% людей с клиническим диагнозом синдрома Дениса-Драша имеют мутацию в гене WT1. По крайней мере, сегодня уже известно о 80 типах мутаций в гене WT1, все они могут вызвать синдром Дениса-Драша. Подавляющее большинство этих мутаций являются миссенс мутациями в экзонах 9 или 8, которые кодируют очень важные соединения называемые цинковыми пальцами.
- Аминокислота которая кодируется экзоном 9, аргинин-394, имеет решающее значение в определении активности связывания ДНК с белками WT1, мутация именно в экзоне 9 считается самой часто встречающейся у лиц с синдромом Дениса-Драша. Мутация аргинина-394 присутствовала у 14 из 30 пациентов с синдромом Дениса-Драша в одном из исследований.
- Увеличение числа мутаций в других экзонах также было описано, также это касается и типов мутаций. Например, пациенты с делециями имеют высокий шанс развития двусторонней опухоли Вильмса по сравнению с пациентами с миссенс мутациями (52% против 17% соответственно).
- Мутантный цитоплазматический белок WT1, как полагают, может поглощать некоторые WT1 белки дикого типа в цитоплазме, что приводит к уменьшению количества ядерного белка WT1.
- Мутации только в одном из двух генов WT1 будет достаточно для развития нефропатии и интерсексуальных расстройств. Одна из гипотез предполагает то, что ненормальный белок WT1 может взаимодействовать с непораженным диким белком типа WT1. Это событие имеет доминантно-негативный признак.
- Подавляющее большинство пациентов с синдромом Дениса-Драша — лица мужского пола и у них часто присутствует широкий спектр половых аномалий и наоборот, люди с синдромом Денис-Драша женского пола имеют менее серьезные половые аномалии или они у них вообще отсутствуют.
- Развитие опухоли Вильмса у пациентов с болезнью Дениса-Драша является результатом мутаций в двух генах WT1. Опухоль Вильмса является следствием двух независимых событий, которые приводят к потере функций обоих генов WT1. Согласно одной теории, конституционные или зародышевые мутации в одном гене WT1 могут привести к развитию нефротомии (как было описано выше), а вот если произойдет соматическая мутация во втором гене, то это вызовет неконтролируемую клеточную пролиферацию и образование опухоли Вильмса.
Синдром Дениса-Драша. Патофизиология
Синдром Дениса-Драша, как мы уже говорили, является результатом мутаций в гене WT1, который расположен на полосе хромосомы 11p13. Белок WT1 (который кодируется одноименным геном) является фактором транскрипции, который преимущественно экспрессируется в эмбриональных клетках почек и в половых железах. Ген WT1 содержит состоит из 10 экзонов, экзоны 1-6 кодируют регулирующий домен, который регулирует экспрессию генов-мишеней, а экзоны 7-10 кодируют четыре цинковых пальца ДНК-связывающей области белка WT1. Белок WT1 опосредует мезенхимально-эпителиальный переход и дифференцировку во время морфогенеза почек и половых желез, подавляя гены, кодирующие факторы клеточной пролиферации и активации генов. И именно точечные мутации в гене WT1 (особенно в экзонах 5,8,9) могут привести к потере его регулирующей функции, что приведет к развитию последующих отклонений в клубочковом формировании и дифференциации половых желез, которые часто встречаются при синдроме Дениса-Драша. Другие, более тяжелые хромосомные аномалии, включают полные делеции группы 11p13, в результате такой аберрации у человека развиваются опухоли Вильмса, аниридии, мочеполовые аномалии и умственная отсталость.
Синдром Дениса-Драша. Симптомы и проявления
У женщин, внутри которых развивается ребенок с синдромом Дениса-Драша, особенно с уклоном на нефропатию, плацента, беременность и роды будут, как правило, нормальными. В начале (обычно в течение первого года жизни), типичные проявления будут включать нефротический синдром (например, отек, вздутие живота, рецидивирующие инфекции). С быстрым снижением скорости клубочковой фильтрации и прогрессированием хронической почечной недостаточности, у человека будут развиваться следующие дополнительные симптомы:
- Снижение активности
- Плохой аппетит и рост
- Потеря этапов развития
- Неспецифические боли
- Олигурия
Знаки синдрома Дениса-Драша, связанные с опухолью Вильмса включают увеличение брюшной полости, это является наиболее распространенным проявлением, которое встречается у 90% детей при обычном осмотре. Другие симптомы и проявления включают в себя:
- Боль в животе
- Гематурия
- Потеря веса
- Плохой аппетит
- Паховая грыжа
Физическое обследование
Признаки, связанные с нефропатией включают знаки развития нефротического синдрома (например, отеки, асцит). Свидетельства развития венозного тромбоза иногда могут развиться вторично к нефротическому синдрому. Бледность может отражать наличие анемии. Если присутствует хроническая почечная недостаточность, то следующие признаки могут развиваться вторично по отношению к почечной остеодистрофии:
- Снижение активности
- Замедление развития
- Снижение темпов роста
- Скелетные аномалии (аналогичные тем, которые встречаются при дефиците витамина Д)
Признаки, связанные с опухолью Вильмса включают ощутимую массу в брюшной полости, гематурию, и гипертонию. Другие признаки могут включать в себя:
- Потеря веса
- Обстипация
- Паховая грыжа
- Дыхательная недостаточность от плеврального выпота
- Признаки застойной сердечной недостаточности
Признаки, связанные с интерсексуальными нарушениями
- Большинство мужчин с синдромом Дениса-Драша с кариотипом 46, XY или 46, XX / 46, XY развивают псевдогермафродитизм. Спектр аномалий наружных половых органов может включать гипоспадии с крипторхизмом, увеличенный клитор, слияние губ, раздвоенность мошонки с пальпированием половых желез и микропенис.
- Аномалии внутренних половых органов у этих лиц также могут включать наличие влагалища и матки.
Синдром Дениса-Драша. Диагностика
Общий анализ мочи – протеинурия является признаком нефропатии, которая развивается при синдроме Дениса-Драша. Гематурия также может быть выявлена.
- Почечные функциональные тесты: уровень АМК и уровень креатинина могут быть в пределах референсных значений на ранних стадиях синдрома Дениса-Драша. Эти уровни могут ухудшиться с наступающей нефропатией или двусторонним развитием опухоли Вильмса. Терминальная стадия заболевания почек сопровождается гиперкалиемией и гиперфосфатемией.
- Опухолевые маркеры Вильмса: повышенные уровни гиалуроновой кислоты, повышенная активность гиалуроновой кислоты, эритропоэтина, и ренин прогормона связаны с опухолью Вильмса.
- Хромосомный анализ может понадобиться для определения типа мутации.
Визуализация
Брюшное и тазовое УЗИ. Его стоит выполнять у всех пациентов, которые жалуются на симптомы предлагающие наличие синдрома Дениса-Драша. Через равные промежутки времени после первоначального диагноза, врачам необходимо продолжать проводить УЗИ почек для выявления опухоли Вильмса. УЗИ – неплохой метод, но его сегодня все чаще заменяют на КТ или МРТ.
Синдром Дениса-Драша. Лечение
Краеугольным камнем в лечении синдрома Дениса-Драша является медикаментозная терапия, которая должна включать в себя контроль баланса жидкости и электролитов, лечение гипертонии, почечные терапии для пациентов с терминальной стадией почечной недостаточности или для пациентов после двусторонней нефрэктомии и химиотерапии.
Хирургическое лечение больных с синдромом Дениса-Драша и опухолью Вильмса включает следующие аспекты:
- Для пациентов без опухоли Вильмса, в момент первой диагностики синдрома Дениса-Драша, будет необходима ранняя профилактическая двусторонняя нефрэктомия с последующей заместительной почечной терапией, это необходимо для того, чтобы можно было избежать повышения риска развития опухоли Вильмса, и это, как следствие, может стать той причиной по которой пострадавшему не проведут трансплантацию почки. Так как риск риск развития злокачественности гонад также высок у пациентов с дисгенезией гонад, хирург может принять решение по выполнению кастрации в момент нефрэктомии. Назначение соответствующей гормональной терапии у этих пациентов в период полового созревания может быть оправданным.
- Если у пациента, на момент диагностики, также уже была обнаружена опухоль Вильмса, то врач может принять решение по проведению трансплантации почки после двусторонней нефрэктомии. Пациенты с опухолью Вильмса еще до операции должны пройти химиотерапию.
Синдром Дениса-Драша. Осложнения
Пациенты с нефротическим синдромом могут столкнуться с развитием рецидивирующих инфекций, недостатком питательных веществ, и, иногда, с венозным тромбозом. Прогрессия к терминальной стадии почечной болезни является неизбежной. Осложнения химиотерапии могут включать развитие угрожающих жизни инфекций и вторичных опухолей. Риск развития опухоли Вильмса в любой остаточной почечной ткани после операции является высоким.
Синдром Дениса-Драша. Прогноз
Все пациенты развивают нефропатию и терминальную почечную болезнь в течение 2 лет. Практически у всех больных с синдромом Дениса-Драша развиваются опухоли Вильмса. Пациенты с односторонней опухолью Вильмса находятся в опасности от развития контралатеральной опухоли.
Источник
Синдром Дени-Дрэша — клиника, диагностикаЭти редкие заболевания вызваны мутациями гена — супрессора опухоли Вильмса (WT1), который кодирует фактор транскрипции, в норме подавляющий образование нефробластомы (опухоли Вильмса). Проявления синдрома Дени—Дрэша и синдрома Фрайзера во многом схожи (нарастающий диффузный мезангиальный склероз и дисгенезия гонад с кариотипом XY), но поскольку в их основе лежат разные мутации, то для синдрома Фрайзера нехарактерно развитие нефробластомы. Диффузный мезангиальный склероз характерен для синдрома Дени—Дрэша, но может быть и самостоятельным заболеванием. У некоторых больных с изолированным диффузным мезангиальным склерозом также есть мутации гена WT1. Фактор транскрипции WT1 может как подавлять, так и активировать транскрипцию генов, в зависимости от того, с каким участком ДНК он связывается. В свою очередь, другие белки могут изменять его активность. Связываясь с мРНК, WT1 может регулировать экспрессию генов, и на уровне транскрипции, и на посттранскрипционном уровне. В период формирования почки WT1 экспрессируется в конденсирующейся мезенхиме, в образующихся при конденсации мезенхимы везикулах и подоцитах, в окончательной почке его экспрессия сохраняется в подоцитах. Такой характер экспрессии наводит на мысль, что WT1 участвует в дифференцировке клеток мезенхимы в подоциты и поддерживает их нормальный фенотип. Нарушение функции WT1 ведет к неконтролируемому росту метанефрогенной ткани и образованию нефробластомы или нарушению дифференцировки подоцитов. Фактор транскрипции WT1 экспрессируется также в клетках полового тяжа, гранулезных клетках яичниковых фолликулов и клетках Сертоли. Возможно, нормальная дифференцировка половых желез также зависит от фактора транскрипции WT1. Для синдрома Дени—Дрэша характерны: нефробластома, дисгенезия гонад с кариотипом XY и наружными половыми органами промежуточного типа и гломерулопатия. Последняя обычно проявляется нефротическим синдромом, возникающим в первый год жизни и приводящим к развитию ХПН к 3 годам. У детей синдром Дени—Дрэша может быть как полным, так и неполным (гломерулопатия и аномалии половых органов без нефробластомы или гломерулопатия и нефробластома без аномалий половых органов). Как и при других формах дисгенезии гонад с кариотипом XY, у этих больных повышен риск гонадобластом. Если диагноз синдрома Дени—Дрэша не вызывает сомнений, то, учитывая высокий риск нефробластомы, показана двусторонняя нефрэктомия. Для больных с синдромом Дени—Дрэша характерно специфическое поражение почек — диффузный мезангиальный склероз. Поражаются интракортикальные нефроны, в них расширяется мезангий и облитерируются капилляры клубочка, из-за чего клубочек превращается в бесформенную массу матрикса с венцом из гипертрофированных подоцитов. Причина заболевания — миссенс-мутация в гене WT1, приводящая к замене аргинина на триптофан в положении 394. Реже встречается замена аспартата на аспарагин в положении 396 и аргинина на гистидин в положении 366. В результате этих мутаций фактор транскрипции WT1 теряет способность связываться с ДНК. В большинстве случаев эти мутации возникают впервые, хотя могут и наследоваться. Хотя больные с синдромом Дени—Дрэша являются носителями лишь одного мутантного рецессивного аллеля гена WT1, но в нефробластоме поражены оба аллеля, причем каждый аллель несет разные мутации. При синдроме Дени—Дрэша в почках остаются очаги метанефрогенной ткани, несущие унаследованную мутацию гена WT1 в одном из аллелей. Если в клетках этой ткани происходит мутация второго аллеля, то это приводит к неконтролируемой пролиферации клеток и возникновению нефробластомы. Механизм развития диффузного мезангиального склероза и дисгенезии гонад при синдроме Дени—Дрэша иной, чем при нефробластоме, поскольку больной гетерозиготен и несет лишь один мутантный аллель гена WT1. Эта мутация проявляется как доминантно-негативная, то есть дефектный белок нарушает функцию продукта нормального аллеля, лишая его способности контролировать экспрессию других генов. Доминантно-негативный характер мутации гена WT1 объясняет, почему поражение почек и аномалии строения наружных половых органов при синдроме Дени—Дрэша более тяжелые, чем при синдроме WAGR, при котором в результате делеции или мутации со сдвигом рамки считывания один аллель гена WT1 становится нулевым, что не мешает экспрессии нормального аллеля.
— Также рекомендуем «Болезнь Фабри — клиника, диагностика» Оглавление темы «Наследственные болезни почек»:
|
Источник
Содержание статьи:
Опухоль Вильмса — нефробластома — злокачественное новообразование почки/почек, которое встречается преимущественно в детском возрасте от 3 до 4 лет.
Присутствие определенных генетических мутаций или наследственная предрасположенность считаются важными факторами в развитии патологии. Около 5% всех раковых заболеваний у детей — опухоли Вильмса.
У взрослых данный рак почки регистрируется крайне редко.
Опухоль Вильмса развивается чаще в одном органе, но зарегистрированы случаи множественных новообразований на одной стороне (5-10%), и около 5 % детей имеют поражение обеих почек.
Нефробластома достигает значительных размеров, прежде чем пациент попадает к врачу. На начальных стадиях заподозрить заболевание сложно, так как клинические проявления отсутствуют. Средний размер опухоли в несколько раз больше самой почки.
Опухоль Вильмса метастазирует в легкие, печень, кости, мозг, но чаще ее отростки обнаруживают в близлежащих лимфатических узлах.
Распространение злокачественного новообразования определяет стадию онкологического процесса. Окончательно диагноз верифицируют с помощью морфологических исследований.
Виды опухоли Вильмса
Существует гистологическая классификация, на основании которой выделяют благоприятный гистологический тип (нет анаплазии) и неблагоприятный (значительные изменения в клетках, полиморфность, анаплазия).
9 из 10 нефробластом принадлежат к первому типу, и шанс на благоприятный исход высокий.
Другие виды рака почки у детей
Большинство видов рака почек у детей являются опухолями Вильмса, но в редких случаях могут развиться другие типы новообразований.
Мезобластная нефрома
Эти опухоли обычно появляются в первые несколько месяцев жизни.
Лечебные мероприятия включают оперативное вмешательство и по показаниям проведение химиотерапии. Маленькие пациенты подлежат диспанесерному наблюдению, чтобы не пропустить рецидив нефромы.
Клеточная саркома почки
Новообразования гораздо чаще распространяются на другие части тела, чем опухоли Вильмса, и их труднее вылечить. Терапия схожа с интенсивным лечением нефробластомы с неблагоприятной гистологией.
Злокачественная рабдоидная опухоль почки
Данный вид новообразований чаще встречаются у младенцев и детей раннего дошкольного возраста. Они быстро распространяются на другие части тела, и большинство из них уже трудно вылечить радикально. Эти опухоли редки, лечение проводят как часть клинического испытания, и оно включает химиотерапию с несколькими различными препаратами.
Рак почки
Рак почки более распространен у взрослых, но иногда его выявляют у детей и подростков.
Нефрэктомия — основной метод лечения этих видов рака, если это возможно. Прогноз во многом зависит от степени (стадии) рака на момент диагностики (может ли рак быть полностью удален с помощью операции) и его гистологического типа. Если процесс перерос начальные стадии, могут потребоваться другие виды лечения.
Что вызывает опухоль Вильмса
Существует четкая связь между развитием нефробластомы и определенными синдромами врожденных дефектов и генетическими изменениями. Но, в то же время, у некоторых детей эти факторы отсутствуют, а опухоль Вильмса носит спорадический характер.
Изменения (мутации) в определенных генах могут привести к проблемам по мере дальнейшего развития. Некоторые из ранних клеток, которые должны стать зрелыми, начинают развиваться иначе. Скопления этих структур иногда остаются после рождения и обычно созревают к 3-4 летнему возрасту ребенка.
Если этого не происходит, начинается неконтролируемое деление и рост, что приводит к опухоли Вильмса. Нормальные клетки человека функционируют на основе информации, содержащейся в хромосомах каждой клетки. ДНК несет в себе инструкции почти для всех действий и делится на единицы, называемые генами. Некоторые гены контролируют деление, жизнь и смерть клеток (онкогены).
Есть и другие, которые замедляют деление клеток или вызывают их гибель в нужное время – гены-подавители опухоли. Рак может быть вызван патологиями ДНК, которые включают онкогены или отключают гены подавления новообразований. Эти изменения могут быть унаследованы от родителя (что бывает при детском раке), или они появляются во время жизни человека под влиянием предрасполагающих факторов. Мутации в некоторых генах увеличивают вероятность того, что некоторые клетки почек останутся в ранней форме и превратятся в опухоль Вильмса.
Например, часть нефробластом вызвано мутациями или потерями генов WT1 или WT2, которые являются генами-супрессорами опухоли, найденными на хромосоме 11. Иногда эти генные изменения передаются от родителя к ребенку, но большинство опухолей Вильмса не связаны с наследственными факторами. Специалисты считают, что они развиваются в результате повреждений генетического материала, которые происходят в начале жизни ребенка, возможно, внутриутробно.
Другой механизм: мутация гена-супрессора опухоли, известного как TX, который находится на Х-хромосоме. Другой ген, причастный к патологическому процессу – CTNNB1. Не совсем ясно, что именно вызывает повреждение этих генов.
Поскольку гены, описанные выше, не обнаруживаются у всех пациентов с опухолью Вильмса, должны быть процессы, которые еще не обнаружены в настоящее время. Во многих случаях встречается более одного повреждения.
Мутации генов могут быть вызваны случайными событиями, которые иногда происходят внутри клетки, не имея внешней причины. Нет известных, связанных с образом жизни или экологическими факторами, причин опухолей Вильмса, поэтому как-то предотвратить заболевание невозможно.
Факторы риска опухоли Вильмса
Факторы риска – это все, что влияет на вероятность развития заболевания, различные виды рака имеют свои факторы риска. Ожирение, низкая физическая активность, неправильное питание и курение рассматривают как триггеры для многих «взрослых» раков.
Но должно пройти много лет, чтобы действительно появилась вероятность онкопроцесса, данные факторы риска не имеют большого влияния на злокачественные новообразования, встречающиеся в детском возрасте.
До сих пор исследования не подтвердили каких-либо связей между опухолью Вильмса и неблагополучием окружающей среды, воздействиями во время беременности, либо после рождения ребенка.
Выделяют следующие факторы риска:
• Возраст
Опухоль Вильмса наиболее часто встречается у маленьких детей, средний возраст которых составляет от 3 до 4 лет, реже у школьников и редко у взрослых.
• Раса
Чернокожие дети более подвержены развитию нефробластомы, причина этого неизвестна.
• Пол
У девочек риск развития опухоли Вильмса несколько выше, чем у мальчиков.
• Отягощенный семейный анамнез
Около 1% до 2% детей с опухолями Вильмса имеют одного или нескольких родственников с одним и тем же раком. Ученые считают, что эти дети наследуют хромосомы с ненормальным или отсутствующим геном от родителя, при этом родственник с нефробластомой обычно не является родителем.
У детей с отягощенным семейным анамнезом вероятность развития опухолей в обеих почках несколько выше, но чаще поражается только одна почка.
• Определенные генетические синдромы/пороки развития
Существует сильная связь между опухолями Вильмса и некоторыми видами врожденных дефектов. По статистике, у 1 ребенка из 10, кроме нефробластомы, регистрируют другие врожденные дефекты. Большинство из них указывает на определенный синдром (группа симптомов, признаков, пороков развития или других аномалий у одного человека) и включает:
• опухоль Вильмса;
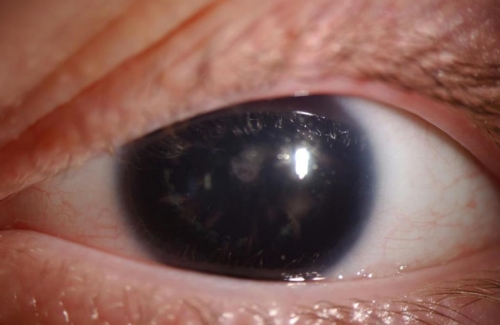
• аниридию (полное или частичное отсутствие радужки глаз);
• аномалии мочеполовых путей (дефекты почек, мочевыводящих путей, полового члена, мошонки, клитора, яичек или яичников);
• умственную отсталость.
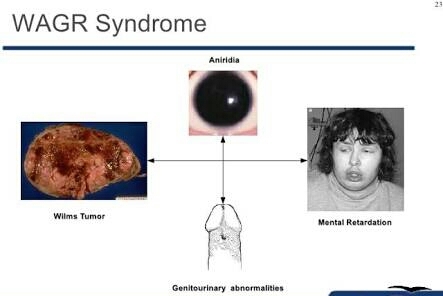
WAGR означает первые буквы физических и психических проблем, связанных с этим синдромом (хотя не у всех пациентов присутствуют все симптомы).
Дети с WAGR в 30%-50% случаев имеют опухоль Вильмса. Клетки при синдроме WAGR являются недостающей частью хромосомы 11, где обычно обнаруживается ген WT1. Дети с WAGR, как правило, заболевают в раннем возрасте, и опухолевый процесс поражает две почки.
Синдром Дениса-Драша и синдром Фрейзера
Эти редкие синдромы также были связаны с изменениями (мутациями) в гене WT1.
При синдроме Дениса-Драша почки утрачивают функциональную способность, когда ребенок очень маленький.
Опухоли Вильмса развиваются уже в пораженных почках.
Репродуктивные органы также имеют пороки развития, и мальчика могут ошибочно принимать за девочку. Поскольку риск развития нефробластомы очень высок, врачи часто советуют удалять почки сразу после того, как этот синдром диагностирован.
При синдроме Фрейзера также есть поражение почек, но функция их сохраняется дольше, до подросткового возраста. Как и при синдроме Дениса-Драша, репродуктивные органы имеют аномалии. Дети с синдромом Фрейзера также подвергаются повышенному риску развития нефробластомы, но все-таки вероятность появления злокачественных новообразований в области урогенитальной сферы выше.
Синдром Беквита-Видемана

Дети с этим синдромом выглядят крупнее и имеют большие, чем обычно, внутренние органы и увеличенный язык. У них может быть нетипичная большая рука и / или нога с одной стороны тела (гемигипертрофия), а также другие медицинские проблемы.
Риска опухоли Вильмса — около 5%. Этот синдром вызван дефектом в хромосоме 11, который влияет на ген WT2.
Другие синдромы
Реже опухоль Вильмса связана с другими синдромами, рассматривают:
• синдром Перлмана;
• синдром Сотоса;
• синдром Симпсона-Голаби-Бемель;
• синдром Блума;
• синдром Ли-Фраумени;
• трисомия 18.
Некоторые врожденные дефекты
Опухоли Вильмса также чаще встречается у детей с определенными врожденными дефектами (без принадлежности к известным синдромам):
• Аниридия (полное или частичное отсутствие радужки глаз);
• Гемигипертрофия (крупногабаритная рука и / или нога с одной стороны тела);
• Крипторхизм (неопустившееся яичко в мошонку) у мальчиков;
• Гипоспадия (открытие наружного отверстия уретры в нетипичном месте).
Клинические проявления опухоли Вильмса
На ранних стадиях течение может быть бессимптомным, позднее регистрируют следующие изменения:
• пальпация опухолевой массы в брюшной полости;
• кровь в моче;
• плохой аппетит, тошноту;
• уменьшение массы тела;
• бледность;
• адинамичность;
• запор;
• повышение температуры без видимой причины.
При значимых размерах новообразования присутствует асимметрия живота.
Болевые ощущения не типичны, но у некоторых детей может проявляться болевой синдром.
У некоторых маленьких пациентов регистрируют высокое артериальное давление с соответствующей симптоматикой:
• головные боли;
• носовые кровотечения;
• инъекция склер;
• изменение сознания.
Несмотря на то, что опухоли Вильмса часто внушительного размера, большинство из них не распространяются на другие области тела, что делает возможным радикальное лечение.
Диагностические мероприятия
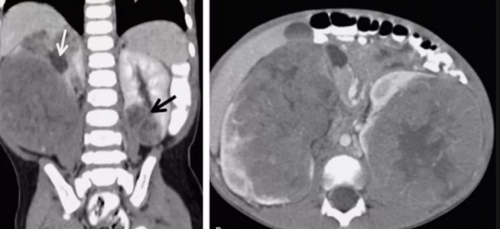
Двухстороннее поражение почек
Исследования, которые помогают установить диагноз, включают:
• Ультразвуковую диагностику – как первичное исследование.
• Компьютерную томографию (КТ), которая позволяет получить детальное поперечное сечение органа при прохождении рентгеновских лучей.
Способ информативен для выявления опухолей и определения распространения рака на другие области. Компьютерное сканирование также незаменимо для оценки инвазии опухоли в близрасположенные вены или другие органы.
• МРТ.
Магнитно-резонансная томография (МРТ) использует радиоволны и сильный магнит для получения детальных снимков внутренних частей тела. Это обеспечивает более сложные изображения, которые позволяют врачам видеть прорастание рака в крупные кровеносные сосуды вблизи почки. МРТ может также использоваться для поиска возможного распространения рака на головной или спинной мозг, при соответствующей клинике.
• Рентгенография.
Рентгеновские лучи используются для поиска любых метастазированных областей, особенно в легких. Это исследование может не понадобиться, если будет выполнена КТ грудной клетки.
• Сканирование костей скелета.
Сканирование костей использует небольшое количество радиоактивного материала, чтобы выявить область пораженной кости, при отдаленном метастазировании.
• Лабораторные анализы.
Лабораторные исследования – анализы крови и мочи – проверяют общее состояние здоровья пациента и выявляют любые неблагоприятные побочные эффекты. Мочу исследуют, чтобы увидеть, есть ли проблемы с почками. Функциональную способность почек уточняют с помощью определения уровня мочевины и креатинина.
• Биопсия почки/хирургия.
В большинстве случаев образец ткани берут во время операции. Иногда, если врачи менее уверены в диагнозе, или есть предположение, что опухоль не может быть удалена полностью, материал может быть взят во время биопсии в качестве отдельной процедуры перед хирургическим вмешательством.
Основную информацию получают при помощи магнитно-лучевых способов обследования.
Стадии опухоли Вильмса
Стадия рака показывает его распространение, от этого зависят лечение и прогноз.
I стадия
Поражение одностороннее, опухоль может быть полностью удалена во время операции. Нет инвазии в почечную капсулу. Кровеносные сосуды и лимфатические узлы не поражены.
40%- 45% — I стадия.
II стадия
Опухоль выросла за пределы почки в жировую ткань, либо в кровеносные сосуды, но может быть удалена полностью. Близлежащие лимфатические узлы визуально не изменены.
20% — II стадия.
III стадия
Эта стадия относится к нефробластомам, которые, возможно, не были удалены полностью. Образование, оставшееся после операции, ограничивается брюшной полостью (животом). Может присутствовать следующее:
• Рак распространился на лимфатические узлы в области живота или таза, но нет поражения отдаленных лимфатических узлов.
• Рак перерос в близлежащие жизненно важные структуры, поэтому хирург не мог полностью удалить его.
Опухоли и ее отростки обнаруживают в брюшной полости.
20 -25% всех нефробластом диагностируют на третьей стадии.
IV стадия
Рак распространился через кровь в органы, удаленные от почек: легкие, печень, мозг, кости, лимфатические узлы. Около 10% всех опухолей Вильмса выявляют на IV стадии.
V стадия
Билатеральное поражение почек (с обеих сторон).
5% — V стадия.
Гистология опухоли
Другим основным фактором, определяющим прогноз и лечение опухоли Вильмса, является гистология, основанная на том, как выглядят клетки под микроскопом. Гистология может быть как благоприятной, так и неблагоприятной (анапластической).
Лечение опухоли Вильмса

Заболевание излечимо в 80-90% случаев.
Основные виды терапии опухоли Вильмса:
• хирургия;
• химиотерапия;
• лучевая терапия.
Большинство детей получают комбинированное лечение.
Подходы к лечению в разных странах вариативны.
В США хирургия является преимущественным методом лечения большинства опухолей Вильмса. В Европе врачи часто предпочитают проводить короткий курс химиотерапии перед операцией.
Основная цель лечения – удаление первичной (основной) опухоли, даже если рак распространился на отдаленные участки тела. Иногда новообразование невозможно убрать, потому что оно распространилась на близлежащие кровеносные сосуды или другие жизненно важные структуры, или находится в обеих почках. В этих случаях врачи могут использовать химиотерапию, лучевую терапию или их комбинацию, чтобы попытаться уменьшить объем новообразования перед возможной операцией.
Если вмешательство было нерадикальным (часть опухоли осталось),
может потребоваться лучевая терапия или повторная операция.
Хирургия чаще всего используется для лечения опухоли Вильмса. Для стадии I-IV проводят радикальную нефрэктомию — удаление рака вместе со всей почкой, мочеточником, надпочечником и окружающей жировой тканью.
Поскольку пациенты стадии V имеют онкологическое поражение обеих почек, билатеральная нефрэктомия приведет к почечной недостаточности и необходимости в трансплантации почки. В процессе хирурги резецируют патологические участки и сохраняют максимально возможное количество здоровой ткани почек, чтобы избежать пересадки органа.
Химиотерапия
Химиотерапия может быть использована перед операцией для уменьшения опухолей и облегчения их удаления; или после, чтобы убить раковые клетки, которые могли остаться в организме.
Химиотерапию применяют для контроля опухоли Вильмса больших размеров на продвинутой стадии (с метастазированием).
Детям, больным раком обеих почек, перед операцией назначают прием химиопрепаратов, что оставляет шанс на сохранение хотя бы одной почки.
Независимо от стадии и гистологии, все схемы лечения включают в себя как хирургию, так и химиотерапию, а запущенные стадии также могут потребовать проведения лучевой терапии.