Синдром фишера эванса у ребенка
Геморрагические состояния — это общее название для заболеваний и специфических состояний, при которых нарушается свертываемость крови или состояние сосудов и капилляров. Эти состояния бывают приобретенными, хроническими, имеют разную степень тяжести, протекают в различных формах: легкой, тяжелой, неуточненной. Одно из таких заболеваний — синдром Эванса.
- Что такое синдром Эванса?
- Причины синдрома Эванса
- Симптомы синдрома Эванса
- Лечение синдрома Эванса
Что такое синдром Эванса?
Синдром Эванса — редкое расстройство, при котором иммунная система организма вырабатывает антитела, ошибочно уничтожающие красные кровяные клетки, тромбоциты и иногда определенный тип лейкоцитов, известный как нейтрофилы. Это приводит к аномально низким уровням этих клеток крови в организме (цитопении). Преждевременное разрушение красных кровяных клеток (гемолиз) — это состояние, известное также под названием аутоиммунной гемолитической анемии, или АМСЗ.
Тромбоцитопения обозначает снижение уровня тромбоцитов (идиопатическая тромбоцитопеническая пурпура, или ИТП в данном случае). Нейтропения — это низкий уровень белых кровяных клеток — нейтрофилов. Синдром Эванса представляет собой сочетание тромбоцитопении и гемолитической анемии, нейтропения для него характерна также, но намного реже.
В некоторых случаях оба состояния происходят одновременно, в других — одно за другим. Симптомы различаются, исходя из состояния здоровья организма до заболевания и различных факторов, в том числе питания, климата, обстановки в семье и общего состояния пациента в момент появления симптомов.
Синдром Эванса может вызывать осложнения, угрожающие жизни больного. Он может проявляться как основное (то есть, идиопатическое) заболевание, либо присутствовать в качестве сопутствующего заболевания наряду с аутоиммунными или лимфопролиферативными болезнями. Последние подразумевают чрезмерно активное производство организмом белых клеток крови. Идиопатическая и сопутствующая форма синдрома Эванса также называются первичной и вторичной. Медики намеренно обращают внимание на это различие, поскольку именно от механизма начала заболевания зависит его дальнейшее лечение.
Причины синдрома Эванса
Синдром Эванса был впервые описан в медицинской литературе в 1951 году доктором Робертом Эвансом и его помощниками. В течение многих лет это заболевание считалось проявлением гемолитической анемии в сочетании с нейтропенией, в настоящее время такая точка зрения тоже существует. Однако всё чаще ученые современности склоняются к тому, что первопричина синдрома — это хроническая «поломка» и дизрегуляция иммунной системы.
Синдром Эванса — это аутоиммунное заболевание. Причина его появления, прежде всего, наследственная, первопричина медиками не установлена. Во время атаки белых кровяных клеток антителами, иммунитет человека падает и становится восприимчивым к различным заболеваниям. Ученые полагают, что пусковым событием синдрома Эванса может быть какая-то инфекция или болезнь, в результате которой антитела начинают «бунтовать».
Синдром Эванса может сопутствовать таким заболеваниям: синдром Шегрена, общая вариабельная иммунная недостаточность, волчанка, антифосфолипидный синдром, хронический лимфолейкоз.
Симптомы синдрома Эванса
Симптомы синдрома Эванса имеют различную интенсивность, зависят от продолжительности периода болезни и состояния больного, его возраста и качества жизни. У многих пациентов течение заболевания хроническое, с периодами обострения симптомов и ремиссией, обычно временной. Практически все симптомы болезни — результат низкого уровня трех видов кровяных клеток. Например, красные кровяные клетки (эритроциты) доставляют кислород к тканям и изымают из них диоксид углерода, тромбоциты оказывают помощь в процессе свертывания, останавливая потерю крови, а белые кровяные клетки помогают бороться с инфекциями.
У некоторых больных разрушение эритроцитов происходит быстрее, чем организм успевает создавать новые. Низкий уровень циркулирующих эритроцитов известен как анемия. Для этого заболевания характерна бледная кожа, головокружение, одышка, потемнение мочи, тахикардия, иногда — желтуха.
У других пациентов первыми «сдаются» тромбоциты. Появляется тромбоцитопения. Она выражается в появлении на коже мелких красных или фиолетовых пятен (петехий), либо же крупных пурпурных участков на поверхности тела. Для больных тромбоцитопенией характерно быстрое появление синяков, внутренние кровотечения, пурпура. У этих людей легко травмируются слизистые оболочки, идет кровь.
Больные с нейтропенией, сопровождающей синдром Эванса, точнее, с активным ее проявлением при этом синдроме, встречаются во врачебной практике реже. Больные с нейтропенией более восприимчивы к рецидивирующим инфекциям. Общие симптомы состояния: лихорадка, общая слабость, язвы на слизистой оболочке рта.
Дополнительные симптомы синдрома Эванса: увеличение лимфатических узлов, селезенки, печени. Эти симптомы могут появляться при обострении заболевания и исчезать в период ремиссии.
Иногда организм больных не отвечает на лечение, в таком случае форма синдрома считается лекарственно устойчивой. Возможны такие осложнения: сепсис, обильные кровотечения, массовые кровоизлияния, сердечно-сосудистые осложнения, в том числе сердечная недостаточность.
Лечение синдрома Эванса
Лечение синдрома Эванса направлено, прежде всего, на снятие основных симптомов. Поскольку первопричину этой болезни установить сложно, специалисты подбирают схему лечения, исходя из индивидуального случая. Будучи аутоиммунным заболеванием, синдром Эванса проявляется в детстве, поэтому к лечению ребенка подключаются такие специалисты, как педиатр, гематолог, иммунолог, ревматолог и даже хирург.
- Первый этап лечения синдрома Эванса заключается в приеме кортикостероидов, таких как преднизолон. Кортикостероиды помогают подавлять активность иммунной системы и уменьшать выработку антител.
- Другой метод: внутривенное введение иммуноглобулина. Этот препарат также модулирует активность иммунной системы. Иммуноглобулин — это раствор, содержащий антитела, подаваемый пациентам при помощи уколов или капельниц.
- Хирургическое удаление селезенки. Спленэктомия обычно показана тем пациентам, которые уже прошли другое лечение, и оно оказалось для них неэффективным, как, например, при лекарственно устойчивой форме синдрома Эванса.
Спленэктомия вызывает долговременное исчезновение симптомов у детей, а для взрослых подобная процедура может оказаться неэффективной, и симптомы заболевания вернутся снова. Во время острой фазы заболевания может потребоваться переливание крови или тромбомассы, однако специалисты советуют избегать этого так долго, как возможно.
Среди инновационных методов лечения хорошие результаты показывает применение препарата Ритуксимаба. Он классифицируется как моноклональное антитело и представляет собой препарат биологической терапии, действующий как антитела, но созданный в лаборатории искусственно.
Преимущества использования Ритуксимаба в том, что он не дает иммуносупрессии и серьезных побочных эффектов, которые свойственны другим типам иммунодепрессантов. Недостатком использования препарата является то, что почти у всех больных развивается гипогаммаглобулинемия, которая после завершения лечения не исчезает.
Гипогаммаглобулинемия — это состояние, при котором иммунная система организма не производит достаточное количество антител, делая людей восприимчивыми к бактериальным и, в меньшей степени, к некоторым вирусным инфекциям.
Еще одно средство лечения синдрома Эванса — Микофенолат мофетил (иммуносупрессор). Это препарат, который используется в качестве второй линии терапии для пациентов, которые не отвечают на лечение кортикостероидами.
Экспериментальное средство лечения — трансплантация аутологичных или аллогенных стволовых клеток. Перед трансплантацией аутологичных стволовых клеток стволовые клетки больного удаляются после предварительного лечения. Здоровые стволовые клетки снова помещают в костный мозг. Донором для подобной процедуры обычно является член семьи больного, близкий кровный родственник.
Источники статьи:
https://emedicine.medscape.com/article/955266-treatment
https://www.bloodjournal.org/content/114/15/3167?sso-checked=true
https://rarediseases.org/rare-diseases/evans-syndrome/
По материалам:
NIH/National Heart, Lung and Blood Institute
Genetic and Rare Diseases (GARD) Information Center
Evans Syndrome Community Network
© 2015 by American Society of Hematology
© 1994-2015 by WebMD LLC.
Смотрите также:
У нас также читают:
Источник
Фишера-Эванса синдром (J. A. Fisher; R. S. Evans, совр. американский врач; синдром; син. синдром Эванса) — сочетание аутоиммунной гемолитической анемии с аутоиммунной тромбоцитопенией.
Заболевание впервые описал Фишер в 1947 г. и предположил иммунный генез анемии и тромбоцитопении. Эванс и сотр. в 1951 г. более подробно описали клинику аутоиммунной гемолитической анемии (см.), сочетающейся с аутоиммунной тромбоцитопенией (см.). Выделяют симптоматическую и идиопатическую форму Фишера-Эванса синдрома.
Симптоматическая форма наблюдается при хроническом гепатите, системной красной волчанке, хроническом лимфолейкозе, лимфоме, саркоме, лимфогранулематозе, ревматоидном артрите, туберкулезе и др. В редких случаях синдром является первым проявлением этих заболеваний. При идиопатической форме установить связь гемолиза и тромбоцитопении с каким-либо другим патологическим процессом не удается.
В основе патогенеза лежит повышенное разрушение эритроцитов и тромбоцитов вследствие фиксации на их поверхности белков иммуноглобулиновой природы — аутоантител (см.). Антиэритроцитарные антитела чаще являются неполными тепловыми агглютининами (см. Агглютинация) и принадлежат к иммуноглобулинам (см.) различных классов (G, реже — M или A). Они специфически связываются с антигенами системы резус (см. Группы крови); в нек-рых случаях направлены против антигенов других систем. Специфичность антитромбоцитарного иммуноглобулина класса G (антител) не установлена, однако доказано, что его содержание на поверхности эритроцитов по сравнению с нормой увеличено. Разрушение эритроцитов и тромбоцитов осуществляется преимущественно в селезенке, иногда в печени и костном мозге. В связи с этим продуцирование кроветворных клеток в костном мозге увеличено, в миелограмме (см.) отмечается увеличение содержания эритроидных клеток и мегакариоцитов (см. Кроветворение).
Клиническая картина характеризуется анемией, высоким ретикулоцитозом и непрямой гипербилирубинемией, сочетающимися с тромбоцитопенией, т. е. симптомами, свойственными аутоиммунной гемолитической анемии (см.) и тромбоцитопенической пурпуре (см. Пурпура тромбоцитопеническая). Чаще болезнь начинается исподволь; больные жалуются на боли в суставах, животе, субфебрильную температуру. Позднее присоединяется умеренная слабость и одышка, на коже обнаруживаются геморрагии (экхимозы, петехии), кровоизлияния в слизистую оболочку рта, конъюнктиву, наблюдаются носовые и маточные кровотечения. Геморрагический синдром (внутренние и наружные кровотечения, кровоизлияния) может предшествовать появлению клин, и лаб. признаков иммунного гемолиза (см.). В нек-рых случаях гемолиз начинается раньше. У ряда больных анемия и тромбоцитопения выявляются одновременно. Тромбоцитопения может развиться через несколько лет после спленэктомии (см.), выполненной по поводу аутоиммунной гемолитической анемии, при этом признаки гемолиза могут отсутствовать.
Диагноз устанавливают на основании клин, картины и прямой пробы Кумбса (см. Кумбса реакция), подтверждающей аутоиммунный характер гемолиза. Отрицательные результаты пробы Кумбса не исключают наличия у больного иммунного гемолиза, т. к. при усилении гемолиза значительная часть нагруженных антителами эритроцитов разрушается. Установить гемолиз помогает также обнаружение повышенного содержания в крови ретикулоцитов, укорочения продолжительности жизни эритроцитов, увеличения клеток эритроидного ряда в костном мозге. При выявлении тромбоцитопении и повышенного (или нормального) количества мегакариоцитов в костном мозге диагностируют тромбоцитолиз (процесс распада тромбоцитов). Иммунный характер тромбоцнтопении подтверждает предложенный Диксоном (R. Dixon) и Россе (W. Rosse) количественный метод определения иммуноглобулинов класса G на поверхности тромбоцитов; при Фишера-Эванса синдроме их содержание на поверхности тромбоцитов повышено.
Лечение проводят глюкокортикоидными гормонами; при отсутствии эффекта производят спленэктомию (см.). Если после операции выраженный гемолиз и (или) тромбоцитолиз рецидивируют, назначают цитостатические препараты (азатиоприн, циклофосфан, винкристин), обычно их комбинируют с глюкокортикоидными гормонами. Детям при отсутствии жизненных показаний назначения цитостатических препаратов следует избегать. При тяжелой анемии, угрожающей жизни больного, показаны трансфузии эритроцитной массы или многократно отмытых эритроцитов, подобранных индивидуально с помощью непрямой пробы Кумбса. Переливание тромбоцитной массы не оказывает эффекта, т. к. донорские клетки быстро разрушаются.
Прогноз часто неблагоприятный. При Фишера-Эванса синдроме нередко наблюдаются тяжелые гемолитические кризы (см.), сильные кровотечения (см.), обусловленные дефицитом тромбоцитов. Нередки осложнения, связанные с необходимостью длительного применения глюкокортикоидных гормонов и цитостатических препаратов.
При Фишера-Эванса синдроме следует уделять особое внимание профилактике рецидивов гемолиза и (или) тромбоцитолиза при возникновении инфекционных болезней, в особенности вирусных (в нек-рых случаях назначают небольшие дозы глюкокортикоидных гормонов). Больные должны избегать инсоляции; исключается прием препаратов, блокирующих функцию тромбоцитов (напр., препаратов салициловой кислоты).
Библиогр.: Идельсон Л. И., Дицковский Н. А. и Ермильченко Г. В. Гемолитические анемии, М., 1975, библиогр.; Руководство по гематологии, под ред. А. И. Воробьева и Ю. И. Лорие, М., 1979; Савченко В. Г. и Идельсон Л. И. Применение метода Диксона и Россе для количественного определения иммуноглобулинов на поверхности тромбоцитов при тромбоцитопенической пурпуре, Пробл. гематол. и перелив, крови, т. 26, № 7, с. 49, 1981; Dixon R., R osse W. а. Ebbert L. Quantitative determination of antibody in idiopathic thrombocytopenic purpura, New Engl. J. Med., v. 292, p. 230, 1975; Evans R. S. a. o. Primary thrombocytopenic purpura and acquired hemolytic anemia, evidence for a common etiology, Arch, intern. Med., v. 87, p. 48, 1951; Pirofsky B. Autoimmunization and the autoimmune hemolytic anemias, Baltimore, 1969; Progress in hematology, ed. by E. B. Brown a. С. V. Moore, v. 6, p. 82, N. Y.— L., 1969.
В. Г. Савченко.
Источник: Большая Медицинская Энциклопедия (БМЭ), под редакцией Петровского Б.В., 3-е издание
Рекомендуемые статьи
Источник
Главная
- >>
Справочник заболеваний
- >>
Орфанные (редкие) заболевания
- >>
- Синдром Эванса
„
Это был душный горячий день, когда один человек упал в обморок прямо посредине шумного перекрестка. Мгновенно образовалась пробка во всех направлениях. Одна женщина помчалась к нему на помощь. Когда она стояла на коленях, ослабляя его воротник, человек появился из толпы, отодвинул ее и сказал:
— Все в порядке, дорогая, я прошел курс первой помощи.
Женщина спокойно наблюдала, как он щупал пульс больного человека и начал было делать искусственное дыхание. В этот момент она потрогала его за пле
”
показать еще
Орфанные (редкие) заболевания
Медучреждения, в которые можно обратиться
Общее описание
Синдром Эванса (СЭ) представляет собой очень редкую болезнь, сочетающую симптоматику аутоиммунных гемолитической анемии и тромбоцитопении. Включает симптоматическую и идиопатическую разновидности.
Причиной симптоматической формы СЭ являются:
- хронический гепатит,
- системные заболевания соединительной ткани,
- онкогематологические заболевания,
- онкологические заболевания лимфатической системы,
- злокачественные опухоли соединительной ткани,
- туберкулез.
Причины идиопатической формы данного синдрома пока не известны. Однако установлено, что при обеих разновидностях болезни, случается деструкция эритроцитов и тромбоцитов вследствие фиксирования на их поверхности аутоантител с последующей утилизацией в органах кроветворной системы. СЭ чреват инфекционными осложнениями, геморрагиями, зачастую с летальным исходом.
Симптомы синдрома Эванса
-
 артралгии,
артралгии, - абдоминальные боли,
- общая слабость,
- гипертермия,
- нарушение частоты, глубины и ритма дыхания,
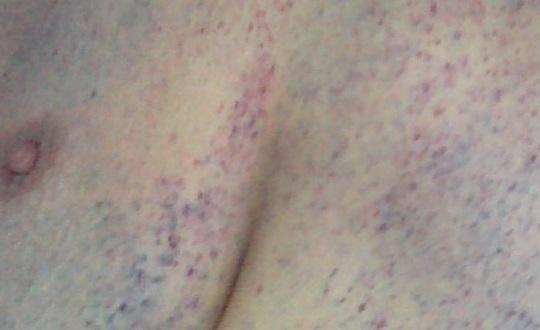
- подкожные кровоизлияния,
- петехиальная сыпь,
- субконъюнктивалные кровоизлияния,
- кровоизлияния в слизистую ротовой полости,
- эпистаксис,
- маточные геморрагии.
Диагностика
Помимо отчетливой клинической симптоматики, диагноз заболевания подтверждают данные лабораторного исследования:
- анемия, тромбоцитопения, высокий ретикулоцитоз;
- непрямая гипербилирубинемия;
- прямая проба Кумбса;
- повышение количества эритроидных клеток и мегакариоцитов в миелограмме.
Лечение синдрома Эванса
Включает назначение системных ГКС (преднизолон, дексаметазон) и цитостатиков (аза-тиоприн, циклофосфан, винкристин). В ряде случаев проводится спленэктомия. При анемии тяжелой степени осуществляют трансфузии эритроцитарной массы. Переливание тромбоцитарной массы не являются эффективными. Следует избегать употребление препаратов ацетилсалициловой кислоты, антитромботических средств. Не рекомендуется подвергаться солнечному облучению. Учитывая вероятность осложнений, прогноз СЭ не является благоприятным.
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.



- Преднизолон (системный ГКС). Режим дозирования: внутрь в начальной дозе 20-30 мг/сут., далее снижение до поддерживающей дозы — 5-10 мг/сут. При необходимости начальная доза может составлять 15-100 мг/сут., поддерживающая — 5-15 мг/сут.
- Имуран (Азатиоприн) — иммунодепрессант. Режим дозирования: принимается внутрь в дозе от 1 мг/кг/сут до 5 мг/кг/сут. Курс терапии продолжительный.
Рекомендации
Рекомендуется консультация гематолога.
Медучреждения, в которые можно обратиться:
Источник
https://doi.org/10.24287/1726-1708-2019-18-3-41-45
Аннотация
Синдром Фишера–Эванса (СФЭ) – двух-/трехростковая иммунная гемапатия в отсутствие других заболеваний. СФЭ может быть первичным/идиопатическим и вторичным, на фоне других заболеваний. У детей СФЭ нередко связан с первичным иммунодефицитным состоянием (ПИДС). В статье представлен ретроспективный анализ данных группы детей (n = 14) с СФЭ, обратившихся в НМИЦ ДГОИ в период 2012–2019 гг., с целью демонстрации необходимости проведения молекулярно-генетического исследования для диагностики ПИДС. Данное исследование поддержано Независимым этическим комитетом и утверждено решением Ученого совета НМИЦ ДГОИ. Всем пациентам было проведено исследование методом секвенирования следующего поколения (NGS). Медиана возраста дебюта заболевания составила 5,5 года (от 5 мес. до 16 лет). Соотношение по полу (мальчики:девочки) – 1,8:1. По результатам генетического обследования у 10 (71,4%) из 14 пациентов СФЭ оказался вторичным. Медиана возраста дебюта заболевания у пациентов с вторичным СФЭ – 4 года; минимальный возраст – 5 мес.; максимальный – 12 лет. Распределение по полу (мальчики:девочки) – 7:3. Чаще встречался дебют заболевания, ассоциированный с ИТП (35,7% больных) или одновременно с ИТП и АИГА (35,7% пациентов); реже начало заболевания было связано с АИГА с последующим присоединением ИТП (21,4% детей). Трехростковая иммунная цитопения отмечена у 1 пациента с СФЭ, ассоциированным с ПИДС. Среди наших пациентов с дебютом заболевания, ассоциированным с АИГА, ни в одном случае не было выявлено ПИДС. Отмечена крайне низкая эффективность ГКС и ВВИГ при СФЭ: практически в 100% случаев пациентам анализируемой группы требовалось назначение второй и последующих линий терапии. Среди других видов терапии, эффективных как при первичном, так и при вторичном СФЭ, следует отметить ритуксимаб (62% пациентов сохраняют ремиссию до 1 года) и ММФ (80% пациентов сохраняют ремиссию до 1 года). На основании проведенного исследования можно сделать вывод, что у пациентов с СФЭ мужского пола до 18 лет, которые дебютировали с ИТП, необходим тщательный поиск ПИДС с включением генетического анализа, так как у больных этой группы, наиболее высокая частота встречаемости ПИДС. Лечение СФЭ ГКС и ВВИГ практически всегда малоэффективно, требуется назначение второй и последующих линий терапии. Препараты выбора, имеющие наибольшую эффективность среди пациентов с СФЭ, – ритуксимаб и ММФ.
Об авторах
Ж. А. Кузьминова
ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России
Россия
Кузьминова Жанна Андреевна, гематолог, научный сотрудник отдела оптимизации лечения гематологических заболеваний Института гематологии, иммунологии и клеточных технологий
117997, Москва, ГСП-7, ул. Саморы Машела, 1
Е. Д. Пашанов
ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России
Россия
Москва
А. В. Павлова
ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России
Россия
Москва
М. А. Курникова
ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России
Россия
Москва
И. В. Мерсиянова
ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России
Россия
Москва
С. А. Плясунова
ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России
Россия
Москва
Н. С. Сметанина
ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России
Россия
Москва
Список литературы
1. Miano M. How I manage Evans syndrome and AIHA cases in children. Br J Haematol 2016; 172: 524–34.
2. Aladjidi N. Jutand M.-A., Beaubois C., Fernandes H., Jeanpetit J., Coureau G., et al. Evans syndrome in children: long-term outcome in prospective French national observation cohort. Front Pediatr 2015; 3: 79.
3. Michel M., Chanet V., Dechartres A., Morin A.S., Piette J.C., Cirasino L., et al. The spectrum of Evans syndrome in adults: new insight into the disease based on the analysis of 68 cases. Blood 2009; 114: 3167–72.
4. Seidel M.G. Autoimmune and other cytopenias in primary immunodeficiencies: pathomechanisms, novel differential diagnoses, and treatment. Blood 2014; 124 (15): 2337–44.
5. Mathew P.I., Chen G., Wang W. Evans syndrome: results of a national survey. J Pediatr Hematol Oncol 1997; 19 (5): 433–7.
6. Jaime-Perez J.C., Elva P., Aguilar-Calderon P.E., Salazar-Cavazos L., Gomez-Almaguer D. Evans syndrome: clinical perspectives, biological insights and treatment modalities. J Blood Med 2018; 9: 171–84.
Для цитирования:
Кузьминова Ж.А., Пашанов Е.Д., Павлова А.В., Курникова М.А., Мерсиянова И.В., Плясунова С.А., Сметанина Н.С. Синдром Фишера–Эванса у детей: анализ генных нарушений и ответа на терапию. Вопросы гематологии/онкологии и иммунопатологии в педиатрии. 2019;18(3):41-45.
https://doi.org/10.24287/1726-1708-2019-18-3-41-45
For citation:
Kuzminova Z.A., Pashanov E.D., Pavlova A.V., Kurnikova M.A., Mersiyanova I.V., Plyasunova S.A., Smetanina N.S. Fisher-Evans Syndrome in Children: an Analysis of Genetic Defects and Therapy Response. Pediatric Hematology/Oncology and Immunopathology. 2019;18(3):41-45.
(In Russ.) https://doi.org/10.24287/1726-1708-2019-18-3-41-45
Просмотров: 464
Источник
