Синдром ди джорджи частота встречаемости

Синдром Ди Джорджи – генетическое заболевание, относящееся к группе первичных иммунодефицитов и, наряду с ослаблением иммунитета, характеризующееся многочисленными пороками развития. Симптомами этого состояния являются частые бактериальные инфекции со склонностью к тяжелому течению, врожденные пороки сердца, аномалии развития лица и другие нарушения. Диагностика синдрома Ди Джорджи основывается на исследовании сердца, щитовидных и паращитовидных желез, изучении иммунологического статуса и данных молекулярно-генетических анализов. Лечение только симптоматическое, включает хирургическую коррекцию пороков сердца и аномалий лица, заместительную иммунологическую терапию, борьбу с бактериальными и грибковыми инфекциями.
Общие сведения
Синдром Ди Джорджи (гипоплазия тимуса и паращитовидных желез, велокардиофациальный синдром) – генетическое заболевание, обусловленное нарушением эмбрионального развития третьего и четвертого фарингеальных мешков. Впервые это состояние было описано в 1965 году американским педиатром Анджело Ди Джорджи, который классифицировал его как врожденную аплазию тимуса и паращитовидных желез. Дальнейшие исследования в области генетики помогли определить, что нарушения при этом заболевании выходят далеко за рамки первичного иммунодефицита. Это дало основание для появления другого названия синдрома Ди-Джорджи. С учетом наиболее часто поражаемых органов (небо, сердце, лицо) некоторые специалисты именуют данную патологию велокардиофациальным синдромом. Ряд современных исследователей разграничивают эти два состояния и считают, что «истинный» велокардиофациальный синдром не сопровождается выраженными иммунологическими нарушениями. Встречаемость синдрома Ди Джорджи составляет 1:3 000-20 000 – такое значительное расхождение данных обусловлено тем, что достоверная и четкая граница между этим заболеванием и велокардиофациальным синдромом до сих пор не установлена. Поэтому один и тот же больной, по мнению разных специалистов, может иметь либо первичный иммунодефицит, сопровождающийся сопутствующими нарушениями, либо многочисленнее пороки развития на фоне снижения иммунитета.

Синдром Ди Джорджи
Причины синдрома Ди Джорджи
Генетическая природа синдрома Ди Джорджи заключается в повреждении центральной части длинного плеча 22-й хромосомы, где предположительно располагаются гены, кодирующие ряд важных факторов транскрипции. Удалось идентифицировать один из этих генов – TBX1, продуктом его экспрессии является белок под названием T-box. Он относится к семейству протеинов, контролирующих процессы эмбриогенеза. Доказательством взаимосвязи синдрома Ди Джорджи и TBX1 является тот факт, что незначительный процент больных не имеет выраженных повреждений 22-й хромосомы, присутствуют только мутации в этом гене. Также высказываются предположения о роли делеций иных хромосом в развитии данного заболевания. Так, аналогичные синдрому Ди Джорджи проявления выявлялись при наличии повреждений 10-й, 17-й и 18-й хромосом.
В большинстве случаев синдрома Ди Джорджи делеция 22-й хромосомы захватывает порядка 2-3 миллионов пар оснований. Чаще всего данный генетический дефект возникает спонтанно во время формирования мужских или женских половых клеток – то есть, носит герминативный характер. Лишь десятая часть всех случаев заболевания представляет собой семейную форму с аутосомно-доминантным характером наследования. Патогенез синдрома Ди Джорджи сводится к нарушению формирования особых эмбриональных образований – фарингеальных мешков (главным образом, 3-го и 4-го), которые являются предшественниками ряда тканей и органов. Главным образом, они отвечают за формирование неба, паращитовидных желез, тимуса, сосудов средостения и сердца, поэтому при синдроме Ди Джорджи возникают пороки развития именно этих органов.
Симптомы синдрома Ди Джорджи
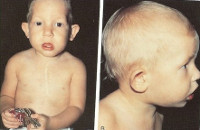
Многие проявления синдрома Ди Джорджи определяются сразу после рождения ребенка, отдельные пороки развития (например, сердца) можно выявить еще раньше – на профилактических ультразвуковых исследованиях. Чаще всего первыми обнаруживаются аномалии развития лица – расщепление неба, иногда в сочетании с «заячьей губой», прогнатия нижней челюсти. Зачастую младенцы с синдромом Ди Джорджи имеют небольшой рот, маленький нос с расширенной переносицей, деформированные или недоразвитые хрящи ушных раковин. При относительно легком течении заболевания все вышеперечисленные симптомы могут быть выражены довольно слабо, даже расщепление твердого неба может возникать только в задней его части и выявляться лишь при тщательном осмотре у отоларинголога.
В первые месяцы жизни больного синдромом Ди Джорджи на первый план выступают проявления врожденных пороков сердца – это может быть как тетрада Фалло, так и отдельные нарушения: дефект межжелудочковой перегородки, незаращение артериального протока и ряд других. Они сопровождаются цианозом, сердечно-сосудистой недостаточностью и при отсутствии квалифицированной медицинской помощи (в том числе и хирургической) могут приводить к ранней смерти больных. Другим распространенным нарушением у детей с синдромом Ди Джорджи считаются судороги и тетания, обусловленная гипоплазией паращитовидных желез и последующей гипокальциемией.
Следующим важнейшим проявлением синдрома Ди Джорджи, отличающим его от других разновидностей велокардиофациального синдрома, является выраженный первичный иммунодефицит. Он развивается по причине аплазии или недоразвития тимуса и поэтому в большей степени затрагивает клеточный иммунитет. Однако из-за тесных взаимосвязей между гуморальным и клеточным отделами иммунной системы это приводит к общему ослаблению защитных сил организма. Больные с синдромом Ди Джорджи крайне чувствительны к вирусным, грибковым и бактериальным инфекциям, которые нередко принимают затяжное и тяжелое течение. Некоторые исследователи отмечают наличие умственной отсталости различной степени, иногда могут наблюдаться судороги неврологического происхождения.
Диагностика синдрома Ди Джорджи
Для определения синдрома Ди Джорджи применяют метод физикального общего осмотра, кардиологические исследования (ЭхоКГ, электрокардиограмма), УЗИ щитовидной железы и тимуса, иммунологические пробы. Вспомогательную роль играет проведение общего и биохимического анализов крови, изучение анамнеза больного, генетические исследования. При осмотре больных синдромом Ди Джорджи могут определяться характерные для заболевания нарушения – расщепление твердого неба, аномалии строения лица, патологии ЛОР-органов. В анамнезе, как правило, выявляются частые эпизоды вирусных и грибковых инфекций, принимающих тяжелое течение, судороги, обусловленные гипокальциемией, нередко обнаруживается обширное кариозное поражение зубов.
На ультразвуковых исследованиях вилочковой железы отмечается значительное уменьшение массы или даже полное отсутствие органа (агенезия). ЭхоКГ и другие кардиологические методы диагностики выявляют многочисленные пороки сердца (например, дефект межжелудочковой перегородки) и сосудов средостения. Иммунологические исследования подтверждают значительное падение уровня Т-лимфоцитов. Это же явление наблюдается в периферической крови и нередко сочетается с уменьшением концентрации белков-иммуноглобулинов. Биохимическое изучение крови свидетельствует о снижении уровня кальция и гормонов паращитовидной железы. Врач-генетик может выполнить поиск делеций в 22-й хромосоме посредством флуоресцентной гибридизации ДНК или мультиплексной полимеразной цепной реакции.
Лечение синдрома Ди Джорджи
Специфического лечения синдрома Ди Джорджи на сегодняшний момент не существует, используют только паллиативные и симптоматические методики. Очень важно как можно раньше выявить врожденные пороки сердца и при необходимости произвести их хирургическую коррекцию, поскольку именно сердечно-сосудистые нарушения являются наиболее частой причиной неонатальной смерти при этом заболевании. Значительную опасность представляют собой судорожные приступы, обусловленные гипокальциемией, что требует своевременной коррекции электролитного баланса плазмы крови. Помощь хирургов при синдроме Ди Джорджи также может потребоваться для устранения пороков развития лица и неба.
Из-за выраженного иммунодефицита любые признаки бактериальной, вирусной или грибковой инфекции являются поводом для срочного применения соответствующих препаратов (антибиотиков, противовирусных и фунгицидных средств). Для улучшения иммунного статуса больного синдромом Ди Джорджи может производиться заместительное вливание иммуноглобулинов, полученных из донорской плазмы. В отдельных случаях осуществлялась пересадка вилочковой железы, которая стимулировала образование собственных Т-лимфоцитов – это способствовало улучшению качества жизни больных.
Прогноз и профилактика синдрома Ди Джорджи
Прогноз синдрома Ди Джорджи большинством исследователей оценивается как неопределенный, так как данное заболевание характеризуется значительной вариабельностью симптомов. В тяжелых случаях имеется высокий риск ранней неонатальной смерти из-за сочетания сердечно-сосудистых и иммунологических нарушений. Более доброкачественные формы синдрома Ди Джорджи требуют достаточно интенсивной паллиативной терапии, особенно важно уделять внимание лечению и профилактике вирусных и грибковых инфекций. Интеллектуальное развитие больных несколько замедлено, однако при правильной педагогической и психологической коррекции проявления задержки развития можно нивелировать. Из-за частого спонтанного характера мутаций профилактика синдрома Ди Джорджи не разработана.
Источник
Синдром Ди Джорджи (СДД) является врожденным заболеванием иммунной системы, развившийся в результате нарушения эмбриогенеза третьего-четвертого глоточных карманов, из которых в норме на шестой неделе внутриутробного развития формируются тимус и паращитовидные железы [1, с. 225].
Заболевание впервые описано американским педиатром и эндокринологом Анджело Мария Ди Джорджи в 1965 г. как врожденное отсутствие тимуса и паращитовидных желез. Частота встречаемости данной патологии 1:4000-1:6000, не зависимо от пола (в одинаковой пропорции у девочек и у мальчиков) [3, с. 121].
Клинически синдром Ди Джорджи определяется как первичный иммунодефицит с дефектом Т-клеточного звена иммунитета в комбинации с гипо- или аплазией паращитовидных желез, врожденными пороками сердца (тетрада Фалло, общий артериальный ствол, удвоение дуги аорты, коарктация аорты, дефект межжелудочковой перегородки) и частым выявлением мальформаций лицевой части черепа. У большинства пациентов наблюдаются задержка физического и психомоторного развития, нарушение когнитивных функций [1, с. 43].
Впервые в 1981 году было высказано предположение, что генетической причиной возникновения синдрома Ди Джорджи является делеция центрального участка длинного плеча 22-ой хромосомы (22q11.2). В большинстве случаев делеция происходит во время мейоза при спермато- или овогенезе. Только в 5-10% случаев дефектная хромосома наследуется по аутосомно-доминантному типу. С началом использования метода флуоресцентной гибридизации (FISH in situ) эта хромосомная аномалия идентифицируется более чем у 90% больных с синдромом Ди Джорджи [6, с. 335].
Сегодня предпринимаются попытки пренатального выявления микроделеционных синдромов с целью выработки тактики ведения беременности и родов, а также курирования таких пациентов в постнатальном периоде.
Клинический случай. Приводим результаты клинического наблюдения у мальчика К., 2012 года рождения, диагноз: «синдром Ди Джорджи».
Пациент неоднократно поступал в педиатрическое отделение № 2 ОГБУЗ «Детская областная клиническая больница» г. Белгорода на плановое обследование в связи с врожденными пороками сердца (ВПС) и частыми рецидивирующими инфекционными заболеваниями дыхательной системы.
В ходе обследования были диагностированы врожденный порок сердца и сосудов: Тетрада Фалло. Перимембранозный ДМЖП 10,1 мм., ДМПП, стеноз легочной артерии с проградиентом 70-90 мм. рт. ст., смещение аорты. Синдром дезадаптации сердечно-сосудистой системы. Недостаточность кровообращения первой степени.
Из анамнеза жизни известно, что мальчик поступил в дом ребенка 09.10.2013 г. в возрасте 1 года 4 месяцев из Борисовской центральной районной больницы, в связи с лишением родительских прав матери в отношении сына. Ребенок от курящей, имеющей туберкулез в анамнезе, матери (состоит на учете в противотуберкулезном кабинете ОГБУЗ «Борисовская ЦРБ» с диагнозом: клиническое излечение диссеминированного туберкулеза легких с наличием больших остаточных изменений в виде плотных очагов и фиброза), являющейся носителем вирусного гепатита С.
Данная беременность VI (I — 2001 г. — самопроизвольный выкидыш в 6 недель; II – 2002 г. – срочные роды девочка 3000 г., здорова; III – 2003 г. – медицинский аборт; IV – 2006 г. – срочные роды, двойня, девочки 2800 г. и 2500 г., здоровы; V – 2007 г. срочные роды, мальчик, 3290 г., здоров), на учете с 15 недель. Беременность протекала на фоне гестоза I половины беременности, ОРИ на сроке 30-31 неделя, хронической фетоплацентарной недостаточности, хронической внутриутробной гипоксии плода, внутриутробной инфекции, синдрома задержки развития плода I степени. УЗИ-скрининг соблюден, без врожденных пороков развития. TORCH-инфекции: хламидии, токсоплазмоз, ЦМВ, ВПГ, краснуха отрицательно. Роды IV самопроизвольные (1 период – 4 часа 15 минут, 2 период – 10 минут, безводный период – 45 минут, воды светлые). Родился мальчик, вес 2900 г., 50см., окружность головы 35 см., окружность груди 33 см., оценка по шкале Апгар 7-8 баллов.
В периоде ранней адаптации состояние ребенка средней степени тяжести, фенотипически признаки синдрома Дауна, иктеричность кожи с 3-х суток, ВУИ: конъюнктивит, на ЭХО-КГ – врожденный порок сердца: перимембранозный ДМЖП 10,1 мм., на НСГ – гипоксические изменения. На 6 сутки переведен в Детскую областную клиническую больницу, педиатрическое отделение для новорожденных, где находился с 28.05.2012 г. по 25.06.2012 г. с диагнозом: Пре- и перинатальное поражение ЦНС смешанного генеза, подострый период, синдром тонусных нарушений. Синдром дезадаптации сердечно-сосудистой системы. Простая трисомия по 21 хромосоме, спорадический вариант. Врожденный порок сердца: тетрада Фалло? Перимембранозный ДМЖП 10,1 мм., ДМПП, стеноз легочной артерии с проградиентом 70-90 мм. рт. ст., смещение аорты. НК I степени. Неонатальная гипербилирубинемия. ВУИ: конъюнктивит, ринит. ЗВУР I степени по гипотрофическому типу. Цитогенетический анализ 31.05.2012г. – трисомия по 21 хромосоме, синдром Дауна.
Тогда же были выявлены гипокальциемия, калий-натриевый дисбаланс. Отмечалась неоднократно лимфопения при гематологических исследованиях (в пределах 24-26%). Был заподозрен синдром Ди Джорджи. Исследование паратиреоидного гормона проводилось однократно и не выявило отклонений от нормативных значений (паратгормон — 11,89 пг/мл).
Искусственное вскармливание с рождения, держит голову с 6 месяцев, переворачивается со спины на бок с 9 месяцев, сидит с 11 месяцев, не ползает, не ходит, не говорит.
Однако с учетом доминирования в клинической картине симптоматики ВПС 10.03.2014 г. ребенок направлен на госпитализацию в г. Москва в НЦССХ им. А. Н. Бакулева РАМН для оперативного лечения ВПС.
С 11.03.2014 г. по 24.03.2014 г. проходил стационарное лечение рецидивирующего обструктивного бронхита в ГКБ № 9 им. Сперанского г. Москва.
24.03.2014 г. переведен в НЦССХ им. Бакулева. 28.03.2014 г. ребенок был прооперирован. Проведена радикальная коррекция двойного отхождения магистральных сосудов правого желудочка с расширением дефекта межжелудочковой перегородки, созданием внутрижелудочкого тоннеля при помощи ксенперикардиальной заплаты с пластикой выводного отдела правого желудочка и ствола ЛА ксеноперикардиальной заплатой, ушивание открытого овального окна, шовная пластика трикуспидального клапана, в условиях ИК, гипотермии, ФХКП. Послеоперационный период осложненный: дыхательная недостаточность, постэкстубационный стридор, реинтубация ИВЛ (8 суток).
С 11.04.2014 г. по 22.04.2014 г. мальчик продолжал лечение на базе НЦССХ им. А.Н. Бакулева с диагнозом: Перикардит. Состояние после операции радикальной коррекции Тетрады Фалло в условиях ИК 2014г.
Выписан из РДКБ 22.04.2014 г., транспортирован на реанимобиле реанимационной бригадой, госпитализирован в ДОКБ г. Белгорода в педиатрическое отделение № 2.
При проведении дополнительного УЗИ-исследования тимуса выявлена гипоплазия тимуса. В ходе неоднократно проводимых гематологических исследований на пред- и постоперационных этапах стабильно выявлялась выраженная лимфопения, что вновь заставило думать о наличии у пациента синдрома иммунологической недостаточности. Минимальные показатели абсолютного и относительного количества лимфоцитов в периферической крови наблюдались в возрасте 1года 6 месяцев жизни и достигали 18% .
Проведенное в возрасте 1 года 8 месяцев иммунологическое исследование выявило нарушения Т-клеточного звена и показателей фагоцитоза. Отмечалось снижение относительного количества лимфоцитов, абсолютных показателей В-лимфоцитов (CD19), НСТ-теста, фагоцитарной активности и фагоцитарного числа. Абсолютные показатели Т-супрессоров (CD 8) находились на нижней границе нормы.
В связи с подозрением на синдром Ди Джорджи была показана госпитализация ФГБУ «РДКБ» Минздрава России для верификации Синдрома Ди Джорджи. Проведено молекулярно-цитогенетическое исследование ФГА-стимулированной культуры лимфоцитов периферической крови методом FISH-анализа на интерфазных ядрах. В результате проведенного исследования был подтвержден диагноз: Синдром Ди Джорджи.
В августе 2015 г. ребенок прошел плановую диспансеризацию на базе ОГБУЗ ДОКБ, по результатам которой имеет следующий диагноз: Иммунодефицитное состояние. Синдром Ди Джорджи. Синдром Дауна. Врожденный порок сердца: тетрада Фалло, состояние после оперативного вмешательства в условиях НЦССХ им. А.Н. Бакулева РАМН от 28.03.2014 г. (по ЭХО-КГ от 06.11.2014 г. – Остаточный Pgr на клапане легочной артерии 25,8 мм. рт. ст. (V — 2,54 м/с). Сброс на МЖП не регистрируется. Умеренная дилатация правых отделов сердца. ТТР 1,5 (+). ТПР 2,5 (+). ТМР 1,5 (+). Открытое овальное окно 2,0 мм., сброс вправо). Аспергиллез. Носитель условно-патогенной флоры в бронхах (грибы рода candida + klebsiella pneumonia). Резидуальное поражение ЦНС на фоне синдромальной патологии. Атонически-астатический синдром. Задержка психо-речевого и моторного развития. Задержка интеллектуального развития на фоне синдрома Дауна. Косоглазие непостоянное сходящееся. Ангиопатия сетчатой оболочки обоих глаз.
На момент поступления ребенка в стационар ДОКБ г. Белгорода в педиатрическое отделение № 2 ребенку было 3 года и 4 месяца. Физическое развитие среднее, снижен индекс массы тела, что соответствует 1-й степени гипотрофии. Нервно-психическое развитие характеризуется некоторым отставанием речевого и сенсорного развития. У ребенка наблюдались выраженные фенотипические признаки синдрома Дауна. Можно отметить также относительно низкое расположение ушных раковин, их незначительную деформацию, низкий лоб. Анализ анамнестических данных позволил отметить позднюю дентацию, перенесенные частые и тяжелые острые респираторные инфекции.
Таким образом, клинико-анамнестические критерии и результаты проведенных исследований позволили предположить о наличии у ребенка синдрома Ди Джорджи. Учитывая высокий инфекционный индекс, а также периодически наблюдаемые нормальные показатели лимфоцитов в периферической крови, можно думать о неблагоприятном прогнозе для данного пациента в плане нивелирования в дальнейшем иммунологической недостаточности.
Представленный случай демонстрирует сложность в постановке диагноза синдрома Ди Джорджи у детей, так как на первый план в клинической картине выходит ВПС, при наличии умеренных или незначительных иммунологических и метаболических нарушений. Ребенку не проводилось повторных исследований иммунограммы, паратиреоидного гормона, не контролировался уровень сывороточного кальция, несмотря на наличие лимфопении при гематологическом обследовании.
В результате проделанного анализа, мы пришли к выводу, что дети с синдромом Ди Джорджи нуждаются в комплексном наблюдении: педиатром, иммунологом, кардиологом, эндокринологом с обязательным проведением УЗИ тимуса, мониторированием иммунологических показателей, уровня паратгормона, кальция и фосфора.
С учетом распространенности синдрома делеции хромосомы 22q11.2 у детей с ВПС комплексный подход к обследованию пациентов с кардиологической патологией должен включать не только динамическое наблюдение узких специалистов, но и проведение иммунологической и генетической диагностики.
Таким образом, тактика ведения пациентов с синдромом Ди Джорджи должна быть ориентирована не только на хирургическую коррекцию ВПС, но и на профилактику повторных инфекционных заболеваний и гипокальциемии, что предупреждает осложненное течение заболевания и значительно улучшает прогноз в отношении продолжительности и качества жизни ребенка.
Список литературы:
- Аллергология и иммунология: Национальное руководство /Под ред. Р.М. Хаитова, Н.И. Ильиной. — М.: ГЭОТАР-Медиа, 2009. — 656 с.
- Белозеров Ю.М. Детская кардиология (наследственные синдромы) / Ю.М. Белозеров. — Элиста: ЗАО «РНН Джангар», 2008. — 400 с.
- Гинтер Е.К. Медицинская генетика: Учебник. – М.: Медицина, 2003. – 448 с.
- Избранные лекции по педиатрии / под ред. А.А. Баранова, P.P. Шиляева, Б.С. Каганова. — М.: Изд. Дом «Династия», 2005. — 640 с.
- Неонатология: национальное руководство / под ред. Н.Н. Володина. — М: ГЭОТАР-Медиа, 2007.
- Practical Guidelines for Managing Patients with 22q11.2 Deletion Syndrome / Anne S. Bassett, Donna M. McDonald-McGinnet al. // The Journal of Pediatrics. — 2011. — Vol. 159, № 2. —P. 332-339.
- Рекомендации по выявлению и ведению пациентов с синдромом делеции 22q11.2 / В.Г. Антоненко, Н.П. Котлукова, Ю.О. Козлова, Т.В. Золотухина // Педиатрия. — 2013. —№ 4. — С. 63-68.7.
- Синдром Ди Джорджи: от классической триады к многообразию клинических проявлений / Н.В. Нагорная, Е.В. Бордюгова, К.В. Муравская и др. // Современная педиатрия. — 2012. —№ 5 (45). — С. 151-155.4.
- Шабалов, Н.П. Педиатрия: учебник для мед. вузов / под ред. Н.П. Шабалова. — СПб.: СпецЛит, 2003.- 893 с.
- Эндокринология /Под ред. Н. Лавина.- 2-е изд. Пер. с англ. — М.: Практика, 1999. –1128 с.
Источник
