Синдром бругада код по мкб 10
Синдром Бругада — наследственное заболевание[1], обусловленное мутацией гена SCN5A, расположенного в плече p 3-й хромосомы, кодирующего биосинтез белковых субъединиц натриевого канала кардиомиоцитов.
Впервые это понятие, позже ставшее эпонимом, предложили испано-бельгийские кардиологи — братья Педро и Хосеп Бругада[2].
Мутации генов[править | править код]
На сегодняшний день известны, по крайней мере, 5 генов, ответственных за развитие этого состояния. В зависимости от мутации гена выделяют следующие варианты:
Патогенез[править | править код]
Заболевание имеет аутосомно-доминантный тип наследования в 25 % семей. Клинические проявления синдрома Бругада развиваются обычно в молодом возрасте (до 35-40 лет), реже — наблюдаются даже в пожилом и старческом возрасте. При исследовании статистических данных, накопленных в странах Юго-Восточной Азии и Дальнего Востока, было отмечено, что в данном регионе значительно распространены случаи внезапной ночной смерти в молодом возрасте (в год от 4 до 10 случаев на 10 000 жителей, в том числе в Лаосе — 1 случай на 10 000 жителей; в Таиланде — 26-38 на 100 000).
[7]
Описаны также случаи приобретенного синдрома Бругада[2].
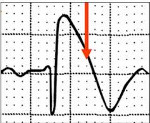
Синдром Бругада характеризуется наличием преходящей полной или неполной блокады правой ножки пучка Гиса, косонисходящим подъёмом сегмента S-T в правых грудных отведениях (V1-V3), рецидивирующей пароксизмальной полиморфной желудочковой тахикардией и высоким риском внезапной сердечной смерти.
Симптомокомплекс[править | править код]
Полная форма синдрома Бругада включает следующие клинико-электрокардиографические проявления:
- Типичная электрокардиографическая картина (косонисходящее повышение сегмента S-T над изолинией на 1 мм и больше в отведениях V1—V3, на некоторых ЭКГ напоминает морду бультерьера, поэтому данное изменение иногда называют «типом бультерьера»[2], спонтанное или индуцированное введением антиаритмических препаратов I класса (блокаторов натриевых каналов, например, аймалина (гилуритмала) в дозе 1 мг/кг или новокаинамида в дозе 10 мг/кг, флекаинида 2 мг/кг); полная или неполная блокада правой ножки пучка Гиса); возможно укорочение интервала Q-T и удлинение P-Q (P-R);
- Пароксизмы полиморфной желудочковой тахикардии, часто рецидивирующие;
- синкопальные (обморочные) состояния;
- высокий риск внезапной сердечной смерти вследствие полиморфной желудочковой тахикардии или фибрилляции желудочков.
Примечания[править | править код]
- ↑ Окороков А. Н., Диагностика болезней внутренних органов: Т. 10. Диагностика болезней сердца и сосудов.: — М.: Мед. лит., 2005. — 384 с.: ил. ISBN 5-89677-091-X; — ст. 239—241.
- ↑ 1 2 3 Л. А. Бокерия, О. Л. Бокерия, Л. Н. Киртбая. СИНДРОМ БРУГАДА: КЛЕТОЧНЫЕ МЕХАНИЗМЫ И ПОДХОДЫ К ЛЕЧЕНИЮ. Анналы аритмологии, № 3, 2010.
- ↑ 1 2 Antzelevitch C; Pollevick GD; Cordeiro JM; Casis, O.; Sanguinetti, M. C.; Aizawa, Y.; Guerchicoff, A.; Pfeiffer, R.; Oliva, A. Loss-of-Function Mutations in the Cardiac Calcium Channel Underlie a New Clinical Entity Characterized by ST-Segment Elevation, Short QT Intervals, and Sudden Cardiac Death (англ.) // Circulation (англ.)русск. : journal. — Lippincott Williams & Wilkins (англ.)русск., 2007. — Vol. 115, no. 4. — P. 442—229. — doi:10.1161/CIRCULATIONAHA.106.668392. — PMID 17224476.
- ↑ Delpon E; Cordeiro JM; Núñez L; Thomsen, P. E. B.; Guerchicoff, A.; Pollevick, G. D.; Wu, Y.; Kanters, J. K.; Larsen, C. T. Functional Effects of KCNE3 Mutation and its Role in the Development of Brugada Syndrome (англ.) // Circulation Arrhythmia and Electrophysiology : journal. — 2008. — Vol. 1, no. 3. — P. 209—218. — doi:10.1161/CIRCEP.107.748103. — PMID 19122847.
- ↑ Watanabe H; Koopmann TT; Le Scouarnec S; Yang, Tao; Ingram, Christiana R.; Schott, Jean-Jacques; Demolombe, Sophie; Probst, Vincent; Anselme, Frédéric. Sodium channel β1 subunit mutations associated with Brugada syndrome and cardiac conduction disease in humans (англ.) // Journal of Clinical Investigation (англ.)русск. : journal. — 2008. — June (vol. 118, no. 6). — P. 2260—2268. — doi:10.1172/JCI33891. — PMID 18464934.
- ↑ 1 2 Bezzina, Connie R; Barc, Julien; Mizusawa, Yuka; Remme, Carol Ann; Gourraud, Jean-Baptiste; Simonet, Floriane; Verkerk, Arie O; Schwartz, Peter J; Crotti, Lia; Dagradi, Federica; Guicheney, Pascale; Fressart, Véronique; Leenhardt, Antoine; Antzelevitch, Charles; Bartkowiak, Susan; Schulze-Bahr, Eric; Zumhagen, Sven; Behr, Elijah R; Bastiaenen, Rachel; Tfelt-Hansen, Jacob; Olesen, Morten Salling; Kääb, Stefan; Beckmann, Britt M; Weeke, Peter; Watanabe, Hiroshi; Endo, Naoto; Minamino, Tohru; Horie, Minoru; Ohno, Seiko; Hasegawa, Kanae; Makita, Naomasa; Nogami, Akihiko; Shimizu, Wataru; Aiba, Takeshi; Froguel, Philippe; Balkau, Beverley; Lantieri, Olivier; Torchio, Margherita; Wiese, Cornelia; Weber, David; Wolswinkel, Rianne; Coronel, Ruben; Boukens, Bas J; Bézieau, Stéphane; Charpentier, Eric; Chatel, Stéphanie; Despres, Aurore; Gros, Françoise; Kyndt, Florence; Lecointe, Simon; Lindenbaum, Pierre; Portero, Vincent; Violleau, Jade; Gessler, Manfred; Tan, Hanno L; Roden, Dan M; Christoffels, Vincent M; Marec, Hervé Le; Wilde, Arthur A; Probst, Vincent; Schott, Jean-Jacques; Dina, Christian; Redon, Richard. Common variants at SCN5A-SCN10A and HEY2 are associated with Brugada syndrome, a rare disease with high risk of sudden cardiac death (англ.) // Nature Genetics : journal. — 2013. — ISSN 1061-4036. — doi:10.1038/ng.2712.
- ↑ Л. М. Макаров. Синдром Бругада. журнал «Лечащий врач».
Источник
Содержание
- Описание
- Дополнительные факты
- Причины
- Классификация
- Симптомы
- Диагностика
- Дифференциальная диагностика
- Лечение
- Профилактика
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Синдром Бругада.

Синдром Бругада
Описание
Синдром Бругада. Генетически обусловленное кардиологическое состояние, характеризующееся различными нарушениями работы сердца, которые приводят к резкому повышению риска развития внезапной сердечной смерти. Симптомами этого состояния являются приступы пароксизмальной тахикардии, обмороки, фибрилляции предсердий и жизнеугрожающие фибрилляции желудочков, чаще всего возникающие во время сна. Диагностика синдрома Бругада производится на основании характерного симптомокомплекса, электрокардиографических данных и изучения наследственного анамнеза, некоторые формы патологии определяются молекулярно-генетическими методами. Специфического лечения заболевания не существует, применяют антиаритмическую терапию, используют разнообразные кардиостимуляторы.
Дополнительные факты
Синдром Бругада – группа генетических нарушений, приводящих к изменению ионной проницаемости мембран кардиомиоцитов, вследствие чего возникают патологии ритма и проводимости, создающие повышенный риск внезапной сердечной смерти. Впервые такое состояние было описано в 1992 году двумя братьями – бельгийскими кардиологами испанского происхождения Хосе и Педро Бругада, обратившими внимание на взаимосвязь определенных электрокардиологических проявлений и нарушений сердечного ритма. В настоящее время установлено, что синдром Бругада является наследственным состоянием с предположительно аутосомно-доминантным механизмом передачи, удалось выявить несколько генов, мутации которых способны вызывать это заболевание. По некоторым данным, практически половина всех случаев внезапной сердечной смерти в мире обусловлены именно этой патологией. Распространенность синдрома Бругада различается в разных регионах планеты – в странах Америки и Европы она составляет примерно 1:10 000, тогда как в африканских и азиатских государствах это заболевание встречается чаще – 5-8 случаев на 10 000 населения. Синдром Бругада примерно в 8 раз чаще поражает мужчин, чем женщин, проявления патологии возникают в разном возрасте, но чаще всего выраженная симптоматика наблюдается в 30-45 лет.
Синдром Бругада
Причины
Причина развития нарушений при синдроме Бругада заключается в патологической работе ионных каналов кардиомиоцитов, в основном натриевых и кальциевых. Их дефект, в свою очередь, обусловлен мутациями генов, кодирующих белки ионных каналов. Методами современной генетики удалось достоверно идентифицировать 6 основных генов, поражение которых приводит к развитию синдрома Бругада, в отношении еще нескольких существует подозрение, но отсутствует необходимая доказательная база. На этой основе построена классификация данного состояния, включающая в себя 6 форм заболевания (BrS):
• BrS. 1 — наиболее распространенный и хорошо изученный вариант синдрома Бругада. Обусловлен мутацией гена SCN5A, расположенного на 3 хромосоме. Продуктом экспрессии данного гена является альфа-субъединица натриевого канала 5 типа, широко представленного в миокарде. Помимо синдрома Бругада мутации данного гена становятся причиной большого количества наследственных кардиологических патологий – семейной фибрилляции предсердий, синдрома слабости синусового узла 1 типа и ряда других.
• BrS. 2 — данная разновидность синдрома Бругада вызывается дефектами гена GPD1L, который локализован на 3 хромосоме. Он кодирует один из компонентов глицерол-3-фосфат дегидрогеназы, принимающей активное участие в работе натриевых каналов кардиомиоцитов.
• BrS. 3 — этот тип синдрома Бругада обусловлен дефектом гена CACNA1C, расположенного на 12 хромосоме. Продуктом его экспрессии является альфа-субъединица кальциевого канала L-типа, также присутствующего в кардиомиоцитах.
• BrS. 4 — как и в предыдущем случае, причиной развития синдрома Бругада 4 типа является поражение потенциал — зависимых кальциевых каналов L — типа. Оно обусловлено мутацией гена CACNB2, расположенного на 10 хромосоме и кодирующего бета-2-субъединицу вышеуказанных ионных каналов.
• BrS. 5 — распространенная разновидность синдрома Бругада, обусловленная мутацией гена SCN4B, локализованного на 11 хромосоме. Он кодирует белок одного из малых натриевых каналов кардиомиоцитов.
• BrS. 6 — вызывается дефектом гена SCN1B, расположенного на 19 хромосоме. Во многом этот вариант синдрома Бругада схож с первым типом заболевания, поскольку в этом случае тоже поражаются натриевые каналы 5 типа. Ген SCN1B кодирует бета-1-субъединицу этого ионного канала.
Кроме того, в развитии синдрома Бругада подозреваются мутации генов KCNE3, SCN10A, HEY2 и некоторых других. Однако на сегодняшний день достоверно доказать их роль в возникновении данного заболевания не удается, поэтому пока количество генетических вариантов синдрома Бругада ограничено шестью. Наследование всех форм данной патологии неясно, лишь у 25% больных определяются признаки аутосомно-доминантной передачи. Предположительно имеет место доминантный тип наследования с неполной пенетрантностью либо влияние спонтанных мутаций. Также непонятны причины того, почему синдром Бругада чаше поражает мужчин, нежели женщин – возможно, выраженность проявлений заболевания находится в зависимости от гормонального фона больного.
Классификация
Патогенез нарушений при любой форме синдрома Бругада примерно одинаков – из-за изменения проницаемости мембраны кардиомиоцитов для ионов натрия происходит нарушение трансмембранного потенциала и взаимосвязанных с ним характеристик возбудимых тканей: возбудимости, сократимости, передачи возбуждения окружающим клеткам. В результате возникают блокады проводящих путей сердца (пучков Гиса), тахиаритмии, усиливающиеся при повышении вагусных воздействий (во время сна). Степень выраженности симптомов при синдроме Бругада зависит от доли пораженных натриевых каналов. Усиливать проявления болезни могут некоторые лекарственные вещества, способны ингибировать ионные каналы сердца.
Симптомы
Возраст появления первых признаков синдрома Бругада сильно отличается у разных больных – были зарегистрированы случаи этой патологии как у детей 3-4 лет, так и у лиц старческого возраста. Одним из первых проявлений патологии становятся изменения на электрокардиограмме при полном отсутствии других клинических симптомов, поэтому данное заболевание нередко выявляется случайно. В большинстве случаев выраженная клиника синдрома Бругада возникает в возрасте 30-45 лет, этому предшествует бессимптомный период продолжительностью 10-12 лет, в течение которого единственным признаком патологии являются изменения на ЭКГ.
Диагностика
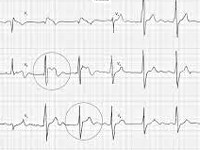
Для определения синдрома Бругада используют электрокардиографические методики, изучение наследственного анамнеза пациента, молекулярно-генетический анализ. Заподозрить наличие этого заболевания можно при наличии синкопальных явлений (головокружений, обмороков) неясного происхождения, жалоб на внезапные приступы тахиаритмий. Изменения на электрокардиограмме при синдроме Бругада могут определяться на фоне полного отсутствия клинических симптомов заболевания. При этом кардиологи выделяют три основных типа изменений на ЭКГ, незначительно отличающихся между собой. Типичная картина электрокардиограммы при синдроме Бругада сводится к элевации (подъему) сегмента ST над изоэлектрической линией и отрицательному зубцу Т на правых грудных отведениях (V1-V3). Также могут определяться признаки блокады правой ножки пучка Гиса, при холтеровском мониторировании выявляются приступы пароксизмальной тахикардии или фибрилляции предсердий.
Как правило, наследственный анамнез больных синдромом Бругада отягощен – среди родственников или предков имеются случаи летальных исходов от сердечной недостаточности, смерти во сне или внезапной сердечной смерти. Этот факт, а также наличие вышеперечисленных симптомов и изменений на ЭКГ дает основания для проведения молекулярно-генетической диагностики. В настоящее время врачи-генетики в подавляющем большинстве клиник и лабораторий производят определение синдрома Бругада, вызванного только мутациями генов SCN5A и SCN4B (1 и 5 типы патологии), в отношении остальных форм методы генетической диагностики пока не разработаны.
Дифференциальная диагностика
Дифференцировать это состояние следует с реакцией организма на прием некоторых лекарственных средств, хроническим миокардитом и другими кардиологическими патологиями.
Лечение
Специфических методов лечения синдрома Бругада на сегодняшний момент не существует, поэтому ограничиваются только борьбой с проявлениями этого заболевания, а также профилактикой жизнеугрожающих приступов тахиаритмии и фибрилляций. Наиболее широко при этом состоянии применяется амиодарон, несколько реже используются дизопирамид и хинидин. Однако медикаментозная терапия при синдроме Бругада в ряде случаев является малоэффективной, единственным надежным средством профилактики аритмии и внезапной сердечной смерти в этом случае становится имплантация кардиовертера-дефибриллятора. Только этот прибор способен оценивать работу миокарда больного и при патологических и жизнеугрожающих изменениях сердечного ритма приводить ее в норму посредством электрического разряда.
Профилактика
Многие традиционные антиаритмические препараты при синдроме Бругада противопоказаны, так как они угнетают деятельность натриевых каналов кардиомиоцитов и усиливают проявления патологии. К средствам, запрещенным при этом заболевании, относят аймалин, пропафенон, прокаинамид. Поэтому больным синдромом Бругада следует обязательно сообщать специалистам об имеющемся диагнозе, чтобы избежать назначения неверного антиаритмического средства. При наличии подобного заболевания у родственников или случаях внезапной сердечной смерти в роду следует регулярно производить ЭКГ-исследование для как можно более ранней диагностики этого состояния.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Рубрика МКБ-10: I49.8
МКБ-10 / I00-I99 КЛАСС IX Болезни системы кровообращения / I30-I52 Другие болезни сердца / I49 Другие нарушения сердечного ритма
Определение и общие сведения[править]
Синдром Бругада
Синонимы: Бангунгут, идиопатическая фибрилляция желудочков по типу Бругада,
Bangungut, синдром внезапной ночной смерти, синдром Поккури, синдром внезапной необъяснимой смерти взрослых
Синдром Бругада проявляется повышением сегмента ST в правых прекордиальных отведениях (V1 до V3), неполной или полной блокадой правой ножки пучка Гиса, возможно также желудочковой тахиаритмией и внезапной смертью. Синдром Бругада не имеет явных признаков нарушения миокарда.
Наибольшая заболеваемость отмечается в Азии, порядка 1 / 700-1 / 800. Распространенность в Европе и США ниже: от 1 300 до 1/10 000.
Сообщалось о спорадических и семейных случаях патологии, анализ наследования предполагает его аутосомно-доминантный характер.
Этиология и патогенез[править]
Затрагиваются семь генов: SCN5A, GPD1-L, CACNA1C, CACNB2, SCN1B, KCNE3 и SCN3B.
Клинические проявления[править]
Симптомы преимущественно проявляются в третьем-четвертом десятилетии жизни и чаще у мужчин, чем у женщин (8: 1). Обморок, обычно происходящий в состоянии покоя или во сне, является общим симтомом патологии. В некоторых случаях, тахикардия не прекращается спонтанно, и это приводит к внезапной смерти. Чаще всего синдром Бругада встречается в на фоне нормального сердца. Тем не менее, тонкие структурные нарушения правого желудочка были описаны при ядерном магнитном резонансе у части пациентов. Триггеры для начала аритмий: лихорадка, обильное питание, некоторые лекарства (включая антиаритмические и антидепрессанты).
Другие уточненные нарушения сердечного ритма: Диагностика[править]
Диагноз основан на клиническом исследовании и электрокардиограмме (а также на тестировании с использованием антиаритмических препаратов класса IC). В некоторых случаях проявления ЭКГ не являются очевидными или не диагностическими. В таких случаях назначение антиаритмических препаратов класса IC (аймалин и флекаинид) требуется для подтверждения / отклонения диагноза. Возможно генетическое тестирование.
Дифференциальный диагноз[править]
Расстройства, которые могут также иметь типичную картину ЭКГ, включают острый перикардит, мышечную дистрофию Дюшенна, аритмогенную правожелудочковую кардиомиопатию, гипертрофию левого желудочка, раннюю реполяризацию, острую ишемию миокарда или инфаркт, легочную эмболию, стенокардию Принцметала, расслаивающуюся аневризму аорты, дефицит тиамина, гиперкалиемию, гиперкальциемию и гипотермию.
Другие уточненные нарушения сердечного ритма: Лечение[править]
Имплантируемый кардиовертер-дефибриллятор — единственный терапевтический вариант с доказанной эффективностью при первичной и вторичной профилактике остановки сердца. Таким образом, правильная стратификация риска является главной целью управления. Хинидин можно рассматривать как вспомогательную терапию для пациентов с более высоким риском и может уменьшить количество случаев шока у пациентов с риском рецидива.
Прогноз
Большинство пациентов с синдромом внезапной смерти остаются бессимптомными, 20-30% испытывают синкопе и 8-12% испытывают по крайней мере один эпизод остановки сердца (потенциально приводящий к внезапной смерти). Факторами риска остановки сердца и внезапной смерти являются характерная картина ЭКГ и анамнез обмороков.
Профилактика[править]
Прочее[править]
Синдром укорочения интервала QT
Определение и общие сведения
Семейный синдром укорочения интервала QT — это недавно описанный кардиологический синдром, который описывает укорочение интервал QT (QT и QTc менее 300 мс) с высоким риском развития обморока или внезапной смерти из-за желудочковой аритмии.
Крайне редкий синдром, поражает в основном молодых людей или младенцев. Наследование аутосомно-доминантное.
Этиология и патогенез
Мутации в трех различных генах KCNQ1, KCNH2 и KCNJ2, кодирующих ионные калиевые каналы миокарда, были идентифицированы при синдроме укорочения интервала QT.
Клинические проявления
Клинический проявления синдрома очень широки: от бессимптомного носительства до обморока или внезапной смерти. Часто сопровождается мерцательной аритмией.
Лечение
В настоящее время автоматический имплантируемый дефибриллятор является единственным эффективным средством профилактики внезапной смерти при синдроме укорочения интервала QT.
Синдром желудочковой тахикардии типа «пируэт» с укороченным интервалом сцепления
Синдром желудочковой тахикардии типа «пируэт» с укороченным интервалом сцепления — крайне редкая тахикардии типа «пируэт», которая характеризуется укороченным интервалом сцепления первого удара TdP на ЭКГ при условии отсутствия какой-либо структурной аномалии сердца. Проявляется в раннем зрелом возрасте обмороком, который часто приводит к фибрилляции желудочков и несет в себе собой высокий риск внезапной смерти от остановки сердца.
Синдром постуральной ортостатической тахикардии
Определение и общие сведения
Синдром ортостатической интолерантности включает в себя три клинические единицы:
- синдром постуральной тахикардии.
- пролапс митрального клапана с вегетативной недостаточностью.
- идиопатическую гиповолемию.
Эти состояния имеют схожую клиническую картину и близкие терапевтические подходы. Наиболее патогенетически изучен синдром постуральной тахикардии, поэтому в основном синдром ортостатической интолерантности описывают на модели этого синдрома. Несмотря на значительное количество больных, синдром ортостатической интолерантности остаётся наименее изученным и понятным среди всех вегетативных нарушений. Заболевают преимущественно молодые люди в возрасте от 15 до 45 лет, пик заболеваемости приходится на возраст около 35 лет, женщины страдают гораздо чаще, чем мужчины (соотношение женщины/мужчины составляет 5-4:1). Как правило, в результате заболевания нарушается работоспособность и даже социальная адаптация. Ортостатическая интолерантность характеризуется развитием во время стояния (в вертикальном положении) симптомов церебральной гипоперфузии (головокружение, ощущение «лёгкости в голове», затуманивание зрения, общая слабость, предобморочное состояние), ассоциирующихся с симптомами симпатической активации (тахикардия, тошнота, дрожь) и чрезмерным учащением сердцебиения (более, чем на 30 ударов в минуту). Часто эти состояния ошибочно диагностируют как тревожные расстройства. Ранее в медицинской литературе больных с похожими симптомами описывали под различными рубриками: «солдатское сердце», «раздражённое сердце», нейроциркуляторная астения, вазорегуляторная астения, частичная дизавтономия, гиперадренергическая ортостатическая гипотензия, синдром усилия и др. В настоящее время существуют убедительные доказательства того, что синдром ортостатической интолерантности в основе своей имеет нарушения, возникающие при вегетативном обеспечении перехода в вертикальное положение, а не первичную тревогу, с которой у него много общих симптомов.
В норме обеспечивают вертикальное положение рефлексы, которые регулируются вегетативной нервной системой и направлены на то, чтобы компенсировать воздействие гравитации на распределение крови. В основе синдрома ортостатической интолерантности лежит неполноценность рефлекторного ответа на изменившееся положение тела в пространстве (вертикальное положение). Нормальный адаптивный ответ на изменение положения тела (переход в вертикальное положение) продолжается приблизительно 60 с. Во время этого процесса сердцебиение учащается на 10-15 в минуту, диастолическое давление повышается на 10 мм рт.ст., очень незначительно меняется систолическое давление. У больных, страдающих ортостатической интолерантностью, во время стояния чрезмерно усиливается сердцебиение, в результате сердечно-сосудистая система работает в усиленном режиме для поддержания АД и перфузии мозга. Вертикальное положение тела также обеспечивается нейрогуморальным ответом, включающим изменение содержания вазопрессина, ренина, ангиотензина и альдостерона, гормонов, вовлечённых в регуляцию АД. Кроме того, артериальные барорецепторы, в частности, находящиеся в каротидном синусе, играют важную роль в регуляции АД и в рефлекторном ответе на изменившееся положение тела. Барорецепторы левого предсердия чувствительны к изменениям венозного давления. Падение венозного давления — триггер компенсаторного ответа на повышение АД. Любые нарушения вышеописанных процессов или их координации могут вызывать неадекватный ответ на переход в вертикальное положение, что клинически проявляется определённым набором симптомов, включая синкопе. Наиболее отличительный симптом синдрома постуральной тахикардии — утрированное повышение ЧСС в ответ на постуральные изменения. В отличие от больных с классической вегетативной недостаточностью у пациентов с синдромом постуральной тахикардии давление не падает, а сердцебиение заметно повышается во время стояния.
Этиология и патогенез
Постулируют, что у больных, страдающих синдромом постуральной тахикардии, имеется симпатическая денервация нижних конечностей, в то время как кардиальная симпатическая иннервация сохранена. Это приводит к неполноценной вазоконстрикции и чрезмерному депонированию крови в нижних конечностях во время стояния, что становится триггером выраженной рефлекторной тахикардии. Среди причин также выделяют вегетативную невропатию, которая может быть поствирусной или иммунозависимой. Существуют отдельные доказательства, свидетельствующие о барорефлекторной дисфункции и изменениях венозных функций. У больных с синдромом постуральной тахикардии иногда отмечают клиническое улучшение после солевых инфузий. Отдельные исследования выявляют гиповолемию, редукцию объёма эритроцитов у этой категории больных. Причина гиповолемии до конца не ясна, предполагают нарушения функционирования ренин-ангиотензин-альдостероновой системы. Высказывают предположения о том, что ренальная денервация может играть основную роль в этиологии синдрома постуральной тахикардии. Альтернативно гиповолемию рассматривают как вторичный феномен за счёт хронической симпатической активации. Повышение симпатической активации — конечная составляющая большинства предполагаемых механизмов синдрома постуральной тахикардии. Повышение симпатической активации подтверждается повышением содержания артериального норадреналина в состоянии покоя и увеличением ЧСС в покое.
Клиническая картина
Больные, как правило, предъявляют множество жалоб, чаще всего на головокружение, ощущение «пустоты в голове», затуманивание зрения, слабость во время стояния. Может беспокоить ощущение пульсации, дискомфорта в груди, дрожь, короткое отрывистое дыхание, головная боль, нервозность, неустойчивое настроение. У некоторых больных возникают гастроинтестинальные симптомы, такие, как тошнота, спазмы в животе, вздутие живота, запор или диарея.
У отдельных пациентов отмечают признаки венозного застоя: акроцианоз, отёки во время стояния. Патогенез симптомов в значительной степени остаётся непонятным. Успешное купирование тахикардии не всегда приводит к разрешению всех проявлений заболевания. Некоторые симптомы свидетельствуют о церебральной гипоперфузии, несмотря на нормальное системное АД. В то же время нет доказательств, что у этой категории больных существуют нарушения кровотока или церебральной ауторегуляции.
Симптомы могут возникать внезапно, часто после вирусных заболеваний. Напротив, у некоторых пациентов заболевание развивается исподволь. Тяжесть симптомов также крайне вариабельна: у некоторых больных бывают незначительные симптомы, часто только в период дополнительного ортостатического стресса (менструальный цикл, относительная дегидратация); у других развивается тяжёлая симптоматика, нарушающая обычное функционирование. Заболевание может разрешиться спонтанно или протекает с обострениями и относительными ремиссиями многие годы.
Диагностика
Характерная находка у больных с синдромом постуральной тахикардии — чрезмерное учащение сердцебиения при тестировании на поворотном столе или при стоянии. Диагностическими критериями считают повышение ЧСС более чем на 30 в минуту или достижение ЧСС более 120 в минуту в первые 10 мин вертикального положения на поворотном столе. Ортостатической гипотензии при этом не возникает. Дополнительным диагностическим тестом служит повысившееся в покое более чем до 600 нг/мл содержание норадреналина в венозной плазме. Дифференциальную диагностику проводят с состояниями, обусловленными вегетативной невропатией, длительным постельным режимом, побочными эффектами медикаментов и дегидратацией. Синдром постуральной тахикардии следует отличать от синдрома синусовой тахикардии. Последний характеризуется увеличением ЧСС, не зависящим от постуральных изменений.
Из-за неопределённости клинической симптоматики у многих больных с синдромом постуральной тахикардии диагностируют панические, тревожные, соматизированные расстройства. Указание на зависимость предъявляемых жалоб от постуральных изменений у таких больных должна заставлять клиницистов активно выявлять у этой категории больных синдром постуральной тахикардии.
Лечение
Оптимальной терапии синдрома постуральной тахикардии не разработано. Необходимо исключать провоцирующие факторы, в частности дегидратацию, длительную иммобилизацию. Поскольку многие больные с синдромом постуральной тахикардии страдают гиповолемией, симптоматика может улучшиться при использовании солевых диет и минералокортикоидов. Предварительные исследования показали успешность применения агонистов адренорецепторов (мидодрин в дозе 2,5 мг три раза в день). Позитивный эффект на ЧСС отмечен во время тестирования на поворотном столе, однако эффективность постоянной терапии пока не исследована. Некоторые пациенты, в частности, жалующиеся преимущественно на адренергические симптомы, откликаются на β-блокаторы (пропранолол). Пропранолол начинают назначать с малых доз и повышают дозу градуированно (например, инициальнальная доза — 10 мг с постепенным повышением до 30 мг три или четыре раза в день). Позитивный эффект β-блокаторов описан в коротких исследованиях. Длительность приёма и терапевтический ресурс пропранолола при длительном использовании остаются неисследованными.
Источники (ссылки)[править]
https://www.orpha.net
«Неврология [Электронный ресурс] : национальное руководство / Под ред. Е.И. Гусева, А.Н. Коновалова, В.И. Скворцовой, А.Б. Гехт. — М. : ГЭОТАР-Медиа, 2016. — (Серия «Национальные руководства»).» — https://old.rosmedlib.ru/book/ISBN9785970436202.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
- Аценокумарол
- Ацетилсалициловая кислота
- Дигоксин
- Ланатозид Ц
- Прокаинамид
Источник
