Синдром апноэ во сне вейн
Апноэ во сне — разновидность апноэ, для которого характерно прекращение лёгочной вентиляции во время сна более чем на 10 секунд. Чаще оно длится 20—30 секунд, хотя в тяжёлых случаях может достигать 2-3 минут и занимать до 60 % общего времени ночного сна. При регулярных апноэ (обычно не менее 10—15 в течение часа) возникает синдром апноэ во сне с нарушением структуры сна и дневной сонливостью, ухудшением памяти и интеллекта, жалобами на снижение работоспособности и постоянную усталость. Различают обструктивное и центральное апноэ во сне, а также их смешанные формы.
Обструктивные апноэ во сне[править | править код]
Сужение верхних дыхательных путей во время сна предрасполагает к обструктивным апноэ. При апноэ длительностью более 10 секунд возникает состояние гипоксии и гиперкапнии с метаболическим ацидозом, с увеличением выраженности изменений по мере нарастания длительности апноэ. На определённом пороге этих изменений наступает пробуждение или переход в поверхностную стадию сна, при которой повышается тонус мышц глотки и рта с восстановлением проходимости глотки. Это сопровождается серией глубоких вдохов, обычно с сильным храпом. По мере нормализации показателей газового состава крови наступает более глубокая фаза сна.
У больных обструктивными апноэ не происходит снижения артериального давления во время сна; во время эпизода апноэ оно, напротив, резко повышается. В связи с этим, обструктивные апноэ во сне являются фактором риска заболеваний сердечно-сосудистой системы — артериальной гипертензии (у 40-90 % больных), ишемической болезни сердца, инсульта[2][неавторитетный источник?], диабета[3].
В некоторых случаях (до 10 %) при обструктивных апноэ развивается лёгочная гипертензия с правожелудочковой недостаточностью, хронической гиперкапнией и гипоксией, связанными с ослаблением нервной импульсации в дыхательной мускулатуре или генерализованной бронхиальной обструкцией. В сочетании с ожирением (являющимся одним из факторов риска обструктивных апноэ) и сонливостью эта картина носит название «пиквикский синдром».
«Золотым стандартом» лечения обструктивного апноэ сна является так называемая СИПАП-терапия (от англ. Constant Positive Airway Pressure, CPAP), выполняемая с помощью СИПАПов — специальных приборов, нагнетающих воздух под давлением в дыхательные пути и создающих постоянное положительное давление. Создается так называемая «воздушная шина», которая препятствует коллапсу во время сна. На сегодня это самый эффективный метод лечения этого заболевания[4].
Также было замечено прекращение храпа, дневной сонливости и уменьшение апноэ во сне у людей, играющих на австралийской дудке диджериду, благодаря тренировке верхних дыхательных путей из-за специфической техники дыхания[5][6][7].
Центральные апноэ во сне[править | править код]
Центральные апноэ во сне наблюдается в норме, чаще при засыпании и в фазе быстрого сна. У здоровых лиц центральные апноэ редки и не сопровождаются патофизиологическими и клиническими проявлениями. При нарушении стабильности функционирования центральных (стволовых) механизмов регуляции дыхания развиваются дыхательные нарушения характерные для обструктивных апноэ. Чаще наблюдается гипокапния без гипоксемии, реже формируется гиперкапния и гипоксемия, сопровождающиеся лёгочной гипертензией и правожелудочковой недостаточностью. Отмечаются частые ночные пробуждения с дневной сонливостью.
Примечания[править | править код]
- ↑ Disease Ontology release 2019-08-22 — 2019-08-22 — 2019.
- ↑ [1]
- ↑ E. Frija-Orvoën. Obstructive sleep apnea syndrome: Metabolic complications (англ.) // Revue Des Maladies Respiratoires. — 2016. — 23 March. — ISSN 1776-2588. — doi:10.1016/j.rmr.2015.11.014.
- ↑ Bing Lam, Kim Sam, Wendy Y. W. Mok, Man Tat Cheung, Daniel Y. T. Fong. Randomised study of three non-surgical treatments in mild to moderate obstructive sleep apnoea (англ.) // Thorax. — 2007. — April (vol. 62, iss. 4). — P. 354–359. — ISSN 0040-6376. — doi:10.1136/thx.2006.063644.
- ↑ Игра на старой дудке останавливает храп. membrana.ru (23 декабря 2005). Дата обращения 14 ноября 2014.
- ↑ Апноэ сна. Пер. с англ. Н. Д. Фирсовой (2017).
- ↑ Milo A Puhan, Alex Suarez, Christian Lo Cascio, Alfred Zahn, Markus Heitz, Otto Braendli. Didgeridoo playing as alternative treatment for obstructive sleep apnoea syndrome: randomised controlled trial (англ.) // The BMJ : еженедельный реферируемый научный журнал. — BMJ Group, 2006. — Vol. 332. — P. 266. — ISSN 0959-8138. — doi:10.1136/bmj.38705.470590.55.
Литература[править | править код]
- Вейн А. М., Елигулашвили Т. С., Полуэктов М. Г. Синдром апноэ во сне. — М.: Эйдос Медиа, 2002. — 312 с. — ISBN 5-94501-002-2.
- Зильбер А. П. Синдромы сонного апноэ: клиническая физиология, лечение, профилактика. — Петрозаводск: Петрозавод.ун-та, 1994. — 183 с.
- Николин К. М. Синдром сонного апноэ (лекция для врачей). — Санкт-Петербург, 2005. — 24 с.
- Пустозеров В. Г., Жулев Н. М. Современные методы диагностики и лечения нарушений сна : учебное пособие. — Санкт-Петербург: СПбМАПО, 2002. — 77 с.
- Зелвеян П. А. Клиника и диагностика синдрома апноэ во сне. Взаимосвязь с артериальной гипертонией
- Апноэ во сне: определение и классификация
Источник
Вернуться в раздел: Терапия
Анисенкова А.Ю., Белокопытов И.Ю., Кудинов П.Ю., Шабалина Е.А.
Факторы риска развития синдрома обструктивного апноэ во сне:
- врожденные особенности дыхательных путей;
- увеличение миндалин, полипы носоглотки;
- ожирение;
- снижение тонуса глоточных мышц при старении, употреблении алкоголя и снотворных.
Пациенту, у которого лечащий врач заподозрил синдром обструктивного апноэ во сне, предлагается проведение кардио-респираторного мониторирования (данное исследование проводиться в отделение функциональной диагностики нашей больницы), по результатам которого Вас может проконсультировать врач-сомнолог. При подтверждении диагноза, врач-сомнолог проводит подбор СИПАП-терапии (данные процедуры оплачиваются в отделе палатных услуг нашей больницы, так как не входят в исследования, проводимые по полису ОМС).
Основным методом лечения пациентов с выраженными формами синдрома обструктивного апноэ является вспомогательная вентиляция легких постоянным положительным давлением во время ночного сна (так называемая СИПАП-терапия — от английских слов «Constant Positive Airway Pressure», CPAP). Для этого используется специальный аппарат, представляющий небольшой компрессор, который подает в дыхательные пути постоянный поток воздуха через гибкую трубку и носовую маску. Эффект лечения достигается в первую же ночь. Аппарат не излечивает пациента, но обеспечивает нормальный сон и значительно уменьшает риск осложнений со стороны сердечно-сосудистой системы.
Любое заболевание легче предупредить или лечить в ранней стадии. В этой связи отдельным важным направлением работы терапевтического отделения является ранняя диагностика и профилактика обострений заболеваний внутренних органов.
Для этого предусмотрен плановый порядок госпитализации в терапевтическое отделение (на стационарную койку или койку дневного пребывания).
Клинический случай
Пациентка С., 56 лет, длительно страдает хронической обструктивной болезнью легких. Имеет длительный стаж курения. В 2009 году диагностирован сахарный диабет 2 типа. В том же году перенесла инфаркт миокарда.
В связи с нарастающей в течение нескольких месяцев одышкой и отечным синдромом 09.12.2012 поступила в терапевтическое отделение ГБ №40. При поступлении также предъявляла жалобы на увеличение массы тела, дневную сонливость вплоть до засыпания во время разговора, храп, частые ночные пробуждения с целью мочеиспускания.
При осмотре: гиперстеническое телосложение, избыточная масса тела (масса тела 95 кг, рост 156 см, ИМТ 39 кг/м2). Выраженный акроцианоз, отеки стоп и голеней (рисунки 1, 2, 3). Тахипноэ (ЧДД 23 в мин), оксигенация артериальной крови кислородом в покое в положении сидя была равна 93% и снижалась до 80 в положении лежа.
Тяжесть состояния была обусловлена ухудшением течения основного заболевания, нарастанием явлений сердечно-легочной недостаточности, нарастанием отеков и одышки, появлением гипоксической энцефалопатии. При обследовании пациентки в отделении было выявлено повышение гемоглобина до 165 г/л, эритроцитов до 6,25×1012/л, гематокрита до 57%; уровня глюкозы до 9,5 ммоль/л; артериальная гипоксемия. При рутинной ЭКГ зарегистрированы одиночные предсердные экстрасистолы, по данным холтеровского мониторирования ЭКГ были выявлены ночная тахикардия и желудочковая экстрасистолия 4а градации по Ryan.
ЭхоКГ показало наличие легочной гипертензии 2 ст. с давлением в легочной артерии 46-51 мм рт.ст. и снижение фракции выброса до 41%.
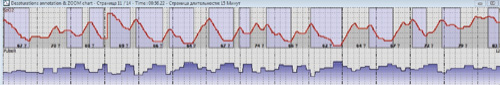 |
| Фрагмент исследования сатурации пациентки С. до начала СИПАП терапии. Циклические десатурации характерные для апноэ во сне |
С учётом жалоб, данных объективного осмотра и результатов обследования был заподозрен синдром обструктивного апноэ сна (СОАС) и выполнена пульсоксиметрия, при которой выявлено большое количество десатураций и хроническая ночная гипоксемия (Мин spO2 – 53%, средняя spO2 – 81%, spO2 менее 88 – 61% времени исследования, ИАГ = 62 в час, колебания пульса: от 60 до 101 уд в мин) (рис. 4).
Форма и цикличность этих эпизодов снижения сатурации, сопутствующие заболевания и жалобы позволили установить диагноз: синдром обструктивного апноэ сна (без уточняющей диагностики) и назначить в качестве лечения СиПАП терапию.
СИПАП – (Constant Positive Airway Pressure, CPAP) — режим искусственной вентиляции лёгких постоянным положительным давлением. СИПАП -терапия была предложена и введена в клиническую практику в 1981 году австралийским врачом профессором Колином Салливаном (Colin Sullivan) для лечения обструктивного апноэ сна. Данный способ искусственной вентиляции лёгких также используется в составе более сложных аппаратов ИВЛ с целью предотвращения повреждения избыточным давлением при длительной искусственной вентиляции лёгочной ткани.
СИПАП – аппарат представляет собой небольшой компрессор, который подает постоянный поток воздуха под определенным давлением в дыхательные пути через гибкую трубку и герметичную носовую маску. Таким образом, он не даёт дыхательным путям смыкаться и блокировать поступление воздуха. В результате исключается риск внезапной смерти от отсутствия кислорода, а также обеспечивается нормальный сон. Пациент высыпается и на следующий день чувствует себя здоровым. Пропадает утренняя усталость, разбитость, сонливость, «неясность» сознания, тяжесть в голове. Существенно уменьшается риск автомобильных аварий и других чрезвычайных происшествий из-за неожиданного засыпания.
В настоящее время СИПАП-терапия используется при лечении храпа, апноэ сна, артериальной гипертонии, дыхательной недостаточности, сердечно-сосудистых заболеваний, дневной сонливости, ожирения, импотенции, сахарного диабета, бессонницы, депрессии.
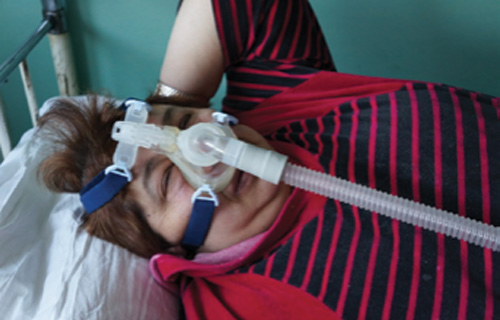 |
| Пациентка с аппаратом для СИПАП-терапии |
Терапия с применением СИПАП продолжается в течение нескольких месяцев, а в тяжёлых случаях – в течение всей жизни.
Подбор режимов использования СИПАП, а также решение вопроса о необходимости его применения, производится во время полисомнографии — исследования сна пациента в специальной лаборатории.
Решение о необходимости подобного лечения может быть принято также на основе результатов кардиореспираторного мониторинга.
На фоне проводимой терапии было отмечено значительное улучшение состояния: улучшился сон, прекратились пробуждения в ночное время с целью мочеиспускания, исчезла дневная сонливость, уменьшилась одышка при физической нагрузке. Надо отметить, что в случаях, когда СОАС сочетается с ХОБЛ и сопровождается хронической гипоксемией, которая не устраняется СИПАП терапией, рекомендуется проводить неинвазивную вентиляцию легких в более сложном режиме БИПАП.
БИПА ‘П (от англ. Biphasic Positive Airway Pressure, BPAP, BiPAP) — аппарат, создающий на вдохе и выдохе пациента давление различного уровня. Однако из-за высокой стоимости оборудования для этого режима неинвазивной вентиляции пациентка отказалась от данного вида терапии. Пациентка выписалась со значительным улучшением в удовлетворительном состоянии с рекомендациями по продолжению СИПАП терапии в домашних условиях.
Заключительный диагноз:
ИБС. Атеросклеротический и постинфарктный кардиосклероз (ОИМ от 2009 г.) Гипертоническая болезнь III стадии, АГ I степени, риск ССО 4 ст.
Ожирение II ст. Синдром обструктивного апноэ сна, тяжелая форма. Альвеолярная гиповентиляция. Хроническая обструктивная болезнь легких, средне-тяжелое течение, стадия обострения. Осложнения: ДН II ст. ХСН II Б ст, III ФК по NYHA. Желудочковая экстрасистолия 4а градации по Ryan Сопутствующий: ЦВБ. Церебральный атеросклероз. ДЭП I ст. Сахарный диабет, 2 тип, субкомпенсация.
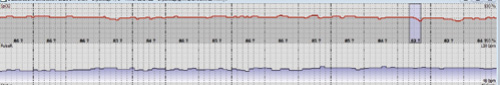
 |
| Фрагмент исследования сатурации пациентки С. на фоне СИПАП-терапии.Кривая сатурации с сохраняющейся хронической гипоксией, но без циклических десатураций |
Для динамического наблюдения и коррекции терапии была проведена госпитализация 27.08.2013 г. (через 8 мес.) Выполнена повторная пульсоксиметрия. Исследование показало, что эпизодов циклической десатурации у пациентки нет, однако сохраняется хроническая ночная гипоксемия, хоть и в меньшей степени выраженности, чем до начала лечения. По данным, полученных с СиПАП аппарата, количество эпизодов апноэ уменьшилось с 62 до 2,4 в час (рис.5).
При осмотре отмечалось отсутствие акроцианоза и отеков нижних конечностей. Сатурация крови в покое была равна 93%. Со слов пациентки, её престала беспокоить дневная сонливость, ушли отеки, значительно уменьшилась одышка при физической нагрузке.
Повторное лабораторное и инструментальное обследование пациентки показало снижение уровня гемоглобина до 153 г/л, эритроцитов до 5,28×1012/л и гематокрита до 45,7 %; тенденцию к нормализации уровня глюкозы крови (до 8,9 ммоль/л), уменьшение давления в легочной артерии до 38 мм рт. ст., значительное уменьшение количества желудочковых экстрасистол, уменьшение явлений хронической легочно-сердечной недостаточности, увеличение фракции выброса левого желудочка.
Комментарий к клиническому случаю
Синдром обструктивного апноэ во сне (СОАС) — состояние, характеризующееся наличием храпа, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением SaO2, грубой фрагментацией сна и чрезмерной дневной сонливостью [Guilleminault C., 1976]. СОАС выделен в отдельную нозологическую форму, которая представлена в Международной классификации болезней в разделе болезни нервной системы, код G 47.3 –апноэ во сне.
В возрастной группе старше 30 лет СОАС наблюдается у 5–9% всей популяции независимо от пола и отмечается у 15% пациентов терапевтического профиля [2, 3, 4, 5], что во многом сопоставимо с распространенностью бронхиальной астмы [7] или сахарного диабета.
У пациентов с СОАС подавляющее большинство жалоб носит неспецифический характер: беспокойный, неосвежающий сон, повышенная двигательная активность рук и ног, при пробуждении ночью – удушье, сердцебиение, дискомфорт в груди, страх, частое мочеиспускание (у взрослых), энурез (у детей), головная боль по утрам, храп, который перемежается промежутками тишины, при возобновлении дыхания: взрывной храп, вздохи, стоны, бормотание. Храп усиливается при сне на спине.
Известно, что СОАС может встречаться в любом возрасте, но наиболее часто выявляется у мужчин среднего возраста с избыточной массой тела, достигая в этой группе 10%. Механизм развития симптомов в данной группе обусловлен отложением висцерального жира рядом с латеральными стенками глотки и сужением просвета глотки, мягкого неба, что приводит к спадению дыхательных путей во время вдоха. У лиц старше 60 лет частота СОАС достигает 30%, но в данной возрастной группе механизм развития несколько отличается — на первый план выходит возрастное снижение тонуса мышц глотки.
У лиц, страдающих этим заболеванием в тяжелой форме, нарушен тонус симпатической системы, что приводит к дестабилизации течения артериальной гипертензии, появлению нарушений ритма и проведения. Доказано, что за 12 лет риск фатальных сердечно-сосудистых осложнений у таких пациентов увеличивается в 3 раза и в 4–5 раз увеличивается риск нефатальных сердечно-сосудистых событий. Своевременное назначение СИПАП (неинвазивная вентиляция легких в режиме постоянного положительного давления) терапии приводит к существенному снижению этих рисков до средних в популяции [6].
Для диагностики СОАС используется пульсоксиметрия, как скрининговый метод оценки насыщения крови кислородом. При этом выявление эпизодов десатурации с характерной цикличностью может говорить о наличии у пациента синдрома апноэ во сне. Для уточнения диагноза используются кардиореспираторное мониторирование или полисомнография. При этих исследованиях дополнительно оцениваются такие показатели, как поток воздуха из носа, движения грудной клетки и живота, ЭКГ, движения ног, глаз, нижней челюсти и энцефалограмма.
У пациентов с диагностированным СОАС проводится подбор СИПАП терапии, целью которой является создание постоянного положительного давления в дыхательных путях, препятствующего спадению мышц глотки. При выявлении изолированного обструктивного апноэ подбор режима вентиляции не представляет сложности и занимает около трех дней. Надо отметить, что СОАС часто ассоциирован с уже имеющейся хронической легочной патологией (хроническая обструктивная болезнь легких), сердечной недостаточностью (кардиомиопатия, пороки сердца и др.), альвеолярной гипоксимией у пациентов с синдромом Пиквика. В этих случаях имеется сочетание хронической гипоксемии и эпизодов десатурации на фоне обструктивного апноэ и методом выбора является БИПАП-терапия, которая позволяет большим объемом воздуха вентилировать легкие, не затрудняя выдох.
Таким образом, применение скрининговой мониторинговой пульсоксиметрии в отделениях терапевтического профиля позволяет своевременно выявить наличие синдрома обструктивного апноэ сна и назначить специфическую терапию.
Своевременное и правильное лечение СОАС в сочетании с консервативной терапией позволяет осуществлять эффективную профилактику коронарных событий и улучшает качество жизни пациентов.
Литература
- Вейн А.М. и др. Синдром апноэ во сне и другие расстройства дыхания, связанные со сном: клиника, диагностика, лечение // Эйдос Медиа, 2002.
- Романов А.И. Медицина сна. – М.: Слово, 1998.
- Jennum P., Soul A. Epidemiology of snoring and obstructive sleep apnoea in the Dannish population age 30–60 // J. Sleep Res. — 1992. — №1. — Р. 240–244.
- Lavie P., Ben-Yosef R., Rubin A.E. Prevalence of sleep apnea syndrome among patients with essential hypertension // Am. Heart. J. – 1984. — Vol.108. — P. 373–376.
- Lindberg E., Gislason T. Epidemiology of sleep-related obstructive breathing. // Sleep Med.Rev. — 2000. — N4. — P. 411–433.
- Marin J.M., Carrizo S.J., Vicente E., Agusti A.G. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. // Lancet. — 2005. — Vol. 365. — P. 1046 –1053.
- Young T., Finn L., Peppard P.E., Szklo-Coxe M. et al. Sleep disordered breathing and mortality: eighteen–year follow-up of the wisconsin sleep cohort // Sleep. — 2008. — Vol.31, N8. – P. 1071–1078.
← Назад
Источник
Для понимания актуальности проблемы приведем клинический пример. Пациент К. 59 лет, поступил в отделение медицины сна Клинического санатория «Барвиха» 9 апреля 2009 г. с жалобами на повышение артериального давления преимущественно в утренние часы, храп, остановки дыхания во сне с последующими всхрапываниями (со слов окружающих), пробуждения от нехватки воздуха и приступов удушья, изжогу по ночам, приступообразный ночной кашель, учащенное ночное мочеиспускание (3–5 раз за ночь полным мочевым пузырем), неосвежающий сон, разбитость и головную боль по утрам, резкую дневную сонливость.
Анамнез: храп отмечает около 10 лет, за это время вес увеличился на 10 кг. Прочие указанные выше жалобы появились около пяти лет назад и постепенно нарастали. Родственники постоянно обращали внимание на остановки дыхания во сне. По поводу вышеперечисленных жалоб пациент неоднократно обращался к врачам, но диагноза «апноэ сна» не выставлялось. За несколько дней до поступления в санаторий «Барвиха» пациент обратился к неврологу с жалобами на плохой сон. Пациенту был назначен Феназепам на ночь, на фоне приема которого у пациента в ранние утренние часы развился тяжелый гипертонический криз, и он был госпитализирован в кардиологическое отделение. На следующее утро сосед по палате рассказал пациенту, что тот громко храпел, периодически переставал дышать на минуту и более и при этом синел. И именно сосед предположил, что у пациента имеется апноэ сна, и порекомендовал обратиться в медицинский центр, где ему смогут помочь. Родственники пациента нашли информацию об отделении медицины сна санатория «Барвиха» в интернете.
При проведении полисомнографии (рис. 1) в отделении у пациента зарегистрировано 364 эпизода апноэ и 22 эпизода гипопноэ обструктивного генеза. Индекс апноэ + гипопноэ = 58 в час. Максимальная остановка дыхания составила 87 секунд. Эпизоды апноэ сопровождались резкими десатурациями (минимальная сатурация — 64%). Следует отметить, что при сатурации ниже 70% развивается диффузный цианоз. У пациента был выставлен диагноз: «синдром обструктивного апноэ сна, тяжелая форма».
В приведенной истории болезни обращает на себя внимание тот факт, что, несмотря на классическую клиническую картину заболевания, диагноз был поставлен не врачами, к которым пациент регулярно обращался, а соседом по палате. Таким образом, врачи еще недостаточно информированы о клинической значимости апноэ сна. А назначение Феназепама у пациента с апноэ сна можно расценить как грубую диагностическую и лечебную ошибку.
Итак, статья будет посвящена синдрому обструктивного апноэ сна (СОАС) — состоянию, характеризующемуся наличием храпа, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением уровня кислорода крови, грубой фрагментацией сна и избыточной дневной сонливостью [Guilleminault C., 1976].
Классификация, эпидемиология
Из определения СОАС видно, что в основе болезни лежит периодическое прекращение дыхания из-за спадения стенок дыхательных путей на уровне глотки во сне. Дыхательные пути могут спадаться полностью, и тогда развивается апноэ — прекращение воздушного потока (легочной вентиляции) длительностью 10 c и более. При неполном спадении дыхательных путей отмечается гипопноэ — существенное снижение воздушного потока (более 50% от исходных значений), сочетающееся со снижением насыщения гемоглобина артериальной крови кислородом (сатурации) на 3% и более.
Общепризнанным критерием степени тяжести СОАС является суммарная частота апноэ и гипопноэ в час — индекс апноэ/гипопноэ (ИАГ). Считается нецелесообразным подсчитывать отдельно количество апноэ и гипопноэ, так как они несут схожие риски в отношении развития сердечно-сосудистых и иных осложнений. В настоящее время большинство международных консенсусов и клинических рекомендаций придерживаются классификации, приведенной в табл.
Распространенность СОАС составляет 5–7% от всего населения старше 30 лет. Тяжелыми формами заболевания страдают около 1–2% из указанной группы лиц (Stradling J. R. и соавт., 1991). Данные показатели сопоставимы с распространенностью бронхиальной астмы (Young T. и соавт., 1993). У лиц старше 60 лет частота СОАС значительно возрастает и составляет около 30% у мужчин и около 20% у женщин. У лиц старше 65 лет частота заболевания может достигать 60% [Ancoli-Israel S., 1991]. Частота СОАС может достигать 50% и более у пациентов с рефрактерной к лечению артериальной гипертонией, ночными брадиаритмиями, ожирением 3–4 степени, метаболическим синдромом, пиквикским синдромом, гипотиреозом и рядом других заболеваний.
Этиология и патогенез
В основе патогенеза СОАС лежит периодическое спадение исходно суженных верхних дыхательных путей на уровне глотки во время сна. Причинами сужения могут быть:
- врожденная узость дыхательных путей;
- анатомические дефекты на уровне носа и глотки (полипы, увеличение миндалин, удлиненный небный язычок, новообразования);
- ретрогнатия и микрогнатия;
- сдавление дыхательных путей извне жировыми отложениями;
- отек глоточных структур (гипотиреоз);
- акромегалия.
Дополнительный вклад в проблему вносит снижение тонуса глоточных мышц, обусловленное рядом факторов:
- нейромышечные заболевания;
- дистрофические процессы на фоне старения;
- миорелаксирующее действие алкоголя или снотворных.
Зона, в которой наступает спадение, может находиться на уровне мягкого неба, корня языка или надгортанника, то есть в нижней части носоглотки и ротоглотке (рис. 2). Реализация указанного механизма обструкции дыхательных путей в патологическое состояние происходит следующим образом. Человек засыпает.
Происходит постепенное расслабление мышц глотки и увеличение подвижности ее стенок. Один из очередных вдохов приводит к полному спадению дыхательных путей и прекращению легочной вентиляции. При этом дыхательные усилия сохраняются и даже усиливаются в ответ на развивающуюся гипоксемию. Острый недостаток кислорода приводит к стрессовой реакции, сопровождающейся активацией симпатоадреналовой системы и подъемом АД. В конце концов, негативная информация от различных органов и систем доходит до мозга и вызывает его частичное пробуждение (активацию). Мозг, в свою очередь, восстанавливает контроль над глоточной мускулатурой и открывает дыхательные пути. Человек громко всхрапывает, делает несколько глубоких вдохов. В организме восстанавливается нормальное содержание кислорода, мозг успокаивается и засыпает вновь… Цикл повторяется снова. За ночь может отмечаться до 400–500 остановок дыхания по 20–30 секунд. Суммарная длительность апноэ может достигать 3–4 часов из 8 часов сна. Это в свою очередь существенно увеличивает риск развития артериальной гипертензии, нарушений ритма сердца, инфаркта миокарда, инсульта и внезапной смерти во сне.
Marin J. M. и соавт. (2005) провели 10-летнее наблюдение и получили достоверное 3 кратное увеличение фатальных (смерть от инфаркта миокарда или инсульта) осложнений и 4–5 кратное увеличение нефатальных сердечно-сосудистых событий (инфаркт, инсульт, операция коронарного шунтирования или баллонной ангиопластики) у пациентов с нелеченным тяжелым СОАС по сравнению со здоровыми добровольцами и пациентами с неосложненным храпом.
При тяжелых формах СОАС развиваются специфические гормональные расстройства. В частности, это касается снижения продукции соматотропного гормона (гормона роста) и тестостерона, пики секреции которых отмечаются в глубоких стадиях сна [Gronfier C. и соавт., 1996]. При СОАС глубокие стадии сна практически отсутствуют, что ведет к недостаточной продукции указанных гормонов [Grunstein R. R. и соавт., 1989]. Одной из функций соматотропного гормона у взрослых людей является регуляция жирового обмена и, в частности, мобилизация жира из депо. При недостатке соматотропина накопленный жир не может превратиться в энергию. Все образующиеся излишки ложатся «мертвым грузом», который не может быть востребован [Rudman D. и соавт., 1990]. Человек начинает полнеть, причем любые усилия, диетические или медикаментозные, направленные на похудание, оказываются малорезультативными. Более того, жировые отложения на уровне шеи приводят к дальнейшему сужению дыхательных путей и прогрессированию СОАС, а это в свою очередь усугубляет недостаток соматотропного гормона. Таким образом, создается порочный круг, разорвать который без специального лечения СОАС практически невозможно [Grunstein R. R. и соавт., 1989]. Недостаток тестостерона в организме ведет к снижению либидо и импотенции у мужчин.
Клиническая картина
В клинической картине, прежде всего, обращает на себя внимание типичный портрет пациента, страдающего СОАС. Обычно это полный человек с гиперстенической конституцией, красным или багрово-синюшным одутловатым лицом, инъецированными сосудами склер и хриплым голосом. Характерный вид пациента с СОАС был описан еще Чарльзом Диккенсом в «Посмертных записках Пиквикского клуба». Это был толстяк с короткой шеей и красным лицом, который постоянно засыпал и начинал храпеть в самых неудобных ситуациях.
Для выявления остановок дыхания во сне проще всего понаблюдать за спящим человеком. Обычно сразу после засыпания у человека появляется храп. Вскоре у больного внезапно останавливается дыхание. В это время не слышно дыхательных шумов, храп прекращается. Однако больной пытается дышать, что видно по движениям грудной клетки и брюшной стенки. Примерно через 15–30 секунд человек громко всхрапывает и делает несколько глубоких вдохов и выдохов. Как правило, сон больного очень беспокоен: он вертится в постели, двигает руками и ногами, иногда что-то говорит.
При СОАС могут отмечаться следующие симптомы:
- храп и остановки дыхания во сне с последующими всхрапываниями;
- учащенное ночное мочеиспускание (> 2 раз за ночь);
- затрудненное дыхание, одышка или приступы удушья в ночное время;
- гастроэзофагеальный рефлюкс (отрыжка) в ночное время;
- ночная потливость;
- частые пробуждения и неосвежающий сон;
- ночная и утренняя артериальная гипертензия;
- разбитость по утрам;
- утренние головные боли;
- выраженная дневная сонливость;
- депрессия, апатия, раздражительность, сниженный фон настроения.
Диагностика
Для скрининга нарушений дыхания во сне может применяться компьютерная мониторинговая пульсоксиметрия — метод длительного мониторирования сатурации и пульса. Компьютерный пульсоксиметр выполняет до 30 000 измерений сатурации и пульса за 8 часов сна и сохраняет полученные данные в памяти. Дальнейшая компьютерная обработка данных позволяет с высокой точностью оценивать средние параметры сатурации, проводить визуальный анализ оксиметрических трендов, выявлять острые эпизоды падения насыщения крови кислородом, характерные для апноэ. Количественная оценка частоты десатураций в час (индекс десатураций) позволяет косвенно судить о частоте эпизодов апноэ/гипопноэ в час (ИАГ).
Для точной диагностики храпа и болезни остановок дыхания во сне используется полисомнография — метод длительной регистрации различных функций человеческого организма в период сна (рис. 1). Исследование позволяет поставить точный диагноз, оценить сердечно-сосудистые и неврологические риски и определить оптимальную тактику лечения.
Одним из многообещающих направлений диагностики расстройств дыхания во сне является добавление к классическим холтеровским мониторам каналов регистрации пневмограммы, сатурации и потока воздуха. Данные системы уже имеются на отечественном рынке. Фактически выполняется полифункциональное холтеровское мониторирование ЭКГ и параметров дыхания во время сна, которое позволяет поставить собственно диагноз СОАС, а также оценить связь ночной ишемии миокарда, аритмий и блокад с нарушениями ритма во сне. Методика имеет большие перспективы как в специализированных аритмологических центрах, так и в учреждениях практического здравоохранения, занимающихся холтеровским мониторированием.
Лечение
Объем статьи позволяет нам лишь в общих чертах описать подходы к лечению храпа и СОАС. Следует подчеркнуть, что выбор конкретного метода или совокупности методов лечения у конкретного пациента зависит от сочетания причин и тяжести расстройств дыхания во сне.
Прежде всего, следует отметить, чего категорически нельзя делать у пациентов с СОАС — это назначать снотворные и транквилизаторы, обладающие миорелаксирующим и респираторно-депрессивным действием, например, бензодиазепиновые транквилизаторы [Вейн А. М., 2002]. В начале статьи мы упоминали пациента, которому был назначен Феназепам, который, по всей видимости, существенно ухудшил состояние и вызвал гипертонический криз. На уровне первичного звена здравоохранения, когда дефицит времени и ресурсов не позволяет исключить СОАС у пациентов с жалобами на плохой сон, а клиническая ситуация требует назначения снотворных, можно с осторожностью, взвешивая пользу и риски, назначать гипнотики, которые в наименьшей степени влияют на респираторную функцию. К ним относятся Донормил или небензодиазепиновые агонисты бензодиазепиновых рецепторв (Z-группа), например, Санвал.
Общепрофилактические мероприятия у пациентов с храпом и СОАС включают снижение массы тела, прекращение курения, ограничение потребления алкоголя, сон на боку. При неосложненном храпе возможно использование спреев для горла, облегчающих храп.
У пациентов с ретро- и микрогнатией возможно применение внутриротовых аппликаторов, смещающих вперед нижнюю челюсть.
При наличии явных анатомических препятствий на уровне носа и глотки (искривление носовой перегородки, резкая гипертрофия миндалин) требуется соответствующее хирургическое лечение.
Следует отдельно остановиться на селективных оперативных вмешательствах на мягком небе (лазерных или радиочастотных). При неосложненном храпе у пациентов с достаточно широким просветом глотки и исходно удлиненным небным язычком эти вмешательства эффективны. Однако у пациентов с исходно узкой глоткой и среднетяжелыми формами СОАС наблюдается мультисегментарное спадение дыхательных путей на уровне неба, корня языка и даже надгортанника. В этой ситуации подрезание небного язычка практически не дает эффекта в отношении апноэ сна. Более того, если после лазерного или радиочастотного ожога происходит ретракция тканей глотки, это может еще больше ее сузить и привести к развитию фарингостеноза. В свете изложенного становится понятным, почему в Стандартах Американской академии медицины сна по применению лазерной увулопалатопластики для лечения храпа и апноэ сна (1994, пересмотр 2000 г.) первый же пункт гласит: «Лазерная увулопалатопластика не рекомендуется для лечения расстройств дыхания во сне, включая синдром обструктивного апноэ сна».
Основным методом лечения пациентов со среднетяжелой формой СОАС и ожирением является неинвазивная вспомогательная вентиляция легких постоянным положительным давлением во время ночного сна (СРАР-терапия — аббревиатура английских слов Continuous Positive Airway Pressure). Суть метода очень проста. Если дыхательные пути немного «раздувать» во время сна, то это будет препятствовать их спадению и устранит основной механизм развития заболевания. Лечение проводится с помощью небольшого компрессора, который подает в дыхательные пути постоянный поток воздуха через гибкую трубку и носовую маску.
Полный эффект лечения достигается в первую же ночь лечения. У больного исчезают храп, остановки дыхания и нормализуется ночной сон. В тяжелых случаях аппарат необходимо использовать каждую ночь. При более легком течении заболевания возможно периодическое применение аппарата (4–5 раз в неделю). Лечение практически не дает побочных эффектов. Отмена аппаратного лечения (даже если оно проводилось несколько лет) не влечет за собой каких-либо осложнений, за исключением постепенного возвращения исходной симптоматики. Применение аппарата не изле?
