Сепсис у ребенка с синдромом дауна
Распространенность онкологических заболеваний при синдроме Дауна существенно выше по сравнению с распространенностью их в общей популяции. Это касается в основном риска развития острой лейкемии, в то время как солидные опухоли, такие как нейробластома или нефробластома, у детей с синдромом Дауна встречаются крайне редко. Также не часто встречаются хронический миелоидный лейкоз и хронический лимфолейкоз. Эти особенности, безусловно, связаны с наличием дополнительного генетического материала 21-й хромосомы. При синдроме Дауна частота лейкозов приблизительно в 18 раз выше, чем в населении в целом.
Лейкозы (лейкемии) — злокачественные опухоли кроветворной ткани с первичной локализацией в костном мозге с последующей диссеминацией их в периферической крови, селезенке, лимфатических узлах и других тканях. Различают острый и хронический лейкоз. Острый лейкоз – это быстро прогрессирующая форма лейкоза, характеризующаяся замещением нормального костного мозга незрелыми бластными клетками без дифференциации их в зрелые нормальные клетки крови. Выделяют две основные группы острого лейкоза: лимфобластный и нелимфобластный (миелоидный).
У большинства новорожденных с трисомией 21-й хромосомы сразу после рождения отмечаются изменения в регуляции гемопоэза (кроветворения), приводящие к различным нарушениям, таким как полицитемия, тромбоцитопения, тромбоцитоз и др. [1]. Эти нарушения обычно имеют транзиторный (проходящий) характер и возникают вследствие несовершенного контроля гемопоэтических клеток одной или нескольких линий [2]. Е. Генри и его коллеги проанализировали результаты клинических анализов крови, проведенных в первые две недели жизни 158 новорожденных с синдромом Дауна. Они обнаружили, что нейтрофилез (увеличение числа нейтрофилов), тромбоцитопения (снижение количества тромбоцитов) и полицитемия (увеличение числа форменных элементов крови) являются наиболее распространенными гематологическими нарушениями, которые встречаются у этих детей с частотой, равной 80, 66 и 33 % соответственно [3].
Более чем у 10 % новорожденных с синдромом Дауна в анализах крови встречается лейкемоидная реакция (транзиторная лейкемия). Причины возникновения лейкемоидной реакции не ясны, но однозначно связаны с дополнительной 21-й хромосомой. С одной стороны, это состояние не требует никакого лечения. С другой – оно говорит о повышенном риске развития лейкоза у этих детей в более старшем возрасте. В одном исследовании отмечается, что у 25 младенцев из 85 с выявленной лейкемоидной реакцией в неонатальном периоде в течение последующих 3 лет развился острый миелоцитарный лейкоз.
Манифестация лейкемии, как правило, приходится на первые 5 лет жизни детей с синдромом Дауна. В первые 3 года при трисомии 21-й хромосомы наиболее распространенной формой является острая миелоидная лейкемия с преобладанием подтипа мегакариоцитарной лейкемии. Отмечена связь развития мегакариоцитарного лейкоза с возникновением у этих пациентов соматической мутации в гене GATA 1 [4].
У заболевших лейкозом детей с синдромом Дауна старше 3 лет приблизительно в 80 % случаев отмечается острая лимфобластная лейкемия и в 20 % — острый миелоцитарный лейкоз.
Специфического лечения лейкоза для детей с синдромом Дауна не разработано, применяется стандартная терапия. При этом оказалось, что дети с трисомией 21-й хромосомы и острым миелоцитарным лейкозом имеют лучшие результаты лечения и более высокие показатели выживаемости, чем дети без трисомии с тем же заболеванием.
В качестве клинического примера приведем историю болезни девочки К. 2,5 лет.
Ребенок от 2-й физиологически протекавшей беременности, серологических и ультразвуковых признаков патологии плода не было. От 2-х самопроизвольных родов в сроке 39—40 недель гестации. При рождении антропометрические показатели в норме: масса 3450 г., длина 50 см. Оценка по шкале АПГАР 7/8 баллов. Отмечались признаки трисомии 21-й хромосомы, и после проведенного хромосомного анализа был установлен диагноз «синдром Дауна». Клинический анализ крови на первом месяце не проводился, а в возрасте 6 месяцев полученные результаты были в пределах нормы. Больше кровь не исследовалась. В возрасте 1 года 2 месяцев у ребенка поднялась температура до субфибрильных значении (37,5—37,8°). Очевидных признаков респираторного заболевания не было, отмечалась припухлость десен. Был установлен диагноз «Синдром прорезывания зубов». Девочка стала капризной, бледной, мало двигалась, отказывалась от еды. Появилась отечность лица. Субфибрилитет сохранялся более 7 дней. Было проведено исследование мочи. Выявлена протеинурия 0,06 г/л. На 7-й день болезни проведено исследование крови: отмечалась тромбоцитопения до 84×109/л, анемия (78 г/л), СОЭ увеличена до 31 мм/ч. В экстренном порядке ребенок госпитализирован в гематологическое отделение Морозовской детской клинической больницы, где диагностирован острый мегакариоцитарный лейкоз, проведено лечение, достигнута ремиссия.
Повышенный риск развития лейкоза у детей с синдромом Дауна требует регулярного исследования крови на протяжении первых 5 лет жизни ребенка. Ввиду связи между транзиторной лейкемией и развитием миелоцитарного лейкоза у этих детей в первые годы жизни обоснованным становится обязательное исследование крови у новорожденных с трисомией 21-й хромосомы. Выявление детей с повышенным риском развития лейкоза позволит своевременно диагностировать возникновение заболевания и начать адекватное лечение, принимая во внимание известные высокие шансы у этих пациентов на достижение полной ремиссии и выздоровление.
Литература
- Weinstein H. S. Congenital leukemia and the neonatal myeloproliferative disorders associated with Down’s syndrome // Clinical Hematology. 1978. № 7. P. 147—156.
- Miller M., Cosgriff J. M. Hematologic abnormalities in newborns with Down’s syndrome // Journal of Medical Genetics. 1973. Vol. 16. P. 173—179.
- Henry E., Walker D., Wiedmeier S. E., Christensen R. D. Hematological abnormalities during the first week of life among neonates with Down syndrome: data from a multihospital healthcare system // American Journal of Medical Genetetic. A. 2007. Vol. 143, № 1. P. 42—50.
- Management of genetic syndromes. 3rd edition / S. B.Cassidy, J. E. Allanson (Eds.). New York, NY : Wiley-Liss, 2008. P. 309—336.
Источник
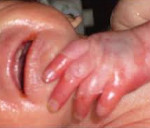
Сепсис новорожденных – генерализованная гнойно-септическая инфекция, характеризующаяся наличием первичного очага и циркуляцией инфекции в крови. Сепсис новорожденных проявляется признаками инфекционного токсикоза (температурной реакцией, вялостью, диспепсией, землистой окраской кожных покровов) и образованием гнойных метастатических очагов в различных органах (мозговых оболочках, легких, костях, печени и пр.). Диагноз сепсиса у новорожденных устанавливается на основании клинических критериев и выделения возбудителя при бактериологическом посеве крови. Лечение сепсиса новорожденных включает системную антибиотикотерапию, санацию первичного и метастатических гнойных очагов, посиндромную терапию.
Общие сведения
Сепсис новорожденных – общий инфекционный процесс, обусловленный попаданием условно-патогенной и гноеродной микрофлоры из локальных очагов в кровяное русло и сопровождающийся тяжелыми системными проявлениями. По данным зарубежной педиатрии, частота сепсиса новорожденных составляет 0,1-0,8%; среди недоношенных и детей с перинатальной патологией, находящихся в ОРИТ, — 14%. Неонатальная смертность, обусловленная сепсисом новорожденных, высока и стабильна – около 30-40%. Развитию сепсиса способствуют недостаточная сформированность барьерных механизмов и иммунитета у новорожденных, пограничные состояния периода новорожденности, патологическое протекание перинатального периода, сложность ранней диагностики септических состояний.
Причины сепсиса новорожденных
В настоящее время доминирующее место (около 50%) среди возбудителей сепсиса новорожденных принадлежит грамположительной флоре (главным образом, стафилококкам, гемолитическому стрептококку группы А). Чуть реже (до 40% случаев) выявляется грамотрицательная микрофлора (кишечная палочка, синегнойная палочка, клебсиелла и др.); в 10% этиологическими агентами выступает смешанная флора (часто ассоциация стафилококка с грибами Candida).
Входными воротами инфекции могут являться кожа и слизистые, пупочная ранка, желудочно-кишечный тракт, мочевые пути. Первичными очагами инфекции, приводящими к развитию сепсиса новорожденных, чаще выступают омфалит, пиодермии, конъюнктивит, отит, фарингит, бронхит, инфекции мочевыводящих путей, энтерит, дисбактериоз и пр. В группе риска по развитию сепсиса новорожденных находятся дети с недоношенностью, внутриутробной гипоксией, внутриутробными инфекциями, внутричерепной родовой травмой; пребывающие в ОРИТ, длительно находящиеся на ИВЛ; получающие парентеральное питание, инфузионную и трансфузионную терапию; перенесшие катетеризацию пупочной и центральной вен, хирургические вмешательства в первые дни жизни.
Со стороны матери факторами, способствующими бактериальной контаминации новорожденного, выступают бактериальный вагиноз, кольпиты, эндометрит. Большое значение имеет степень и характер иммуносупрессии у новорожденного, которые могут быть связаны с неполноценным питанием или приемом лекарств беременной, наследственным иммунодефицитом или ВИЧ-инфекцией. В отдельных случаях причиной вспышек сепсиса новорожденных становится несоблюдение санитарного режима в родильных или детских отделениях.
Классификация сепсиса новорожденных
По времени развития выделяют внутриутробный и постнатальный (ранний неонатальный и поздний неонатальный) сепсис новорожденных. Внутриутробный сепсис предполагает антенатальное или интранатальное инфицирование плода; при этом первичный гнойно-септический очаг располагается вне организма ребенка (чаще всего в его роли выступает плацентит, хорионит, хориоамнионит и т. д.). В случае постнатального сепсиса первичный гнойно-воспалительный очаг всегда располагается в организме самого новорожденного.
Ранний неонатальный сепсис новорожденных развивается в первые 4-ро суток жизни ребенка. Клинические течение заболевания обычно молниеносное, с быстрым развитием полиорганнной недостаточности, летальным исходом в 5-20% случаев. Поздний неонатальный сепсис новорожденных манифестирует на 5-й день и позднее. Характеризуется медленно прогрессирующим течением, возникновением вторичных септических очагов, 5-10%-ной летальностью.
Течение сепсиса новорожденных может быть молниеносным (3-7 дней), острым (до 4-8 недель), подострым (до 1,5-3 месяцев), затяжным (более 3 месяцев). С учетом локализации первичного септического очага и входных ворот различают: пупочный, кожный, легочный, ринофарингеальный, отогенный, риноконъюнктивальный, кишечный, урогенный, катетеризационный и др. виды сепсиса новорожденных. Сепсис новорожденных может протекать в форме септицемии или септикопиемии.
Симптомы сепсиса новорожденных
Септицемия или сепсис новорожденных без метастазов обычно развивается на фоне предшествующего мокнущего пупка, конъюнктивита, гнойничковой сыпи, опрелостей, стоматита. Предвестниками сепсиса новорожденных могут выступать вялость или беспокойство, снижение аппетита, обильные частые срыгивания, плохая прибавка в весе. В период разгара развивается температурная реакция (гипер- или гипотермия), отечный синдром или эксикоз, гипотрофия. Характерным признаком сепсиса новорожденных является грязновато-серый (землистый) оттенок кожных покровов, желтушность, мраморность кожи, сыпь.
Вследствие токсического поражения различных органов возникают гепатоспленомегалия, пневмопатия (тахипноэ, цианоз), кардиопатия (тахикардия или брадикардия, артериальная гипотензия), диспепсия, мочевой синдром (олигурия, анурия, ОПН), геморрагический синдром, надпочечниковая недостаточность. Чаще всего септицемия осложняется присоединением пневмонии, которая выступает как самостоятельное интеркуррентное заболевание.
Септикопиемия или сепсис новорожденных с гнойными метастазами характеризуется возникновением на фоне интоксикации вторичных очагов отсева в мозговых оболочках, легких, костях, печени, других органах. Чаще всего септикопиемия протекает с развитием гнойного менингита, абсцедирующей пневмонии, остеомиелита; реже – с формированием абсцесса печени, гнойного артрита, панофтальмита, медиастинита, флегмоны желудка или кишечника. В восстановительном периоде происходит санация пиемических очагов, стихание токсикоза, постепенное восстановление нарушенных функций.
Молниеносная форма сепсиса новорожденных протекает с развитием септического шока: стремительным ухудшением состояния ребенка, снижением температуры тела, брадикардией, кровоточивостью, отеком легких, острой почечной недостаточностью. Летальный исход при молниеносном течении сепсиса новорожденных наступает в течение 3-5 суток.
Диагностика сепсиса новорожденных
Диагноз сепсиса новорожденного может быть заподозрен неонатологом или педиатром на основании лихорадки свыше 3 дней или прогрессирующей гипотермии; гиперлейкоцитоза, сменяющегося лейкопенией; повышением содержания в крови маркеров инфекционного процесса (СРБ, интерлейкина-8, прокальцитонина).
Факт бактериемии при сепсисе новорожденных подтверждается путем посева крови на стерильность. Важное значение имеет выявление первичного гнойного очага и метастатических очагов, микробиологического исследование отделяемого из них (бактериологическое исследование мазка с конъюнктивы, мочи на микрофлору, соскоба/отделяемого с кожи на микрофлору, мазка из глотки, кала на дисбактериоз и т. п.).
Дифференциальная диагностика сепсиса новорожденных осуществляется с локализованными гнойно-воспалительными заболеваниями (пневмонией, медиастинитом, перитонитом, менингитом, энтероколитом), генерализованными вирусными инфекциями (цитомегалией, герпесом, энтеровирусной инфекцией) и микозами (кандидозом, аспергиллезом) и др. Для этого используются дополнительные лабораторные методы – ПЦР, ИФА, микроскопия.
Лечение сепсиса новорожденных
Терапия при сепсисе новорожденных проводится одновременно в нескольких направлениях и включает санацию септического и пиемических очагов, подавление циркуляции возбудителя в крови, коррекцию нарушенных функций.
Основу этиологического лечения сепсиса новорожденных составляет антибиотикотерапия: эмпирическая комбинированная до уточнения характера микрофлоры) и целенаправленная после получения антибиотикограммы. Противомикробные препараты вводятся внутривенно, в максимальных возрастных дозировках в течение 10-15 суток с последующей сменой. Чаще всего в клинической практике для лечения сепсиса новорожденных в различных сочетаниях используются цефалоспорины, аминогликозиды, аминопенициллины, карбапенемы и др.
С целью местного лечения гнойных очагов производится вскрытие фурункулов и абсцессов, перевязки с антибактериальными и ферментными препаратами; назначается УВЧ, СВЧ, электрофорез.
Патогенетическая терапия сепсиса новорожденных включает иммунокоррекцию (плазмаферез, гемосорбцию, введение иммуноглобулинов), проведение дезинтоксикационной терапии (внутривенной инфузии глюкозо-солевых растворов и свежезамороженной плазмы), адекватную кислородотерапию и т. д. При сепсисе новорожденных обязательно проводится мониторинг состояния жизненно-важных функций: АД, ЧСС, ЭКГ, КОС и газового состава крови, биохимических показателей (сахара крови, креатинина, электролитов), гематокрита.
В остром периоде сепсиса целесообразно пребывание новорожденных в кувезе, кормление материнским молоком, тщательный уход. В восстановительном периоде к лечению подключается гимнастика, массаж, лечебные ванны.
Прогноз и профилактика сепсиса новорожденных
Прогноз сепсиса новорожденных серьезный: летальность составляет от 30-40% до 60% среди глубоко недоношенных детей. У выздоровевших детей в отделенном периоде могут отмечаться частые ОРВИ, пиелонефрит, анемия, перинатальная энцефалопатия.
Профилактика сепсиса новорожденных включает выявление и санацию инфекций мочеполовой сферы у беременной, соблюдение противоэпидемических мероприятий медперсоналом родильных домов и отделений новорожденных, тщательный гигиенических уход за новорожденным, естественное вскармливание. Вопрос о сроках вакцинации новорожденных с сепсисом против туберкулеза и против гепатита В , проводимой в первые дни жизни, решается в индивидуальном порядке.
Источник
С появлением на свет ребёнка у молодых родителей возникает много вопросов, страхов, опасений. Ведь забота о малыше – ответственная и непростая работа. Мамы и папы должны многое знать и уметь, чтобы их кроха росла здоровой и счастливой. Но иногда радость от рождения ребёнка смешивается с ощущением страха за его жизнь. Особенно это случается, когда беременность или роды протекали не лучшим образом и малыш родился с патологией.
На долю маленьких пациентов выпадают значительные испытания, которые иногда не по силам и взрослому человеку. Непонятное родителям слово «сепсис», упомянутое врачом, говорит о серьёзной проблеме со здоровьем крохи. Родители должны знать о заболевании и понимать, как его предупредить. Если болезнь уже развилась у малыша, стоит ориентироваться в тактике лечения и возможных прогнозах болезни.
Что такое сепсис новорождённых?
Неонатальный сепсис – заражение крови, возникшее в период новорожденности, которое приводит к повреждению всех органов и систем организма. В основе болезни лежит системный ответ всего организма на внедрение бактериальной микрофлоры. Происходит генерализованное повреждение кровеносных сосудов, повышение их проницаемости, нарушение микроциркуляции и расстройство гемостаза.
Сепсис новорождённых – крайне опасное заболевание и без надлежащего лечения приводит к смерти ребёнка. До появления антибиотиков у младенцев с неонатальным сепсисом не было шансов выжить. В настоящее время летальность составляет 30 – 40%.
Что вызывает сепсис?
Наиболее частая причина развития сепсиса – внедрение бактериальной микрофлоры в организм малыша. Возбудителями сепсиса являются различные патогенные микроорганизмы, условно-патогенные бактерии, стафилококки, стрептококки. Но не исключено развитие болезни при инфицировании синегнойной и кишечной палочками, клебсиеллой, пневмококками. В некоторых случаях выделяется более одного возбудителя, возникает микст-инфекция, сопряженная с грибковой.
Входными воротами, через которые микроорганизмы попадают в кровь, чаще всего являются кожный покров, пупочная ранка, дыхательная система ребёнка, желудочно-кишечный тракт. Проникновение возбудителя возможно через ротовую и носовую полость, слизистую оболочку глаз, мочеполовые пути.
Возникновение сепсиса объясняется не только болезнетворностью микроорганизма, но и состоянием иммунитета ребёнка. Слабость иммунной системы заключается в неспособности справиться с бактерией или локализовать, ограничить воспалительный очаг. В итоге микроорганизмы попадают в кровеносное русло и распространяются по всему организму ребёнка.
Получается, что к развитию распространенных инфекционных процессов предрасполагают некоторые факторы, зная которые можно вовремя заподозрить и предупредить развитие болезни.
Факторы, предрасполагающие к развитию сепсиса у новорождённых
- инфекции у матери.
Урогенитальные болезни у женщины в течение беременности и во время родов, вагиниты, эндометриты, хориоамниониты – могут вызывать бактериальный сепсис новорождённых. Неблагоприятный фактор – обнаружение стрептококка группы В в родовых путях роженицы. Безводный период длительностью более 12 часов опасен для здоровья крохи;
- неблагоприятный анамнез.
Женщины со множественными абортами и выкидышами, патологией беременности, гестозом, длительностью более 4 недель, относятся к группе риска по развитию патологий у малыша. Много внимания уделяется женщине, предыдущая беременность которой закончилась смертью ребёнка. Дети, рожденные от таких матерей, требуют дополнительного обследования и тщательного наблюдения;
- заболевания новорождённого.
Среди новорождённых особого внимания требуют недоношенные дети, особенно с низкой и очень низкой массой при рождении. Заболеваемость сепсисом в данной группе достигает 1%, в сравнении с 0,1% у доношенных новорождённых.
Дети, рожденные в асфиксии, которые не смогли совершить первых вдох сразу после рождения, а потребовали реанимационных мероприятий, также относятся к группе риска. Особенно опасна энтеральная пауза, когда из-за тяжести состояния малышу было противопоказано кормление.
Дети с врождёнными пороками развития, дефектами иммунной системы, болезнями лёгких, внутриутробными инфекциями требуют пристального наблюдения и правильного ухода;
- вмешательства.
Любые хирургические вмешательства, искусственная вентиляция лёгких, катетеризация пупочной и центральных вен снижают защитную функцию естественных барьеров и травмируют ткани. Неблагоприятно сказываются и массивные курсы антибактериальной терапии у новорождённых, без учета чувствительности бактерий.
Каким бывает сепсис новорождённых?
Выставляя диагноз, врач обязательно уточняет, какой именно клинический вариант заболевания присутствует у ребёнка.
В зависимости от времени развития болезни различают следующие формы:
- ранний неонатальный сепсис.
Симптомы заражения при этом виде сепсиса появляются в первые 6 суток жизни ребёнка. Столь раннее развитие болезни указывает на заражение крохи во время беременности или в период родов. Отличительной особенностью недуга является отсутствие первичного гнойно-воспалительного очага, входных ворот инфекции;
- поздний неонатальный сепсис.
Признаки болезни появляются позже, начиная с 7 дня после рождения ребёнка. Чаще всего причиной позднего сепсиса является инфицирование крохи после рождения. Обнаруживается первичный очаг воспаления, который приводит к попаданию возбудителя в кровь малыша.
По расположению первичного гнойно-воспалительного очага выделяют следующие виды:
- пупочный сепсис новорождённых, возникающий при дефектах ухода за пупочной ранкой, длительной катетеризации пупочной вены;
- лёгочной сепсис, появляющийся при заболевании тканей лёгких, а также во время проведения искусственной вентиляции дыхательных органов;
- отогенный, входные ворота при котором – полость уха;
- ринофарингеальный и риноконъюнктивальный – первичные ворота инфекции расположились на слизистой оболочке носа, горла, глаза;
- урогенный и абдоминальный – инфекция проникла через мочеполовую систему или систему пищеварения;
- катетеризационный.
Клинические формы сепсиса новорождённых
- септицемия.
Данная форма более характерна для раннего неонатального сепсиса и проявляется наличием возбудителя в крови ребёнка, тяжёлым состоянием крохи, выраженными явлениями интоксикации. Особенность септицемии заключается в поражении внутренних органов без образования гнойных очагов;
- септикопиемия.
При развитии септикопиемии возбудитель проникает в различные органы и образует в них гнойные очаги. Данная форма болезни чаще встречается при позднем сепсисе, возникшем не ранее 7 дня жизни крохи.
Отличается сепсис и в зависимости от течения болезни:
- при молниеносной форме заболевание может протекать быстро, состояние малыша в таком случае ухудшается на глазах. Длительность болезни не превышает недели, в течение которой микроорганизм успевает проникнуть во все органы и системы;
- острый сепсис длится от 1 до 2 месяцев, подострый – до 3 месяцев, а затяжной протекает более 3 месяцев. Возможно развитие хронического течения болезни, длящейся до года и рецидивирующего варианта с чередованием периодов улучшения и ухудшения состояния малыша.
Хотя проявления сепсиса отличаются в зависимости от формы и течения болезни, при любом варианте существуют общие клинические проявления, характерные симптомы сепсиса.
Признаки сепсиса у новорождённых
- тяжесть состояния.
Вне зависимости от формы болезни, сепсис – очень серьёзное заболевание, при котором происходит значительное ухудшение состояния малыша. Ребёнок становится вялым, заметно снижение аппетита. Малыш перестаёт набирать в весе, развивается гипотрофия, происходит заострение черт лица;
- изменение температуры тела.
У доношенных детей повышается температура тела, достигая фебрильных цифр, более 38°С.
Особенностью недоношенных детей является слабость иммунного ответа, температура при сепсисе у недоношенных детей, в отличие от зрелых малышей, понижается. Гипотермия не превышает 36 °С, согреть ребёнка становится сложно;
- изменение цвета кожного покрова.
На развитие сепсиса указывает изменение цвета кожи – появление грязновато-серого или бледного оттенка кожи. Нередко такой цвет сочетается с желтушностью и признаками расстройства кровообращения. Обращают на себя внимание геморрагии (кровоизлияния), мраморность и нарушение циркуляции крови, синюшный оттенок кистей и стоп. Часто возникает общая отёчность и склонность к кровоточивости;
- развитие дыхательной и сердечно-сосудистой недостаточности.
Появляется одышка, частота дыхательных движений превышает 60 в минуту. Со стороны сердца может отмечаться как тахикардия, более 160 ударов в минуту, так и брадикардия – до 110 сердечных сокращений;
- дисфункция желудочно-кишечного тракта.
Появляются срыгивания и рвота, ребёнок перестает усваивать пищу. При осмотре обращает на себя внимание увеличенный и вздутый живот с венозной сетью на передней брюшной стенке. Печень и селезёнка увеличиваются в размерах;
- поражение мочевыделительной системы.
Ребёнок становится отёчным, почки производят недостаточное количество мочи. В тяжёлом состоянии моча отсутствует полностью (анурия);
- расстройство нервной системы.
Отмечается угнетение нервной системы, снижение или отсутствие рефлексов новорождённых. Малыш становится вялым и практически не реагирует на окружающих. Иногда возникает наоборот, повышенная возбудимость, раздражительность крохи. Состояние может ухудшаться и приводить к судорогам.
Диагностика сепсиса
Чтобы правильно установить диагноз, нужно придерживаться определённого алгоритма, предположить наличие болезни, выявить возбудителя и оценить степень поражения внутренних органов.
В связи с отсутствием у новорождённых первичного инфекционного очага, первые проявления сепсиса легко спутать с другими распространёнными заболеваниями. Дыхательные расстройства, поражения желудочно-кишечного тракта часто «маскируют» сепсис.
Для выявления раннего сепсиса в первые 6 дней жизни малыша стоит обратить внимание на вероятные симптомы:
- тяжёлое состояние крохи, выраженная интоксикация;
- температура тела более 37,5 °С или менее 36,2 °С в течение трёх суток;
- изменения клинического анализа крови – повышение количества лейкоцитов и снижение уровня тромбоцитов;
- высокий уровень С-реактивного белка;
- повышение количества прокальцитонина и ИЛ-8 в сыворотке крови.
Если признаки сепсиса возникли после 6 дня жизни крохи, то для постановки диагноза необходимо выявление первичного воспалительного очага и изменений лабораторных показателей крови.
Для дальнейшей диагностики и определения наиболее эффективного лечения проводят:
- анализ крови на стерильность.
Хотя выявление бактерий в крови может встречаться при различных инфекционных заболеваниях, этот анализ помогает подобрать наилучшее лечение, выбрать самые эффективные препараты, антибиотики;
- микробиологическое исследование.
Для выявления возбудителя инфекции исследуется отделяемое из гнойно-воспалительного очага. Возможно микробиологическое исследование, посев на питательную среду и другого материала – гноя, спинномозговой жидкости, мочи (в зависимости от поражённого органа);
- лабораторные и инструментальные методы обследования.
Другие исследования применяются для определения степени функционального и структурного поражения всех жизненно важных органов.
Лечение сепсиса у новорождённых
Сепсис – серьёзное, опасное заболевание, которое без правильного лечения приводит к недостаточности жизненно важных органов и летальному исходу.
Начинать лечебные мероприятия нужно при первых подозрениях на инфекционный процесс, не дожидаясь результатов посевов. Для точного определения возбудителя потребуется несколько дней, которые могут стать решающими в состоянии ребёнка.
Направления терапии сепсиса
- Антибиотикотерапия.
Даже до получения результатов посевов и точного определения возбудителя назначается, как правило, 2 сильных антибиотика. Лекарственные препараты вводят внутривенно, чтобы добиться максимальной эффективности. Коррекцию антибиотикотерапии проводят после получения результатов анализов, выделения возбудителя.
- Интенсивная терапия.
В зависимости от тяжести состояния крохи, малышу может потребоваться дыхательная поддержка, коррекция артериального давления, инфузионная терапия, внутривенное введение лекарств. В тяжёлых случаях не исключено применение гормональных препаратов, переливание крови и свежезамороженной плазмы.
- Коррекция иммунитета.
Для повышения защитных сил организма, создания иммунитета против бактерий, используют иммуноглобулины, например, пентаглобин, интерфероны. Лекарства усиливают противоинфекционную защиту, активируют иммунитет, снижают явления интоксикации.
- Устранение очага инфекции.
Чаще всего первичным очагом инфекции является пупочная ранка, неправильный уход за которой приводит к инфицированию и распространению инфекции. При пупочном сепсисе проводят лечение омфалита (воспаления пупочной ранки), удаляют выделения и нагноения из пупочной ранки. Медсестра проводит ежедневный гигиенический уход и круглосуточное наблюдение за пациентом.
- Симптоматическая терапия.
Симптоматическое лечение включает в себя коррекцию анемии, восстановление нормальной микрофлоры кишечника, противогрибковую и другие виды терапии.
- Восстановительные мероприятия.
Младенца, перенёсшего сепсис, ждёт длительный реабилитационный период. Нередко малышам показан массаж, гимнастические упражнения, физиотерапевтические процедуры. Зачастую кроха остается на диспансерном учёте у нескольких специалистов до 3-летнего возраста.
Профилактика сепсиса новорождённых
Предупреждение болезни во многом зависит от сознательности будущей матери. Ещё во время планирования беременности пара должна посетить специалистов, тщательно обследоваться и избавиться от хронических воспалительных процессов.
Стоит отказаться от вредных привычек во время планирования беременности и вынашивания ребёнка, что повысит сопротивляемость организма женщины и обезопасит малыша от развития патологий.
Во время беременности будущая мать должна регулярно посещать гинеколога и выполнять все предписания. Если всё-таки произошло заражение инфекцией, важно вовремя выявить и вылечить недуг, не допускать распространение и хронизации процесса.
Во избежание генерализации инфекции медперсонал должен тщательно следить за чистотой в родзалах, дезинфекцией инструментов и помещений. Все сотрудники проходят регулярные медицинские осмотры и проверку на носительство инфекций.
Обязательно соблюдение правил ухода за новорождённым ребёнком, обучение матерей. При выписке из родильного дома мама должна знать всё о гигиене ребёнка и уметь осуществлять уход за новорождённым.
Заключение
Неонатальный сепсис – тяжёлое и опасное заболевание новорождённых. При лечении этого недуга требуется много сил и терпения. К сожалению, болезнь в 40 % случаев приводит к летальному исходу, поскольку быстро поражает многие органы. Но при своевременно оказанной помощи и тщательном уходе возможно полное излечение.
Родителям важно знать простые правила профилактики инфекционных заболеваний, вовремя посещать врача и следить за своим здоровьем и самочувствием крохи. Заботиться о здоровье чада нужно с момента планирования беременности, необходимо внимательно относиться к врачебным рекомендациям. Таким образом будущая мать сможет обезопасить кроху от серьёзных проблем.
Источник
