Рефераты на тему двс синдрома
Содержание
1 Введение ………………………………………………………………….
.2
2 Система свертывания крови ……………………………………………….2-3
3 Система гемостаза…………………………………………………………4
5 Общие положения, этиологические факторы…………………………….5-6
6 Патогенез …………………………………………………………………..7-8
7 Клиническая классификация………………………………………………8-12
8 Клиника…………………………………………………………………….12-13
9 Методы диагностики………………………………………………………13-15
10 Лечение……………………………………………………………………15-20
11 Список литературы………………………………………………………..21-22
Введение
ДВС-СИНДРОМ –
состояние, характеризующееся рассеянным
внутрисосудистым свертыванием и агрегацией
клеток крови, активацией и истощением
компонентов свертывающей и фибринолитической
систем (в том числе физиологических антикоагулянтов),
нарушением микроциркуляции в органах
с их дистрофией и дисфункцией, выраженной
наклонностью к тромбозам и кровоточивости.
Наблюдается при многих заболеваниях
и всех терминальных состояниях. Микротромбообразование
и блокада микроциркуляции могут распространиться
на всю систему кровообращения с преобладанием
процесса в органах-мишенях (или шок-органах
— легких, почках, печени, головном мозге,
желудке и кишечнике, надпочечниках и
др.) либо в отдельных органах и частях
тела (региональные формы). Процесс может
быть острым (часто молниеносным), подострым,
хроническим и рецидивирующим с периодами
обострения и стихания. Другими словами,
ДВС-синдром — тяжелая катастрофа организма,
ставящая его на грань между жизнью и смертью,
характеризующаяся тяжелыми фазовыми
нарушениями в системе гемостаза, тромбозами
и геморрагиями, нарушением микроциркуляции
и тяжелыми метаболическими нарушениями
в органах с выраженной их дисфункцией,
протеолизом, интоксикацией, развитием
или углублением явлений шок
Система свертывания крови
На рисунке изображена довольно сложная
схема свертывания крови. Номера и наиболее
распространенные названия факторов свертывания
представлены в таблице
Международная номенклатура плазменных
факторов свертывания крови (по З.С.Баркагану)
Цифровое обозначение | Наиболее употребительные наименования |
I | Фибриноген |
II | Протромбин |
III | Тканевой тромбопластин, тканевой фактор |
IV | Ионы кальция |
V | Ас-глобулин, проакцелерин, лабильный |
VII | Проконвертин, стабильный фактор |
VIII | Антигемофильный глобулин |
IX | Плазменный компонент тромбопластина, фактор Кристмасса, антигемофильный |
X | Фактор Стюарта-Праузра, протромбиназа |
XI | Плазменный предшественник тромбопластина |
XII | Фактор Хагемана, контактный фактор. |
XIII | Фибринстабилизирующий фактор |
Имеется два различных механизма активации
свертывания крови. Один обозначается
как внешний механизм, поскольку запускается
поступлением из тканей или из лейкоцитов
крови тканевого фактора (фактор III). При
взаимодействии с фактором VII , быстро
активируется Х фактор, который трансформирует
протромбин (II) в тромбин (IIa), а тромбин
в свою очередь преобразует фибриноген
(I) в фибрин (Is). Второй путь активации называется
внутренним, он начинается с активации
XII фактора. Это возникает вследствие разных
причин — контакт крови с поврежденной
сосудистой стенкой, с измененными клеточными
мембранами, под влиянием адреналина или
протеаз. Далее процесс идет по каскаду
как это видно на рисунке, в конце концов,
протромбин переходит в тромбин, а тот
в свою очередь переводит фибриноген в
фибрин и образуется тромб.
Система гемостаза является саморегулирующейся,
активация системы свертывания сразу
включает в действие противосвертывающую
систему и систему фибринолиза.
Система гемостаза
Сосудисто-тромбоцитарный гемостаз —
одна из систем, реализующих гемостаз
в организме, т.е. обеспечивает сохранение
жидкого состава крови, предупреждает
кровотечение или останавливает его путем
поддержания структурной целостности
стенок кровеносных сосудов и достаточно
быстрого их тромбирования в случае повреждения.
Стенки сосудов играют важную роль в
поддержании нормального гемостаза. Эндотелий
сосудов синтезирует и секретирует мощный
ингибитор агрегации тромбоцитов — простациклин;
фиксирует на своей поверхности ряд естественных
антикоагулянтов, вырабатывает активаторы
фибринолиза. Остановка кровотечения
обеспечивается выработкой эндотелиальными
клетками факторов, направленных на образование
тромба — фактора Виллебранда, коллагена.
В тесной связи с сосудистым находится
тромбоцитарный фактор. Тромбоциты влияют
на процессы гемостаза по четырем направлениям.
Во-первых, они обладают ангиотрофической
функцией, поддерживают нормальную структуру
и функцию эндотелиальных клеток микрососудов.
При уменьшении количества тромбоцитов,
нарушениях их функции резко возрастает
проницаемость сосудистой стенки для
эритроцитов. Во-вторых, при малейшем повреждении
стенки сосудов тромбоциты приклеиваются
к поврежденному месту (адгезия) и способствую
организации тромбоцитарных агрегатов,
в этом процессе активно участвует тромбоксан
— метаболит арахидоновой кислоты, синтезирующийся
в тромбоцитах. В-третьих, тромбоциты поддерживают
спазм сосудов, который закономерно развивается
при их повреждении. В-четвертых, тромбоциты
непосредственно активируют систему свертывания
крови путем выработки ряда факторов,
а также влияют на систему фибринолиза.
Все факторы противосвертывающей системы
— антикоагулянты — можно разделить на
две группы: 1) физиологические антикоагулянты,
образующиеся независимо от свертывания
крови, фибринолиза; 2) образующиеся в процессе
протеолиза, вторично.
К I группе относятся антитромбин III, гепарин,
альфа-1-антитрипсин, альфа-2-макроглобулин
и некоторые другие. Наиболее универсален
из них антитромбин. Ко второй группе относятся
антитромбин I, продукты деградации фибриногена.
Активация свертывания крови неизбежно
вызывает усиление противосвертывающих
механизмов. Точные механизмы включения
противосвертывающих факторов до конца
не изучены.
Лизис фибрина в организме осуществляется
фибринолитической или плазминовой системой.
Основной компонент ее — фибринолизин
или плазмин, который содержится в плазме
в виде профермента плазминогена. Кроме
того, существует система неферментативного
фибринолиза.
Общие положения, этиологические
факторы
Термином ДВС-синдром обозначается неспецифический
общепатологический процесс, в основе
которого лежит рассеянное диффузное
свертывание крови в микрососудах с образованием
множества микросгустков и агрегатов
клеток крови, блокирование кровообращения
в органах и развитие в них глубоких дистрофических
изменений.
Перечень заболеваний и состояний, часто
осложняющихся ДВС-синдромом:
- Злокачественные (солидные) новообразования
различных локализаций. - Карциноид, нейробластома.
- Рабдомиосаркома.
- Острый промиелоцитарный лейкоз.
- Эритремия.
- Хронический егакариоцитарный лейкоз.
- Внутрисосудистый гемолиз.
- Серповидноклеточная анемия (криз).
- Гистиоцитоз.
- Септический аборт.
- Отслойка плаценты.
- Эмболия околоплодными водами.
- Внутриутробная смерть плода.
- Внематочная беременность.
- Тяжелая эклампсия.
- Кесарево сечение.
- Конфликт матери и плода по системам
АВ0 и Rh. - Аневризмы.
- Коарктация аорты.
- Ангиоматоз Казабаха–Меррит (множественные
и гигантские ангиомы). - Аортит Такаясу.
- Хирургическая ангиопластика.
- Врожденные «синие» пороки сердца.
- Иммунокомплексные заболевания (васкулиты).
- Тромбоэмболии легочной артерии.
- Гемолитико-уремический синдром.
- Инфаркт миокарда.
- Сепсис.
- Шок (травматический, геморрагический,
ожоговый, - анафилактический, септический).
- Массивные поражения тканей (crush-синдром,
травматичные хирургические операции). - Синдром гомологичной крови.
- Переливание несовместимой крови.
- Эксикоз.
- Жировая эмболия.
- Гемоперфузия (на угольных фильтрах).
- Отравления и интоксикации (змеиным адом,
лекарственными средствами). - Ацидоз, гипоксия.
- Острый панкреатит.
- Гиперлипидемия.
- Амилоидоз.
- Острые и хронические заболевания печени.
- Вирусные инфекции (герпес, краснуха,
оспа, цитомегаловирус). - Геморрагическая лихорадка.
- Малярия.
Глистная инвазия (кара-азар).Этиологические
факторы и нарушения, вызывающие ДВС-синдром(
по R.I.Handin)
Группы этиологических факторов | Патологические состояния |
Высвобождение тканевых факторов | Акушерская патология ( отслойка плаценты, Гемолиз Опухоли Жировая эмболия Повреждение тканей ( ожоги, отморожения, |
Повреждения эндотелия | Аневризма аорты Гемолитический уремический синдром Острый гломерулонефрит Синдром Казабаха — Мерритт |
Инфекции | Бактериальные ( стафилококковые, стрептококковые, Вирусные (арбовирусы, вирусы оспы, ветряной Паразитарные ( малярия, кала-азар) Риккетсиозные ( пятнистая лихорадка Грибковые ( острый гистоплазмоз) |
Патогенез
ДВС-синдром представляет собой такой
вариант коагулопатии, когда особенно
четко происходит нарушение равновесия
между свертывающей, антисвертывающей
и фибринолитической системами организма.
Особенностью «трагедии» ДВС-синдрома
является диссеминированное, рассеянное,
множественное образование тромбов и
фибринных сгустков, по сути дела там,
где гемостаза не требуется. В самом общем
виде патогенез ДВС-синдрома представлен
на схеме. Этиологические факторы приводят
к гиперкоагуляции, образованию мелких
рыхлых сгустков фибрина или микротромбов
практически во всей микроциркуляторной
системе. Они сразу же растворяются фибринолитической
системой. Образуются новые тромбы и новые
сгустки и постепенно истощаются все основные
факторы свертывающей системы — тромбоциты,
протромбин, фибриноген. Развивается гипокоагуляция
вследствие коагулопатии потребления.
Если где-то нарушается целостность сосудистой
стенки, тромб уже образоваться не может.
При этом в избытке имеются антикоагулянтные
субстанции, из-за которых кровотечение
также очень остановить. Образующиеся
в микрососудах фибринные сгустки и микротромбы
блокируют тканевой кровоток, вызывают
ишемию тканей, нарушают функцию таких
жизненно важных органов как сердце, легкие,
почки.
Механизм развития ДВС-синдрома
I фаза. Образование активного тромбопластина
— самая продолжительная фаза гемостаза.
В ней принимают участие факторы плазменные.
(XII, XI, IX, VIII, X, IV, V) и факторы тромбоцитарные
(3, 1).
II фаза. Переход протромбина в
тромбин. Происходит при действии
активного тромбопластина и участии ионов
кальция (фактор IV).
III фаза. Образование фибрин-полимера.
Тромбин (при участии ионов кальция (фактор
IV) и фактора тромбоцитов (4) переводит
фибриноген в фибрин-мономер, который
при действии VIII фактора плазмы и тромбоцитарного
фактора 2 превращается в нерастворимые
нити фибрина-полимера.
Изменение прокоагулянтов в звене гемостаза,
активация тромбоцитарного звена приводят
к агрегации тромбоцитов с выделением
биологически активных веществ: кининов,
простагландинов, катехоламинов и др.
Они влияют на сосудистую систему.
При замедленном течении крови через
разветвления мелких сосудов происходит
ее расслоение на плазму и эритроциты,
заполняющие разные капилляры. Теряя плазму,
эритроциты теряют способность к передвижению
и скапливаются в виде медленно циркулирующих,
а затем нециркулирующих образований.
Происходит стаз, агрегация, а затем и
лизис, высвобождается связанный со стромой
эритроцитов кровяной тромбопластин.
Поступление в кровоток тромбопластина
вызывает процесс внутрисосудистого свертывания
крови. Выпадающие при этом нити фибрина
опутывают глыбки эритроцитов, образуя
«сладжи» — комочки, оседающие в капиллярах
и еще больше нарушающие однородность
структуры крови. Важную роль в развитии
«сладж»-феномена играют два взаимосвязанных
явления — снижение кровотока и увеличение
вязкости крови (М.А. Репина, 1986). Происходит
нарушение кровоснабжения тканей и органов.
В ответ на активацию системы коагуляции
включаются защитные механизмы — фибринолитическая
система и клетки ретикулоэндотелиальной
системы.
На фоне диссеминированного внутрисосудистого
свертывания крови вследствие повышенного
потребления прокоагулянтов и усиления
фибринолиза развивается повышенная кровоточивость.
Разными авторами предложены различные
классификации стадий в течении ДВС-синдрома,
хотя в клинической практике синдром ДВС
не всегда проявляется в такой четкой
форме.
Клиническая классификация
Клиническая картина ДВС-синдрома складывается
из признаков основного заболевания, обусловившего
внутрисосудистое свертывание крови,
и самого ДВС-синдрома.
По клиническому течению он бывает:
- острым (вплоть до молниеносного);
- подострым;
- хроническим;
- рецидивирующим.
Стадии ДВС-синдрома:
- Гиперкоагуляция и агрегация тромбоцитов.
- Переходная с нарастающей коагулопатией
потребления, тромбоцитопенией, разнонаправленными
сдвигами в общих коагуляционных тестах. - Глубокой гипокоагуляции вплоть до полной
несвертываемости крови. - Неблагоприятный исход или восстановительная.
Источник
Диссеминированное внутрисосудистое свертывание (ДВС) ㅡ клинико-патологический синдром, осложняющий течение различных заболеваний. ДВС характеризуется системной активацией патологических путей, приводящей к нарушению регуляции коагуляции; проявляется образованием фибриновых сгустков с последующей органной дисфункцией и сопутствующим потреблением тромбоцитов и факторов свертывания, клинически проявляющимся кровотечениями.
Смертность от ДВС за последние годы значительно снизилась. По данным министерства здравоохранения Японии, смертность от ДВС упала с 65 % в 1998 году до 46 % в 2010 и 2012 годах, такая же тенденция наблюдается и в США (с 76 до 51 % между 2006 и 2010 годами). Данное снижение смертности обусловлено более глубоким пониманием патогенеза заболевания, улучшением ранней диагностики и применением новых протоколов лечения ДВС.
Этиология
ДВС часто развивается на фоне сепсиса либо инфекции (30–51 %), травмы (черепно-мозговая травма, ожоги, жировая эмболия) или больших оперативных вмешательств (45 %). Другими причинами ДВС могут быть деструкция органов (тяжелый панкреатит), злокачественный процесс, тяжелые акушерские патологии (эмболия амниотической жидкостью, отслойка плаценты, тяжелая преэклампсия, послеродовое кровотечение), фульминантная печеночная недостаточность, цирроз печени, тяжелые токсические или иммунологические реакции (отравление ядами змей, переливание несовместимой крови, отторжение трансплантата), сосудистые заболевания (гемангиомы, аневризмы аорты, синдром Казабаха-Мерритта).
Патофизиология ДВС
К развитию ДВС приводит нарушение регуляции противосвертывающей и свертывающей систем крови. Формирование фибринового сгустка является продуктом целого каскада реакций, в которых задействованы как факторы свертывания, так и клеточные элементы. Выделяют внутренний и внешний пути активации коагуляции. Инициация процесса свертывания при ДВС зачастую начинается с попадания в кровоток тканевого фактора ― фактора VII (внешний путь) (рис. 1).
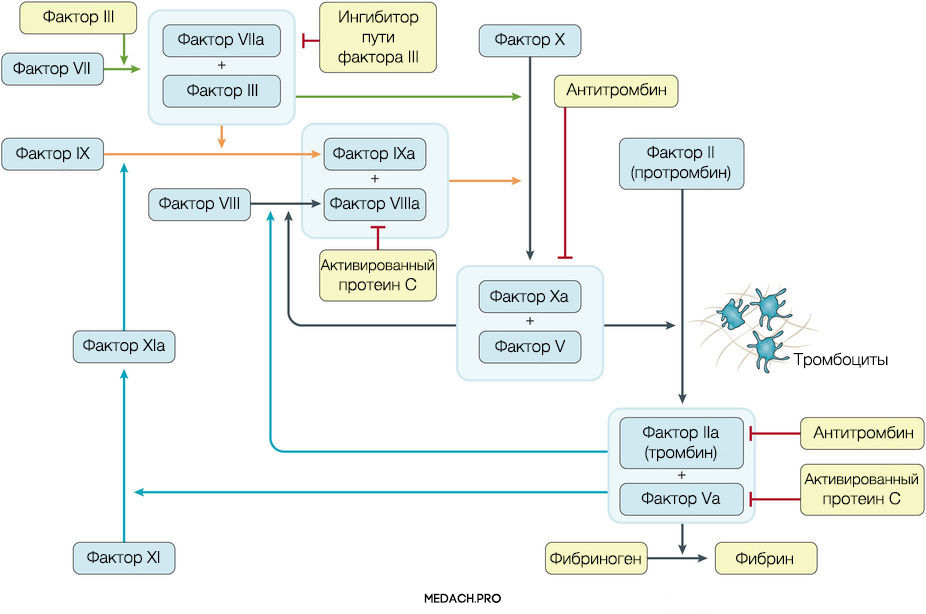
Рисунок 1 | Инициация процесса свертывания при ДВС зачастую начинается с попадания в кровоток тканевого фактора ― фактора VII (внешний путь)
Тканевой фактор (ТФ) представляет собой мембрано-ассоциированный гликопротеин, находящийся в субэндотелиальном слое сосудов, в физиологических условиях не контактирующий с кровью. Выброс тканевого фактора могут спровоцировать различные процессы, такие как прямое повреждение сосудов, воспалительные и иммунологические реакции. При сепсисе ТФ непосредственно продуцируется моноцитами, а также выделяется в результате взаимодействия тромбоцитов со стенкой сосудов, что приводит к значительному усилению коагуляции. Выброс провоспалительных цитокинов и хемокинов провоцируется взаимодействием ТФ, тромбина и других факторов коагуляции с воспалительными клетками через специфические протеаза-активируемые рецепторы (PARs) 1–4 типа, а также дополнительно тромбином через Toll-like рецепторы 4 типа (TLR4). Развитие ДВС на фоне онкологических процессов имеет свои особенности, так как некоторые опухоли могут производить прокоагулянтные факторы (тканевой фактор и цистеиновая протеаза фактора X) (рис. 2).
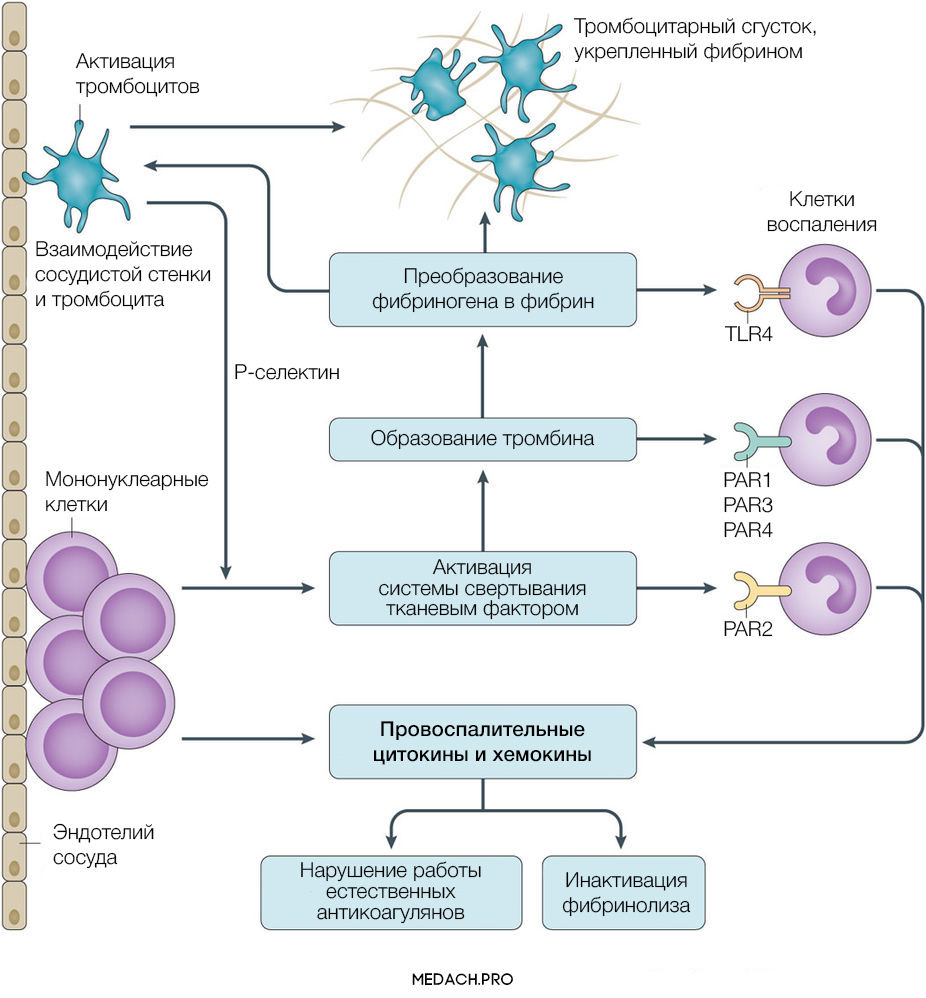
Рисунок 2 | Активация прокоагулянтных факторов в патогенезе ДВС-синдрома
Важное место в процессе свертывания занимает тромбин: он не только участвует в преобразовании фибриногена в фибрин, но также активирует другие факторы и ко-факторы свертывания (факторы VII, IX и XI). Тромбин инициирует скрепление частиц фибриногена в мономеры, а затем и в полимеры. Последующая стабилизация тромба происходит с помощью тромбин-активируемых факторов XIII (фактора XIIIа).
Реакции коагуляции контролируются противосвертывающей системой крови, включающей в себя: антитромбин (блокирует фактор Xa и тромбин), протеин С (протеолитически разрушает Va и VIIIa факторы), ингибитор пути тканевого фактора (ингибирует комплекс тканевой фактор-VIIa фактор).
При сепсис-индуцированном ДВС нарушаются все три компонента противосвертывающей системы. Во-первых, снижается уровень антитромбина в результате нарушения его синтеза в печени, увеличения его клиренса из-за образования протеаза-антитромбинового комплекса, экстраваскулярных потерь из-за повышения проницаемости клеточной стенки и разрушения эстеразой нейтрофилов. В дополнение к этому, в стенке сосудов нарушается синтез протеогликанов, способствующих связи антитромбина с гепарин-сульфатом. Во-вторых, при сепсисе снижается активность протеина С и его кофактора — протеина S, который обладает как антикоагулянтным, так и в некоторой степени противовоспалительным эффектами. В-третьих, нарушается работа системы ингибитора пути активации тканевого фактора (ИПТФ). В норме ИПТФ присутствует на поверхности эндотелия сосудов или циркулирует в крови в связанном с липопротеинами виде. Его роль в развитии ДВС пока плохо изучена.
Повреждение тромбоцитов играет центральную роль в нарушении коагуляции при ДВС. Тромбоциты могут активироваться как напрямую, через провоспалительные медиаторы (фактор активации тромбоцитов), так и опосредованно через тканевой фактор и тромбин. Впоследствии на мембране активированных тромбоцитов происходит фиксация фибрина. Тромбин стимулирует экспрессию на мембране тромбоцитов Т-селектина, который регулирует адгезию тромбоцитов к лейкоцитам и эндотелию сосудистой стенки, а также ускоряет секрецию ТФ мононуклеарами. В дополнение ко всему повреждение эндотелия и взаимодействие тромбоцит-сосудистая стенка вызывает выброс в кровь ультра-больших мономеров фактора фон Виллебранда (vWF). Фактор фон Виллебранда является важным медиатором адгезии тромбоцитов и коагуляции крови, его деградация осуществляется с помощью металлопротеиназы ADAMTS-13. Доказано, что недостаток металлопротеиназы и, вследствие этого, снижение деградации vWF способствует развитию ДВС-синдрома и более тяжелому его течению.
Фенотип ДВС синдрома
Повышенное образование тромбина при ДВС-синдроме приводит к манифестации различных фенотипов, которые не обязательно характеризуются повышенным тромбообразованием. Например, ранняя гиперфибринолитическая (геморрагическая) фаза, вызывающая всплеск продукции тромбина в ранней фазе тяжелой травмы. Через 24–48 часов она сменяется прокоагулянтной (тромботической) фазой, характерной чертой которой является гиперпродукция плазмин-ингибирующего комплекса, приводящая к супрессии активности протеина С. Фенотип ДВС частично зависит от этиологического фактора, но в большей степени обусловлен преобладающим нарушением в регуляции гемостаза организма [2, 3]. Часто наблюдается активация системы свертывания (повышение тромбин-антитромбинового комплекса), однако степень фибринолитической активности (ингибитора активатора плазминогена) варьирует в зависимости от причины (рис. 3).
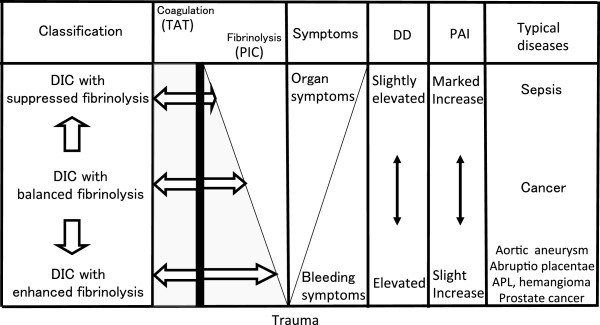
Рисунок 3 | Фенотипы ДВС-синдрома. TAT — комплекс тромбин-антитромбин; PIC — комплекс плазмин-альфа-2-антиплазмин; DD — Д-димер; PAI — ингибитор активатора плазминогена
В столбце «Symptoms» обозначен переход от кровотечений к органному поражению (развитие микро- и макротромбозов). На данном рисунке не обозначены продукты деградации фибрина (ПДФ), тем не менее при гиперфибринолитическом фенотипе ДВС имеется тенденция к преобладанию ПДФ над количеством Д-димеров. При терапии препаратами транс-ретиноевой кислоты при остром промиелоцитарном лейкозе ингибируется экспрессия опухолевыми клетками аннексина II, в результате чего меняется и фенотип ДВС (теряет характеристики гиперфибринолитического, приобретая характеристики прокоагулянтного фенотипа).
Диагностика
Критерии для выявления ДВС-синдрома по шкале ISTH (International Society of Thrombosis and Haemostasis Scoring System):

Рисунок 4 | ISTH (International Society of Thrombosis and Haemostasis Scoring System)
Критерии Japanese Association for Acute Medicine (JAAM):

Рисунок 5 | Japanese Association for Acute Medicine (JAAM)
Данные шкалы отличаются различной чувствительностью в отношении прогнозирования смертности: считается, что шкала JAAM имеет бо́льшую чувствительность к неявному ДВС-синдрому, в результате чего смертность при ДВС-синдроме, выявленном по данной шкале, почти в два раза ниже (около 22%).
Критерии ДВС Japanese Ministry of Health, Labor and Welfare (JMHLW):

Рисунок 6 | Japanese Ministry of Health, Labor and Welfare (JMHLW)
Данные критерии не адаптированы для пациентов с заболеваниями печени или нефротическим синдромом.
На основании представленных выше шкал выставляется диагноз ДВС. Наиболее подходящая шкала выбирается в зависимости от возможности проведения определенных лабораторных тестов и клинической ситуации. При возможности пациенту рекомендуется проводить контроль лабораторных показателей коагуляции каждые 8 часов.
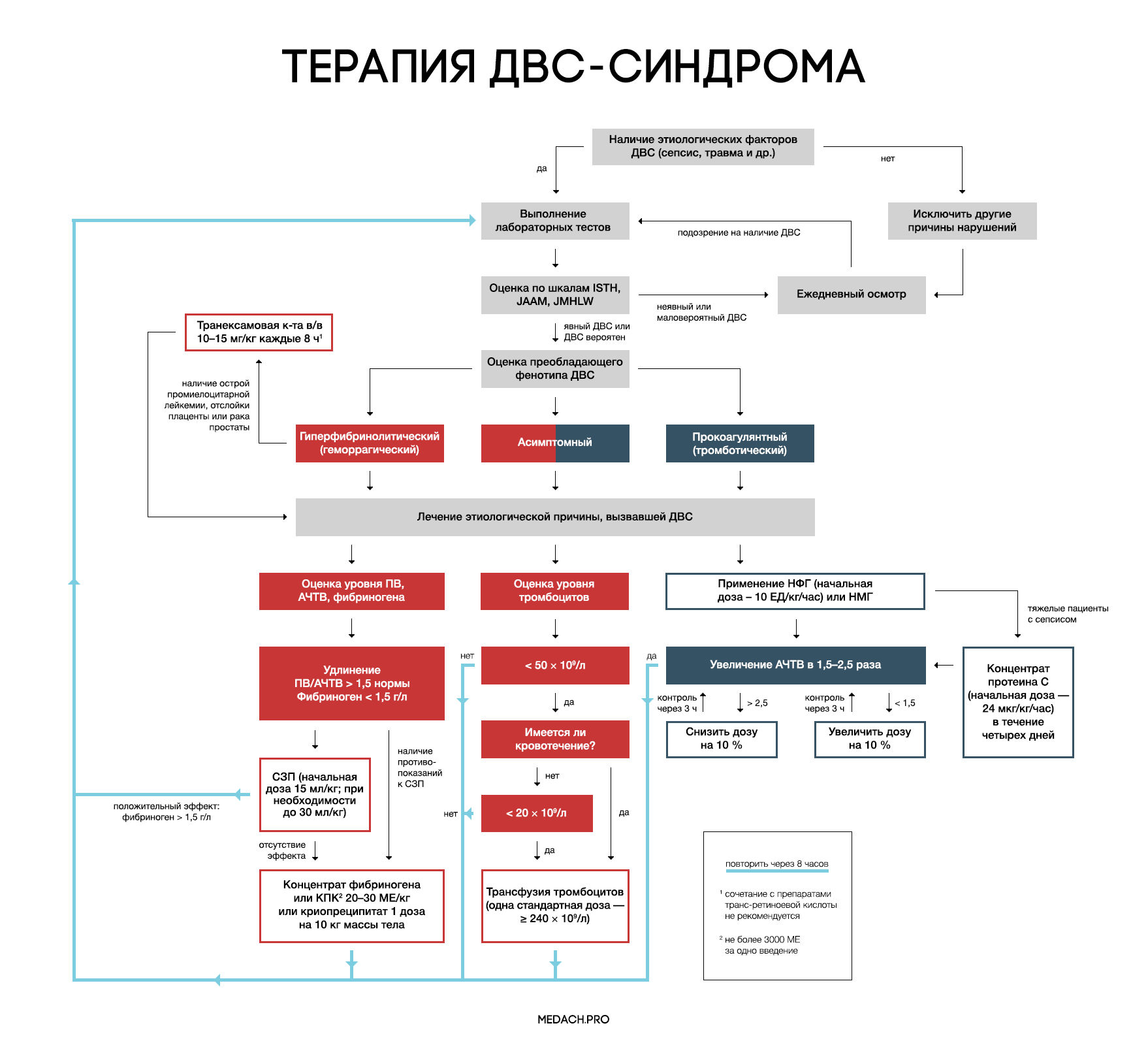
Лечение

Рисунок 7 | Алгоритм тактики ведения пациентов с ДВС-синдромом (авторская работа Medach)
Терапия этиологического фактора
Главным в терапии ДВС-синдрома является лечение состояния, вызвавшего его развитие. Выделяют два варианта течения ДВС-синдрома:
— Контролируемый ДВС-синдром: характеризуется временным нарушением регуляции коагуляционных механизмов и быстрым восстановлением после ликвидации провоцирующего состояния (трансфузионная реакция, отслойка плаценты). В ряде случаев может разрешаться самостоятельно.
— Неконтролируемый ДВС-синдром (вызван сепсисом или травмой): в этом случае помимо ликвидации основной этиологической причины требуется незамедлительное начало терапии.
Важно отметить, что раннее начало применения препаратов, влияющих на систему свертывания крови (до развития ДВС-синдрома), может в значительной степени нарушить регуляцию гемостаза и, вследствие этого, ухудшить состояние пациента.
Заместительная терапия
Рекомендации по заместительной терапии ДВС сделаны на основании объединения данных гайдлайнов различных сообществ (British Committee for Standards in Haematology (BCSH), Japanese Society of Thrombosis and Hemostasis (JSTH), Italian Society for Thrombosis and Hemostasis (SISET)), занимающихся интенсивной терапией ДВС. При сочетании активного кровотечения или риска его развития и определенных уровней лабораторных показателей рекомендуется применение тромбоцитарной массы, свежезамороженной плазмы (СЗП), криопреципитата или концентрата фибриногена, концентрата протромбинового комплекса (КПК). Все нижеперечисленные рекомендации касаются категории пациентов с активным кровотечением.
Рекомендуется трансфузия тромбоцитов при наличии признаков активного кровотечениями и уровне тромбоцитов < 50 × 10^9 /л либо при отсутствии кровотечения, но наличии высокого риска его развития и уровне тромбоцитов < 20 × 10^9 /л. Трансфузия тромбоцитарной массы начинается с одной стандартной взрослой дозы (более 240 × 10^9/л). Переливание СЗП может применяться при удлинении ПВ/АЧТВ (больше 1,5 от нормы) или снижении уровня фибриногена менее 1,5 г/дл. Начальная доза СЗП составляет 15 мл/кг, при необходимости более жесткой коррекции уровня факторов свертывания допустимо использование дозы 30 мл/кг, однако следует помнить, что такие высокие дозы СЗП могут вызвать перегрузку объемом. КПК или концентрат фибриногена применяются при наличии подтвержденной тяжелой гипофибриногенемии (< 1,5 г/дл), несмотря на использование СЗП либо при наличии противопоказаний к ее применению. При применении 3 грамм концентрата фибриногена уровень фибриногена плазмы крови повышается примерно на 1 г/л. Такой же эффект достигается при переливании 4 единиц СЗП или 2 доз криопреципитата (10 донорских единиц). При планировании у пациентов инвазивных процедур необходимо контролировать уровень лабораторных показателей свертывания крови, и при необходимости превентивно провести трансфузию тромбоцитов или СЗП. Эффективность и безопасность применения рекомбинантного фактора VIIа у пациентов с ДВС требует дальнейшего исследования.
Антикоагулянтная терапия
Применение антикоагулянтов противопоказано при развитии ДВС-синдрома в результате травмы, или при травматическом шоке в сочетании с активным кровотечением. Для использования при ДВС-синдроме с преобладанием тромбозов рекомендуется нефракционированный гепарин (НФГ) или низкомолекулярные гепарины (НМГ). НФГ применяется в начальной дозе 10 ЕД/кг/час под контролем АЧТВ с поддержанием его увеличения в 1,5–2,5 раза от нормы. Необходимо помнить о профилактике тромбоэмболии НФГ или НМГ у тяжелых пациентов без признаков кровотечений. Уровень антитромбина III может частично использоваться для оценки дальнейшей эффективности применения гепарина, но зачастую имеются сложности (высокая стоимость, отсутствие реагентов) при измерении активности антитромбина III. На данный момент крупные исследования о применении НМГ у пациентов с ДВС-синдромом отсутствуют, и возможность профилактики НМГ строится на данных их использования у пациентов хирургического профиля.
Синтетические ингибиторы протеаз (габексата мезилат, нафамостата мезилат) разрешены к использованию в Японии, однако крупные РКИ, показывающие их эффективность при ДВС-синдроме, отсутствуют.
Концентраты антикоагулянтных факторов
Исследования в данном направлении ведутся на протяжении уже многих лет; так, с 1980 года проводятся испытания концентрата антитромбина, однако его эффективность при ДВС-синдроме до сих пор не доказана. На основании предположения, что при ДВС происходит угнетение выработки протеина С, зародилась идея применения активированного протеина С. После проведения больших исследований данный препарат показал эффективность в группах с тяжелой сопутствующей патологией (сепсис). Крупных исследований, сравнивающих эффективность рекомбинантного активированного человеческого протеина С и полученного из плазмы концентрата протеина С, не проводилось. Концентрат протеина С применяется в виде продолжительной инфузии со скоростью 24 мкг/кг/час в течении четырех дней. При необходимости проведения инвазивных процедур введение протеина С прерывается до их выполнения (период полувыведения около 20 минут), а затем возобновляется через несколько часов. При применении протеина С необходимо учитывать повышение рисков кровотечения (2–3,5 %) и внутричерепного кровоизлияния (0,1–0,3 %), а также то, что в исследованиях препарата не участвовали пациенты с тромбоцитопенией ( < 30 x 10^9/л). Для контроля терапии используется АЧТВ. Исследования по применению тифакогина (рекомбинантного ингибитора пути тканевого фактора) не увенчались успехом.
На данный момент имеется ряд исследований по безопасности и эффективности рекомбинантного растворимого человеческого тромбомодулина (rhTM), однако их результаты гетерогенны. Проведенный метаанализ данных исследований показал, что препараты rhTM оказывают положительный эффект на выживаемость в группе тяжелого сепсиса и пациентов с количеством баллов по шкале APACHE II более 24 или по шкале SOFA более 11. На данный момент исследования препаратов rhTM перешли в третью фазу.
Антифибринолитики
При ДВС-синдроме фибринолиз заблокирован повышением уровня ингибитора активатора плазминогена (PAI-1). Следовательно, при кровотечениях, вызванных ДВС-синдромом, применение антифибринолитиков не рекомендуется, за исключением случаев развития гиперфибринолитического фенотипа ДВС, возникшего на фоне острой промиелоцитарной лейкемии, отслойки плаценты или карциномы простаты.
Отличительными лабораторными особенностями гиперфибринолитического фенотипа является наличие повышенного уровня тромбин-антитромбинового комплекса (≥ 20 мкг/л) и плазмин-ингибирующего комплекса (≥ 10 мкг/л), а также снижение активности альфа-2-ингибитора плазмина более чем на 50 %.
При таком фенотипе показано использование транексамовой кислоты в дозе по 1 грамму (10–15 мг/кг) через каждые 8 часов. У пациентов с лейкемией часто проводится лечение препаратами транс-ретиноевой кислоты, но, по данным исследований, ее сочетание с транексамовой кислотой повышает риск развития тромбозов. Данную комбинацию необходимо применять в крайнем случае, при наличии признаков жизнеугрожающего кровотечения.
Источники
Levi M. et al. Guidelines for the diagnosis and management of disseminated intravascular coagulation //British journal of haematology. – 2009. – Т. 145. – №. 1. – С. 24-33.
Gando S., Levi M., Toh C. H. Disseminated intravascular coagulation //Nature Reviews Disease Primers. – 2016. – Т. 2. – С. 16037.
Gando S., Wada H., Thachil J. Differentiating disseminated intravascular coagulation (DIC) with the fibrinolytic phenotype from coagulopathy of trauma and acute coagulopathy of trauma‐shock (COT/ACOTS) //Journal of Thrombosis and Haemostasis. – 2013. – Т. 11. – №. 5. – С. 826-835.
ISTH, International Society on Thrombosis and Haemostasis. Adapted with permission from from Taylor Jr. FB, Toh CH, Hoots WK, et al. Towards Definition, Clinical and Laboratory Criteria, and a Scoring System for Disseminated Intravascular Coagulation. Thromb Haemost 2001; 86: 1327–30.
Gando S, Iba T, Eguchi Y, Ohtomo Y, Okamoto K, Koseki K, Mayumi T, Murata A, Ikeda T, Ishikura H, Ueyama M, Ogura H, Kushimoto S, Saitoh D, Endo S, Shimazaki S, Japanese Association for Acute Medicine Disseminated Intravascular
Coagulation (JAAM DIC) Study Group: A multicenter, prospective validation of disseminated intravascular coagulation diagnostic criteria for critically ill patients: comparing current criteria. Crit Care Med 2006, 34: 625-631.
Kobayashi N. et al. Criteria for diagnosis of DIC based on the analysis of clinical and laboratory findings in 345 DIC patients collected by the Research Committee on DIC in Japan //Disseminated intravascular coagulation. – Karger Publishers, 1983. – Т. 49. – С. 265-275.
Wada H. et al. Guidance for diagnosis and treatment of disseminated intravascular coagulation from harmonization of the recommendations from three guidelines //Journal of thrombosis and haemostasis. – 2013. – Т. 11. – №. 4. – С. 761-767.
Afshari, A., Wetterslev, J., Brok, J. & Moller, A. M. Antithrombin III for critically ill patients. Cochrane Database Syst. Rev. 3, CD005370 (2008).
Abraham, E. et al. Efficacy and safety of tifacogin (recombinant tissue factor pathway inhibitor) in severe sepsis: a randomized controlled trial. JAMA 290, 238–247 (2003).
Asakura H. Classifying types of disseminated intravascular coagulation: clinical and animal models //Journal of intensive care. – 2014. – Т. 2. – №. 1. – С. 20.
Источник
