Прогноз при нефротическом синдроме у детей
Осложнения нефротического синдрома у детей. ПрогнозГлавное осложнение нефротического синдрома — инфекционные заболевания. При рецидивах синдрома у детей из-за потери с мочой иммуноглобулинов и пропердинового фактора В, нарушения клеточного иммунитета, иммуносупрессивной терапии, нарушений питания и наличия среды для бактерий в виде отеков и асцита возрастает восприимчивость к бактериальным инфекциям. Чаще всего развивается бактериальный перитонит, возможны также сепсис, пневмония, абсцесс и инфекция мочевых путей. Возбудителем перитонита наиболее часто является Streptococcus pneumoniae, хотя высевается также грамотрицательная флора (например, Escherichia coli). Поскольку на фоне кортикостероидной терапии лихорадка и другие признаки инфекции могут отсутствовать, важнейшее значение приобретают высокая настороженность врача, своевременные исследования (включая посев крови и перитонеальной жидкости) и раннее начало антибиотикотерапии. Профилактическая роль антибиотиков при рецидивах нефротического синдрома остается спорной.
Неиммунизированные дети, заболевшие ветряной оспой в период ремиссии нефротического синдрома, должны получать иммуноглобулин против вируса varicella-zoster в первые 72 ч после начала заболевания. Вакцинацию против гриппа проводят ежегодно. При нефротическом синдроме возрастает риск тромбоэмболии. Частота этого осложнения у детей составляет 2-5 %, что гораздо ниже, чем у взрослых больных. Возможен как артериальный, так и венозный тромбоз, включая тромбоз почечных вен, эмболию легочной артерии, тромбоз сагиттального синуса, а также тромбирование постоянных артериальных или венозных катетеров. Риск тромбоза объясняется повышением в крови уровня фибриногена, тромбоцитозом, сгущением крови и постельным режимом, равно как и потерей с мочой таких фибринолитических факторов, как антитромбин III и протеины С и S. Профилактически вводить детям антикоагулянты в отсутствие тромбоэмболических осложнений в анамнезе не рекомендуется. Нельзя чересчур форсировать диурез; следует ограничить и использование постоянных катетеров, так как все это способствует тромбообразованию. Прогноз нефротического синдрома у детейУ большинства детей с кортикостероидчувствительным нефротическим синдромом наблюдаются рецидивы, но с возрастом их частота снижается. У детей со кортикостероидрезистентным нефротическим синдромом чаще всего имеет место фокально-сегментарный гломерулосклероз, прогноз которого гораздо хуже: поражение почек прогрессирует, приводя в конце концов к терминальной стадии ХПН, требующей диализа или трансплантации почки. При фокально-сегментарном нефросклерозе у 30-50 % реципиентов почки наблюдается рецидив нефротического синдрома. Снижению протенурии способствуют плазмаферез, иммуносорбция плазмы на колонках с белком А (компонентом клеточной стенки стафилококков), высокие дозы циклоспорина или такролимуса и ингибиторы АПФ. — Также рекомендуем «Вторичный и врожденный нефротические синдромы у детей. Диагностика» Оглавление темы «Заболевания почек у детей»:
|
Источник
Нефротический синдром у детей – общий термин, обозначающий совокупность внутренних или внешних факторов, которые способствуют разрушению почечной ткани, вызывая развитие органной недостаточности. Разница между вторичной и первичной формами патологии заключается в причине, вызвавшей болезнь. Нефротический синдром диагностируют на основании данных лабораторных исследований, предъявляемых жалоб. При обнаружении характерных признаков нефроурологической патологии важно начать своевременное лечение.
Нефротический синдром у детей – комплекс симптомов, указывающих на недостаточность функции почек
Особенности состояния
Нефротический синдром – обширный симптомокомплекс, развитие которого обусловлено поражением почек и почечных структур различной тяжести. Состояние характеризуется появлением белка в моче, отечностью нижних конечностей и лица, дистрофией слизистых оболочек или кожных покровов. Существуют две основных формы нефротического синдрома:
- первичная, когда патология развивается изолированно (врожденный нефрит);
- вторичная, когда симптомокомплекс становится следствием провоцирующих факторов: инфекции, аутоиммунной патологии, воспалительного процесса, синдрома Альпорта.
Клиницисты выделяют генетическую форму нефротического синдрома, появление которой обусловлено наследственной предрасположенностью. По статистике, почти в 25% нефротический синдром значительно ухудшает функцию почек, осложняет течение основного урологического или нефрологического заболевания. Вторичный патологический синдром клинически обратим, но только при сохранении функции почек до 60–75%.
Причины и факторы развития
Механизм возникновения заключается в повышении проницаемости клубочковых структур почек для белкового компонента на фоне повреждения. Потеря белка с мочой свидетельствует о развитии гипопротеинемии, гипоальбуминемии. Если истинная причина возникновения синдрома у детей остается невыясненной, то диагностируют идиопатический тип болезни. Запустить механизм выхода белка в мочу и разрушения клубочков могут следующие факторы:
- вакцинация, длительное применение средств, так или иначе влияющих на иммунитет;
- длительное или постоянное применение противосудорожных препаратов;
- перенесенные инфекции, особенно органов мочеполовой и мочевыделительной системы;
- гломерулонефрит любой природы;
- туберкулез любой локализации;
- интоксикации различного генеза.
В группе риска – часто болеющие дети, больные с осложненным клиническим анамнезом: аномалиями развития почек и внутренних органов, дисплазиями, гиперплазиями, первичной артериальной гипертензией, кардиологическими патологиями. Частые обострения при пиелонефрите способствуют развитию симптомокомплекса в 45% случаев.
Симптоматический комплекс
Симптоматический комплекс при нефропатиях типичен, однако варьирует в зависимости от основной причины, тяжести поражения почек. Выявляют следующие признаки:
- при анализе мочи – обширная протеинурию, гипопротеинемию ниже 40 г/л, гипоальбуминемию;
- анализе крови – увеличение уровня мочевины и креатинина, повышение холестерина, снижение клиренса креатинина.
Острый нефротический синдром возникает стремительно, объем суточной мочи резко снижается, отмечаются повышение артериального давления, отечность. Хроническое течение может протекать латентно, отражаясь только в данных лабораторных исследований. Другими симптомами нефротического синдрома являются:
- мышечные боли;
- отечность, вплоть до гидроторакса, анасарки, асцита;
- олигурия – уменьшение суточного диуреза.
Функция почек страдает умеренно, интоксикация сопровождается головной болью, рвотой, постоянной жаждой, отсутствием или нарушением аппетита. Присоединение пищеварительных расстройств связано с раздражением слизистых оболочек из-за воздействия остаточного азота. При хронической нефропатии внешний вид детей болезненный, кожные покровы бледные, лицо одутловатое. При осмотре отмечается обложенный язык, пульс несколько замедлен, тоны сердца часто приглушены.
Для нефротического синдрома характерно волнообразное течение с периодическими обострениями и ремиссией.
Диагностические мероприятия
Лечение определяется характером поражения почечных структур
Нефротический синдром является областью исследования нефрологии, а при осложнениях в мочевыделительной системе – урологии. При появлении первых симптомов рекомендуется наблюдение у детского нефролога. Первичное исследование включает в себя:
- анализ мочи – определяют плотность, наличие и количество лейкоцитов, белка, холестеринова, нейтрального жира, эритроцитов;
- анализ крови – определяют скорость оседания эритроцитов, наличие и количество гемоглобина, тромбоцитов, лейкоцитов, креатинина, мочевины.
Для уточнения патологии возможно проведение проб мочи по Зимницкому, Ребергу, Нечипоренко. Идиопатический тип заболевания также включает в себя все клинические критерии патологии. Обязательно проводят инструментальные исследования:
- ультразвуковое исследование почек, органов брюшины (оценивается мочевой пузырь и его функции);
- рентгенконтрастную урографию для оценки выделительной функции почек;
- биопсию.
Последнее исследование подразумевает лапароскопический забор биоптата для гистологического исследования. Метод не применяется при хаотичном почечном кровотоке, когда риски угрожающих жизни осложнений достигают 95%.
По результатам исследований важно выяснить причину поражения почек, дифференцировать состояние от системной красной волчанки, хронического воспаления с тяжелым поражением почечной ткани и гломерул. При идиопатической форме исключают синдром БМИ (болезнь минимальных изменений), IgA-нефропатию. Напоминать течение нефротического синдрома могут мезангиокапиллярный гломерулонефрит, туберкулез почек, васкулиты, аутоиммунные патологии.
Лечение
Лечение нефритов направлено на устранение пускового механизма развития симптомокомплекса, восстановление почечной ткани и предупреждение ее дальнейшего разрушения. Перспективным направлением является медикаментозная терапия. Хирургическое лечение, физиотерапия, народные рецепты неэффективны. Типичная медикаментозная схема предполагает назначение следующих препаратов:
- плазмовосстанавливающие растворы для внутривенного введения. Способствуют улучшению реологических свойств крови, восполнению утраченных альбуминов;
- гормональная терапия для восстановления утраченного белка;
- цитостатики для предупреждения дальнейшего разрушения тканей почек, развития опухолевых процессов, малигнизации клеток;
- диуретики для выведения избыточной жидкости из организма, лечения отеков. Диуретические средства применяются в комплексе антигипертензивной терапии;
- антикоагулянты для улучшения кровотока, разжижения крови.
Острый тип нефропатии нередко требуется сеанса заместительной терапии для облегчения состояния ребенка, очищения крови.
Обязательно назначают препараты кальция и витамин Д для предупреждения размягчения, деформации и истончения костной ткани. Если патологический синдром вызван частыми обострениями инфекционных или воспалительных процессов, то назначаются витаминные комплексы, иммуномодулирующие средства.
Диета и рацион
Гломерулонефрит, пиелонефрит и прочие нефропатии требуют обязательной коррекции рациона
Диета при нефропатиях любой природы является неотъемлемой частью успешного лечения. Пациенты с отечностью, выраженным изменением электролитного и общего состава крови, характерными признаками патологии нуждаются в коррекции питания, лечебном рационе. Существенные ограничения накладывают на жидкость, соль, белок.
При остром течении заболевания полностью исключают соль. Ограничения варьируют в зависимости от данных лабораторных исследований. Протеинурия требует увеличения суточного белка наряду со снижением количества углеводов. При выраженных отеках снижают потребление жидкости.
При нефротическом синдроме в рацион требуется включить следующие продукты и блюда:
- овощные бульоны, супы;
- мясо курицы, индейки, крольчатины;
- желе из ягодных и фруктовых морсов;
- свежие фрукты, овощи, зелень;
- кисломолочные продукты.
Важно соблюдать режим питания. Детей необходимо кормить часто малыми порциями. Пища должны быть приготовлена на пару, методом тушения или варки. Примерное меню на день выглядит так:
- утро – сухарики, чай зеленый или теплый морс, безмолочная каша;
- обед – суп-пюре из тыквы с куриной грудкой, галетное печенье, салат из свеклы;
- полдник – снежок или сладкий кисель, сдобная булочка;
- ужин – тушеные овощи с зеленью, тосты, теплый отвар из ягод шиповника с медом.
Меню дополняют свежими фруктами, паровыми овощами. Диета должна быть сбалансированной, разнообразной. Обязательно исключают агрессивную пищу, копчености, фастфуд, в частности, чипсы, соленые орешки.
Детям резко ограничивают сладости, газированную воду. Заменить кондитерские изделия можно медом, сухофруктами, грецкими орехами. Однако с сухофруктами следует быть осторожным, так как курага и чернослив в больших количествах способствуют нарастанию гиперкальциемии.
Возможные осложнения
При постоянной недостаточности белка в организме значительно снижается иммунитет, обостряются инфекционно-воспалительные процессы, хронические заболевания органов, систем. При стойком нарушении почечной функции нарастает азотемия, возникает артериальная гипертензия. Опасным осложнением является вторичная гипертензия с риском развития сердечной недостаточности и отека легких, хроническая почечная недостаточность.
Профилактика и прогноз
При своевременном лечении патологического синдрома обычно наблюдается положительная динамика по выздоровлению, однако прогноз напрямую зависит от степени поражения почечных тканей, стадии органной недостаточности. Врожденный тип патологии при отсутствии наблюдения приводит к хронической почечной недостаточности (ХПН) в раннем возрасте, прогноз всегда серьезный. Профилактика дальнейших разрушений почечных тканей у детей заключается в следующих мероприятиях:
- правильное питание;
- возрастные физические нагрузки;
- соблюдение диеты, охранительного режима;
- организация режима питания, сна, бодрствования.
Для улучшения клинического прогноза и уменьшения прогрессии ХПН важно вовремя лечить респираторные инфекции, обострения хронических инфекций.
Прогноз течения нефротического синдрома у детей тесно связан с характером провоцирующих факторов. При устранении основного заболевания можно рассчитывать на обратимость патологического симптомокомплекса. При отсутствии лечения почечная недостаточность прогрессирует, что в дальнейшем требует заместительной терапии и трансплантации почек.
Читайте далее: синдром Альпорта у детей
Источник
Нефротический синдром впервые описан в начале XIX века. Доктор Брайт отметил такие его признаки, как отечность, протеинурия, липидемия, проследил связь патологии с основными урологическими заболеваниями. В наши дни недуг изучен хорошо. Он регистрируется примерно у 15 новорожденных из 100 тыс. В большинстве случаев нефротический синдром поддается лечению. Родителям важно знать об основных симптомах патологии, чтобы вовремя начать терапию.
Понятие и причины нефротического синдрома у детей
Нефротический синдром (НС) – следствие патологии работы почек. Он проявляется аномальными показателями анализов мочи и крови. Наблюдается высокий уровень белка в моче. В крови, наоборот, значение альбумина снижено, однако крайне высок показатель холестерина. При некоторых формах на тельце малыша появляются отеки.
Патология имеет первичную и вторичную природу. Врожденный синдром может носить наследственный характер и проявляется у детей до 3 месяцев. Первичная форма диагностируется у детей до года. Идиопатическая встречается после года, и ее причины не установлены. Вторичная форма НС возникает в подростковом возрасте и ранее при:
- нарушениях белкового обмена;
- волчанке;
- наследственном нефрите;
- вирусных процессах в почках;
- тромбозе почечной вены;
- микроангиопатии.
Повышение уровня белка в моче при синдроме связано с нарушением проницаемости гломерулярного фильтра. Жидкость задерживается в тканях организма, не выводится полностью в сосудистое русло из-за изменения онкотического давления плазмы. Нередко даже при снижении уровня альбуминов в крови отеки у детей не проявляются.
Разновидности и симптомы патологии
НС классифицируют по клиническим проявлениям на следующие формы:
- чистая – проявляется характерными клиническими симптомами (отеками, низким уровнем белка в крови и повышенными липидами);
- смешанная – с присоединением гипертензии и гематурии (крови в моче);
- полная – имеет все симптомы;
- неполная – при этой форме наблюдается отсутствие некоторых признаков.
Определить форму нефротического синдрома позволит комплексное обследование. Проводится общий осмотр ребенка, сдаются анализы мочи и крови на биохимию, иммунологическое исследование крови, мочи по Нечипоренко, Зимницкому, бакпосев.
При диагностике принимаются во внимание следующие симптомы:
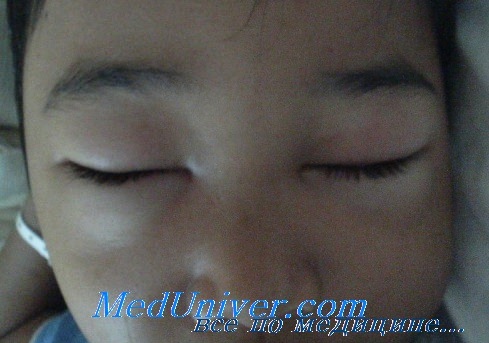
- отеки в области век, которые быстро распространяются на зону паха, живот, конечности малыша;
- снижение суточного выделения мочи;
- простуды инфекционного происхождения;
- тошнота, рвотные позывы;
- сухость во рту;
- отсутствие аппетита, вялость;
- повышение внутричерепного давления.
Особенности лечения детей разного возраста
Лечение патологии проводится в условиях стационара, где есть необходимое оборудование для диагностики и оказания неотложной помощи. Задача терапии – прекращение вывода белка и коррекция работы мочевыделительной системы. С этой целью показана немедикаментозная и медикаментозная терапия в течение 2-6 месяцев. Выбор лекарств зависит от причины и формы патологии.
Медикаментозная терапия
Первичная и идиопатическая формы НС устраняются с помощью кортикостероидов. Длительность терапии – от 2 до 6 месяцев. Первоначально ребенку дают большие дозы препаратов, которые постепенно уменьшают до полной отмены. Прерывать курс лечения запрещено — его начинают в больнице, а заканчивают амбулаторно. Недолеченная патология грозит рецидивами и осложнениями вплоть до почечной недостаточности. При вторичной форме лечение дополняют медикаментами, направленными на борьбу с основным заболеванием, а также цитостатиками.
Немедикаментозные методы
В стационаре и домашних условиях детям назначают комплекс мероприятий, от выполнения которых во многом зависит успех лечения. Показаны:
- бессолевая белковая диета с низким содержанием жира;
- исключение солений, копченостей, пряностей, мясных бульонов;
- ограничение питья в соответствии с предыдущим суточным диурезом.
После того как рецидив заболевания пройдет, ребенку будет разрешено подсаливать еду и пить столько жидкости, сколько положено по возрасту. Не следует ограничивать прием жидкости на длительное время. После рецидива, при котором показан постельный режим, врачи постепенно переходят к упражнениям ЛФК. Они позволят сохранить тонус мышц. В период ремиссии ребенка ставят на диспансерный учет.
При диагностике патологии на ранних этапах ее развития прогноз благоприятен. Чем позже будет оказана медицинская помощь, тем сложнее исправить НС, а это может привести к почечной недостаточности.
Врач-педиатр, врач аллерголог-иммунолог, окончила Самарский государственный медицинский университет по специальности «Педиатрия». Подробнее »
Источник
