Постперикардиотомный синдром что это такое
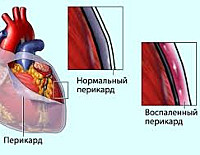
Постперикардиотомный синдром – воспалительное заболевание перикарда аутоиммунного генеза, развивающееся как осложнение хирургических вмешательств на открытом сердце. Его основные симптомы – лихорадочная реакция и боли в грудной клетке, возникающие через неделю или позже после операции. При диагностике учитываются лабораторные признаки воспалительного процесса, данные рентгенографии грудной клетки, ЭКГ, УЗИ и МРТ сердца. Для лечения патологии используются нестероидные противовоспалительные средства (НПВС) или кортикостероиды. Развитие осложнений заболевания нередко требует дополнительного кардиохирургического вмешательства.
Общие сведения
Постперикардиотомный синдром (ППТС) — патологическое состояние, возникающее после хирургического рассечения перикарда – перикардиотомии. Впервые ППТС описан в 50-х годах XX века у пациента, перенесшего открытую митральную комиссуротомию. Заболевание обычно протекает как одиночный эпизод, но впоследствии может рецидивировать. Чаще всего кардиохирурги сталкиваются с этим осложнением после вмешательств по поводу тетрады Фалло, дефектов межпредсердной или межжелудочковой перегородки, трансплантации сердца. Постперикардиотомный синдром осложняет от 2 до 30% подобных операций. Обычно он встречается у детей старше 2 лет и взрослых. Одним из вариантов патологии является постинфарктный синдром Дресслера. Несмотря на отсутствие травмы сердечной сумки, он также вызван ее аутоиммунным воспалением.

Постперикардиотомный синдром
Причины ППТС
Причина формирования постперикардиотомного синдрома – аутоиммунная реакция, возникающая после кардиохирургических операций. Она является следствием врожденных или приобретенных изменений клеточного иммунитета. После повреждения перикардиальных листков организм начинает вырабатывать антитела, взаимодействующие с тканями сердца. Это ведет к развитию аллергической реакции по типу гиперчувствительности замедленного типа и аутоиммунному воспалению.
Развитие синдрома описано после коррекции врожденных и приобретенных пороков сердца, имплантации электрокардиостимулятора, стентирования коронарных артерий, аортокоронарного шунтирования, перикардиальной пункции, радиочастотной аблации, тупой травмы грудной клетки, операций по поводу заболеваний аорты. Фактором риска ПТТС является инфицирование вирусом Коксаки В, цитомегаловирусом, аденовирусом.
Патогенез
Повреждение тканей перикарда вызывает образование антител к мембране клеток (антисарколемных), мышечным волокнам (антифибриллярных) и к клеточным ядрам. Реакция между собственными тканями и аутоантителами сопровождается привлечением к очагу патологии иммунных клеток-макрофагов, эозинофилов, нейтрофильных лейкоцитов. Начинается воспалительная реакция, сопровождающаяся выбросом медиаторов воспаления, лизосомальных ферментов, активных форм кислорода, разрушающих клетки сердечной сумки.
Еще один фактор развития ППТС – системная реакция организма на операционную травму. Она сопровождается эндотоксемией, повреждением клеток миокарда, повышением концентрации гистамина, серотонина, кининов, эйкозаноидов, цитокинов, компонентов комплемента. Это приводит к кислородному голоданию тканей, повышению сосудистой проницаемости, развитию интоксикации, что усиливает местный воспалительный процесс.
Вследствие повышения сосудистой проницаемости в очаге воспаления между двумя перикардиальными листками появляется жидкость, богатая фибрином. Этот белок образует отложения на стенках околосердечной сумки. Кроме того, подобная реакция начинается в плевральной полости. Трение листков перикарда и плевры вызывает появление важного признака, сопровождающего постперикардиотомный синдром, – боли в груди.
Симптомы постперикардиотомного синдрома
Заболевание развивается через 1–6 недель после перенесенной операции. У пациента повышается температура тела до 38-40°C. Продолжительность лихорадочного периода составляет до 3-х недель. Больных беспокоит тупая боль в левой половине грудной клетки. Она не связана с физической активностью, но может усиливаться во время глубокого дыхания, а также в положении лежа. Ухудшается аппетит, появляется слабость, раздражительность. Иногда пациентов беспокоит одышка в состоянии покоя, при незначительной нагрузке, а также ноющие суставные боли.
Когда объем выпота увеличивается, болевой синдром становится менее интенсивным. Образовавшийся экссудат сдавливает сердце, поэтому появляется учащенное сердцебиение, усиливается одышка, набухают шейные вены. Могут присоединяться отеки, постоянная тяжесть в подреберье справа, вызванная увеличением печени. Кроме того, ППТС вызывает затруднения глотания, постоянный сухой кашель, осиплость голоса, тошноту, приступы икоты. У детей признаком тяжелого течения синдрома служит рвота.
Осложнения
Постперикардиотомный синдром сопровождается накоплением выпота внутри перикардиальной полости. Если медицинская помощь оказана несвоевременно, это может привести к развитию опасного для жизни осложнения – тампонады сердца. Сдавление органа вызывает ухудшение сократительной способности миокарда и становится причиной острой сердечной недостаточности. Частота возникновения такого осложнения составляет 10%. Если объем перикардиального выпота мал, сгущение экссудата и образование наслоений фибрина могут спровоцировать появление констриктивного («сдавливающего») перикардита. Данное осложнение развивается у 5% больных ППТС и также сопровождается тяжелой сердечной недостаточностью.
Диагностика
При физикальном обследовании пациента определяется шум трения перикарда и плевры, отеки, увеличение печени. Может обнаруживаться парадоксальный пульс, который сопровождается снижением систолического АД на 10 мм рт. ст. и более, одновременным уменьшением пульсового наполнения на лучевой артерии во время вдоха. Лабораторная диагностика ППТС включает следующие исследования:
- Общий и биохимический анализ крови. Определяется увеличение количества лейкоцитов, появление незрелых форм белых клеток («сдвиг формулы влево»), нарастание СОЭ. Эти признаки характеризуют тяжесть воспалительного процесса. Иногда отмечается увеличение содержания эозинофилов – один из признаков аллергической реакции. Выявляется увеличение концентрации С-реактивного белка, фибриногена, интерлейкина-6. Эти данные свидетельствуют об остром воспалительном процессе.
- Определение антимиокардиальных антител. Исследование подтверждает аутоиммунный характер заболевания. В крови и перикардиальном выпоте определяется высокий титр антител к клеточной оболочке (сарколемме), компонентам мышечных волокон (актину, миозину, тропомиозину), клеточным ядрам. Для ПТТС характерно высокое содержание лимфоцитов, альбумина в перикардиальном экссудате, при назначении антикоагулянтов возможно появление эритроцитов. При бактериоскопии и посеве на питательную среду патогенные микроорганизмы не обнаруживаются.
Для диагностики ПТТС наиболее информативны визуализирующие методики. Они дают возможность оценить количество выпота, его локализацию, угрозу тампонады, состояние легочной ткани. Основные способы инструментальной диагностики заболевания включают:
- УЗИ сердца (ЭхоКГ). С его помощью обнаруживается жидкость в перикардиальной полости, оценивается ее количество и расположение, выявляется уменьшение амплитуды движений (гипокинез) стенок сердца, парадоксальная сократимость сердечных камер, увеличение диаметра нижней полой вены. Кроме трансторакальной, применяется чреспищеводная ЭхоКГ, дающая более точные диагностические сведения. При трудностях проведения или интерпретации данных УЗИ назначается МРТ или МСКТ сердца.
- Рентгенографию органов грудной клетки. На рентгенограммах определяется увеличение сердечной тени, пропорциональное количеству экссудата. При развитии воспаления обнаруживаются признаки пневмонита, скопление плеврального выпота.
- ЭКГ в динамике. Для ПТТС наиболее характерны преходящие подъем сегмента ST, депрессия сегмента PR, формирование отрицательных зубцов Т в нескольких отведениях, прогрессирующее снижение вольтажа (высоты) зубцов. По мере стихания воспаления ЭКГ возвращается к исходной.
Диагностические критерии патологии предложены Американской Кардиологической Ассоциацией. Постперикардиотомный синдром предполагается, если у больного имеются по крайней мере два из перечисленных признаков: лихорадка; боль, вызванная перикардитом или плевритом; шумы трения перикарда или плевры; увеличение количества жидкости в сердечной сумке; экссудативный перикардит, сопровождающийся повышением количества С-реактивного протеина в крови. Дифференциальная диагностика осуществляется с констриктивным перикардитом, застойной сердечной недостаточностью, инфекционным эндокардитом и перикардитом, миокардитом вирусной или иной этиологии.
Лечение посткардиотомного синдрома
Пациенты с ПТТС обычно наблюдаются у кардиолога амбулаторно. Показанием к госпитализации в отделение кардиологии или торакальной хирургии является нарастание объема плеврального выпота, угроза тампонады сердца. Во время лихорадочного периода и сохраняющихся электрокардиографических изменений необходим постельный режим. Специальных диетических ограничений нет, рекомендуется полноценное богатое витаминами питание. Лечение назначается с учетом выраженности и скорости развития клинических проявлений, тяжести заболевания, общего состояния пациента. Преимущественно используется медикаментозная терапия, в некоторых случаях показано хирургическое вмешательство:
- Фармакотерапия. Основу медикаментозной терапии составляют НПВС. В более тяжелых ситуациях или при рецидивирующем течении патологии показан 7-дневный курс глюкокортикоидных гормонов с их постепенной отменой. Эти препараты вызывают более быструю положительную динамику по сравнению с НПВС.
- Кардиохирургические методы. При неэффективности медикаментов, нарастании объема перикардиального выпота, увеличении риска осложнений требуется операция. Возможны следующие варианты хирургических вмешательств: перикардиоцентез, перикардиостомия, чрескожная баллонная перикардиотомия, перикардэктомия. Цель подобных операций – удаление выпота из полости перикарда и профилактика его повторного накопления.
Прогноз и профилактика
Несмотря на высокую частоту развития синдрома, в большинстве случаев прогноз благоприятный. Под влиянием лечения проявления воспалительной реакции постепенно исчезают. Развитие тяжелых осложнений наблюдается у 15% пациентов. Постперикардиотомный синдром рецидивирует у 2% прооперированных, иногда через несколько лет после вмешательства. Для профилактики ПТТС необходимо соблюдение техники кардиохирургических операций: использование прерывистого шва для закрытия перикарда, послеоперационное дренирование его полости, предотвращение попадания крови в сердечную сумку. Есть данные об эффективности у взрослых пациентов послеоперационного назначения колхицина, однако они требуют дальнейшего подтверждения.
Источник
Немцов С. В., Лебедева В. К., Коношкова Р. Л. и др. Nemtsov S. V. , Lebedeva V. K., Konoshkova R. L. et al.
Постперикардиотомный синдром как редкое осложнение имплантации предсердного электрода Postpericardiotomy syndrome as a rare complication of atrial electrode implantation
© НЕМЦОВ С. В., ЛЕБЕДЕВА В. К., КОНОШКОВА Р. Л., НИКОЛАЕВ Г. В., ЛЕБЕДЕВ Д. С.
УДК 616-089; 617.5
Б01: 10.20333/2500136-2018-1-92-95
ПОСТПЕРИКАРДИОТОМНЫЙ СИНДРОМ КАК РЕДКОЕ ОСЛОЖНЕНИЕ ИМПЛАНТАЦИИ ПРЕДСЕРДНОГО ЭЛЕКТРОДА
С. В. Немцов, В. К. Лебедева, Р. Л. Коношкова, Г. В. Николаев, Д. С. Лебедев
Национальный медицинский исследовательский центр имени В. А. Алмазова, Санкт-Петербург 197341, Российская Федерация
Резюме. На сегодняшний день имплантация электронных устройств, таких как кардиостимулятор или имплантируемый кардиовертер-дефибриллятор, нашла широкое применение в клинической практике для лечения различных видов нарушений ритма сердца. Число имплантированных устройств неуклонно растет с каждым годом. Возможные осложнения процедуры установки подобных устройств хорошо известны. В частности, электрод-ассоциированные осложнения нередки для имплантации кардиостимулятора или кардиовертера-дефибриллятора. В литературе описан ряд редких осложнений: операция может осложниться кровотечением или выпотом в плевральную полость, полость перикарда. Нами описывается случай развернутого постперикардиотомного синдрома у 71-летнего пациента после операции репозиции предсердного электрода, диагностическая и лечебная тактика. Данный случай является показательным для специалистов, поскольку даже незначительная травма сердца может явиться причиной упомянутой симптоматики.
Ключевые слова: дефибриллятор, осложнение, предсердный электрод, постперикардиотомный синдром, нарушение ритма сердца, гидроторакс. Для цитирования: Немцов СВ, Лебедева ВК, Коношкова РЛ, Николаев ГВ, Лебедев ДС. Постперикардиотомный синдром как редкое осложнение имплантации предсердного электрода. Сибирское медицинское обозрение. 2018;(1): 92-95. Б01: 10.20333/2500136-2018-1-92-95
POSTPERICARDIOTOMY SYNDROME AS A RARE COMPLICATION OF ATRIAL ELECTRODE IMPLANTATION
S. V. Nemtsov, V. K. Lebedeva, R. L. Konoshkova, G. V. Nikolaev, D. S. Lebedev Almazov National Research Centre, Saint Petersburg 197341, Russian Federation
Abstract. To date, the implantation of electronic devices, such as a pacemaker or implantable cardioverter-defibrillator, has been widely used in clinical practice to treat various types of heart rhythm disturbances. The number of implanted devices is growing steadily every year. Possible complications of the installation procedure for such devices are well known. In particular, electrode-associated complications are not uncommon for the implantation of a pacemaker or a cardioverter-defibrillator. A number of rare complications are described in the literature: surgery can be complicated by bleeding or effusion into the pleural cavity, pericardial cavity. We are describing the case of postpericardiotomy syndrome in a 71-year-old patient after an operation of atrial electrode reposition, diagnostic and therapeutic tactics. This case is indicative for specialists, since even a minor injury of the heart can cause this symptomatology. Key words: defibrillator, complication, atrial electrode, postpericardiotomy syndrome, cardiac rhythm disturbance, hydrothorax Citation: Nemtsov SV, Lebedeva VK, Konoshkova RL, Nikolaev GV, Lebedev DS. Postpericardiotomy syndrome as a rare complication of atrial electrode implantation. Siberian Medical Review. 2018;(1): 92-95. DOI: 10.20333/2500136-2018-1-92-95
Клинический случай
Известно, что электрод-ассоциированные осложнения при постановке кардиостимулятора (ЭКС) или кардиовертера-дефибриллятора достаточно часто встречаются в клинической практике. Наиболее известные из них: дислокация электрода, перфорация миокарда, тампонада сердца, блокада выхода, — хорошо описаны в литературе. Общая частота их встречаемости доходит до 10 % [1]. Известно, что ряд осложнений, например, дислокация, перикардит, более характерны для предсердного электрода, встречаемость последнего доходит до 1,4-5 % [2, 3]. Наряду с ними в клинической практике встречаются и редкие осложнения, более типичные для открытых операций на сердце.
Постперикардиотомный синдром — частое (до 1015 % [4], по другим данным до 30-50 % [5, 6] осложнение «больших» кардиохирургических операций, сопровождающихся кардиотомией и/или вскрытием
полости перикарда. Возникновение данной патологии обычно приходится на 1-6 недели после операции, при этом не исключается как более раннее его возникновение, так и позднее — до года после операции [7] с возможностью его рецидива [8]. Описаны случаи развития данного синдрома при стен-тировании коронарных артерий, а R. W. Peters et al. еще в 1980 г докладывали о подобном осложнении при постановке кардиостимулятора с эпикардиаль-ным электродом. Опубликован ряд работ, в которых описывался постперикардиотомный синдром при постановке эндокардиального электрода трансвенозным доступом [9]. В 1995 году Goutal et al. докладывали о подобном осложнении при имплантации предсердного электрода [10]. Нередким оно является и при инфарктах миокарда (синдром Дресслера).
Для диагностики постперикардиотомного синдрома предложены большие и малые критерии [11],
однако предполагается их низкая чувствительность и чуть более высокая специфичность. К большим относятся: боль в грудной клетке, лихорадка до 38 °С, шум трения плевры/перикарда. Малые включают в себя лейкоцитоз крови, повышение уровня С-реак-тивного белка, ускорение СОЭ. Лечение предполагает назначение нестероидных противовоспалительных средств, гормональных препаратов. Исход, как правило, благоприятный. Также необходимо отметить, что в ряде исследований было выявлено повышение уровня провоспалительных цитокинов (интерлейки-на-6, -8) при развитии постперикардиотомного синдрома.
С подобным осложнение мы встретились в клинической практике.
Больной К., 71 года, 01.11.2016 поступил в клинику центра в плановом порядке для оперативного лечения по поводу синдрома бинодальной слабости (транзиторной синоатриальной (СА) блокады 2 степени, транзиторной атриовентрикулярной (АВ) блокады 2 степени). В дооперационном периоде обследован в полном объеме. Выявлена тромбоцитопения до уровня 93х109/л.
02.11.2016 выполнено плановое оперативное вмешательство — имплантация ПЭКС DDDR (Medtronic Advisa DR MRI SureScan). Предсердный электрод установлен в основании ушка правого предсердия, амплитуда электрограммы — 1,5 мВ, порог стимуляции — 0,8 мА, импеданс — 700 Ом. В послеоперационном периоде 08.11.2016 при плановом программировании выявлено повышение порога стимуляции предсердного электрода до транзиторного отсутствия захвата предсердий на максимальных параметрах стимуляции. При рентгеноскопии дислокации выявлено не было, но, учитывая высокий порог электростимуляции, принято решение о ревизии системы ЭКС. При ревизии обращали на себя внимание обширные подкожные гематомы в местах пункции периферических сосудов, наличие сгустков крови в ложе (около 50 мл). Выполнена репозиция предсердного электрода. Предсердный электрод установлен в основании ушка правого предсердия, амплитуда электрограммы — 2 мВ, порог стимуляции — 0,8 мА, импеданс
— 700 Ом. При контрольном программировании
— удовлетворительные параметры, без нарушения стимуляции и чувствительности по предсердному каналу. 10.11.2016 в удовлетворительном состоянии больной выписан на амбулаторное лечение в поликлинику по месту жительства.
На следующие сутки (11.11.2016) в связи с резким ухудшением состояния в виде появления давящих болей за грудиной, снижения АД до 60/40 мм рт.ст. (также отметил боль в грудной клетке с иррадиацией в спину при глубоком вдохе и выраженную
икоту) больной был экстренно госпитализирован в ЦРБ по месту жительства, где при рентгенографии органов грудной клетки был выявлен правосторонний гидроторакс, падение уровня гемоглобина до 92 г/л. (исходный при выписке от 10.11.2016 — 142 г/л), уровень эритроцитов — 3,06х1012/л. Проведена ин-фузионная терапия. 16.11.2016 пациент переведен в СЗФМИЦ им. В. А. Алмазова. При поступлении состояние пациента относительно удовлетворительное, АД 110/70 мм рт.ст., пульс 64 в мин. — ритм ПЭКС. Температура тела повышалась до 37,5-38 °С. Дыхание жесткое, резко ослаблено в нижних отделах справа. При рентгенологическом исследовании подтвержден правосторонний гидроторакс с компрессией жидкостью правого легкого, левое — без особенностей. При МСКТ органов грудной клетки в правой плевральной полости — жидкостное содержимое толщиной слоя в задних отделах до 6-7 см. (рис. 1).
SgfMlTSinvV А АЕгкдоуа^. SOMATOM Dcfntna^^
Рисунок 1. МСКТ органов грудной клетки от 16.11.2016. Правосторонний гидроторакс, гемопе-рикард (?) с расхождением листков перикарда до 14 мм. Незначительное количество жидкости в левой плевральной полости.
Нижняя доля правого легкого безвоздушна, верхняя и средняя доли правого легкого уменьшены за счет компрессии жидкостью. В левой плевральной полости — небольшое количество жидкости, до 24 мм толщины слоя в задних отделах. По данным МСКТ в полости перикарда выявлено предположительно геморрагическое содержимое с расхождением листков перикарда до 14 мм. Выполнено дренирование правой плевральной полости, одномоментно эвакуировано 1000 мл слабо-мутной жидкости желтого цвета. Дополнительно проведена гемотрансфузия 2 доз эритроцитарной массы. Анализ плевральной жидкости: ПЦР, бактериологическое исследование на ВК, микроскопическое, цитологическое. В исследуемом материале — зрелые
Немцов С. В., Лебедева В. К., Коношкова Р. Л. и др. Nemtsov S. V. , Lebedeva V. K., Konoshkova R. L. et al.
Постперикардиотомный синдром как редкое осложнение имплантации предсердного электрода Postpericardiotomy syndrome as a rare complication of atrial electrode implantation
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
лимфоциты (эритроцитов нет), единичные клетки мезотелия с реактивными изменениями, что свидетельствует о реактивном выпоте с лимфоидной реакцией, предусматривающей аутоиммунный ответ. Дренирование полости перикарда не показано. Следует также отметить повышение уровня С-реактивного белка до 12,5 г/л. В дальнейшем на фоне проводимой терапии, включающей НПВС (кетонал 1,0 мл внутримышечно 3 раза в сутки), наблюдался регресс симптоматики. С 18.11.2016 -нормотермия. Отделение жидкости по дренажу из плевральной полости уменьшалось, 21.11.2016 дренаж удален. На контрольном рентгеновском снимке от 24.11.2016 легкие расправлены, воздуха, жидкости в плевральных полостях не выявлено (рис. 2).
Рисунок 2. Рентгенография органов грудной клетки от 24.11.2016. Легкие расправлены, воздуха, жидкости в плевральных полостях не наблюдается.
Количество жидкости в полости перикарда также уменьшалось, 24.11.2016 при контрольном ЭХО-КГ исследовании выявлено расхождение листков перикарда до 5-6 мм.
Клиническая картина заболевания, данные лабораторных и инструментальных исследований: время возникновения (1-2 недели после операции), лихорадка до 38 °С, выпот в плевральную полость и полость перикарда, доказанный характер реактивного плеврита, быстрое исчезновение жидкости из полости перикарда, незначительное повышение уровня С-реактивного белка, — позволяют установить диагноз — постперикардиотомный синдром. Пунктиро-вание полости перикарда не проводилось, однако быстрое исчезновение жидкости из полости перикарда
не характерно для геморрагического отделяемого. Остается неясным падение уровня гемоглобина, что не позволяет исключить кровотечение, как причину гидроперикарда.
Таким образом, данное наблюдение является примером того, что малоинвазивное оперативное вмешательство может явиться причиной развития реактивного полисерозита по типу постперикардиотомного синдрома. Вероятно, в основе его патогенеза лежала локальная травма миокарда, незначительное кровотечение в полость перикарда при репозиции предсердного электрода с развитием реактивного процесса с участием плевры и перикарда аутоиммунного характера.
Литература / References
1. Gul EE, Kayrak M. Common Pacemaker Problems: Lead and Pocket Complications, Modern Pacemakers. In: Prof. Mithilesh R Das, ed.; 2011:299-318.
2. Ghani A, Delnoy PPHM, Ramdat Misier AR, Smit JJJ, Adiyaman A, Ottervanger JP, Elvan A. Incidence of lead dislodgement, malfunction and perforation during the first year following device implantation. Netherlands Heart Journal. 2014;22(6):286-291. DOI: 10.1007/s12471-014-0556-6
3. Witt CM, Lenz CJ, Shih HH, Ebrille E, Rosenbaum AN, Aung H, van Zyl M, Manocha KK, Deshmukh AJ, Hodge DO, Mulpuru SK, Cha YM,Espinosa RE, Asir-vatham SJ, McLeod CJ. Right atrial lead fixation type and lead position are associated with significant variation in complications. Journal of Interventional Cardiac Electro-physiology. 2016;47(3):313-319.
4. Light RW. Pleural effusions following cardiac injury and coronary artery bypass graft surgery. Seminars in Respiratory and Critical Care Medicine. 2001;22(6):657-64.
5. Engle MA, Zabriskie JB, Senterfit LB. Heart-reactive antibody, viral illness, and the postpericardiotomy syndrome. Correlates of a triple-blind, prospective study. Transactions of the American Clinical and Climatological Association. 1976;(87):147-60.
6. Miller GL, Horneffer PJ, Gardner TJ, Rykiel MF, Pearson TA. The epidemiology of the postpericardiotomy syndrome: a common complication of cardiac surgery. American heart journal. 1988;(116):1323-9.
7. Spindler M, Burrows G, Kowallik P, Ertl G, Voelker W. Postpericardiotomy syndrome and cardiac tamponade as a latecomplication after pacemaker implantation. Pacing and Clinical Electrophysiology. 2001;24(9):1433-4.
8. Imazio M, Brucato A, Rovere ME, Gandino A, Cemin R, Ferrua S, Maestroni S, Barosi A, Simon C,-Ferrazzi P, Belli R, Trinchero R, Spodick D, Adler Y. Contemporary features, risk factors, and prognosis of the post-pericardiotomy syndrome. American Journal
of Cardiology. 2011;108(8):1183-7. DOI: 10.1016/j.amj-card.2011.06.025
9.Sasaki A, Kobayashi H, Okubo T, Namatame Y, Ya-mashina A, Repeated postpericardiotomy syndrome following a temporary transvenous pacemaker insertion, a permanent transvenous pacemaker insertion and surgical pericardiotomy. Japanese Circulation Journal. 2001;65(4):343-4.
10.Goutal H, Baur F, Bonnevie L, Monnier G, Le Blainvaux M, Brion R. Postpericardiotomy syndrome; a rare com complication of transcavitary cardiac pacing: apropos of a case. Archives Des Maladies Du Coeur Et Des Vaisseaux. 1995;88(12):1901-3.
11. Bartels C, Honig R, Burger G, Diehl V, De Vivie R. The significance of anticardiolipin antibodies and anti-heart muscle antibodies for the diagnosis of post-pericardiotomy syndrome. European Heart Journal. 1994;(15):1494-9.
Сведения об авторах:
Немцов Сергей Викторович, сердечно-сосудистый хирург, аспирант; Национальный медицинский исследовательский центр имени В. А. Алмазова; адрес: Российская Федерация, 197341, г. Санкт-Петербург, ул. Аккуратова д. 2; тел.: +7(812)7023730; e-mail: nemtsovsvs@mail.ru
Лебедева Виктория Кимовна, старший научный сотрудник; Национальный медицинский исследовательский центр имени В. А. Алмазова; адрес: Российская Федерация, 197341, г. Санкт-Петербург, ул. Аккуратова д. 2; тел.: +7(812)7023730; e-mail: viktkim@ rambler.ru
Коношкова Раиса Леонидовна, к.м.н., заместитель главного врача по кардиологии, врач-кардиолог высшей категории; Национальный медицинский исследовательский центр имени В. А. Алмазова; адрес: Российская Федерация, 197341, г. Санкт-Петербург, ул. Аккуратова д. 2; тел.: +7(812)7023730; e-mail: konoshkova_rl@ almazovcentre.ru
Николаев Герман Викторович, к.м.н., официальный эксперт по трансплантации от России в совете Европы (г. Страсбург), главный трансплантолог Санкт-Петербурга, заведующий НИЛ торакальной хирургии, торакальный хирург, врач высшей категории; Национальный медицинский исследовательский центр имени В. А. Алмазова; адрес: Российская Федерация, 197341, г. Санкт-Петербург, ул. Аккуратова д. 2; тел.: +7(812)7023730; e-mail: g_nikolaev@list.ru
Лебедев Дмитрий Сергеевич, руководитель, профессор; Национальный медицинский исследовательский центр имени В. А. Алмазова; адрес: Российская Федерация, 197341, г. Санкт-Петербург, ул. Аккуратова д. 2; тел.: +7(812)7023730; e-mail: lebede-vdmitry@mail.ru
Author information
Sergey V. Nemtsov, Cardiovascular Surgeon, Postgraduate Student; Almazov National Research Centre; Address: 2, Akkuratov Str., St. Petersburg, Russian Federation 197341; Phone: +7(812)7023730; e-mail: nemtsovsvs@mail.ru
Victoria K. Lebedeva, Senior Researcher; Almazov National Research Centre, Address: 2, Akkuratov Str., St. Petersburg, Russian Federation 197341; Phone: +7(812)7023730; e-mail: viktkim@rambler.ru
Raisa L. Konoshkova, Dr. Med. Sci., Deputy Chief Physician for Cardiology, Cardiologist of the Highest Category; Almazov National Research Centre; Address: 2, Akkuratov Str., St. Petersburg, Russian Federation 197341; Phone: +7(812)7023730; e-mail: konoshkova_rl@ almazovcentre.ru
German V. Nikolaev, Cand. Med. Sci., the Official Expert on Transplantation from Russia in the Council of Europe (Strasbourg), the Chief Transplantologist of St. Petersburg, the Head of the NRL of Thoracic Surgery, the Thoracic Surgeon, the Doctor of the Highest Category; Almazov National Research Centre; Address: 2, Akkuratov Str., St. Petersburg, Russian Federation 197341; Phone: +7(812)7023730; e-mail: g_nikolaev@list.ru
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Dmitriy S. Lebedev, the Head, Professor, Almazov National Research Centre; Address: 2, Akkuratov Str., St. Petersburg, Russian Federation 197341; Phone: +7(812)7023730; e-mail: lebedevdmitry@mail.ru
Поступила 15.03.2017 г.
Принята к печати 12.12.2017 г.
© ГУЗЕЙ Т. Н., КАРАЧЕВА Ю. В., КОЛЕНЧЕНКО В. В., ЕРЕМЕЕВА З. В., МАКСИМЕНКО В. Г. УДК 616.521.8-06:616.33-006.6 Б01: 10.20333/2500136-2018-1-95-99
КЛИНИЧЕСКИЙ СЛУЧАЙ ЗЛОКАЧЕСТВЕННОЙ ФОРМЫ ЧЕРНОГО АКАНТОЗА У БОЛЬНОГО АДЕНОКАРЦИНОМОЙ ЖЕЛУДКА
Т. Н. Гузей1, Ю. В. Карачева1, В. В. Коленченко2, З. В. Еремеева3, В. Г. Максименко 1
‘Красноярский государственный медицинский университет имени профессора В.Ф. Войно-Ясенецкого, Красноярск 660022, Российская Федерация
2Институт медицинской косметологии ООО «Омекс — ИМК», Красноярск 660017, Российская Федерация красноярский краевой кожно-венерологический диспансер №1, Красноярск 660099, Российская Федерация
Резюме. В данной статье представлен литературный обзор по проблеме пигментной сосочковой дистрофии кожи (черный акантоз). Авторы описывают клинический случай злокачественного варианта черного акантоза у больного аденокарциномой желудка. Поражение кожи предшествовало постановке диагноза злокачественного образования в течение года, в связи с чем авторы акцентируют внимание на необходимость повышенной настороженности при интерпретации клинических симптомов данной кожной патологии.
Ключевые слова: черный акантоз, литературный обзор, патогенез, клинические варианты, клинический случай, аденокарцинома желудка. Для цитирования: Гузей ТН, Карачева ЮВ, Коленченко ВВ, Еремеева ЗВ, Максименко ВГ. Клинический случай злокачественной формы черного акантоза у больного аденокарциномой желудка. Сибирское медицинское обозрение. 2018;(1): 95-99. DOI: 10.20333/2500136-2018-1-95-99
CLINICAL CASE OF MALIGNANT FORM OF BLACK AKANTOSIS IN PATIENT WITH ADENOCARCINOMA OF THE STOMACH
T. N.Guzey1, J. V. Karacheva1, V. V. Kolenchenko2, Z. V. Eremeeva3, V. G. Maximenko 1
‘Professor V. F. Voino-Yasenetsky Krasnoyarsk State Medical University, Krasnoyarsk 660022, Russian Federation 2 Institute of Medical Cosmetology «Omex-IMK, LTD», Krasnoyarsk 660017, Russian Federation 3Krasnoyarsk Regional Dermatovenerologic Dispensary №1, Krasnoyarsk 660099, Russian Federation
Abstract. This article presents a literature review on the problem of pigmentary papillary dystrophy of the skin (black acanthosis). The authors describe the clinical case of a malignant variant of black acanthosis in a patient with gastric adenocarcinoma. The defeat of the skin preceded the diagnosis of malignant
Источник
