Острый миелобластный лейкоз код мкб
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Симптомы
- Причины
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Острый миелоидный лейкоз.
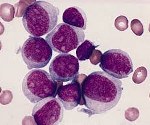
Острый миелоидный лейкоз
Описание
Острый миелоидный лейкоз (ОМЛ, острый нелимфобластный лейкоз, острый миелогенный лейкоз) — это злокачественная опухоль миелоидного ростка крови, при которой быстро размножаются изменённые белые кровяные клетки. Накапливаясь в костном мозге, они подавляют рост нормальных клеток крови. ОМЛ самый распространённый вид острого лейкоза у взрослых, заболеваемость им с возрастом увеличивается. Хотя острый миелоидный лейкоз заболевание относительно редкое — на его долю приходится лишь 1,2 % смертельных случаев злокачественных опухолей в США -, ожидается его учащение вместе с постарением населения.
Симптомы острого миелоидного лейкоза вызываются замещением нормального костного мозга лейкемическими клетками, что приводит к снижению количества красных кровяных клеток, тромбоцитов, и нормальных лейкоцитов. Болезнь проявляется быстрой утомляемостью, одышкой, частыми мелкими повреждениями кожи, повышенной кровоточивостью, частыми инфекционными поражениями. До сих пор явная причина заболевания неизвестна, однако некоторые факторы риска его возникновения выявлены. Как всякое острое заболевание, ОМЛ развивается быстро, и без лечения оборачивается летальным исходом за несколько месяцев, иногда — недель.
Встречаются несколько разновидностей ОМЛ, лечение и прогноз для них оказывается разным. Уровень выживаемости на протяжении пяти лет колеблется между 15-70 %, а частота ремиссии — от 78 до 33 % в зависимости от подвида заболевания. В начале ОМЛ лечат химиопрепаратами для того, чтобы добиться ремиссии; затем может проводиться поддерживающее химиолечение, или проводится пересадка кроветворных стволовых клеток. Последние исследования ОМЛ на генетическом уровне позволили разработать тесты, с помощью которых можно довольно точно определить вероятность выживания больного и эффективность того или иного лекарства для индивидуального случая ОМЛ.
Симптомы
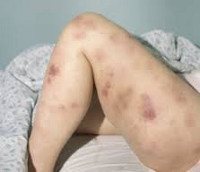
Большая часть симптомов ОМЛ вызывается замещением нормальных клеток крови лейкозными клетками. Недостаточное образование лейкоцитов обусловливает высокую восприимчивость больного к инфекциям — несмотря на то, что лейкемические клетки происходят от предшественников лейкоцитов, способность противостоять инфектам у них отсутствует. Снижение количества красных кровяных телец (анемия) может вызывать усталость, бледность, и одышку. Недостаток тромбоцитов может привести к легкой повреждаемости кожи и повышенной кровоточивости.
Гематома.
Ранние признаки ОМЛ часто неопределённы и неспецифичны, и могут походить на признаки гриппа или других распространённых болезней. Вот некоторые общие симптомы ОМЛ: лихорадка, усталость, потеря веса или снижение аппетита, одышка, анемия, повышенная повреждаемость кожи и слизистых оболочек и кровоточивость, петехии (плоские, размером с булавочную головку пятнышки внутри кожи на месте кровоизлияний), гематомы, боль в костях и суставах, и стойкие или частые инфекции.
При ОМЛ может быть увеличение селезёнки но обычно оно незначительно и бессимптомно. Увеличение лимфоузлов при ОМЛ случается нечасто, в отличие от острого лимфобластного лейкоза. В 10 % случаев развиваются изменения кожи в виде кожного лейкоза. Изредка при ОМЛ возникает Синдром Свита, он же паранеопластический синдром — воспаление кожи вокруг поражённых хлоромой участков.
У некоторых больных ОМЛ появляется припухлость дёсен из-за инфильтрации тканей лейкозными клетками. Изредка первым признаком лейкоза оказывается хлорома — плотная лейкемическая масса за пределами костного мозга. Иногда заболевание протекает бессимптомно, и лейкоз выявляется общим анализом крови в ходе профилактического осмотра.
Боль в шейном отделе позвоночника. Высокая температура тела. Изменение аппетита. Изменение веса. Истощение. Ломота в суставах. Ломота в теле. Нарушение терморегуляции. Общая потливость. Отсутствие аппетита. Потеря веса. Ретикулоцитоз. Слабость. Холодный пот.

Острый миелоидный лейкоз
Причины
Был выявлен ряд факторов, способствующих возникновению ОМЛ — иные расстройства системы кроветворения, воздействие вредных веществ, ионизирующее излучение, и генетическое влияние.
Прелейкоз.
»Прелейкозные нарушения кроветворения, такие, как миелодиспластический синдром или миелопролиферативный синдром могут привести к ОМЛ; вероятность заболевания зависит от формы миелодиспластического или миелопролиферативного синдрома.
Воздействие химических веществ.
Противоопухолевое химиотерапевтическое воздействие, особенно алкилирующими веществами, может увеличивать вероятность возникновения ОМЛ в последующем. Наивысшая вероятность заболевания приходится на 3—5 лет после химиотерапии. Другие химиотерапевтические препараты особенно эпиподофилотоксины и антрациклины, также связываются с постхимиотерапевтическими лейкозами. Лейкозы такого вида часто объясняют специфическими изменениями в хромосомах лейкозных клеток.
Воздействие бензола и других ароматических органических растворителей, связанное с профессиональной деятельностью, в качестве возможной причины ОМЛ остаётся спорным. Бензол и многие его производные проявляют канцерогенные свойства in vitro Данные некоторых наблюдений подтверждают возможность влияния профессиональных контактов с этими веществами на вероятность развития ОМЛ, однако другие исследования подтверждают, что если и существует такая опасность, то она является лишь добавочным фактором.
Ионизирующее излучение.
Воздействие ионизирующего излучения повышает вероятность заболеваня ОМЛ. У переживших атомную бомбардировку Хиросимы и Нагасаки заболеваемость ОМЛ повышена, так же как у рентгенологов, получивших высокие дозы рентгеновского излучения в то время, когда меры радиологической защиты были недостаточными.
Генетические факторы.
Вероятно, существует наследственно повышенная вероятность заболевания ОМЛ. Есть большое количество сообщений о множестве семейных случаев ОМЛ, когда заболеваемость превышала среднестатистическую. Вероятность возникновения ОМЛ у ближайших родственников больного втрое выше.
Ряд врождённых состояний может повышать вероятность ОМЛ. Чаще всего это синдром Дауна, при котором вероятность ОМЛ повышена в 10 — 18 раз.
Лечение
Лечение ОМЛ состоит в основном из химиотерапии, и делится на два этапа: индукция и постремиссионное лечение(или консолидация). Цель индукционной терапии является достижение полной ремиссии за счет уменьшения количества лейкозных клеток до не обнаруживаемого уровня; цель консолидирующей терапии заключается в ликвидации остаточных, не обнаруживаемых современными методами остатками болезни и излечение.
Индукция.
Для всех подтипов ОМЛ за исключением M3 по классификации ФАБ, обычно используют индукционную химиотерапию цитарабином и антрациклином, (например, даунорубицином или идарубицином. Этот способ индукционной химиотерапии известен под названием «7+3» — из-за того, что цитарабин вводят внутривенно капельно семь дней подряд, а затем три дня подряд струйно вводят видарабин в суточной дозе. При таком способе лечения ремиссия наступает почти у 70 % больных ОМЛ. Могут применяться и другие способы индукционного лечения, включая монотерапию высокими дозами цитарабина, или препаратами, находящимися на стадии исследования. Вследствие токсического воздействия лечения, в том числе подавления миелоидного ростка и повышения вероятности инфекционных осложнений очень старым больным индукционная химиотерапия не предлагается, и назначается менее интенсивное паллиативное лечение химиопрепаратами. Подвид ОМЛ M3, также известный под названием острый промиелоцитарный лейкоз, почти во всех случаях лечится препаратом ПТРК (полностью транс- ретиноевая кислота) в дополнение к индукционной терапии. При лечении острого промиелоцитарного лейкоза нужно учитывать возможность развития синдрома диссеминированного внутрисосудистого свёртывания вследствие поступления содержимого гранул промиелоцитов в периферическую кровь. Лечение острого промиелоцитарного лейкоза исключительно эффективно, это достоверно доказано множеством документированных случаев лечения.
Целью индукционного этапа лечения является достижение полной ремиссии. Полная ремиссия не означает, что заболевание полностью вылечено. Скорее, состояние полной ремиссии говорит о невозможности обнаружить болезнь существующими способами диагностики. Полная ремиссия достигается у 50-70 % взрослых больных с впервые выявленным ОМЛ, разница зависит от прогностических факторов, о которых сказано выше. Длительность ремиссии зависит от прогностических качеств исходного лейкоза. В основном, все случаи ремиссии без дополнительного, консолидирующего лечения закачиваются рецидивом.
Консолидационное лечение.
Даже после достижения полной ремиссии вероятно, немногие лейкозные клетки всё же выживают. Их так мало, что обнаружить их пока невозможно. В случае не проведения послеремиссионного, или консолидационного лечения почти у всех больных в конце — концов возникает рецидив. Поэтому для того, чтобы избавиться от неопределимых больных клеток и предотвратить рецидив — то есть, достичь полного излечения, нужна дополнительная терапия. Вид лечения после достижения ремиссии определяется индивидуально в зависимости от прогностических факторов и общего состояния здоровья больного. При прогностически благоприятных подвидах лейкозов (например, при inv(16), t(8;21) и t(15;17) обычно назначают 3-5 дополнительных курса интенсивной химиотерапии, известной как консолидационное лечение. Больным с высоким риском рецидива (например, при наличии цитогенетических изменений, сопутствующего миелодиспластического синдрома, или при ОМЛ, связанном с предшествующим лечением обычно рекомендуется транплантация аллогенных стволовых клеток гемопоэтического ряда, если позволяет общее состояние и есть подходящий донор. При ОМЛ со средней вероятностью рецидива (при нормальных цитогенетических показателях или с такими цитогенетическими изменениями, которые не попадают в группы риска)вопрос консолидационного лечения не столь ясен и определяется рядом специфических показателей — возрастом больного, общим состоянием его здоровья, системой ценностей, и наконец, наличием донора подходящих стволовых клеток.
Тем больным, которым пересадка стволовых клеток после консолидационного лечения не показана, проводят иммунотерапию комбинацией гистамина гидрохлорида (цеплена) и пролейкина. Такое лечение позволяет снизить вероятность рецидива на 14 %, удлиняя ремиссию на 50 %.
Таким образом, стандартной терапией ОМЛ признаны высокоинтенсивная химиотерапия (ВХТ) и трансплантация костного мозга.
Однако результаты лечения, несмотря на относительно высокие ответы у молодых, остаются неудовлетворительными у лиц старше 65 лет (30-50%) связанные с ранней летальностью (10%) и непродолжительностью ремиссии. Больше половины с ОМЛ – это больные старшего возраста и/или со значимой сопутствующей патологией, которые, как правило, не могут получать высокотоксичные схемы химиотерапии, поэтому для их терапии применяют низкие дозы цитарабина цитарабина и поддерживающее лечение: антибиотики и гемотрансфузии.
С 2010 года в США для лечения ОМЛ рекомендовано применять гипометилирующие агенты (5-азацитидин, децитабин) у пациентов, которые не подходят для трансплантации костногомозговых клеток/интенсивной химиотерапии. В процессе метилирования ДНК гипометилирующие агенты ковалентно связываются с ДНК-метилтрансферазой, что приводит к реактивации генов, после чего восстанавливается дифференцировка гемопоэтических клеток-предшественников и нормальное кроветворение. 5-азацитидин обладает двойным механизмом действия. Он встраивается не только в молекулу ДНК, но и в молекулу РНК. Тем самым 5-азацитидин понижает количество РНК в клетках, что приводит к цитостатическому эффекту вне зависимости от клеточной фазы.
На основании результатов исследования 3 фазы AZA-001 — международное, мультицентровое, контролируемое исследование в параллельных группах, в котором пациенты МДС высокого риска/ОМЛ (ВОЗ критерии) сравнивались со стандартно используемой терапией (сопроводительная терапия, интенсивная химиотерапия, низкие дозы цитарабина), азацитидин был зарегистрирован, в том числе и в РФ, для лечения этих групп больных. Было показано, что азацитидин в 2,5 раза увеличивает общую выживаемость пациентов с ОМЛ (критерии ВОЗ).
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Рубрика МКБ-10: C92.0
МКБ-10 / C00-D48 КЛАСС II Новообразования / C00-C97 Злокачественные новообразования / C81-C96 Злокачественные новообразования лимфоидной, кроветворной и родственных им тканей / C92 Миелоидный лейкоз миелолейкоз
Определение и общие сведения[править]
Острый миелоидный лейкоз
Синонимы: острый нелимфобластный лейкоз (ОНЛЛ), острый миелобластный лейкоз (ОМЛ)
Гетерогенная группа опухолевых заболеваний системы крови, характеризуемая повышенным уровнем предшественников миелоидных, моноцитарных, эритроидных или мегакариоцитарных клеток в костном мозге.
Эпидемиология
ОМЛ в детском возрасте встречают в 15-20% случаев среди всех лейкозов, заболеваемость составляет 5,6 случаев на 1 млн детского населения в год.
Этиология и патогенез[править]
Известны довольно частые случаи развития ОМЛ и хронического миелолейкоза (ХМЛ) у людей, перенёсших атомную бомбардировку Хиросимы. У этой группы больных было выявлено достоверно более высокое содержание субклонов с моносомией 7 и делецией 20q13.3 участка. Среди популяции, проживавшей около Чернобыля во время аварии на атомной станции, чаще стали диагностировать FAB M4 и M5 варианты. Исследуют влияние длительного воздействия пестицидов, принимаемых с пищей, прием алкоголя и ингибиторов топоизомеразы II во время беременности матери, развитие у детей вторичного лейкоза или миелодиспластического синдрома (МДС) при лечении другой опухоли вследствие приема алкилирующих агентов или ингибиторов топоизомеразыII. Риск развития ОМЛ связан также со спленомегалией, суммарной дозой алкилирующих агентов, дозой и объёмом лечебного облучения и возрастом. Дети, получавшие химиотерапию во время лечения другой опухоли, рискуют заболеть вторичным ОМЛ в большей степени, чем другие дети. Наибольший риск (23%) развития вторичных лейкозов отмечен у больных с метастатической саркомой Юинга, подвергнутых интенсивному лечению с использованием ифосфамида, циклофосфамида и радиотерапии.
Патогенез
ОМЛ возникает при трансформации гемопоэтической клетки — родоначальницы клональной популяции опухолевых клеток, которая замещает при этом нормальные клетки костного мозга, а также может поражать экстрамедуллярные ткани. Точное количество генных мутаций, участвующих в возникновении и патогенезе ОМЛ, до сих пор не известно. Несмотря на расширение знаний о природе человека, точные цели этих мутаций не вполне ясны. В большинстве случаев ОМЛ нельзя определить клеткуродоначальницу опухолевого клона.
В настоящее время известны, как минимум, три потенциальные механизма, посредством которых лейкозные клетки могут аккумулироваться в костном мозге. Один из них способствует более быстрой пролиферации опухолевых клеток по сравнению с нормальными клетками костного мозга. Другой потенциальный механизм клеточной трансформации — выход из нормального пути апоптоза. Третий механизм развития ОМЛ состоит в блокировке нормальной дифференцировки клеток — предшественников гемопоэза.
Молекулярный механизм до сих пор ясно не представлен.
Одним из его примеров служит острый промиелоцитарный лейкоз (ОПЛ), при котором в результате транслокации t(15;17) возникает аномальный ген PML/RARα и клетка начинает синтез аномального белка PML/RARα, который блокирует клеточную дифференцировку путем ингибирования рецептора к ретиноидам. Лейкозные клетки нормально дифференцируются до промиелоцитов, после чего возникает полный блок дифференцировки клеточной линии. Этот блок может быть преодолен назначением полностью — трансретиноевой кислоты (ATRA). Такой пример иллюстрирует возможность лечения ОМЛ посредством агентов клеточной дифференцировки.
Клинические проявления[править]
Клиническая картина ОМЛ выражена следующими синдромами: анемическим, геморрагическим, токсическим, которые отражают снижение продукции эритроцитов, тромбоцитов и гранулоцитов. Первыми симптомами ОМЛ у детей могут быть лейкозные экстрамедуллярные поражения. Повышенная утомляемость, бледность кожных покровов, выраженная слабость, головокружение, головная боль, одышка, тахикардия — проявления анемии, которая обычно бывает нормохромной. Уровень гемоглобина в периферической крови в пределах 27-140 г/л, в среднем составляет 70 г/л. Часто родители не обращают внимания на повышенную утомляемость, бледность кожных покровов, объясняя эти симптомы большими нагрузками в школе и недостаточным нахождением ребёнка на свежем воздухе. Тромбоцитопения обычно вызывает развитие геморрагического синдрома, который может быть представлен как кожными проявлениями (петехии, пурпура, экхимозы, гематомы), так и различными кровотечениями (носовыми, кишечными, из полости матки, из слизистой дёсен и полости рта). На момент диагностики уровень тромбоцитов, по данным анализов периферической крови, составляет не более 50×109/л приблизительно у 50% детей, больных ОМЛ. Кроме того, геморрагический синдром часто бывает проявлением синдрома диссеменированного внутрисосудистого свёртывания (ДВС), который может возникнуть при любом варианте ОМЛ, но особенно характерен для ОПЛ. Активированный тромбопластин из гранул опухолевых промиелоцитов выходит в сосудистое русло при их лизисе, который происходит под воздействием индуктивной цитостатической терапии, что усиливает ДВС-синдром.
Как правило, в дебюте заболевания у детей с ОМЛ снижено абсолютное количество гранулоцитов (менее 1×109/л в анализе периферической крови); у больных часто возникают инфекции, вызванные сапрофитными микроорганизмами полости рта, кишечника, параректальной области, лёгких, кожи. Чаще повышение температуры обусловлено инфекционным процессом. В связи с этим фебрильную температуру до начала цитостатической терапии необходимо рассматривать как признак инфекции, для диагностики которой проводят бактериологическое исследования крови, кала, мочи, мазков из полости рта, носа и с поверхности кожи, а также назначают эмпирическую антибактериальную терапию с последующей её коррекцией в зависимости от результатов высевов.
Гепатоспленомегалию встречают более чем в половине всех случаев ОМЛ у детей. Выраженный гепатолиенальный синдром обнаруживают у 25% больных ОМЛ, что более характерно для пациентов с моноцитоидным компонентом опухолевых клеток (М4 и М5 FABварианты).
Лимфатические узлы у большинства больных небольших размеров, безболезненные, не спаяны с кожей и друг с другом. В редких случаях наблюдают увеличенные лимфатические узлы размером 2,5-5 см с образованием конгломератов в шейнонадключичной области.
Проявлениями изменений в костносуставной системе в некоторых случаях служат выраженные оссалгии в нижних конечностях и в области позвоночного столба, что сопровождается нарушением движений и походки.
На рентгенограммах костной системы отмечают деструктивные изменения различной локализации, периостальные реакции, явления остеопороза. Проявления экстрамедуллярных опухолевых поражений чаще выражены гингивитом и экзофтальмом, в том числе двусторонним. В редких случаях отмечают опухолевую инфильтрацию мягких тканей, гипертрофию нёбных миндалин, поражение носоглотки и лицевого нерва. Экстрамедуллярные проявления ОМЛ объединяет термин гранулоцитарная (миелоидная) саркома, включая классическую хлорому и непигментированные опухоли.
По данным аутопсии, миелоидную саркому диагностируют у больных ОМЛ в 3-8% случаев. Она может предшествовать поражению костного мозга или сочетаться с признаками ОМЛ, а также возникать при рецидиве заболевания. Орбитальная ткань и внутренние структуры черепа — наиболее частые зоны локализации опухолевого роста. Бластные клетки чаще представлены FAB М2 вариантом и транслокацией t(8;21), а у детей в возрасте до 1 года — М4 и М5 вариантами ОМЛ. Ряд авторов указывают на более плохой прогноз у этих больных, чем у детей с ОМЛ без экстрамедуллярной инфильтрации.
Поражение ЦНС может быть как локальным, представленным миелоидной саркомой этой зоны, так и диссеминированным поражением оболочек головного мозга. Клинически отмечают головную боль, тошноту, рвоту, фотофобию. Поражение ЦНС должно быть подтверждено анализом цитологических препаратов, приготовленных путём центрифугирования ликвора. Вовлечение в лейкозный процесс ЦНС отмечают у 5-15% детей с ОМЛ в сочетании с высоким лейкоцитозом или возрастом пациентов менее 2 лет на момент диагностики ОМЛ, а также у детей с М4Ео и М5 вариантами.
Острый миелоидный лейкоз: Диагностика[править]
Анамнез
При ретроспективном анализе родители пациента обычно отмечают появление симптомов ОМЛ за 2-4 нед, иногда за 1-2 мес до установления диагноза.
Физикальное обследование
При осмотре обращают внимание на анемию, геморрагический синдром, увеличение печени, селезёнки, периферических лимфатических узлов, а также возможное экстрамедулярное поражение мягких тканей (кожа, периорбитальная клетчатка и др.).
Лабораторные исследования
Уровень гемоглобина в периферической крови подвержен колебаниям от 27 до 140 г/л, в среднем составляет 70 г/л, увеличено количество лейкоцитов (у 25% больных более 100×109/л). Количество бластных клеток в анализе периферической крови может быть как выраженным (более 80%), так и незначительным, вплоть до их полного отсутствия.
При оценке миелограммы диагноз ОМЛ устанавливают при наличии более 25-30% бластных клеток, классифицируемых по FABклассификации.
Моноклональные антитела используют при иммунофенотипировании для определения линейноспецифических и стадия специфических антигенов лимфоидной и миелоидной дифференцировки бластов. Моноклональные антитела помогают установить диагноз ОМЛ и дифференцировать его от ОЛЛ, если это затруднительно при морфоцитохимическом исследовании. Некоторые миелоидные маркёры могут определять и на лимфобластах, тогда диагноз ОМЛ не может быть установлен только на основе результатов иммунофенотипирования.
Клональные хромосомные аномалии определяют в большинстве случаев ОМЛ, что способствует более точной диагностике. Существуют хромосомные аномалии, характерные для определённых морфологических вариантов ОМЛ: t(15;17), t(8;21) для М2 ОНЛЛ и inv(16) для М4 ОМЛ. Но в то же время другие аномалии, например, вовлекающие ген MLL, локализованный на 11q23, могут определяться не только при различных морфологических вариантах ОМЛ, но и при ОЛЛ. Исследование с помощью FISH даёт возможность определить генетические аномалии при ограниченных возможностях стандартного цитогенетического исследования. Применяя FISHисследование, можно выявить хромосомные аберрации не только на метафазных, но и на интерфазных ядрах, что особенно важно для обнаружения остаточного клона клеток после химиотерапии. Для выявления ДВСсиндрома необходимы данные коагулограммы.
Инструментальные тсследования
В целях диагностики поражения ЦНС необходимы дополнительные методы исследования: МРТ, КТ, ЭЭГ и ЭхоЭГ.
Дифференциальный диагноз[править]
Апластическая анемия, тромбоцитопеническая пурпура, миелодиспластический синдром, ОЛЛ (острый лимфобластный лейкоз), ХМЛ (хронический миелобластный лейкоз), нейробластома, ретинобластома.
Острый миелоидный лейкоз: Лечение[править]
Цель лечения
Максимальная эрадикация лейкозного клона.
Показания к госпитализации
Проведение интенсивной ПХТ и лечение осложнений.
Немедикаментозное лечение
Лучевая терапия при инициальном поражении ЦНС и для профилактики её лейкозного поражения при inv(16)/t(16;16).
Медикаментозное лечение
При проведении индуктивного и консолидирующего курсов химиотерапии необходима максимальная интенсификация, что приводит к наиболее быстрому достижению полной ремиссии. Следствие такой терапии — аплазия костного мозга, во время которой резко возрастает опасность возникновения инфекционных и геморрагических осложнений. В связи с этим больным необходимо массивное сопроводительное лечение, включающее в себя заместительную, антибактериальную и дезинтоксикационную инфузионную терапию с ежедневной коррекцией электролитов и белка. Основные препараты, входящие в используемые программы ПХТ, цитарабин в сочетании с антрациклиновыми антибиотиками: этопозидом, флударабином, кладрибином. Аллогенная трансплантация гемопоэтических стволовых клеток показана у больных с очень медленным ответом на проведённую химиотерапию (отсутствие ремиссии после курса индукции ремиссии).
Хирургическое лечение
Не показано.
Профилактика[править]
Прочее[править]
Показания к консультации других специалистов
При появлении определённой симптоматики.
Примерные сроки нетрудоспособности
В течение 6 мес интенсивной ПХТ.
Дальнейшее ведение
Наблюдение врачом онкогематологом один раз в 2 нед в течение 2 лет, затем один раз в 2 мес (3 года), далее один раз в 6 мес (5 лет).
Информация для пациента
Охранительный режим (ограничить физические нагрузки, избегать прямых солнечных лучей), полноценное питание.
Прогноз
В первую очередь прогноз зависит от кариотипа опухолевых клеток. Так, к благоприятному кариотипу относят следующие аномалии: t(8;21), t(15;17), inv(16), t(9;11) и другие аномалии 11q23, исключая t(10;11), к промежуточному кариотипу — нормальный кариотип и к кариотипу с высоким риском развития рецидива — 5, 7, 5q, более 5 различных аномалий, исключая стандартные. До сих пор нет определённых данных о значении инициального уровня лейкоцитов, размеров паренхиматозных органов для прогноза ОМЛ. Возможно, это связано с различной по интенсивности терапией, используемой различными исследовательскими группами и гетерогенностью ОМЛ. Отмечают неблагоприятное течение ОМЛ при FAB М4 без inv(16), М5, М6 и М7 морфологических вариантах. Довольно часто прогностически неблагоприятные генетические аномалии сочетаны с прогностически неблагоприятными морфологическими вариантами.
Источники (ссылки)[править]
Онкология [Электронный ресурс] / Под ред. Чиссова В.И., Давыдова М.И. — М. : ГЭОТАР-Медиа, 2013. — https://www.rosmedlib.ru/book/ISBN9785970423684.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
- Азацитидин
- Гилтеритиниб
- Гласдегиб
- Даунорубицин
- Даунорубицин/цитарабин
- Доксорубицин
- Гемтузумаб озогамицин
- Меркаптопурин
- Мидостаурин
- Митоксантрон
- Циклофосфамид
- Цитарабин
- Энасидениб
- Этопозид
Источник
