Острый лейкоз и двс синдром

Сюжет Пандемия коронавируса нового типа, распространившегося из Китая
Коронавирусная инфекция COVID-19 может вызывать осложнение в виде синдрома диссеминированного внутрисосудистого свертывания (ДВС-синдром). В связи с этим Комитет Госдумы по охране здоровья планирует направить в Минздрав предложение о корректировке клинических рекомендаций по лечению пациентов с коронавирусной инфекцией.
Что такое ДВС-синдром?
Синдром диссеминированного внутрисосудистого свертывания — это универсальное неспецифическое нарушение системы гемостаза (функциональная система организма, позволяющая поддерживать жидкое состояние крови, а также предупреждающая и тормозящая кровотечения; она обеспечивает устойчивость основных физиологических функций). Нарушение характеризуется внутрисосудистым свертыванием крови и образованием в ней множества микросгустков фибрина и скоплений клеток крови: тромбоцитов и эритроцитов. Эти клетки оседают в капиллярах органов, в результате чего в них возникают глубокие микроциркуляторные и дистрофические нарушения.
Согласно Справочнику фельдшера, во время ДВС-синдрома активируются свертывающая и фибринолитическая системы (растворяет тромбы и сгустки крови), после чего наступает их истощение. В тяжелых случаях это приводит к полной несвертываемости крови.
В медицинских источниках этот патологический процесс также называют коагулопатией потребления, тромбогеморрагическим синдромом (ТГС), синдромом рассеянного внутрисосудистого свертывания (РВС), гиперкоагуляционным синдромом.
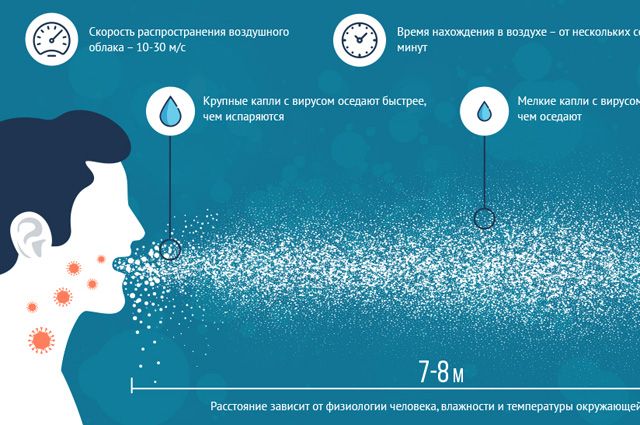
Из-за чего возникает ДВС-синдром?
Медикам известно огромное количество причин, способных вызвать у больного развитие ДВС-синдрома. По данным Справочника фельдшера, его развитие неизбежно или высоковероятно при акушерской патологии (предлежание плаценты, преждевременная отслойка плаценты, закупорка сосудов матки околоплодными водами, внутриутробная смерть плода), сепсисе, деструктивных процессах в печени, почках, при панкреатите.
ДВС-синдром возникает во время шока любого происхождения (геморрагический, травматический, ожоговый, анафилактический и т. д.). При этом степень тяжести синдрома прямо пропорциональна выраженности и продолжительности шокового состояния. Этот синдром также развивается при остром внутрисосудистом гемолизе (разрушение клеток внутри кровеносных сосудов), в том числе при несовместимых переливаниях крови, которые не подходят больному по групповой принадлежности.
Согласно Медицинскому справочнику, ДВС-синдром также могут вызывать оперативные вмешательства, ставшие особо травматичными для больного. Например, операции при злокачественных новообразованиях, на паренхиматозных органах (почки, печень, легкие, селезенка, поджелудочная железа, щитовидная железа), с использованием аппарата искусственного кровообращения (АИК) а также внутрисосудистые вмешательства.
Его вызывают опухоли, особенно гемобластозы, лейкозы, рак легкого, печени, поджелудочной, предстательной железы, почки. ДВС-синдром возникает при иммунных и иммунокомплексных болезнях (в том числе при системной красной волчанке, ревматизме, ревматоидном артрите с висцеральными поражениями и пр.).
ДВС-синдром учащают кровотечения, коллапс, переливания большого объема крови. Этот патологический процесс может возникать на фоне аллергических реакций, отравления змеиными ядами, лечения определенными препаратами.

Как протекает ДВС-синдром и какие у него симптомы?
ДВС-синдром может протекать как в острой форме — при всех видах шока и терминальных состояниях, так и иметь затяжное, волнообразное течение. Его клиническая картина включает симптомы основного заболевания, послужившего его причиной, признаки развившегося шока (при острых формах), глубокие нарушения системы гемостаза, возникновение тромбозов и кровотечений, анемию (снижение в крови красных телец), нарушения функций в органах, нарушения метаболизма.
ДВС-синдром имеет четыре стадии (или фазы) протекания. На первой агрегантные свойства тромбоцитов повышаются, что приводит к распространенному свертыванию крови и образованию множественных тромбов в сосудах различных органов. Из-за образования тромбов в большом количестве расходуются факторы свертывания и наступает переходная стадия, во время которой нарастает коагулопатия (нарушение свертываемости крови) и тромбоцитопения — количество тромбоцитов в периферической крови сильно снижается, в результате чего повышается кровоточивость и замедляется процесс остановки кровотечений из мелких сосудов. Также во время переходной фазы могут происходить сдвиги в свертываемости крови как в сторону гипер-, так и в сторону гипокоагуляции.
Первая фаза — гиперкоагуляции и микротромбозов — может быть кратковременной при остром ДВС-синдроме или протекать скрыто, из-за чего патология может сразу проявиться в виде кровотечений.
На третьей стадии возникает глубокая гипокоагуляция, способность крови к свертыванию может полностью утрачиваться. Последняя стадия — восстановительная. В случае неблагоприятного течения синдрома на последней стадии возникают различные осложнения, которые в большинстве случаев приводят к летальному исходу.

Как лечат ДВС-синдром?
Больные с синдромом диссеминированного внутрисосудистого свертывания проходят лечение в отделениях реанимации либо в палатах интенсивной терапии. Они нуждаются в интенсивном наблюдении и лечении, во время которого специалисты следят за эффективностью дыхания и кровообращения, проводят частые повторные лабораторные исследования.
Терапия ДВС-синдрома комплексная. Во-первых, врачи проводят лечение, направленное на устранение причины синдрома. Например, при сепсисе назначается антибактериальная терапия, при акушерской и гинекологической патологии применяются радикальные меры (экстирпация матки, кесарево сечение и т. д.).
Пациенту назначают противошоковую терапию, а также лечение, направленное на поддержание необходимого объема циркулирующей крови. Для этого показано переливание свежезамороженной плазмы с гепарином, которая содержит все факторы свертывания. Параллельно с медикаментозным лечением, направленным на восстановление системы гемостаза, врачи ведут борьбу с полиорганной недостаточностью. Пациенту может потребоваться поддержка функций легких, почек, желудочно-кишечного тракта, надпочечников и других органов.
Оставить
комментарий (0)
Источник
А
Б
В
Г
Д
Ж
З
И
Й
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Ш
Э
Ю
Я
- Что такое Острый промиелоцитарный лейкоз
- Что провоцирует Острый промиелоцитарный лейкоз
- Патогенез (что происходит?) во время Острого промиелоцитарного лейкоза
- Симптомы Острого промиелоцитарного лейкоза
- Диагностика Острого промиелоцитарного лейкоза
- Лечение Острого промиелоцитарного лейкоза
- К каким докторам следует обращаться если у Вас Острый промиелоцитарный лейкоз
Что такое Острый промиелоцитарный лейкоз
Острый промиелоцитарный лейкоз — ОПЛ (МЗ по FAB-классификации) — довольно редкий вариант острого лейкоза, на его долю приходится не более 10% среди всех острых нелимфобластных лейкозов. Яркая клиническая картина и морфологические особенности заболевания позволили Hillestad еще в 1957 г., задолго до создания FAB-классификации, выделить его в качестве отдельной формы острого лейкоза.
Что провоцирует Острый промиелоцитарный лейкоз
Причиной острого промиелоцитарного лейкоза, является хромосомная транслокация t (15;17) ведущая к соединению гена рецептора ретиноевой кислоты (RAR-aльфа) c геном опухолевого супрессора PML [Rabbits, ea 1994, Sanchez-Garcia, ea 1997, Tenen, ea 1997], продукт которого образует в ядре специфические матрикс-ассоциированные ядерные тельца PML. Цитогенетический анализ выявляет в клетках больных APL транслокации, захватывающие хромосомы 15 и 17. Это специфические транслокации q(15;17) (q22;q11.2) не были вывлены ни в одном другом типе лейкемии миелоцитов или другом злокачественном заболевании. Транслокация (15;17) прерывает RARальфа ген и часть его сливается с локусом PML хромосомы 15, образуя химерный слитый белок PML-RARa. Ген PML кодирует белок, содержащий «цинковые пальцы», и может являться важным транс- действующим транскрипционным фактором в процессе дифференцировки гранулоцитов.
Предполагается, что химерный белок PML/RAR-a инактивирует по доминантно-негативному механизму апоптогенную функцию нормального белка PML, образуя с ним гетеродимеры. Механизмы индукции апоптоза при гиперэкспрессии PML пока не совсем ясны. Экспрессия химерного белка PML/RAR-a, вызывающая инактивацию нормальной функции белка PML, как и перестройка BCR/ABL, ведет одновременно и к изменениям регуляции клеточного цикла, и к частичному блокированию индукции апоптоза (следует заметить, что в отличие от BCR/ABL перестройка PML/RAR-a вызывает также и блок дифференцировки). В результате многонаправленного характера действия гибридных молекул появляются клетки с повышенным пролиферативным потенциалом и одновременно с устойчивостью к негативным регуляторным сигналам и/или неблагоприятным условиям окружающей среды. Предполагается, что такие изменения могут быть уже достаточными для развития по крайней мере некоторых форм гемобластозов. И, действительно, перестройки BCR/ABL или PML/RAR-a часто являются единственными генетическими изменениями, обнаруживаемыми соответственно при хроническом миелоидном и остром промиелоцитарном лейкозах.
Было идентифицировано множество лейкемия-специфических генов, но в результате слияния генов рецептора ретиноидной кислоты (RAR альфа) и гена лейкемии промиелоцитов (PML) возник новый интересный пример таких генов, приводящих к возникновению острой лейкемии миелоцитов (APL).
Три разных химерных гена PML-RARa, длинный (L), средний (M) и короткий (S) являются результатом различного типа сплайсинга экзонов гена PML при сплайсинге транслоцированного гена RARa. Транс-ретиноидная кислота (ATRA) приводит к выздоровлению больных APL, позволяя предполагать, что в процессе транслокации образуется гормон-связывающий белок. Химерный белок PML-RARa, по- видимому, блокирует дифференцировку миелоидных клеток, а обработка ATRA снимает этот эффект.
Гены, вовлеченные в патологический процесс при APM, по-видимому, приводят к структурным изменениям нормального гена (протоонкогена), и его белковый продукт, действуя на клетку-хозяина, вызывает злокачественное перерождение. Этот белок в норме вовлечен в процессы пролиферации и дифференцировки.
Молекулярные и клинические исследования APL больных выявляют, что клетки больных могут начать дифференцировку под воздействием ATRA. Обнаружение транслокации 15;17 дает хороший прогноз. При терапии ATRA перестройка гена RARa существует 2-3 недели, а затем исчезает; после выздоровления восстанавливается нормальная структура гена RARа. Использование ATRA для восстановления созревания клеток и их дифференцировку в гранулоциты приводит к выздоровлению 85-90% пациентов. Это является первым примером лечения рака человека.
В некоторых случаях больных APL, ген RARa может быть вовлечен в другие транслокации и перестройки. Были выявлены два пациента, один с перестройкой 11;17, а другой с транслокацией 15;17, но без перестройки гена PML. На обоих пациентов терапия ATRA не подействовала. Наблюдения о необходимости сайтов перед геном PML для взаимодействия с ATRA повышает необходимость молекулярной диагностики APL перед назначением или продолжением ATRA терапии. Химерный белок PML-RARa клинически удобен для диагностики и наблюдения при лечении APL.
Патогенез (что происходит?) во время Острого промиелоцитарного лейкоза
Симптомы Острого промиелоцитарного лейкоза
Острый промиелоцитарный лейкоз отмечает очень быстрое течение. Ему присущи выраженная интоксикация, кровоточивость и гипофибриногенемия (понижение свертываемости крови), обусловленные ДВС-синдромом (синдром диссеминированного внутрисосудистого свертывания). Лимфатические узлы, печень и селезенка чаще всего не увеличены. В анализе крови: анемия, выраженная тромбоцитопения, в костном мозге, а обычно и в периферической крови выявляется большой процент нетипичных бластов. Ядра этих лейкозных клеток в крови нередко имеют двудольчатую форму, еще чаще их форму бывает трудно различить из-за обилия зернистости в цитоплазме. Непосредственной причиной смерти больного чаще всего бывает кровоизлияние в мозг.
Острый промиелоцитарный лейкоз характеризуется чрезвычайной злокачественностью процесса, быстрым нарастанием тяжелой интоксикации, выраженным геморрагическим синдромом, приводящим к кровоизлиянию в мозг и к гибели больного.
Острый миелобластный лейкоз характеризуется прогрессирующим течением, выраженной интоксикацией и лихорадкой, тяжелой анемией, умеренной интенсивностью геморрагических проявлений (склонностью к кровоточивости), частных язвенно-некротических поражений слизистых и кожи.
Диагностика Острого промиелоцитарного лейкоза
Лечение Острого промиелоцитарного лейкоза
Лечение острого промиелоцитарного лейкоза может осложниться двумя угрожающими жизни состояниями — ДВС-синдромом и ретиноидным синдромом .
ДВС-синдром обусловлен гибелью под действием цитостатиков лейкозных клеток и массивным поступлением из них в кровь прокоагулянтов. Во многих случаях эффективно лечение гепарином. Дефицит факторов свертывания возмещают криопреципитатом и свежезамороженной плазмой.
Третиноин в отличие от цитостатиков способствует дифференцировке лейкозных клеток. Лечение им острого промиелоцитарного лейкоза позволяет избежать кровотечений, но вызывает лейкоцитоз.
Проявления ретиноидного синдрома включают лихорадку, одышку, плевральный выпот и перикардиальный выпот, артериальную гипотонию. И сам лейкоцитоз, и его последствия можно предупредить назначением цитостатиков.
Летальность ДВС-синдрома и ретиноидного синдрома при изолированном назначении цитостатиков и третиноина достигает 15-20%. Одновременное назначение цитостатиков и третиноина снижает летальность, предотвращая развитие обоих синдромов.
К каким докторам следует обращаться если у Вас Острый промиелоцитарный лейкоз
Гематолог
А
Б
В
Г
Д
Ж
З
И
Й
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Ш
Э
Ю
Я
Акции и специальные предложения
Медицинские новости
01.06.2020
Фотовыставка «Видеть главное», посвященная пациентам с псориазом, открылась на портале МБОО «Кожные и аллергические болезни» в виртуальном формате. «Видеть главное» — это 12 портретов, выполненных в технике стерео-варио, которая позволяет увидеть фото со следами псориаза и без них в зависимости от того, под каким углом смотрит посетитель.
23.05.2020
Статистика показывает, что ишемическая болезнь сердца и инсульт уносят больше всего человеческих жизней во всем мире. Коронавирус COVID-19 — серьезное явление, но про здоровье других органов в тоже время забывать не стоит. На здоровье сердца влияет не так много факторов…
Медицинские статьи

Офтальмология является одной из наиболее динамично развивающихся областей медицины. Ежегодно появляются технологии и процедуры, позволяющие получать результат, который еще 5–10 лет назад казался недостижимым. К примеру, в начале XXI века лечение возрастной дальнозоркости было невозможно. Максимум, на что мог рассчитывать пожилой пациент, — это на…
Почти 5% всех злокачественных опухолей составляют саркомы. Они отличаются высокой агрессивностью, быстрым распространением гематогенным путем и склонностью к рецидивам после лечения. Некоторые саркомы развиваются годами, ничем себя не проявляя…
Вирусы не только витают в воздухе, но и могут попадать на поручни, сидения и другие поверхности, при этом сохраняя свою активность. Поэтому в поездках или общественных местах желательно не только исключить общение с окружающими людьми, но и избегать…
Вернуть хорошее зрение и навсегда распрощаться с очками и контактными линзами – мечта многих людей. Сейчас её можно сделать реальностью быстро и безопасно. Новые возможности лазерной коррекции зрения открывает полностью бесконтактная методика Фемто-ЛАСИК.
Источник
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке «Файлы работы» в формате PDF
Распространение острых лейкозов повсеместное, в различных странах среднегодовой показатель данным заболеванием находится в пределах от 1,8 до 4,3 на миллион жителей. У взрослого населения 80% случаев приходится на миелобластный вариант острых лейокозов, у детей до 90% — на острый лимфобластный лейкоз [4].
В конце ХХ века в России для лечения данного заболевания был принят протокол ALL-BFM-90, благодаря чему значительно изменился исход острых лейкозов, которые еще недавно считались абсолютно фатальными заболеваниями, но также предустановленное им лечение ведет к тяжелым последствиям – инфекционно-септическим, органотоксическим осложнениям [3,5,6]. В данный момент ремиссия достигает 93%.
Нельзя забывать таком опасном осложнении острых лейкозов – геморрагическом синдроме(ГС), который отрицательно сказывается на итоге лечения больных и не позволяет проводить лечение в полной мере.
Информация из литературных источников говорит о неполном и не вовремя начинающемся распознавании нарушений системы гемостаза и их корректировка у людей с острым лейкозом во время химиотерапии [1,5]. Возникновение геморрагического синдрома при острых лейкозах — сложный вопрос, так как имеет прямую связь с самим опухолевым процессом, лечением и осложнениями. Учитывая вышеизложенное, необходимо изучать воздействие нарушения системы гемостаза на развитие геморрагического синдрома у пациентов с острым лейкозом.
Геморрагический синдром — это важнейшее проявление острых лейкозов. Он вызван тромбоцитопенией (вытеснение костного мозга), повышением проницаемости стенки сосудов (тяжелая анемия – расстройство питания эндотелия и сосудистой стенки vasa vasorum; тромбоцитопения – расстройство питания сосудов со стороны эндотелия), дефицитом свертывающих факторов ( нарушение синтеза плазменных факторов свертывания крови из-за инфильтрации печени бластами).
Нарушения свертываемости при опухолевых заболеваниях системы крови обусловлены самой неоплазией [6]; механизмы часто обсуждаются в литературе. По мнению одних исследователей, ГС чаще всего бывает вызван развитием амегакариоцитарной тромбоцитопении по причине угнетения нормального кроветворения [7]. Другие авторы причиной ГС считают возможность бластных клеток выделять тканевой фактор и активированные факторы свертывания, а также раковые прокоагулянты, являющиеся прямыми активаторами факторами свертывания II и Х. Также лейкемические клетки, находящиеся в периферической крови, производят множество фибринолитических и антифибринолитических средств, которые приводят к повышенному свертыванию крови, понижение фибринолитической активности и возникновению продуктов фибринолиза [3, 8]. Существенную роль имеет выделение цитокинов и других метаболитов, вызывающих дефект эндотелия сосудов и усиливающих адгезию и агрегацию тромбоцитов [1,3]. Тромботические осложнения у лиц с острыми лейкозами соотносят в первую очередь с тем, что при гиперлейкоцитозе в остром периоде заболевания возникает агрегация лейкоцитов в микрососудистом русле, что приводит к ДВС-синдрому, который усугубляет лейкостаз и развивается полиорганная недостаточность [3].
Начальная стадия острого лейкоза с выраженными геморрагическими явлениями — наблюдается у 10% пациентов, проявляется различными профузным кровотечением (носовым, желудочно-кишечным, церебральным и др.)
В развернутой (второй) стадии острого лейкоза геморрагическому синдрому свойственны кожные геморрагии петехиально-пятнистого характера [8].
Проявления | Причины развития |
Полиморфная, полихромная сыпь (от петехий до экхимозов), локализованная несимметрично, включая слизистые оболочки. | При остром лимфоидном лейкозе вследствие уничтожения опухолевой массой эритроидного ростка. |
Кровотечения (по времени возникновения ранние). | При остром миелоидном лейкозе вследствие первичного поражения эритроидного ростка. |
При парентеральном введении препаратов появляются значительные по размерам кровоизлияния в местах инъекций. В последней стадии на месте данных кровоизлияний в стенке ЖКТ появляются язвенные и некротические изменения. Ярко проявляющийся геморрагический синдром зафиксирован при промиелоцитарном лейкозе.
Частота встречаемости данной формы лейкозов у взрослых — 3,7 % случаев, у детей промиелоцитарный лейкоз отмечается очень редко. Эта форма ярко демонстрирует геморрагический синдром, который зачастую является одним из первых симптомов промиелоцитарного лейкоза. У больных промиелоцитарным лейкозом появляются кровоизлияния на местах травм, эпистаксис, маточные кровотечения, кровоизлияния в жизненно важные органы. В развитии геморрагий немаловажную роль играют сами лейкозные клетки, которые содержат большое количество тромбопластина на своей поверхности и в цитоплазматических гранулах. При разрушении лейкозных клеток потенцируется развитие синдрома дессименированного внутрисосудистого свертывания крови из-за высвобождения фактора свёртывания крови III и лизосомальных протеаз вне клетки.
Геморрагический синдром зачастую отсутствует при остром лимфобластном лейкозе.
В 15-20% случаев геморрагический синдром является основным фактором, приводящим к гибели пациентов из-за массивных кровотечений и кровоизлияний, так самая частая причина гибели пациентов с острым лейкозом — апоплексический удар, легочное кровотечение. Это связано с несколькими обстоятельствами. Первое, что ведет к данным последствиям — при острых лейкозах в различных органах и тканях, в том числе в сосудистой стенке, появляются очаги экстрамедуллярного кроветворения. Это говорит о том, что в стенке кровеносного сосуда появляется кроветворная ткань, из-за чего стенка сосуда становится хрупкой, что является базой для геморрагий. Второе, у пациентов появляется тромбоцитопения, данное явление при условии повреждения сосудистой стенки является основанием для длительного кровотечения [7].
Система гемостаза у пациентов с острым лейкозом страдает еще до начала лечения и ее состояние ухудшается на фоне терапии по программе, нарушения имеют разнонаправленный характер.
В первой стадии болезни и после лечения они вызваны активацией внутрисосудистого свертывания крови с умеренной и высокой тромбинемией.
Типы кровоточивости при остром лейкозе — микроциркуляторный и смешанный.
В начале заболевания геморрагический синдром вызван тромбоцитопенией, а в ходе проведения химиотерапии и использованием факторов свертывания крови и становлением синдрома дессименированного внутрисосудистого свертывания [2].
Тяжелая аплазия кроветворения, вызванная лейкозным процессом, является причиной развития бактериальных инфекций в первично-активной фазе заболевания [9]. Поскольку инфекции и тромбогеморрагические осложнения, в том числе зависящие от самого лейкозного процесса, могут повысить летальность, актуальными остаются вопросы дальнейшего изучения патогенеза острых лейкозов и разработки методов ранней диагностики осложнений.
Список литературы:
1) Алексеев Н.А., Воронцов И.М. // Лекозы у детей — Л.: Медицина. — 1988. — С. 248.
2) Рощик A.C., Колесникова О.И., Волоскова Н.И. Роль нарушений системы гемостаза у детей с острым лимфобластным лейкозом. II Проблемы патологии системы гемостаза, Барнаул, 2007, с. 187-190.
3) Румянцева Ю.В., Карачунский А.И. // Оптимизация терапии острого лимфобластного лейкоза у детей в России и Белоруссии: стратегия Москва — Берлин. Вопросы гематологии/онкологии и иммунопатологии в педиатрии. — 2007. — Т.6, №4. — С. 13.
4) Третяк Н.М. Гематологія / Н.М. Третяк – К.: Зовнішня торгівля, 2005. – 240 с.
5) Экспериментальные модели в патологии: учебник/ В.А. Черешнев, Ю.И. Шилов, М.В. Черешнева, Е.И. Самоделкин, Т.В. Гаврилова, Е.Ю. Гусев, И.Л. Гуляева. – Пермь: Перм. гос. ун-т., 2011. – 267 с.
6) Холмогорова О.П., Гуляева И.Л., Асташина Н.Б. Стоматологический статус пациентов с хроническим лейкозом // Международный студенческий научный вестник. – 2017. — № 4-9. – С. 1304-1307.
7) Breiteeld P.P. // Acutae lymphoblastic leukemia. Blood Disease of infancy and Childhood/ed D.R.Miller. — Baltimore. — 1990. — P. 175.
8) Lukens J.N. // Acute lymphoblastic leukemia. Wintrobe´s Clinical Hematology/Eds G.R.Lee et al. — London. — 1993. — P.1892.
9) [Электронный ресурс] Патология крови и кроветворения URL: https://www.4astniydom.ru/8/patologiya-krovi-i-krovetvoreniya/leikozy (дата обращения: 26.05.2017)
Источник
