Острая гипоксия код по мкб 10
Тактика лечения: восстановление мозговых функций, после перенесенной гипоксии активно происходит в первые 3-6 месяцев, затем дефект стабилизируется. Лечение исходов гипоксической энцефалопатии — симптоматическое. В связи с этим важны ранние комплексные реабилитационные мероприятия, включающие нейропсихологический тренинг, ЛФК, санаторно-курортное лечение.
Цели лечения:
1. Восстановление утраченных мозговых функций.
2. Обеспечить больному социальную адаптацию.
3. Определить вариант терапии и обеспечить ее подбор в зависимости от неврологического дефекта.
4. Осуществить коррекцию двигательных, когнитивных, речевых нарушений.
Немедикаментозное лечение:
1. Психотерапия, нейропсихологический тренинг.
2. Соблюдение режима дня: избегать стрессовых ситуаций, умственные перегрузки, длительные занятия на персональном компьютере.
3. Массаж воротниковой зоны.
4. ЛФК — групповые и индивидуальные занятия.
5. Физиолечение — электросон, дарсонвализация волосистой части головы, кислородный коктейль.
6. Фитотерапия — экстракт валерианы, пустырника, пассифлоры, хмеля, мелиссы, мяты.
Медикаментозное лечение
В первые часы после остановки кровообращения:
1. Борьба с отеком мозга (осмотические диуретики, кортикостероиды, ИВЛ в режиме гипервентиляции).
2. Предупреждение повторных эпилептических припадков (карбамазепин, вальпроевая кислота, фенитоин и другие антиэпилептические средства).
3. Поддержание водно-электролитного, кислотно-щелочного баланса, нормогликемии.
4. Предупреждение и лечение осложнений (мочевой инфекции, аспирационной пневмонии и т.д.).
5. Целесообразно применение препаратов, снижающих энергетические потребности мозга: диазепам 0,5% раствор, тиопентал.
6. Кортикостероиды, обладающие мембраностабилизирующим действием — метилпреднизолон.
7. Антиоксиданты: витамин Е, 30% раствор, капсулы.
8. Антигипоксанты: актовегин.
9. Низкомолекулярные декстраны: реополиглюкин.
10. Препараты, активирующие метаболические процессы в мозге: ноотропные средства (пирацетам, пиритинол, глиатилин, церебролизин, гинкго-билоба и другие).
Лечение исходов гипоксической энцефалопатии — синдромальное.
С целью улучшения обменных процессов в головном мозгу широко используются стимуляторы нейрометаболизма. Ноотропы — это вещества, оказывающие специфическое влияние на высшие интегративные функции мозга, улучшающие память, облегчающие процесс обучения, стимулирующие интеллектуальную деятельность, повышающие устойчивость мозга к повреждающим факторам, улучшающие кортикально-субкортикальные связи.
Ноотропные препараты способны улучшать когнитивные (познавтельные) функции, согласно современным представлениям к ноотропным препаратам относятся:
— пирацетам (ноотропил, луцетам, фезам);
— церебролизин;
— производные пиридоксина: пиритинол (энцефабол, пиридитол);
— препараты нейроаминокислот: производные гамма-аминомасляной кислоты (фенибут), гопантеновой кислоты (пантогам), глицин, глутаминовая кислота;
— препараты гинкго-билоба (танакан);
— холиномиметик центрального действия: холин альфосцерат (глиатилин), 1-3 г/сут. в/в капельно или внутримышечно в течение 10-30 сут., в дальнейшем внутрь по 400 мг 3 раза в день, в течение 60-90 дней;
— антигипоксанты — актовегин обладает выраженным антигипоксическим действием;
— антиоксиданты — аскорбиновая кислота, витамин Е, мексидол;
При эпилепсии назначают антиэпилептические препараты:
1. Клоназепам 0,01-0,03 мг/кг/сут. с повышением дозы до 0,1-0,2 мг/кг/сут. в 2-3 приема.
2. Карбамазепин 10-15 мг/кг/сут.
3. Ламотриджин с 0,5 мг/кг до 1-1,5 мг/кг, медленное титрование в течение месяца.
4. Топамакс, капсулы 15 мг и 25 мг.
При спастических парезах показано назначение миорелаксантов:
1. Баклофен 30-60 мг/сут.
2. Толпиризон гидрохлорид (мидокалм), детям в возрасте от 3 мес. до 6 лет в суточной дозе из расчета 5-10 мг/кг в 2-3 приема; в возрасте 7-14 лет — в суточной дозе 2-4 мг/кг.
3. Тизанидин гидрохлорид, (сирдалуд), миорелаксант центрального действия.
Для лечения депрессивного состояния в последние годы широко используют антидепрессанты — селективные ингибиторы обратного захвата серотонина, которые лучше переносятся больными и не требуют длительного титрования дозы. Эффективность антидепрессантов повышается при их комбинации с нейролептиками.
— флуоксетин 20 мг 3-6 месяцев;
— флувокасамин (феварин) 50 мг/сут.
Общеукрепляющая терапия: витамины группы В, фолиевая кислота, препараты магния.
Седативная терапия: персен, ноофен, грандаксин, ново-пассит.
Профилактические мероприятия:
— соблюдение режима дня — достаточный сон, отдых;
— профилактика инфекций;
— соблюдение режима дня — избегать умственной, эмоциональной и физической перегрузки, длительных занятий на персональном компьютере, просмотр телевизионных программ.
Дальнейшее ведение:
— диспансерный учет у невропатолога по месту жительства;
— социальная адаптация ребенка;
— регулярные занятия ЛФК.
Основные медикаменты:
1. Актовегин, ампулы 2 мл по 80 мг
2. Винпоцетин, таблетки 5 мг
3. Глицин, таблетки 0,1
4. Гопантеновая кислота (пантокальцин), таблетки 0,25
5. Магния лактат+пиридоксина гидрохлорид — магне В6
6. Ново-пассит, таблетки покрытые оболочкой, раствор для внутреннего применения
7. Ноофен, таблетки 0,25
8. Пиридоксин гидрохлорид — ампулы 1 мл 5%, витамин В6
9. Тиамин бромид, ампулы 1 мл 5%
10. Тиамин бромид, ампулы 1 мл 5%
11. Фолиевая кислота, таблетки 0,001
12. Цианкобаламин, ампулы 1 мл 200 и 500 мкг
13. Циннаризин (стугерон), таблетки 25 мг
Дополнительные медикаменты:
1. Аевит в капсулах
2. Амитриптиллин, таблетки 25 мг
3. Баклофен, таблетки 10 мг и 25 мг
4. Винкамин (оксибрал), капсулы 30 мг
5. Галоперидол, таблетки 1,5 мг, 5мг, 10 мг и 20 мг
6. Грандаксин 50 мг
7. Диазепам, ампулы по 2 мл 5%
8. Имипрамин (мелипрамин) 25 мг
9. Инстенон, ампулы 2 мл
10. Инстенон, таблетки
11. Клоназепам, таблетки 2 мг
12. Клоразепат (транксен), капсулы 0,01 и 0,005
13. Ницерголин (сермион), таблетки 5 мг
14. Пирацетам, таблетки 0,2, 0,4
14. Танакан, таблетки 40 мг
15. Тизанидин гидрохлорид (сирдалуд), таблетки 2 и 4 мг
16. Тиоридазин (сонапакс), таблетки 10 и 25 мг
17. Толпиризон гидрохлорид (мидокалм), таблетки 50 мг
18. Топамакс, таблетки 25 мг, капсулы 15 мг и 25 мг
19. Флувоксамин малеат (феварин), таблетки 100 мг
20. Флуоксетин гидрохлорид, капсулы 20 мг
21. Хлорпротиксен 15, таблетки
22. Холин альфосцерат (глиатилин), ампулы 1000 мг, капсулы 400 мг
23. Эктракт валерианы, таблетки 20 мг
Индикаторы эффективности лечения:
— восстановление или улучшение двигательных функций;
— улучшение речевых функций;
— повышение эмоционального и психического тонуса;
— купирование приступов судорог.
Источник
Рубрика МКБ-10: P91.6
МКБ-10 / P00-P96 КЛАСС XVI Отдельные состояния, возникающие в перинатальном периоде / P90-P96 Другие нарушения, возникающие в перинатальном периоде / P91 Другие нарушения церебрального статуса у новорожденного
Определение и общие сведения[править]
Гипоксически-ишемическая энцефалопатия
Синонимы: перинатальное гипоксическое поражение мозга, постасфиктическое поражение головного мозга.
Гипоксически-ишемическая энцефалопатия — синдром, характеризуемый наличием признаков острого повреждения головного мозга в результате недостаточного кровоснабжения головного мозга ребенка во время беременности матери, родов или в течение первого месяца его жизни.
Гипоксически-ишемическая энцефалопатия является наиболее распространенным поражением среди всей перинатальной патологии нервной системы.
Этиология и патогенез[править]
Основными причинами перинатальной гипоксии-ишемии являются:
• внутриутробная гипоксия (нарушения маточно-плацентарного и/или фетоплацентарного кровотока);
• интра- и постнатальная асфиксия, РДС (Респираторный дистресс — синдром), повторяющиеся приступы апноэ, врожденная пневмония или аспирационный синдром;
• ВПС (врожденные пороки сердца), гемодинамически значимый ОАП (открытый артериальный проток), персистирование фетальных коммуникаций;
• постнатальные нарушения системной гемодинамики, приводящие к резкому падению системного АД и снижению церебральной перфузии.
Патогенез
Развивающийся мозг является гетерогенным образованием по степени зрелости (морфологической и функциональной) его тканевых и сосудистых компонентов. Особенности архитектоники и морфологии церебральных сосудов новорожденных лежат в основе специфических механизмов, обеспечивающих регуляцию интенсивности мозгового кровотока на региональном уровне в ответ на асфиксию.
В настоящее время показано, что у недоношенных новорожденных (при сроке гестации менее 35 нед) гипоксемия приводит к повышению кровотока в стволе головного мозга и перивентрикулярных областях белого вещества. У доношенных новорожденных при поддержании системного АД на нормальном уровне гипоксемия вызывает усиление кровотока во всех областях мозга, но более всего в области ствола, глубоких отделов больших полушарий и базальных ганглиев как структур, обеспечивающих жизненно важные функции и рефлекторно-двигательные реакции. Дефицит кровоснабжения мозга приводит к ишемическому поражению зон пограничного или коллатерального кровоснабжения бассейнов мозговых артерий, имеющих различное расположение в зависимости от гестационного возраста.
Последствия острой ишемии и степень ее повреждающего воздействия определяются тяжестью и длительностью снижения мозгового кровотока. При снижении уровня кровотока на 20-30% нормативных показателей возникает первая реакция в виде торможения белкового синтеза. Дальнейшее снижение кровотока до 50% нормальной величины сопровождается активацией анаэробного гликолиза, увеличением в плазме крови лактата, развитием лактат-ацидоза и тяжелыми нарушениями энергетического обмена. Если недостаточность мозгового кровотока носит транзиторный характер и/или восстановление его компенсируется за счет коллатерального кровообращения, наступает «постишемическая реперфузия».
В этих условиях поступление обогащенной кислородом крови в участки, перенесшие ранее ишемическое воздействие, приводит к активации процессов свободнорадикального окисления, сопровождающегося накоплением токсичных продуктов и возбуждающих аминокислот (глутамат, N-метил-D-аспарагиновая кислота и др.). В итоге каскада патологических процессов, инициированных тканевой гипоксией-ишемией в очагах повреждения под действием цитокинов и ИЛ, развивается воспалительная реакция нейроглии, что обусловливает дальнейшее повреждение паренхимы мозга, длительность которого может варьировать от нескольких часов до нескольких недель.
Клинические проявления[править]
Церебральная гипоксия — ишемия I степени (легкая)
Возбуждение ЦНС чаще возникает у доношенных новорожденных, угнетение — у недоношенных длительностью не более 5-7 сут.
Церебральная ишемия II степени (средней тяжести)
Возникают угнетение ЦНС, возбуждение или смена фаз церебральной активности (длительностью более 7 дней); неонатальные судороги редки. У недоношенных судороги чаще тонические или атипичные (судорожное апноэ, стереотипные спонтанные оральные автоматизмы, трепетание век, миоклонии глазных яблок, гребущие, плавающие движения рук, педалирующие движения ног). У доношенных — мультифокальные клонические судороги. Приступы обычно кратковременные, однократные, реже повторные. Внутричерепная гипертензия (транзиторная, чаще у доношенных новорожденных). Вегетативно-висцеральные нарушения.
Церебральная ишемия III степени (тяжелая)
Прогрессирующая потеря церебральной активности — свыше 10 дней (в первые 12 ч жизни глубокое угнетение или кома, в период с 12-24 ч кратковременное нарастание уровня бодрствования, с 24-72 ч — нарастание угнетения или кома). Повторные судороги (чаще мультифокальные клонические или тонические), возможен эпилептический статус. Дисфункция стволовых отделов мозга (нарушения ритма сердца и дыхания, зрачковых реакций, сосания и глотания, глазодвигательные расстройства). Поза разгибательная (декортикация или децеребрация). Вегетативновисцеральные нарушения. Прогрессирующая внутричерепная гипертензия (отек мозга).
Гипоксически-ишемическая энцефалопатия новорожденного: Диагностика[править]
Диагноз церебральной гипоксии-ишемии и степень ее тяжести устанавливаются на основании данных анамнеза о наличии внутриутробной гипоксии плода или интра-/постнатальной асфиксии у новорожденного, оценки по шкале Апгар, клинических неврологических симптомов и дополнительных методов исследования, включающих НСГ, КТ, ДГ, ЭЭГ. Также учитывают динамическое определение КОС, гематокрита, гемоглобина и газового состава крови. Широко используются результаты суточного мониторинга за такими показателями, как ЧСС, АД, температура тела, SO2, исследование лабораторных показателей в сыворотке (креатинина и билирубина) и плазме (глюкозы, калия, кальция, магния, натрия, остаточного азота) крови. При необходимости (по показаниям) проводится исследование цереброспинальной жидкости. При возможности контролируют содержание нейроспецифических белков, таких как нейроспецифическая енолаза, глиальный фибриллярный кислый белок, основной белок миелина и др.
Дифференциальный диагноз[править]
Гипоксически-ишемическая энцефалопатия новорожденного: Лечение[править]
Лечение и профилактика см. Другие внутричерепные (нетравматические) кровоизлияния у плода и новорожденного
Профилактика[править]
Прочее[править]
Источники (ссылки)[править]
Неонатология. Национальное руководство. Краткое издание [Электронный ресурс] / Под ред. Н.Н. Володина — М. : ГЭОТАР-Медиа, 2013. — https://www.rosmedlib.ru/book/ISBN9785970424438.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
Связанные заболевания и их лечение
Описания заболеваний
Стандарты мед. помощи
Содержание
- Описание
- Дополнительные факты
- Причины
- Классификация
- Симптомы
- Возможные осложнения
- Диагностика
- Лечение
- Прогноз
- Профилактика
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Дыхательная недостаточность.

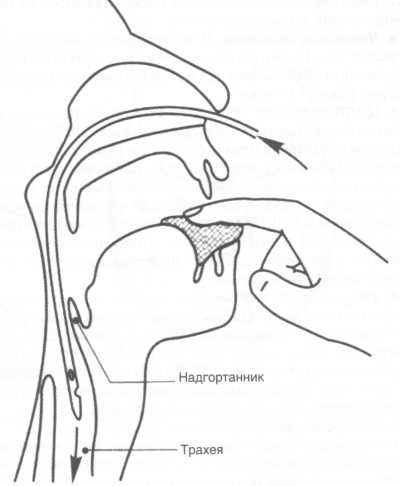
Первая помощь при острой дыхательной недостаточности
Описание
Дыхательная недостаточность. Патологический синдром, сопровождающий ряд заболеваний, в основе которого лежит нарушение газообмена в легких. При дыхательной недостаточности (ДН) не обеспечивается необходимый газовый состав крови, либо он поддерживается за счет перенапряжения компенсаторных возможностей системы внешнего дыхания. Дыхательная недостаточность может развиваться при различных острых и хронических воспалительных заболеваниях, повреждениях, опухолевых поражениях органов дыхания; при патологии со стороны дыхательной мускулатуры и сердца; при состояниях, приводящих к ограничению подвижности грудной клетки. Основу клинической картины дыхательной недостаточности составляют признаки гипоксемии и гиперкапнии, синдром утомления дыхательной мускулатуры и одышка.
Дополнительные факты
Дыхательная недостаточность. Патологический синдром, сопровождающий ряд заболеваний, в основе которого лежит нарушение газообмена в легких. При дыхательной недостаточности (ДН) не обеспечивается необходимый газовый состав крови, либо он поддерживается за счет перенапряжения компенсаторных возможностей системы внешнего дыхания.
Внешнее дыхание поддерживает непрерывный газообмен в организме: поступление атмосферного кислорода и удаление углекислого газа. Любое нарушение функции внешнего дыхания приводит к нарушению газообмена между альвеолярным воздухом в легких и газовым составом крови. В результате этих нарушений в крови нарастает содержание углекислоты и уменьшается содержание кислорода, что ведет к кислородному голоданию, в первую очередь, жизненноважных органов – сердца и головного мозга.
Угрожающее для организма состояние развивается при дыхательной недостаточности, характеризующейся снижением парциального давления кислорода в артериальной крови менее 60 мм , а также повышением парциального давления углекислоты более 45 мм.
Причины
К нарушению легочной вентиляции и развитию дыхательной недостаточности могут приводить различные острые и хронические заболевания бронхолегочной системы (бронхоэктатическая болезнь, пневмония, ателектаз, кавернозные полости, дессиминированные процессы в легком, абсцессы и тд ), поражения ЦНС, анемия, гипертензия в малом круге кровообращения, сосудистая патология легких и сердца, опухоли легких и средостения и тд.
Дыхательная недостаточность классифицируется по ряду признаков: 1. По патогенезу (механизму возникновения):
• паренхиматозная (гипоксемическая, дыхательная или легочная недостаточность I типа).
Для дыхательной недостаточности по паренхиматозному типу характерно понижение содержания и парциального давления кислорода в артериальной крови (гипоксемия), трудно корригируемое кислородной терапией. Наиболее частыми причинами данного типа дыхательной недостаточности служат пневмонии, респираторный дистресс-синдром (шоковое легкое), кардиогенный отек легких.
• вентиляционная («насосная», гиперкапническая или дыхательная недостаточность II типа).
Ведущим проявлением дыхательной недостаточности по вентиляционному типу служит повышение содержания и парциального давления углекислоты в артериальной крови (гиперкапния). В крови также присутствует гипоксемия, однако она хорошо поддается кислородотерапии. Развитие вентиляционной дыхательной недостаточности наблюдается при слабости дыхательной мускулатуры, механических дефектах мышечного и реберного каркаса грудной клетки, нарушении регуляторных функций дыхательного центра. 2. По этиологии (причинам):
• обструктивная.
Дыхательная недостаточность по обструктивному типу наблюдается при затруднении прохождения воздуха по воздухоносным путям – трахее и бронхам вследствие бронхоспазма, воспаления бронхов (бронхита), попадания инородных тел, стриктуры (сужения) трахеи и бронхов, сдавления бронхов и трахеи опухолью При этом страдают функциональные возможности аппарата внешнего дыхания: затрудняется полный вдох и особенно выдох, ограничивается частота дыхания.
• рестриктивная (или ограничительная).
Дыхательная недостаточность по рестриктивному (ограничительному) типу характеризуется ограничением способности легочной ткани к расширению и спаданию и встречается при экссудативном плеврите, пневмотораксе, пневмосклерозе, спаечном процессе в плевральной полости, ограниченной подвижности реберного каркаса, кифосколиозе Дыхательная недостаточность при этих состояниях развивается из-за ограничения максимально возможной глубины вдоха.
• комбинированная (смешанная).
Дыхательная недостаточность по комбинированному (смешанному) типу сочетает признаки обструктивного и рестриктивного типов с преобладанием одного из них и развивается при длительном течении сердечно-легочных заболеваний.
• гемодинамическая.
Причиной развития гемодинамической дыхательной недостаточности могут служить циркуляторные расстройства (например, тромбоэмболия), ведущие к невозможности вентиляции блокируемого участка легкого. К развитию дыхательной недостаточности по гемодинамическому типу также приводит право-левое шунтирование крови через открытое овальное окно при пороке сердца. При этом происходит смешение венозной и оксигенированной артериальной крови.
• диффузная.
Дыхательная недостаточность по диффузному типу развивается при нарушении проникновения газов через капиллярно-альвеолярную мембрану легких при ее патологическом утолщении. 3. По скорости нарастания признаков:
• острая.
Острая дыхательная недостаточность развивается стремительно, за несколько часов или минут, как правило, сопровождается гемодинамическими нарушениями и представляет опасность для жизни пациентов (требуется экстренное проведение реанимационных мероприятий и интенсивной терапии). Развитие острой дыхательной недостаточности может наблюдаться у пациентов, страдающих хронической формой ДН при ее обострении или декомпенсации.
• хроническая.
Развитие хронической дыхательной недостаточности может происходить на протяжении нескольких месяцев и лет, нередко исподволь, с постепенным нарастанием симптомов, также может быть следствием неполного восстановления после острой ДН. 4. По показателям газового состава крови:
• компенсированная (газовый состав крови нормальный);
• декомпенсированная (наличие гипоксемии или гиперкапнии артериальной крови). 5. По степени выраженности симптомов дыхательной недостаточности:
• ДН I степени – характеризуется одышкой при умеренных или значительных нагрузках;
• ДН II степени – одышка наблюдается при незначительных нагрузках, отмечается задействованность компенсаторных механизмов в покое;
Классификация
• ДН III степени – проявляется одышкой и цианозом в покое, гипоксемией.
Симптомы
Признаки ДН зависят от причин ее возникновения, типа и тяжести. Классическими признаками дыхательной недостаточности служат:
• проявления гипоксемии;
• проявления гиперкапнии;
• синдром слабости и утомления дыхательной мускулатуры;
• одышка.
Гипоксемия клинически проявляется цианозом (синюшностью), степень которого выражает тяжесть дыхательной недостаточности и наблюдается при снижении парциального давления кислорода (РаО2) в артериальной крови ниже 60 мм Для гипоксемии характерны также нарушения гемодинамики, выражающиеся в тахикардии и умеренной артериальной гипотонии. При понижении РаО2 в артериальной крови до 55 мм наблюдаются нарушения памяти на происходящие события, а при снижении РаО2 до 30 мм пациент теряет сознание. Хроническая гипоксемия проявляется легочной гипертензией.
Проявлениями гиперкапнии служат тахикардия, нарушения сна (бессонница ночью и сонливость днем), тошнота, головные боли. Быстрое нарастание в артериальной крови парциального давления углекислоты (РаСО2) может привести к состоянию гиперкапнической комы, связанной с усилением мозгового кровотока, повышением внутричерепного давления и развитием отека головного мозга. Синдром слабости и утомления дыхательных мышц характеризуется увеличением частоты дыхания (ЧД) и активным вовлечением в процесс дыхания вспомогательной мускулатуры (мышц верхних дыхательных путей, мышц шеи, брюшных мышц). ЧД более 25 в мин. Может служить начальным признаком утомления дыхательной мускулатуры. Урежение ЧД менее 12 в мин. Может предвещать остановку дыхания. Крайним вариантом синдрома слабости и утомления дыхательной мускулатуры служит парадоксальное дыхание. Одышка субъективно ощущается пациентами как нехватка воздуха при чрезмерных дыхательных усилиях. Одышка при дыхательной недостаточности может наблюдаться как при физическом напряжении, так и в спокойном состоянии.
Возможные осложнения
Дыхательная недостаточность является неотложным, угрожающим для здоровья и жизни состоянием. При неоказании своевременного реанимационного пособия острая дыхательная недостаточность может привести к гибели пациента. Длительное течение и прогрессирование хронической дыхательной недостаточности приводит к развитию правожелудочковой сердечной недостаточности в результате дефицита снабжения сердечной мышцы кислородом и ее постоянных перегрузок.
Альвеолярная гипоксия и неадекватная вентиляция легких при дыхательной недостаточности вызывает развитие легочной гипертензии. Гипертрофия правого желудочка и дальнейшее снижение его сократительной функции ведут к развитию легочного сердца, проявляющегося в застое кровообращения в сосудах большого круга.
Диагностика
На начальном диагностическом этапе тщательно собирается анамнез жизни и сопутствующих заболеваний с целью выявления возможных причин развития дыхательной недостаточности. При осмотре пациента обращается внимание на наличие цианоза кожных покровов, подсчитывается частота дыхательных движений, оценивается задействованность в дыхании вспомогательных групп мышц.
В дальнейшем проводятся функциональные пробы для исследования функции внешнего дыхания (спирометрия, пикфлоуметрия), позволяющая провести оценку вентиляционной способности легких. При этом измеряется жизненная емкость легких, минутный объем дыхания, скорость движения воздуха по различным отделам дыхательных путей при форсированном дыхании.
Обязательным диагностическим тестом при диагностике дыхательной недостаточности является лабораторный анализ газового состава крови, позволяющий определить степень насыщения артериальной крови кислородом и углекислым газом (PаО2 и PаСО2) и кислотно-щелочное состояние (КОС крови).
При проведении рентгенографии легких выявляются поражения грудной клетки и паренхимы легких, сосудов, бронхов.
Лечение
Лечение пациентов с дыхательной недостаточностью предусматривает:
• восстановление и поддержание оптимальной для жизнеобеспечения вентиляции легких и оксигенации крови;
• лечение заболеваний, явившихся первопричиной развития дыхательной недостаточности (пневмонии, экссудативного плеврита, пневмоторакса, хронических воспалительных процессов в бронхах и легочной ткани ).
При выраженных признаках гипоксии в первую очередь проводится оксигенотерапия (кислородная терапия). Кислородные ингаляции подаются в концентрациях, обеспечивающих поддержание PаО2 = 55— 60 мм , при тщательном мониторинге рН и PаСО2 крови, состояния пациента. При самостоятельном дыхании пациента кислород подается масочно или через носовой катетер, при коматозном состоянии проводится интубация и поддерживающая искусственная вентиляция легких.
Наряду с оксигнотерапией проводятся мероприятия, направленные на улучшение дренажной функции бронхов: назначаются антибактериальные препараты, бронхолитики, муколитики, массаж грудной клетки, ультразвуковые ингаляции, лечебная физкультура, проводится активная аспирация секрета бронхов через эндобронхоскоп.
При дыхательной недостаточности, осложненной легочным сердцем, назначаются диуретики. Дальнейшее лечение дыхательной недостаточности направлено на устранение вызвавших ее причин.
Прогноз
Дыхательная недостаточность является грозным осложнением многих заболеваний и нередко приводит к летальному исходу. При хронических обструктивных заболеваниях легких дыхательная недостаточность развивается у 30% пациентов.
Прогностически неблагоприятно проявление дыхательной недостаточности у пациентов с прогрессирующими нейромышечными заболеваниями (БАС, миотония и тд ). Без соответствующей терапии летальный исход может наступить в течение одного года.
При всех прочих патологиях, приводящих к развитию дыхательной недостаточности, прогноз разный, однако невозможно отрицать, что ДН является фактором, сокращающим продолжительность жизни пациентов.
Профилактика
Предупреждение развития дыхательной недостаточности предусматривает исключение патогенетических и этиологических факторов риска.
Основные медуслуги по стандартам лечения | ||
Клиники для лечения с лучшими ценами
|
Источник
