Острая анемия код по мкб 10
Связанные заболевания и их лечение
Описания заболеваний
Стандарты мед. помощи
Содержание
- Описание
- Дополнительные факты
- Причины
- Патогенез
- Симптомы
- Диагностика
- Лечение
- Прогноз
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Постгеморрагическая анемия.

Постгеморрагическая анемия
Описание
Постгеморрагическая анемия. Комплекс клинических и гематологических изменений, возникающий вследствие острой или хронической кровопотери. Постгеморрагическая анемия характеризуется бледностью, одышкой, потемнением в глазах, головокружением, гипотермией, артериальной гипотонией. В тяжелых случаях — заторможенностью, нитевидным пульсом, шоком, потерей сознания. Постгеморрагическую анемию диагностируют по данным клинической картины и общего анализа крови; для установления источника кровотечения проводятся инструментальные исследования. При развитии данного состояния необходимо устранение источника кровопотери, проведение трансфузионной и симптоматической терапии.
Дополнительные факты
Постгеморрагическая анемия – гипогемоглобинемия, развивающаяся вследствие геморрагического синдрома и сопровождающаяся ощутимым снижением объема циркулирующей крови (ОЦК). Постгеморрагическая анемия протекает с эритропенией, но часто без уменьшения концентрации гемоглобина (Hb). В норме уровень общего Hb и объем циркулирующих эритроцитов крови составляет соответственно: у мужчин – не ниже 130 г/л и 29-30 мл/кг веса, у женщин – не ниже 120 г/л и 22-23 мл/кг. Постгеморрагическая анемия может осложнять течение самых различных патологический состояний в хирургии, гематологии, гинекологии, гастроэнтерологии, кардиологии и тд Постгеморрагическая анемия может носить острый или хронический характер. Хроническая форма является вариантом железодефицитной анемии, так как механизм развития и симптомы патологии обусловлены усиливающимся дефицитом железа.
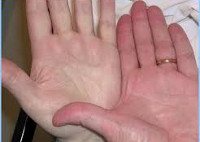
Постгеморрагическая анемия
Причины
Непосредственной причиной постгеморрагической анемии выступает острая или хроническая потеря крови, возникшая вследствие наружного или внутреннего кровотечения. Острая постгеморрагическая анемия возникает при быстрых, массивных кровопотерях, вызванных обычно механическим повреждением стенок крупных кровеносных сосудов или полостей сердца при различных травмах и хирургических операциях, разрывом стенок сердечных камер в зоне инфаркта, разрывом аневризмы аорты и ветвей легочной артерии, разрывом селезенки, разрывом фаллопиевой трубы при внематочной беременности.
Острая постгеморрагическая анемия характерна для обильных маточных кровотечений (менорагий, метрорагий), может сопровождать течение язвы желудка и 12-перстной кишки. У новорожденных постгеморрагическая анемия может быть вызвана плацентарным кровотечением, родовой травмой.
Хроническая постгеморрагическая анемия обусловлена продолжительными, часто возникающими потерями небольших объемов крови при желудочно-кишечных, геморроидальных, почечных, носовых кровотечениях, нарушениях механизмов свертывания крови (ДВС-синдроме, гемофилии). Опухолевые процессы (рак желудка, рак толстой кишки), протекающие с разрушением тканей и органов, проводят к развитию внутреннего кровотечения и постгеморрагической анемии. Гипогемоглобинемия может быть связана с повышением проницаемости стенок капилляров при лейкозах, лучевой болезни, инфекционно-септических процессах, недостаточности витамина C.
Патогенез
Основными факторами развития постгеморрагической анемии выступают явления сосудистой недостаточности, гиповолемия с уменьшением общего объема плазмы и циркулирующих форменных элементов, в частности, эритроцитов, осуществляющих транспорт кислорода. Этот процесс сопровождается снижением артериального давления, кровенаполнения внутренних органов и тканей, гипоксемией, гипоксией и ишемией, развитием шока.
Степень выраженности защитно-приспособительных реакций организма определяется объемом, скоростью и источником кровотечения. В раннюю рефлекторно-сосудистую фазу компенсации кровопотери (первые сутки) благодаря возбуждению симпатико-адреналовой системы наблюдается вазоконстрикция и усиление сопротивления периферических сосудов, стабилизация гемодинамики за счет централизации кровообращения с первоочередным кровоснабжением головного мозга и сердца, уменьшение возврата крови к сердцу и сердечного выброса. Концентрация эритроцитов, Hb и гематокрит пока близки к норме («скрытая» анемия).
Вторая гидремическая фаза компенсации (2-3 сутки) сопровождается аутогемодилюцией — поступлением в кровеносное русло тканевой жидкости и восполнением объема плазмы. Усиление секреции катехоламинов и альдостерона надпочечниками, вазопрессина – гипоталамусом способствует стабильности уровня электролитов в плазме крови. Происходит прогрессирующее снижение показателей эритроцитов и Hb (общего и в единице объема), гематокрита; значение цветового показателя в норме (постгеморрагическая нормохромная анемия).
В третью, костномозговую фазу компенсации (4-5 сутки) из-за недостатка железа анемия становится гипохромной, усиливается образование эритропоэтина почками с активацией ретикулоэндотелиальной системы, эритропоэза костного мозга, очагов экстрамедуллярного кроветворения. В красном костном мозге наблюдается гиперплазия эритроидного ростка и увеличение общего числа нормоцитов, в периферической крови — значительное повышение количества молодых форм эритроцитов (ретикулоцитов) и лейкоцитов. Уровни Hb, эритроцитов и гематокрит понижены. Нормализация уровня эритроцитов и Hb при отсутствии дальнейшей кровопотери происходит через 2-3 недели. При массивной или длительной кровопотере постгеморрагическая анемия приобретает гипорегенеративный характер, при истощении адаптационных систем организма развивается шок.
Симптомы
Клинические признаки постгеморрагической анемии однотипны вне зависимости от причины кровопотери, определяются ее объемом и длительностью.
В первые сутки после острой кровопотери у пациентов отмечается резкая слабость, бледный оттенок кожи и слизистых, одышка, потемнение и мелькание мушек в глазах, головокружение, шум в ушах, пересыхание во рту, снижение температуры тела (особенно, конечностей), холодный пот. Пульс становится частым и слабым, появляется артериальная гипотония. Следствием геморрагического синдрома является малокровие внутренних органов, жировая дистрофия миокарда, печени, ЦНС и других органов. Дети, особенно новорожденные и 1-го года жизни, кровопотерю переносят намного тяжелее, чем взрослые пациенты.
Постгеморрагическая анемия при массивной и быстрой кровопотере сопровождается геморрагическим коллапсом, резким падением артериального давления, нитевидным аритмичным пульсом, адинамией и заторможенностью, учащенным поверхностным дыханием с возможным развитием рвоты, судорог, потерей сознания. Если давление падает до критического уровня, вызывая острое нарушение кровоснабжения и гипоксию органов и систем, смерть наступает от паралича дыхательного центра и остановки сердца.
Кровянистые выделения из влагалища. Низкая температура тела. Одышка. Патологические выделения. Рвота. Ретикулоцитоз. Судороги. Шум в ушах.
Диагностика
Диагностика постгеморрагической анемии проводится по данным клинической картины, лабораторных и инструментальных исследований (общего и биохимического анализов крови и мочи, ЭКГ, УЗ-диагностики, пункции костного мозга, трепанобиопсии). При осмотре пациента с острой постгеморрагической анемией обращает внимание гипотония, частое дыхание, слабый аритмичный пульс, тахикардия, приглушенность сердечных тонов, небольшой систолический шум на верхушке сердца.
В крови — абсолютное снижение эритроцитарной массы; при продолжающейся кровопотере наблюдается прогрессирующее равномерное падение содержания Hb и эритроцитов. При умеренной кровопотере гематологические признаки постгеморрагической анемии обнаруживается только на 2-4 сутки. Обязателен контроль диуреза, уровня тромбоцитов, электролитов и азотистых продуктов в крови, АД и ОЦК.
При острой постгеморрагической анемии нет необходимости в исследовании костного мозга, его проводят при трудно диагностируемых кровопотерях. В образцах костномозговой пункции признаками анемии являются повышение активности красного костного мозга, в препаратах трепанобиопсии – замещение жировой ткани костного мозга красным кроветворным мозгом.
При диагностике внутренних кровотечений показателен синдром острого малокровия и лабораторные данные. В селезенке, печени, лимфоузлах выявляются очаги экстрамедуллярного кроветворения, указывающие на повышенную нагрузку на гемопоэтическую систему. В крови — транзиторное понижение уровня железа, небольшое увеличение АлТ.
Для выявления и устранения источника кровопотери больные нуждаются в консультациях гематолога, хирурга, гинеколога, гастроэнтеролога и других специалистов; проведении УЗИ органов брюшной полости и малого таза, ФГДС и пр. ЭКГ при постгеморрагической анемии может демонстрировать снижение амплитуды Т-зубца в стандартном и грудном отведении.
Лечение
Первостепенным в лечении постгеморрагической анемии является установление источника кровотечения и его немедленная ликвидация за счет перевязки и ушивания сосудов, резекции и ушивания поврежденных органов и тканей, повышения свертываемости крови.
Для восстановления ОЦК и снижения степени гемодинамических нарушений по наблюдением трансфузиолога проводится неотложное переливание консервированной крови, кровезаменителей, плазмы и плазмозаменителей. При незначительном, но продолжительном кровотечении трансфузия цельной крови или плазмы показана в небольших гемостатических дозах. При значительной потере ОЦК трансфузии должны выполняться в дозах, превышающих кровопотерю на 20-30%. Тяжелая постгеморрагическая анемия лечится переливаниями больших доз крови («трансплантация крови»). В период коллапса гемотрансфузии дополняют гипертоническими кровозамещающими растворами.
После восстановления ОЦК проводится коррекция качественного состава крови – восполнение ее компонентов: эритроцитов, лейкоцитов, тромбоцитов. При большой одномоментной кровопотере и остановившемся кровотечении необходимы массивные дозы эритроцитарной массы ( 500 мл). Об эффективности гемотрансфузий судят по повышению АД, гематологическим сдвигам.
Также необходимо введение белковых и электролитных растворов (альбумина, физ. Раствора, глюкозы), восстанавливающих водно-солевой баланс. В лечении постгеморрагической анемии используются препараты железа, витамины группы B. Назначается симптоматическая терапия, направленная на нормализацию функциональных нарушений со стороны сердечно-сосудистой и дыхательной систем, печени, почек и тд.
Прогноз
Прогноз постгеморрагической анемии зависит от длительности и объема кровотечения. Резкая потеря 1/4 ОЦК приводит к острой анемии и состоянию гиповолемического шока, а потеря 1/2 ОЦК является несовместимой с жизнью. Постгеморрагическая анемия при медленной потере даже значительных объемов крови не столь опасна, поскольку может компенсироваться.
Основные медуслуги по стандартам лечения | ||
Клиники для лечения с лучшими ценами
|
Источник
Рубрика МКБ-10: D62
МКБ-10 / D50-D89 КЛАСС III Болезни крови, кроветворных органов и отдельные нарушения, вовлекающие иммунный механизм / D60-D64 Апластические и другие анемии
Определение и общие сведения[править]
Этиология и патогенез[править]
Острая постгеморрагическая анемия (ОПГА) — нормохромная нормоцитарная гиперрегенераторная анемия, возникающая вследствие острой кровопотери в течение короткого периода времени. Тяжесть клинической картины определяется количеством потерянной крови, скоростью и источником кровотечения. Клиническая симптоматика может проявиться при потере примерно 1/8 объема циркулирующей крови (для взрослых — 500-700 мл).
Потеря крови может быть видимой (кровотечение из ран, кровавая рвота, носовые, легочные и маточные кровотечения). Первоначально скрытая потеря крови наблюдается при желудочно-кишечных кровотечениях, не всегда сопровождающихся кровавой рвотой или меленой, а также при кровотечениях в полость живота (чаще всего внематочная беременность) или в плевральную полость, больших гематомах в околопочечной клетчатке или гематомах другой локализации, расслаивающейся аневризме аорты.
Патологоанатомически после большого кровотечения красный костный мозг в плоских костях находится в состоянии повышенной активности, а жировой костный мозг в трубчатых костях замещается красным, т. е. кроветворным, костным мозгом. При повторных кровотечениях может возникнуть и экстрамедуллярное кроветворение в селезенке, печени, лимфатических узлах и других органах.
Клинические проявления[править]
Головокружение, обморочное состояние, тошнота, иногда рвота (при пищеводно-желудочных кровотечениях — с алой кровью или цвета кофейной гущи), бледность кожных покровов, сухость и обложенность языка, жажда, заостренные черты лица, холодный пот, акроцианоз. Пульс малый, частый (при больших кро-
вопотерях нитевидный), гипотония. Переход пациента в вертикальное положение вызывает усиление головокружения, потемнение в глазах, нередко потерю сознания. Изменения в периферической крови носят стадийный характер и зависят от времени, прошедшего после начала кровотечения
Острая постгеморрагическая анемия: Диагностика[править]
В течение первых суток от начала кровотечения нормоцитемическая гиповолемия вызвана эквивалентным уменьшением общего содержания форменных элементов и плазмы крови. В этот период о тяжести кровопотери следует судить не по уровню гемоглобина и содержанию эритроцитов, а по снижению объема циркулирующей крови, которое ориентировочно можно оценить по шоковому индексу.
Шоковый индекс = частота пульса/АД систол.
При значительных кровопотерях этот индекс превышает 1, а при массивных — 1,5.
На 2-3-и сутки тромбоцитопения связана с гемодилюцией и потреблением кровяных пластинок в процессе тромбообразования, а лейкопения — с потерей лейкоцитов во время кровотечения и последующей гемодилюции. На более поздних сроках гипохромия эритроцитов обусловлена отставанием скорости синтеза гемоглобина от темпа пролиферации эритроидных клеток. Увеличение числа молодых клеток эритроидного ряда (ретикулоциты, полихроматофильные и оксифильные эритробласты) является показателем высокой регенераторной способности костного мозга. Иногда может наблюдаться преходящий тромбоцитоз.
Даже при однократной острой кровопотере отмечается кратковременное снижение уровня железа в плазме. При достаточных его запасах в депо уровень железа в плазме быстро восстанавливается, а при истощенных депо — развивается картина ЖДА.
Дифференциальный диагноз[править]
Острая постгеморрагическая анемия: Лечение[править]
Первоначальные мероприятия направлены на остановку кровотечения: механические способы — наложение жгута, давящих повязок, прижатие кровоточащих сосудов, тампонада носа и т.д. Используют препараты, способствующие локальной остановке кровотечения: наложение на место кровотечения гемостатической губки или фибринной пленки с тромбином или без него, биоклея, орошение места кровотечения 5% раствором аминокапроновой кислоты. При кровотечениях, связанных с патологией печени и передозировкой антикоагулянтов непрямого действия, внутримышечно вводят 1,0% раствор викасола по 1,5-3 мл.
Восполнение потери крови следует начинать со струйного внутривенного введения кристаллоидных растворов: 0,9% раствора натрия хлорида, раствора Рингера, 5% раствора глюкозы, лактосола и др. На догоспитальном этапе при резко выраженном падении артериального давления в эти растворы однократно можно ввести 1-2 мл 0,2% раствора норадреналина. Объем вводимых кристаллоидов должен значительно превышать объем кровопотери. Для поддержания гемодинамики внутривенно капельно вводят 5% раствор альбумина (100 мл и более) или коллоидные кровезаменители осмотического действия от 400 до 1000 мл и более в зависимости от тяжести состояния. При снижении диуреза и признаках нарушения микроциркуляции следует ввести 400-800 мл реополиглюкина внутривенно капельно. Оптимальное соотношение объемов кристаллоидных и коллоидных растворов — 2:1 или 3:1. Коллоидные растворы частично могут заменяться трансфузиями донорской плазмы.
Больных ОПГА направляют в стационары соответствующего профиля — хирургические, травматологические, акушерско-гинекологические и др.
После купирования кровотечений и стабилизации гемодинамики проводят лечение ЖДА препаратами железа: при глубокой анемизации (гемоглобин менее 40 г/л) их вводят внутривенно, при более легкой анемизации предпочтительнее пероральный прием. В первые 3-4 дня можно комбинировать внутривенные или внутримышечные введения препаратов железа с последующим назначением их внутрь. К трансфузиям донорских эритроцитов прибегают лишь при тяжелой анемизации и прекращают их при достижении уровня гемоглобина выше 60-70 г/л. Витамин В12, ФК и другие стимуляторы кроветворения при ОПГА не показаны.
Профилактика[править]
Прочее[править]
Источники (ссылки)[править]
«Анемии [Электронный ресурс] : руководство / Дементьева И.И., Чарная М.А., Морозов Ю.А. — М. : ГЭОТАР-Медиа, 2013. — (Серия «Библиотека врача-специалиста»).» — https://www.rosmedlib.ru/book/ISBN9785970423608.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
Утратил силу — Архив

РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Архив — Клинические протоколы МЗ РК — 2007 (Приказ №764)
Категории МКБ:
Анемия, связанная с питанием, неуточненная (D53.9)
Общая информация
Краткое описание
Железодефицитная анемия (ЖДА) — патологическое состояние, характеризующееся снижением концентрации гемоглобина из-за дефицита железа в организме в результате нарушения его поступления, усвоения или патологических потерь.
Клинические признаки характеризуются сидеропеническим синдромом: эпителиальные нарушения (трофические нарушения кожи, ногтей, волос, слизистых оболочек), извращение вкуса и обоняния, астено-вегетативные нарушения, нарушение процессов кишечного всасывания, дисфагия и диспептические изменения, снижение иммунитета.
Согласно рекомендациям ВОЗ, нижней границей нормы гемоглобина у детей в возрасте до 6 лет следует считать 110 г/л, Ht=33; у детей 6-12 лет — 115 г/л, Ht=34; 12-13 лет — 120 г/л, Ht=36.
Код протокола: PN-P-001 «Железодефицитная анемия у детей»
Профиль: педиатрический
Этап: ПМСП (медицинский пункт)
Код (коды) по МКБ-10:
D53 Другие анемии, связанные с питанием
D50 Железодефицитная анемия
Мобильное приложение «MedElement»
— Профессиональные медицинские справочники. Стандарты лечения
— Коммуникация с пациентами: вопросы, отзывы, запись на прием
Скачать приложение для ANDROID
Мобильное приложение «MedElement»
— Профессиональные медицинские справочники
— Коммуникация с пациентами: вопросы, отзывы, запись на прием
Скачать приложение для ANDROID
Классификация
По этиологии:
1. ЖДА при недостаточном исходном уровне железа (анемия недоношенных, близнецов).
2. Нутритивная (или алиментарная) ЖДА.
3. ЖДА инфекционного или инфекционно-алиментарного генеза.
4. ЖДА при резорбционной недостаточности железа (синдром мальабсорбции и др.).
5. Хроническая постгеморрагическая ЖДА.
По степени тяжести: легкая, средней тяжести, тяжелая.
По патогенезу: острая постгеморрагическая, хроническая.
Факторы и группы риска
1. Анемия беременных.
2. Недоношенность.
3. Нерациональное питание.
4. Заболевания ЖКТ.
5. Глистная инвазия.
6. Кровотечение.
7. Низкий социум.
Диагностика
Диагностические критерии: у детей младше 5 лет жизни ЖДА определяется при концентрации гемоглобина крови менее чем 110 г/л или уровне гематокрита менее 33%.
Перечень основных диагностических мероприятий:
1. Общий анализ крови (6 параметров).
2. Определение гемоглобина.
3. Определение ретикулоцитов.
Перечень дополнительных диагностических мероприятий:
1. ЭКГ.
2. Определение общей железосвязывающей способности.
3. Консультация гастроэнтеролога.
Лечение
Тактика лечения
До достижения 6-месячного возраста рекомендуется исключительно грудное вскармливание.
Детям с ЖДА, находящимся на грудном вскармливании, рекомендуется начало приема железа в 6-месячном возрасте.
Большинству детей, получающих искусственное вскармливание, рекомендуется использование смеси для питания, обогащенной железом, до начала приема ребенком жесткой еды (до 12-месячного возраста). Необходимо проводить обучение и консультации родителей по рациональному питанию для профилактики ЖДА.
Для лечения
недоношенных детей, находящихся на раннем искусственном и смешанном вскармливании с ферментопатиями и нарушениями кишечного всасывания, рекомендуется назначение декстрана железа III (25-100 мг/0,5 мл-2 мл) с 4-месячного возраста 1 раз в сутки с индивидуальным подбором курса.
Доношенные дети должны быть проверены на ЖДА (определение уровня НЬ и Ht) в 6-месячном возрасте, а недоношенные младенцы — не позднее чем в З-месячном возрасте.
Дети с установленной ЖДА должны получать препараты железа – железа соли**, однокомпонентные и комбинации препараты, оральные растворы, содержащие более 20 мг/мл соли железа с аскорбиновой кислотой по 1 табл. или 1-2 драже 3 раза в день, фолиевой кислотой** по 1 табл. 3 раза в день.
Препараты железа назначаются из расчета 3 мг/кг веса в сутки до нормализации гемоглобина, ребилитационная терапия — 1-2 мг/кг веса, не менее 2-3 месяцев. При резистентности к пероральному железу, а также при острых постгеморрагических анемиях с целью быстрого и эффективного восстановления уровня железа рекомендуется назначение декстрана железа III (100 мг/2 мл), 1 раз в сутки с индивидуальным подбором курса.
Питание, обогащенное железом (смесь). Для подтверждения эффективности назначенной терапии у всех детей младшего возраста с ЖДА через 4 недели после начала лечения ЖДА должны быть повторно определены НЬ и Ht. Если отмечается положительный результат на назначенное лечение (увеличение гемоглобина выше или равное 10 г/л, а увеличение Ht на 3% или более) или эти показатели определяются в пределах нормы, то лечение должно продолжаться еще 2 месяца и после этого назначение железа должно быть остановлено. В случае же отсутствия положительного результата на проводимое лечение или при увеличении гемоглобина менее 10 г/л, а увеличении Ht менее чем на 3%, врач должен определить другие возможные причины анемии путем последующего направления больного к гематологу.
Дети младшего возраста с
умеренной или тяжелой ЖДА (НЬ ниже 90 г/л или Ht менее 27%) должны быть проконсультированы гематологом, т.е. рекомендуется внутримышечное введение декстрана железа III (100 мг/2 мл).
Дети 6-12 лет, имеющие факторы риска на ЖДА (плохие условия жизни или питания), требуют повторного скрининга.
Девочки подросткового возраста должны быть обследованы на наличие ЖДА, по крайней мере, один раз между 15 и 25 годами. При присутствии факторов риска (плохое питание, большие менструальные потери крови, донорство и др.) или наличии в анамнезе диагноза ЖДА требуется более частый скрининг (каждый год).
Если ЖДА заподозрена на основании анализа периферической крови, взятой из пальца, то наличие ЖДА желательно подтвердить анализом крови, взятой из вены. Для девочек-подростков анемия определяется на уровне гемоглобина ниже 120 г/л, Ht- ниже 36%.
При концентрации гемоглобина ниже вышеуказанной границы более чем на 20 г/л, подростки должны получать терапевтическую дозу элементарного железа — 60 мг два раза в день (общая доза 120 мг железа), кроме того, необходимо обучение правильному питанию.
Врач должен проверить эффективность назначенной терапии через 1 месяц. Если результат незначительный или его вообще нет (увеличение гемоглобина менее 10 г/л; или увеличение Ht менее 3 единиц), клиницист должен определить другие возможные причины анемии путем последующего направления больной к гематологу.
При наличии воспалительного или инфекционного процессов, низкая концентрация гемоглобина или объем гематокрита может свидетельствовать о развитии ЖДА вследствие нарушения распределения железа в организме и требует дополнительного лечения. При получении положительного результата на назначение препарата железа, терапия должна продолжаться до достижения концентрации гемоглобина 120 г/л, после чего доза железа может быть снижена до 120 мг в неделю, и продолжаться в течение 6 месяцев.
Тяжелая ЖДА обычно нетипична для девочек подросткового возраста и дефицит железа редко является причиной такой анемии. Подробная информация о развитии болезни, включая характер питания, более глубокое обследование и дополнительные u1083 лабораторные анализы (общий анализ крови, сывороточное железо, содержание трансферрина, концентрация ферритина, количество ретикулоцитов, общий белок, общий билирубин и его фракции) показаны для окончательного подтверждения ЖДА.
У девочек подросткового возраста применение сбалансированного питания для профилактики ЖДА может остановить развитие ЖДА и предотвратить назначение препаратов железа. Поэтому необходимо уделять особое внимание, потреблению мяса и продуктов, богатых аскорбиновой кислотой (для увеличения всасывания железа из продуктов питания), исключить потребление чая и кофе во время приема пищи. У девочек подросткового возраста с высоким риском множественной микроэлементной недостаточности, назначить мультивитаминно — минеральные препараты, содержащие около 30 мг железа в таблетке.
После окончания курса лечения рекомендуется прием препарат элементарного железа с профилактической целью один раз неделю в течение 6 месяцев:
— возраст 6-12 мес. — доза препарата элементарного железа — сироп 30 мг или 3 мг/кг;
— возраст 12-18 мес. — доза препарата элементарного железа — 60 мг.
Перечень основных медикаментов:
— **железа соли, однокомпонентные препараты и комбинированные препараты, содержащие более 20 мг/мл соли железа
— **аскорбиновая кислота 50 мг, 100 мг, 500 мг табл.; 50 мг драже
— фолиевая кислота 1 мг табл.
— декстран железа III (100 мг/2 мл) для внутримышечного введения, амп.
Перечень дополнительных медикаментов: препараты элементарного железа 30-60 мг табл.
Показания для госпитализации: отсутствие нормализации клинико-лабораторных показателей через 2 недели.
Индикаторы эффективности лечения: нормализация показателей Hb и общего состояния ребенка, увеличение Hb на 10 г/л или более при лечении препаратами железа через 4 недели.
* – препараты, входящие в список основных (жизненно важных) лекарственных средств
** — входит в перечень видов заболеваний, при амбулаторном лечении которых лекарственные средства отпускаются по рецептам бесплатно и на льготных условиях
Информация
Источники и литература
- Протоколы диагностики и лечения заболеваний МЗ РК (Приказ №764 от 28.12.2007)
- Список использованной литературы:
1. Клиническое руководство по скринингу, профилактике и лечению
железодефицитной
анемии. Ташкент 2004, 68 с.
2. PRODIGY Guidance — Anaemia — iron deficiency Clinical Practice Guidelines, 2005
3. Screening for Iron Deficiency. Anemia—Including Iron Prophylaxis. Clinical guidelines
4. Iron Deficiency Anaemia. Assessment, Prevention and Control. A guide for programme
managers.
- Список использованной литературы:
Информация
Список разработчиков: Джаксон Н.Л., Республиканский Медицинский Колледж
Прикреплённые файлы
Внимание!
Если вы не являетесь медицинским специалистом:
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Источник
