Неврологические синдромы при болезни паркинсона

 Паркинсонизм – один из наиболее распространенных синдромов в клинической неврологии, который чрезвычайно полиэтиологичен. Классическая триада симптомов паркинсонизма включает: а) брадикинезию (это облигатный признак, без которого не может быть выставлен диагноз паркинсонизма); экстрапирамидную мышечную ригидность; в) тремор покоя. Два последних проявления при некоторых вариантах паркинсонизма могут отсутствовать. В зависимости от конкретной нозологической формы, к указанным проявлениям добавляется ряд других – постуральная неустойчивость при болезни Паркинсона, более сложный по формуле тремор конечностей при некоторых генетических вариантах паркинсонизма и т.д.
Паркинсонизм – один из наиболее распространенных синдромов в клинической неврологии, который чрезвычайно полиэтиологичен. Классическая триада симптомов паркинсонизма включает: а) брадикинезию (это облигатный признак, без которого не может быть выставлен диагноз паркинсонизма); экстрапирамидную мышечную ригидность; в) тремор покоя. Два последних проявления при некоторых вариантах паркинсонизма могут отсутствовать. В зависимости от конкретной нозологической формы, к указанным проявлениям добавляется ряд других – постуральная неустойчивость при болезни Паркинсона, более сложный по формуле тремор конечностей при некоторых генетических вариантах паркинсонизма и т.д.
Согласно современным представлениям, синдром паркинсонизма может быть подразделен на следующие категории:
- Первичный (идиопатический) паркинсонизм. К нему относятся болезнь Паркинсона и особая генетически обусловленная форма раннего паркинсонизма – так называемый ювенильный паркинсонизм.
- Вторичный паркинсонизм. Данный синдром развивается в качестве одного из клинических проявлений (осложнений) ряда самостоятельных заболеваний и поражений ЦНС. Наиболее известными вариантами вторичного паркинсонизма являются сосудистый, токсический (в т.ч. лекарственный), посттравматический, постинфекционный.
- Паркинсонизм при мультисистемных нейродегенеративных заболеваниях (так называемый паркинсонизм «плюс»). Среди заболеваний, закономерно проявляющихся синдромами паркинсонизм «плюс», следует в первую очередь назвать прогрессирующий надъядерный паралич, множественную системную атрофию, деменцию с тельцами Леви, кортико-базальную дегенерацию.
- Паркинсонизм при наследственных заболеваниях ЦНС. Это весьма обширная группа самых разных по генезу заболеваний, которая включает гепатолентикулярную дегенерацию (болезнь Вильсона–Коновалова), нейроферритинопатию (болезнь Галлервордена–Шпатца), дофа-чувствительную дистонию, ригидную форму болезни Гентингтона, ряд форм липидозов, митохондриальных энцефалопатий и т.д.
На практике около 75% всех случаев паркинсонизма приходятся на первичный (идиопатический) паркинсонизм и, в первую очередь, на наиболее изученную и социально значимую разновидность первичного паркинсонизма – болезнь Паркинсона.
Болезнь Паркинсона представляет собой второе по частоте нейродегенеративное заболевание человека (после болезни Альцгеймера), общая распространенность болезни Паркинсона в популяциях мира составляет примерно 200 случаев на 100 000 населения. Согласно имеющимся данным, в 2007 году в мире насчитывалось свыше 6 млн. человек с болезнью Паркинсона. Заболевание встречается чаще всего у лиц пожилого возраста: так, у лиц старше 60 лет оно отмечается примерно в 1% случаев, а у лиц после 75 лет – уже в 2–3% случаев и более. В то же время, примерно каждый десятый пациент заболевает болезнью Паркинсона до 50 лет, а каждый двадцатый – до 40 лет. В связи с этим выделяют отдельную подгруппу – болезнь Паркинсона с ранним началом, отличающуюся рядом особенностей механизмов развития болезни, клинической картиной и течением, а также реакцией на противопаркинсонические препараты и прогнозом.
В большинстве случаев заболевание имеет спорадический характер, и только у 5–10% лиц развитие болезни Паркинсона обусловлено мутациями ряда генов, имеющих отношение к функционированию митохондрий, антиоксидантной защите клетки и процессингу нейрональных белков. Достижения молекулярной биологии позволили идентифицировать сложный патобиохимический каскад болезни Паркинсона, в центре которого лежит нарушение конформации клеточного белка альфа-синуклеина – основного компонента телец Леви (тельца Леви, представляющие собой крупные эозинофильные включения в цитоплазме дегенерирующих нейронов, считаются патогномоничным морфологическим признаком болезни Паркинсона).
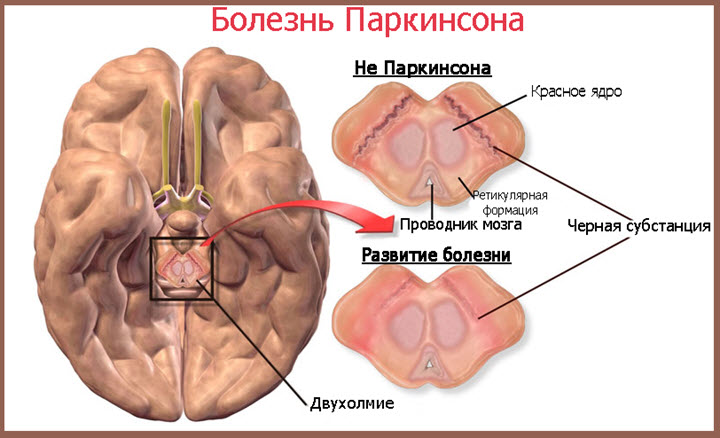
Основные симптомы болезни Паркинсона (брадикинезия, мышечная ригидность, тремор покоя, постуральные нарушения) являются результатом гибели крупных дофамин-продуцирующих нейронов в компактной части черной субстанции среднего мозга, нарушения нигростриарных и других связей и недостаточности дофаминергической трансмиссии в различных отделах головного мозга, в первую очередь – в базальных ганглиях. Благодаря механизмам нейропластичности симптоматика появляется лишь в случае гибели более половины клеток черной субстанции, что соответствует снижению уровня дофамина в полосатом теле на 80-85%. В норме в результате процессов естественного старения организма, начиная с 5-го десятилетия жизни гибнет от 4,7 до 6% клеток черной субстанции в каждое десятилетие, что и определяет возраст-зависимый характер болезни Паркинсона.
Следует отметить, что в последние годы представления об «ограниченности» морфологического субстрата болезни Паркинсона, затрагивающего в основном дофамин-продуцирующие нейроны черной субстанции, претерпели существенные изменения. Последние данные свидетельствуют о наличии патологических синуклеин-позитивных включений в обонятельных луковицах, клетках каудальных отделов ствола мозга, ядрах шва и ретикулярной формации уже в ранней стадии болезни. Более того, даже в продромальном периоде четкие нейродегенеративные изменения «паркинсонического» типа выявляются в периферических вегетативных нейронах (например, в клетках мезентериального сплетения), что позволяет по-новому взглянуть на этиологию заболевания и, в частности, переосмыслить значимость алиментарно-токсических факторов в ее происхождении. Таким образом, существование длительной, многолетней стадии «предболезни» у пациентов с идиопатическим паркинсонизмом в настоящее время не вызывает сомнений.
Установлено, что нейродегенеративный процесс при болезни Паркинсона имеет нелинейный характер: основная и наиболее «драматическая» гибель нейронов происходит за несколько лет до манифестации клинических симптомов или в первые 2–3 года болезни. Это делает чрезвычайно актуальным поиск биомаркеров, которые позволили бы достоверно верифицировать развивающуюся патологию в ее скрытой (латентной) стадии. Именно максимально ранняя диагностика является залогом успеха превентивной нейропротективной терапии, подходы к которой интенсивно разрабатываются в ведущих лабораториях мира. При болезни Паркинсона в качестве биомаркеров изучаются разнообразные биохимические, электрофизиологические, радиологические признаки, однако специфичность и чувствительность большинства применяемых тестов пока недостаточна, а ряд исследовательских технологий (таких как ПЭТ) в силу их сложности и высокой стоимости остаются практически недоступными для реального применения на практике. Большой интерес в последние годы вызывают новые технологии нейровизуализации, такие как транскраниальнаясонография (выявление гиперэхогенности черной субстанции) или специальные режимы МРТ-исследования (морфометрия, трактография и др.), которые не только расширяют дифференциально-диагностический арсенал паркинсонологов, но и позволяют получить новые важные данные о стадийности и механизмах развития паркинсонизма. Большое значение в ранней диагностике болезни Паркинсона имеют немоторные проявления – вегетативные, чувствительные, диссомнические, когнитивные и аффективные. Они развиваются за 3–15 лет (а некоторые даже ранее) до появления классических двигательных расстройств, а по мере течения болезни именно немоторные проявления могут быть главным фактором, определяющим качество жизни.
В настоящее время существует 6 основных групп противопаркинсонических средств:
- препараты леводопы;
- агонисты дофаминовых рецепторов;
- ингибиторы катехол-орто-метилтрансферазы (КОМТ);
- ингибиторы моноаминоксидазы Б (МАО-Б);
- амантадины;
- центральные холинолитики.
Препаратами первого ряда при болезни Паркинсона остаются разнообразные формы леводопы и агонисты дофаминовых рецепторов. Современная концепция лечения болезни Паркинсона предполагает использование методов, обеспечивающих постоянство дофаминергической стимуляции, что может достигаться с помощью пролонгированных форм соответствующих препаратов, ингибирования ферментов метаболизма леводопы, применения специальных помп-систем (дуоденальных, подкожных) и трансдермальных пластырей. Препараты из других групп находят свое применение в основном в лечении наиболее ранних стадий болезни (ингибиторы МАО-Б) либо, напротив, в развернутой стадии патологического процесса для коррекции нарушений, возникающих на фоне длительного лечения пациентов леводопой.
Значительный прогресс наблюдается в разработке хирургических методов лечения болезни Паркинсона. Два используемых в настоящее время нейрохирургических подхода – стереотаксическая деструкция определенных групп подкорковых ядер либо хроническая высокочастотная электростимуляция глубоких структур мозга с использованием имплантированных электродов – относятся к методам функциональной нейрохирургии и имеют целью прерывание патологически функционирующих паллидо-таламо-кортикальных нейрональных «контуров». Использование данных операций во многих случаях сопровождается уменьшением выраженности тремора и других моторных проявлений болезни Паркинсона, в том числе леводопа-индуцированных дискинезий и двигательных флюктуаций, что позволяет сочетать нейрохирургический подход с традиционной фармакотерапией болезни. Глубокая электростимуляция имеет несомненные преимущества перед деструктивными операциями, поскольку она может проводиться с двух сторон (в то время как 2-сторонняя деструкция вентролатерального ядра таламуса и других типичных мишеней чревата развитием псевдобульбарного синдрома), характеризуется меньшим числом осложнений и более отчетливым эффектом в отношении всех основных клинических проявлений паркинсонизма. В мире опыт глубокой электростимуляции мозга при болезни Паркинсона насчитывает уже более 20 лет и показывает стойкость достигаемого клинического улучшения, поддержание достойного качества жизни оперированных больных, возможность снижения дозы леводопы и ряд других существенных преимуществ.
Новые технологии лечения болезни Паркинсона развиваются благодаря достижениям фундаментальныхнейронаук. Так, постепенно все шире внедряются экспериментальные технологии генной и клеточной терапии с использованием рекомбинантных вирусных векторов и нанолипосомальных систем доставки. Однако, при наличии отчетливого симптоматического эффекта нейрохирургических вмешательств, важнейшей и пока нерешенной проблемой остается оценка нейропротективного потенциала данных операций. Важнейшим «прорывом» последних лет стало интенсивное изучение противопаркинсонических соединений недофаминового ряда, воздействующих на аденозиновые, серотониновые, опиатные, каннабиноидыне рецепторы, что может позволить добиться лучшего контроля за многообразными симптомами болезни Паркинсона, особенно в ее развернутых стадиях.
Полезная информация
- Питание при болезни Паркинсона…
- Школа для пациентов с болезнью Паркинсона…
Источник
Тремор конечностей, замедленность движений и другие признаки синдрома паркинсонизма могут быть вызваны целым рядом заболеваний. В связи с улучшением результатов лечения различных заболеваний, продолжительность жизни населения растёт, частота развития данного синдрома увеличивается. Это состояние характерно для старших возрастных групп населения, в основном для мужчин.
Понятие синдром паркинсонизма включает в себя симптомокомплекс, характеризующийся:
- тремором;
- неспособностью удерживать равновесие;
- повышением тонуса мышц;
- появлением неконтролируемого сопротивления мышечной ткани в ответ на попытку изменить положение тела;
- замедленностью движений;
- неспособностью начать движение, адекватное по скорости и силе и др.
Причины возникновения
Синдром паркинсонизма является следствием следующих заболеваний:
- перенесенные в прошлом геморрагические или ишемические инсульты в базальных отделах головного мозга;
- повторные многочисленные черепно-мозговые травмы;
- указание на заболевание энцефалитом в прошлом;
- лекарственные интоксикации нейролептиками, препаратами лития;
- нейросифилис;
- рассеянный склероз, сирингомиелия, боковой амиотрофический склероз, деменция;
- атаксия-телеангиэктазия;
- глиома третьего желудочка;
- на фоне гепатоцеребральной недостаточности, патологии щитовидной железы;
- атрофия мозжечка с сообщающейся гидроцефалией, повышением внутричерепного давления (ВЧД);
- острый энцефалит Экономо.
Синдром паркинсонизма классифицируется по причинам возникновения:
- Первичный идиопатический – болезнь Паркинсона.
- Генетический дефект, проявляющийся в молодом возрасте, – ювенильный паркинсонизм.
- Вторичный – синдром Паркинсона, развившийся как осложнение, последствие других заболеваний и травм центральной нервной системы (ЦНС).
- Паркинсонизм-плюс – состояние, когда симптомы паркинсонизма имеются наряду с другими разнообразными синдромами тяжелых заболеваний ЦНС, например, эссенциальный тремор.
Клиническая картина
Болезнь Паркинсона, ювенильный паркинсонизм, синдром Паркинсона и паркинсонизм-плюс характеризуются общими симптомами и отличительными чертами.
Общие симптомы
Общие симптомы включают в себя следующие нарушения:
- двигательные;
- вегетативные;
- сенсорные;
- психические;
- патология сна и бодрствования.
Двигательные симптомы
Нарушения движения представлены отсутствием активных движений, тремором в покое, скованностью и напряжением в мышцах.
- Тремор, или дрожание, пальцев рук встречается при большом количестве заболеваний. В каждой ситуации он характеризуется своими особенностями:
- Тремор, который возникает в покое, чаще встречается при паркинсонизме. Ослабевает при движении, ходьбе, если отвлечь внимание пациента.
Мозжечковый тремор проявляется дрожанием головы, рук, туловища. Важно! Крупноразмашистые движения при патологии мозжечка развиваются в основном в момент окончания движения, а при паркинсонизме – в покое. Проверяется при выполнении пальценосовой и пяточно-коленной пробы. - Тремор, развивающийся при патологии щитовидной железы, психоэмоциональном перенапряжении, синдроме отмены алкоголя, болезнях обмена веществ. Максимально проявляется при попытке сохранить позу. Хорошо виден на кончиках пальцев кистей при вытянутых руках.
- Ортостатический тремор не наблюдается при паркинсонизме, появляется в ногах во время ходьбы, отмечается дрожание в четырёхглавой мышце бедра.
Главное отличие дрожательного феномена при паркинсонизме – несимметричность. При данной патологии у больных имеется характерная поза просителя: наклонённая вперёд голова, опущенные плечи.
К нарушениям движения относятся:
- шаркающая походка;
- замедленная, монотонная речь;
- гипомимичное выражение лица;
- почерк становится мелким;
- утрачиваются содружественные движения рук при ходьбе, которые в норме есть у всех людей;
- человеку сложно начать выполнять какое-либо движение и так же трудно остановиться.
Вегетативные симптомы
Вегетативная недостаточность характеризуется следующими проявлениями:
- нарушение глотания, ощущение удушья;
- склонность к запорам;
- разнообразные нарушения мочеиспускания от императивных позывов до затруднения с неполным опорожнением мочевого пузыря, недержанием мочи;
- нарушения эрекции, снижение либидо;
- склонность к ортостатическим коллапсам;
- снижение потоотделения, гипер- или гипосаливация.

Сенсорные симптомы
Пациенты не обращают внимания на нарушение чувствительности или сенсорные симптомы, которые являются ранними проявлениями синдрома паркинсонизма. Чувствительные нарушения формируются раньше паркинсонических двигательных расстройств. К ним относятся:
- нарушение обоняния;
- чувство бегания мурашек, жжение или боль в конечностях, в основном в ногах.
Психические симптомы
Болезнь Паркинсона и паркинсонизм в равной степени часто сопровождаются нарушением психики:
- Депрессия. Люди, склонные к депрессивным состояниям, чувству вины, заниженной самооценке, больше подвержены паркинсонизму. Важно! Пациенты фиксируют своё внимание на нарушении движения и не говорят об имеющейся тревожности, отчаянии. Но эти явления присутствуют всегда.
- Психозы, чередующиеся с апатией, безразличием, вялостью. Возможно развитие спутанного сознания с галлюцинациями и психозом. Чем дольше имеется клиническая симптоматика паркинсонизма, тем чаще появляются психотические реакции. Сначала критика сохранна. Со временем критическое отношение к галлюцинациям у больного исчезает и развивается такое состояние, как паранойяльный психоз.
- Пониженная работоспособность, ощущение усталости, вялости, постоянное чувство утомлённости. Отсутствует радостное настроение, нет потребности получать удовольствие и наслаждение.
- Нарушение познавательных функций, появляется вязкость мышления, резко снижается внимание. Нарушение памяти отличается характерными особенностями. Больные могут запоминать механическую информацию и вообще не способны фиксировать эмоционально окрашенную.
- Навязчивые состояния, патологические влечения.
Нарушение сна и бодрствования
Нарушения сна и бодрствования имеются у 98 % больных с паркинсонизмом и появляются на 5 – 10 лет раньше, чем основная двигательная симптоматика синдрома Паркинсона.
Имеются следующие проявления:
- нарушается засыпание;
- дневная сонливость;
- частые ночные или ранние утренние пробуждения;
- увеличивается продолжительность ночного сна, сохраняется чувство усталости и разбитости после пробуждения;
- слишком яркие устрашающие сновидения.
При синдроме паркинсонизма на первый план выходит симптоматика того заболевания, которое привело к его развитию.

Диагностика
Для правильного лечения синдрома паркинсонизма надо выявить причину, его вызвавшую, и исключить сходные состояния, которые могут симулировать заболевание.
Синдром Паркинсонизма развивается как осложнение следующих приобретённых заболеваний:
- лекарственный;
- посттравматический;
- токсический;
- постэнцефалитический;
- паркинсонизм при других нейроинфекциях;
- паркинсонизм при гидроцефалии;
- сосудистый;
- постгипоксический.
Первично проявляется симптоматика вышеуказанных заболеваний, а потом как осложнение присоединяется дрожательно-ригидный синдром.
При дегенеративных заболеваниях ЦНС развивается паркинсонизм-плюс, при котором на первый план выходят неврологические синдромы:
- пирамидный;
- мозжечковый;
- вегето-сосудистая дистония;
- деменция;
- последним присоединяется паркинсонизм-плюс.
К этой же группе относятся:
- мультисистемная атрофия;
- прогрессирующий надъядерный паралич;
- болезнь диффузных телец леви;
- кортикобазальная дегенерация;
- гемипаркинсонизм-гемиатрофия;
- болезнь Альцгеймера;
- болезнь Крейтцфельдта – Якоба;
- наследственные формы;
- болезнь Гентингтона;
- спиноцеребеллярные дегенерации;
- болезнь Галлервордена – Шпатца;
- гепатолентикулярная дегенерация;
- паллидарные дегенерации;
- семейная кальцификация базальных ганглиев;
- нейроакантоцитоз;
- дистония-паркинсонизм.

Лечение
Выделяют 4 важных направления лечения:
- Лечение основного заболевания, если это возможно.
- Препараты, направленные на купирование явлений паркинсонизма.
- Использование ноотропов, сосудистых средств для защиты мозга от дальнейшего разрушения.
- Реабилитация.
Для симптоматического лечения используют следующие средства:
- препараты леводопы;
- агонисты дофаминовых рецепторов;
- антихолинергические средства;
- препараты амантадина;
- ингибиторы моноаминоксидазы типа В;
- ингибиторы катехол-О-метилтрансферазы.
Лечение паркинсонизма назначается индивидуально лечащим врачом с учётом основного заболевания, выраженности дополнительных неврологических расстройств, индивидуальной чувствительности.
Основная задача лечения больных с паркинсонизмом – восстановление нарушенных двигательных функций. В некоторых случаях, когда проявления заболевания минимальные, лекарство можно не назначать.
При нарастании симптоматики используется монотерапия, а в дальнейшем – комбинированная лекарственная терапия.
Для лечения вегетативных расстройств применяются:
- ношение эластичных чулок;
- увеличенное употребление соли, воды;
- флудрокортизон;
- «Мидодрин» – адреналиноподобный симпатомиметик с сосудосуживающим эффектом. Назначается внутрь по 2,5 мг 3 раза;
- «Индометацин» хорошо снимает головную, мышечную, суставную боль при сенсорных проявлениях;
- Кофеин улучшает выносливость ЦНС к нагрузке и устойчивость к повреждающим факторам. Повышает артериальное давление, применяется для лечения ортостатических нарушений;
- «Дигидроэрготамин» обладает стимулирующим действием на серотониновые рецепторы, является блокатором адренорецепторов сосудов. Препарат сужает сосуды головного мозга.

При нейрогенных нарушениях мочеиспускания используют:
- «Оксибутинин» применяется при нейрогенной слабости мочевого пузыря и недержании мочи. Эффективен также при повышении спазма гладкой мускулатуры желудочно-кишечного тракта, матки, желчного пузыря. Продолжительность лечения до 2 лет.
- «Толтеродин» – м-холинолитик, применяемый при гиперактивности мочевого пузыря, императивных позывах, непроизвольном мочеиспускании.
- «Альфузозин» блокирует альфа-1-адренорецепторы мочеполовых органов, назначается при функциональных нарушениях по 5 мг 2 раза.
- «Доксазозин» снижает артериальное давление, уровень холестерина и липидов высокой плотности в крови, даёт хороший эффект при синдроме паркинсонизма на фоне хронической ишемической болезни головного мозга с артериальной гипертензией.
- «Празозин» – гипотензивный препарат, обладающий способностью расслаблять мышцы сосудов на периферии и не влияющий на артерии и вены головного мозга.
- «Тамсулозин» эффективен у пожилых мужчин при дизурических нарушениях, развивающихся на фоне гиперплазии предстательной железы.
- «Теразозин» используется для симптоматической терапии доброкачественной гиперплазии предстательной железы, артериальной гипертензии.
- «Десмопрессин» эффективен в отношении мочевых нарушений, никтурии.
При склонности к запорам:
- диета, богатая клетчаткой;
- достаточная физическая активность;
- «Домперидон» или «Мотилиум» улучшают моторику ЖКТ, блокируя при этом рвотный центр;
- «Цизаприд» – серотонинергическое средство, стимулирующее моторику желудочно-кишечного тракта при желудочно-пищеводном рефлюксе, гастропарезе, анорексии, функциональном и идиопатическом запорах, функциональной диспепсии, гипокинезии желчного пузыря;
- слабительные средства лучше использовать растительного происхождения. Они обладают более мягким, постепенным эффектом, не вызывают нарушения водно-электролитного баланса, дефицита витаминов и микроэлементов в организме. К таким препаратам относятся «Гутталакс», «Регулакс», сенна, белладонна, «Мукофальк», «РектАктив».
Для лечения когнитивных расстройств применяют:
- «Ривастигмин»;
- «Донепезил»;
- «Галантамин»;
- «Мемантин»;
- «Ипидакрин»;
- «Холина альфосцерат»;
- «Пирацетам».
Для лечения аффективных нарушений используют:
- «Пирибедил»;
- «Прамипексол»;
- «Мелипрамин» – антидепрессант, хорошо устраняющий явления тревоги, применяется по 25 мг 3 раза;
- психотерапию.
Лечение проблем сна требует:
- откорректировать вечернюю дозу противопаркинсонических средств;
- если этого не достаточно, то на ночь назначается «Клозапин»;
- «Тразодон», «Амитриптилин», «Доксепин»;
- снотворные назначаются на очень непродолжительное время из-за реально существующей угрозы развития привыкания.
Немедикаментозное лечение
Для сохранения качественной социально активной жизни пациент должен иметь необходимую информацию о своём заболевании, научиться с ним жить, чтобы контролировать болезнь.
Обычно в лечение включают:
- нейропсихологический тренинг;
- речевую терапию;
- ЛФК;
- соблюдение диеты, режима дня.
Профилактика
Специфических мер профилактики синдрома паркинсонизма не существует. Но учитывая, что он развивается как симптом либо осложнение других болезней нервной системы, необходимо проводить первичную профилактику заболеваний и травм ЦНС.
Основные направления профилактики включают:
- избегание стрессов;
- ведение здорового образа жизни;
- достаточную физическую активность;
- отказ от употребления алкоголя, никотина;
- профилактику производственного и дорожно-транспортного травматизма и др.
Будучи достаточно частым заболеванием ЦНС, особенно в пожилом возрасте, сидром паркинсонизма развивается на фоне хронической ишемической болезни головного мозга. Последствия ишемического и геморрагического инсультов, дисциркуляторная энцефалопатия, атеросклеротическое поражение сосудов могут привести к синдрому паркинсонизма. Следовательно, профилактика вышеперечисленных заболеваний является необходимым условием предотвращения явлений паркинсонизма.
Источник
