Миодистрофия беккера код мкб

Содержание
- Описание
- Дополнительные факты
- Причины
- Симптомы
- Диагностика
- Дифференциальная диагностика
- Лечение
Названия
Название: Прогрессирующая мышечная дистрофия Беккера.
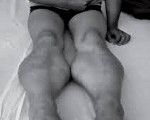
Прогрессирующая мышечная дистрофия Беккера
Описание
Прогрессирующая мышечная дистрофия Беккера. Вариант наследственной сцепленной с Х — хромосомой миодистрофии, отличающейся более замедленным и доброкачественным течением. Заболевание характеризуется постепенно усугубляющейся и распространяющейся мышечной слабостью, гипотонией и атрофией, первоначально возникающей в мышцах бедер и тазового пояса. Диагностический поиск включает неврологическое обследование, консультацию генетика и кардиолога, нейрофизиологическое тестирование нервно-мышечного аппарата, ДНК диагностику, биопсию мышц с морфологическим, иммунологическим и гистохимическим изучением полученных образцов. Лечение симптоматическое и, к сожалению, малоэффективное. Прогрессирование болезни приводит к потери больными способности самостоятельно передвигаться к возрасту 40 лет.
Дополнительные факты
Прогрессирующая мышечная дистрофия Беккера впервые была описана в 1955 г. Как доброкачественный вариант течения мышечной дистрофии Дюшенна. В последующем многочисленные исследования в области неврологии, генетики и биохимии обнаружили существенные отличия в характере течения, биохимической и морфологической основе этих заболеваний. В результате клиническая форма Беккера была выделена как самостоятельная нозология.
Мышечная дистрофия Беккера входит в группу миопатий (миодистрофий) — заболеваний, возникающих вследствие нарушений строения и метаболизма мышечной ткани и проявляющихся мышечной слабостью. Патология наследуется рецессивно сцеплено с Х-хромосомой, поэтому болеют только лица мужского пола. Частота встречаемости составляет 1 новорожденный на 20 тыс. Детей.
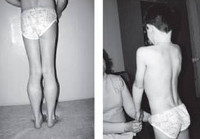
Прогрессирующая мышечная дистрофия Беккера
Причины
В основе заболевания лежит мутация в гене, ответственном за кодирование белка дистрофина. Примерно 30% от общего числа случаев мышечной дистрофии Беккера приходится на т. Н. «свежие» мутации. Ген располагается в 21 локусе (в регионе Хр21. 2–р21. 1) короткого плеча Х-хромосомы. Примерно у 65-70% больных обнаруживаются крупные делеции указанного участка, у 5% — дупликации, у остальных — точковые мутации. Указанные структурные перестройки гена не влекут за собой полного прекращения синтеза дистрофина, как при дистрофии Дюшенна, а потенцируют синтез аномального усеченного белка, в некоторой степени способного выполнять свои функции. Это и обуславливает более доброкачественный характер дистрофии Беккера в сравнении с вариантом Дюшенна.
В норме белок дистрофин поддерживает целостность сарколеммы — мембраны миоцитов (мышечных волокон), обеспечивает эластичность и устойчивость миофибрилл при мышечном сокращении. Неспособность аномального дистрофина адекватно выполнять эти функции приводит к нарушению целостности мембран мышечных волокон. В следствие этого происходят дегенеративные изменения цитоплазматических компонентов последних и повышенная транспортировка ионов калия внутрь миоцитов. Результатом таких биохимических и морфологических сдвигов является гибель миофибрилл и разрушение мышечных волокон. На месте погибших миоцитов происходит образование соединительной ткани, что обуславливает феномен псевдогипертрофии — увеличение объема и плотности мышцы при резком снижении ее сократительной способности.
Симптомы
Прогрессирующая мышечная дистрофия Беккера манифестирует обычно в период от 10 до 15 лет, в некоторых случаях раньше. Начальными признаками заболевания выступают чрезмерная утомляемость и мышечная слабость в тазовом поясе и нижних конечностях. У ряда пациентов первыми проявлениями являются периодические болезненные мышечные судороги (крампи), локализующиеся в ногах. Мышечная слабость обуславливает затруднение при подъеме по лестнице, при необходимости встать из положения сидя. Со временем формируется переваливающаяся «утиная» походка. Для того, чтобы встать, пациент вынужден использовать вспомогательные миопатические приемы — опираться руками о расположенные рядом предметы мебели или, при отсутствии таковых, использовать в качестве опоры собственное тело (симптом Говерса).
Как и другие наследственные миопатии, заболевание Беккера характеризуется симметрично развивающимися атрофиями мышц. В первую очередь поражаются мышцы бедра и тазового пояса, затем процесс распространяется на мускулатуру плечевого пояса и проксимальных мышц рук. В начале болезни формируются псевдогипертрофии, наиболее выраженные в икроножных, дельтовидных, трех- и четырехглавых мышцах. По мере прогрессирования миодистрофии они трансформируются в мышечные гипотрофии.
Слабость в руках. Слабость мышц (парез). Судороги.
Диагностика
Прогрессирующая мышечная дистрофия Беккера диагностируется неврологом на основании анамнеза, клинических данных, дополнительных обследований и генетического тестирования. В неврологическом статусе наблюдается снижение мышечной силы и умеренное снижение мышечного тонуса в проксимальных отделах конечностей, выпадение коленных рефлексов при симметричном снижении сухожильных рефлексов дистальных отделов ног и верхних конечностей, полная сохранность чувствительности.
Среди клинических анализов наибольшее значение имеет биохимический анализ крови, который выявляет многократное повышение уровня КФК. Данные электронейрографии позволяют исключить поражение нервных волокон, электромиография свидетельствует о первично-мышечном типе поражения. Биопсия мышц проводится только после отрицательных результатов генетического анализа. Морфологическое исследование полученного материала определяет диффузную разнокалиберность, дистрофические и некротические изменения мышечных волокон, разрастание соединительной ткани. Проводится специальное иммунное окрашивание образцов с последующим определением наличия в них дистрофина.
Подтвердить диагноз мышечной дистрофии Беккера позволяет консультация генетика с проведением анализа ДНК. Выявление дупликаций или делеций в гене Хр21 дает возможность установить точный диагноз. Отрицательный результат анализа ДНК не говорит об отсутствии патологии, поскольку могут иметь место точковые мутации, поиск которых представляет собой сложную и более дорогостоящую процедуру.
С целью выявления сердечной патологии назначается электрокардиография, Эхо-КГ, консультация кардиолога. Кардиологическое обследование может обнаружить нарушение внутрижелудочковой проводимости, АВ-блокаду, дилатацию желудочков, гипертрофические изменения миокарда, кардиомиопатию, сердечную недостаточность.
Дифференциальная диагностика
Дифференциальная диагностика проводится с прогрессирующей мышечной дистрофией Дрейфуса, миодистрофией Дюшена, мышечной дистрофией Эрба-Рота, метаболической миопатией, полимиозитом и дерматомиозитом, воспалительной миопатией, спинальной амиотрофией, наследственной полиневропатией.
Пренатальная диагностика рекомендована, когда мать является носителем патогенного гена. Если ребенок мужского пола, то вероятность развития заболевания у него составляет 50%. Биопсия хориона может проводиться в сроке 11-14 нед. Беременности, амниоцентез — после 15-й недели, забор пуповинной крови (кордоцентез) — на сроке больше 18 нед.
Лечение
На современном этапе несколькими группами ученых ведутся настойчивые исследования в области поиска эффективных методов лечения прогрессирующих миодистрофий. В настоящее время пациенты получают в основном метаболическую и симптоматическую терапию. Разработаны различные схемы лечения, позволяющие улучшить двигательные возможности больного и несколько замедлить прогрессирование болезни. Пациентам назначают актопротекторы (этилтиобензимидазол), неостигмин, АТФ, анаболические стероиды (метиландростендиол), сердечные средства. По вопросу длительной терапии глюкокортикоидами (преднизолоном) клиницисты имеют различные мнения. Одни считают, что подобное лечение тормозит прогрессирование миодистрофии, другие отвергают это предположение.
Наблюдения показали, что постельный режим усугубляет мышечную слабость. Поэтому пациентам рекомендуется умеренная физическая активность, занятия плаваньем. Поддержание мышечной эластичности и силы, а также профилактика контрактур проводится средствами массажа, физиотерапии и лечебной гимнастики. По показаниям проводится хирургическое лечение контрактур. Применение различных ортопедических средств (ходунков, инвалидных колясок, фиксаторов для ног, экзоскелетов) позволяет расширить двигательные возможности пациентов и их способность к самообслуживанию. По показаниям проводится хирургическое лечение контрактур.
Источник
- Описание
- Причины
- Симптомы (признаки)
- Диагностика
- Лечение
Краткое описание
Мышечная дистрофия Дюшенна — наследственная прогрессирующая мышечная дистрофия, характеризующаяся началом в раннем возрасте, симметричной атрофией мышц в сочетании с сердечно — сосудистыми, костно — суставными и психическими нарушениями, злокачественным течением; наследуется по рецессивному X — сцепленному типу. Вариант мышечной дистрофии Дюшенна — мышечная дистрофия Беккера — имеет более доброкачественное течение.
Код по международной классификации болезней МКБ-10:
- G71.0 Мышечная дистрофия
- M62.5 Истощение и атрофия мышц, не классифицированные в других рубриках
- M62.8 Другие уточненные поражения мышц
Причины
Генетические аспекты • Псевдогипертрофическая прогрессирующая мышечная дистрофия (мышечная дистрофия Дюшенна–Беккера, *310200, Xp21.2, ген DMD дистрофина, À рецессивное) — возникает в результате дефектов гена, кодирующего белок дистрофин • Дистрофин локализован в плазматической мембране скелетных мышечных волокон и кардиомиоцитов • Преобладающий пол — мужской, тем не менее мышечные дистрофии Дюшенна и Беккера могут встречаться у девочек при кариотипе X0, мозаицизмах X0/XX, X0/XXX и структурных аномалиях хромосом.
Патоморфология • Дистрофия мышечных волокон, первично — мышечный тип поражения • Фиброзные изменения в мышечных пучках • Местная воспалительная реакция.
Симптомы (признаки)
Клиническая картина
• Мышечная дистрофия Дюшенна начинается в первые 1–3 года жизни обычно со слабости мышц тазового пояса.
• Уже на первом году жизни отмечают отставание в психомоторном развитии. Больные дети позднее начинают садиться, вставать, ходить.
• Постепенно развиваются слабость, патологическая мышечная утомляемость при физической нагрузке, изменение походки по типу утиной. Из горизонтального положения дети встают поэтапно с использованием рук (взбирание лесенкой).
• Отмечаются симметричные атрофии проксимальных групп мышц нижних конечностей (мышцы таза и бедра). Атрофия через 1–3 года распространяется на проксимальные группы мышц верхних конечностей.
• Атрофии мышц приводят к развитию лордоза, крыловидных лопаток, осиной талии.
• Характерна псевдогипертрофия икроножных мышц.
• Мышцы при пальпации плотные, безболезненные.
• Мышечный тонус обычно снижен в проксимальных группах мышц.
• Изменения рефлексов •• Коленные рефлексы исчезают на ранних стадиях заболевания •• Позднее исчезают рефлексы с двуглавой и трёхглавой мышц плеча •• Ахилловы рефлексы обычно длительное время остаются сохранными.
• Дистальная мускулатура конечностей поражается на поздних стадиях заболевания.
• Костно — суставные нарушения — деформации позвоночника, стоп, грудной клетки; рентгенологически обнаруживают сужение костномозгового канала, истончение коркового слоя диафизов длинных трубчатых костей.
• Сердечно — сосудистые расстройства — лабильность пульса, АД, приглушение тонов, расширение границ сердца, сердечная недостаточность, изменения на ЭКГ.
• Нейроэндокринные нарушения выявляют у 30–50% больных — синдром Иценко–Кушинга, адипозогенитальная дистрофия.
• Психические нарушения — олигофрения в форме дебильности или имбецильности.
• Клинические проявления мышечной дистрофии Беккера обычно начинаются в 10–15 лет. От мышечной дистрофии Дюшенна отличается доброкачественным течением и более поздним возникновением тяжёлых симптомов. Сухожильные рефлексы долгое время остаются сохранными. Поражения внутренних органов менее выражены, интеллект сохранён.
Диагностика
Лабораторные исследования. Для мышечной дистрофии Дюшенна типично раннее (с 5 дня жизни) увеличение активности КФК в крови (в 30–50 раз выше нормы).
Дифференциальная диагностика. Мышечную дистрофию Дюшенна–Беккера дифференцируют от других мышечных дистрофий, рахита, врождённого вывиха бедра.
Лечение
ЛЕЧЕНИЕ
Режим амбулаторный с наблюдением у невропатолога, хирурга — ортопеда, терапевта и профпатолога, работника социальной сферы и протезиста.
Мероприятия • Лечение мышечной дистрофии Дюшенна направлено на поддержании физической активности пациента и улучшение качества его жизни; как правило, быстро становится неэффективным • Физические упражнения выполняют систематически и по определённой схеме. Короткие перерывы показаны при возникновении болей в мышцах и мышечной усталости • Использование протезов позволяет больным двигаться и замедляет формирование сколиоза • Поддержание дыхания, ИВЛ во время сна для предотвращения синдрома ночной гиповентиляции • Экспериментальные методы, в особенности генная терапия (гены дистрофина и утрофина), чрезвычайно перспективны, хотя и не получили пока клинического распространения.
Оперативное лечение. Ортопедическое вмешательство необходимо при наличии контрактур и фиксации суставов.
Лекарственная терапия • ГК (преднизолон по 0,75 мг/кг/сут) увеличивают мышечную силу у мальчиков, страдающих мышечной дистрофией Дюшенна, замедляя прогрессирование заболевания • При длительной стероидной терапии необходим тщательный контроль развития побочных эффектов, включающий наблюдение за массой тела, АД, состоянием слизистой оболочки ЖКТ и иммунной системы.
Наблюдение. Ранняя диагностика поражения внутренних органов позволяет увеличить продолжительность жизни пациентов.
Течение и прогноз • Течение мышечной дистрофии Дюшенна быстропрогрессирующее, злокачественное • Значительные двигательные расстройства, развивающиеся ко второму десятилетию жизни, ограничивают самостоятельное передвижение больных • Смерть наступает на втором или третьем десятилетии жизни, часто в результате пневмонии • Течение мышечной дистрофии Беккера медленнопрогрессирующее. Больные длительное время сохраняют работоспособность.
Профилактика состоит в генетическом консультировании.
Синонимы • Прогрессирующая мышечная дистрофия Дюшенна • Псевдогипертрофическая мышечная дистрофия Дюшенна • Дистрофия Дюшенна • Болезнь Дюшенна • Миопатия псевдогипертрофическая • Миопатия псевдогипертрофическая Дюшенна.
МКБ-10 • G71.0 Мышечная дистрофия • M62.5 Истощение и атрофия мышц, не классифицированные в других рубриках • M62.8 Другие уточнённые поражения мышц
Примечания • Термин «псевдогипертрофическая прогрессирующая мышечная дистрофия» объединяет мышечные дистрофии Дюшенна и Беккера • Мышечная дистрофия Дюшенна описана в 1853 г. Дюшенном • Мышечная дистрофия Беккера описана в 1955 г. Беккером.
Лекарственные средства и Медицинские препараты применяемы для лечения и/или профилактики «Дистрофия мышечная Дюшенна».
Источник
Врожденное неврологическое заболевание, характеризующееся неконтролируемым и длительным сокращением мышц, называется миотонией. Болезнь может развиваться по доминантному или рецессивному типу и характерна для лиц обоего пола. Миотония Томсена отличается многолетним течением и при позднем выявлении значительно снижает качество жизни. Данная статья содержит полные сведения об отличительных особенностях и главных признаках этого заболевания.
О заболевании
 Для начала нужно разобраться, что это такое.
Для начала нужно разобраться, что это такое.
Миотония Томсена – это хроническое нервно-мышечное заболевание с медленно прогрессирующим течением.
Некоторые путают имя доктора и ошибочно полагают, что заболевание названо в честь некоего Томпсона, однако это неверно.
Болезнь относится к врожденным генетическим недугам и наследуется по аутосомно-доминантному типу. Частота выявления – 0,3-0,7% на 100 000 новорожденных. Проявляется замедленным расслаблением поперечнополосатой мускулатуры в сочетании с тоническим спазмом вслед за началом произвольного движения.
Код по МКБ-10: G71.1.
Этиология и патогенез
Развитие болезни связано с генетической мутацией, развивающейся во время внутриутробного периода. Поврежденный ген, ответственный за работу хлорных каналов и синтез белка дистрофина, расположен на длинном плече 7 хромосомы. В результате мутации происходит недостаточное образование или полное отсутствие белка, регулирующего сокращение мышц.
В норме дистрофин отвечает за поддержание мышечной работы и правильную последовательность расслабления и сокращения. Из-за нарушения его синтеза происходит задержка хлора на мембранах мышечных клеток. Пучки поперечно-полосатой мускулатуры теряют способность к расслаблению и остаются сокращенными после выполнения движения.
Перенапряжение волокон вызывает еще большее накопление ионов хлора на поверхности клеточных мембран. Нарушается баланс между остальными ионными каналами. Накопленный хлор провоцирует выброс вне клеток ионов кальция. Избыток кальция оказывает прямое повреждающее влияние и приводит к разрушению мышечных клеток.
СПРАВКА. Тонические спазмы постепенно вызывают деформацию всего осевого скелета. Из-за повреждения дыхательных мышц развиваются эпизоды одышки или удушья. Повреждение поперечно-полосатой мускулатуры сердца приводит к кардиомиопатиям.
Классификация
 Заболевание подразделяется на две клинические формы: генерализованную и локализованную.
Заболевание подразделяется на две клинические формы: генерализованную и локализованную.
Генерализованная форма – поражение всей скелетной мускулатуры тела. При этой форме гипертонус мимических мышц может наблюдаться, а может отсутствовать.
Локализованная форма – поражение одной мышечной группы. Наблюдают развитие миотонии:
- Мимических мышц – двусторонней, односторонней;
- Языка;
- Жевательной мускулатуры;
- Круговых мышц глаза;
- Плечевого пояса и верхней конечности;
- Мышц туловища;
- Мышц таза и нижней конечности.
ВАЖНО: Одна форма заболевания никогда не переходит во вторую, что говорит об изначально заданном характере поражения.
Клиника заболевания
Главные симптомы – миотонический спазм и мышечная скованность:
- Миотонический спазм – это длительное сокращение мышц вслед за активным движением, длящееся несколько десятков секунд. Пациент не в состоянии устранить спазм произвольно;
- Скованность мышц — трудность при выполнении движений после периода покоя. Скованность проходит после того, как больной пытается выполнить движение несколько раз.
Первые проявления болезни наблюдают в грудном периоде. Во время плача младенец внезапно начинает задыхаться, его голос изменяется. После успокоения гримаса остается на лице в течение 1-2 минут.
Уже в детстве в силу гипертрофии мускулатуры дети напоминают профессиональных атлетов, однако сила мышц значительно снижена. Во время физических занятий, бега, плавания дети значительно уступают сверстникам, несмотря на внешний вид.
СПРАВКА. Заболевание не сопровождается болевыми ощущениями и прогрессирует в холодное время года. Мышечная скованность часто охватывает пациентов после сна и приводит к нарушениям походки (симптомы «железного дровосека», «утиной походки», «подъема лесенкой»).
При генерализованной форме вследствие сокращения нескольких мышечных групп пациенты теряют равновесие. Падение сопровождается невозможностью самому подняться до тех пор, пока не исчезнет мышечный спазм.
При локализованной форме наблюдаются следующие тонические сокращения:
- Мышц кисти — во время письма и выполнения мелких движений;
- Мышц стопы – во время ходьбы и физкультурных занятий;
- Языка – во время разговора;
- Мышц глаза – во время зажмуривания;
- Жевательных мышц – во время жевания, разговора.
Гипертрофия мышц и в зрелом возрасте выдает в больных «профессиональных спортсменов», однако их физическая подготовка значительно ниже, чем у сверстников. Бытовые, профессиональные движения, а также ходьба затруднены, подчас невозможны. Пациент не может быстро разжать кисти, открыть глаза, рот, изменить положение.
Миотония Беккера
Это врожденное неврологическое заболевание из группы миотоний, наследующееся по аутосомно-рецессивному типу. Относится к болезням, сцепленным с полом (вызвано генетической мутацией в области Х-хромосомы). Отличается поздним началом, более мягким течением и замедленным прогрессированием. В отличие от болезни Томсена, характерно начало клинических проявлений в 8-10 лет.
Клиническая картина при обоих заболеваниях идентична, но при миотонии Беккера проявления менее выражены. Обе болезни относятся к гипертрофическим миотониям.
| Беккера | Томсена | |
|---|---|---|
| Расположение мутации | Х-хромосома | Седьмая хромосома |
| Возраст начала | 8-10 лет | Грудной период |
| Наследование | Рецессивное (мутация гена имелась у обоих родителей) | Доминантное (мутация имелась хотя бы у одного родителя) |
| Клиническая картина | Менее выражена | Яркая |
Дистрофическая миотония Россолимо-Штейнерта-Куршмана
Этот вид миотонии также наследственный. Это заболевание прогрессирующее, в его основе заложен дефект миотонин-протеинкиназы. Это приводит к дистрофическим изменениям мышечной ткани.
Классическая форма этой болезни проявляется в возрасте от 10 до 20 лет. В редких случаях эта миотония бывает врожденной. В таком случае заболевание уже видно при рождении. При миотонии Россолимо-Штейнерта-Куршмана наблюдается замещение части мышечных волокон жировой и соединительной тканью.
Диагностика
 Для выявления заболевания пользуются методами опроса, осмотра, прощупывания и простукивания, а также лабораторно-инструментальной диагностикой.
Для выявления заболевания пользуются методами опроса, осмотра, прощупывания и простукивания, а также лабораторно-инструментальной диагностикой.
- Опрос: выявляют возраст начала заболевания, его характерные проявления, зависимость от переохлаждения, семейный анамнез;
- Осмотр: атлетическое телосложение, выявление мышечной гипертрофии;
- Прощупывание: слабость мышц в сочетании с плотными валиками;
- Простукивание: миотонический феномен – при постукивании по мышечному валику происходит его сокращение с длительным расслаблением;
- Сухожильные рефлексы: не нарушены;
- Биохимический анализ крови: повышение уровня креатин-фосфокиназы (фермента, разрушающего мышечный белок);
- Генетическое обследование: выявление генной мутации и подтверждение доминантной природы наследования;
- Электромиография: множественные сокращения мышечных клеток до 80 раз в секунду (миотоническая реакция). Частота сокращений постоянно меняется, что сопровождается гулом аппарата (симптом «пикирующего бомбардира»).
СПРАВКА. Как правило, для постановки диагноза достаточно клинической картины и данных электромиографии. В затруднительных случаях проводится биопсия, на которой выявляют удлинение и неравномерное расширение мышечных волокон. Диагностике помогает и рентгенография костей (определяют остеопороз, истончение надкостницы).
Лечение
Проводится патогенетическая терапия. Методов, способных повлиять на генетическую мутацию, не существует, поэтому этиологическое лечение не разработано. Лечение назначается каждому пациенту в индивидуальном порядке после консультации с врачом.
Лекарственная терапия
 Терапия медикаментами не исключается в любом случае.
Терапия медикаментами не исключается в любом случае.
Чаще всего назначают препараты из следующих групп:
- Противосудорожные препараты – способствуют расслаблению сокращенных мышц и снятию скованности. Используют дифенин, карбамазепин, новокаинамид строго в средних противосудорожных дозах;
- Мочегонные препараты, влияющие на проницаемость клеточных мембран. Способствуют восстановлению внутриклеточного обмена. Из данной группы применяют диакарб по схеме;
- Блокаторы ионных каналов – предупреждают развитие тонических сокращений. Используют мексилетин по схеме;
- Антагонисты кальция – препятствуют разрушению миофибриллярных волокон, а также обладают кардиопротективным действием. Применяют нифедипин, дизопирамид 3 раза в день по схеме.
Курс лечения каждым препаратом составляет 3 недели, после чего доктор определяет время перерыва, и лечение продолжают.
Физиотерапия
Практически всегда врач назначает физиотерапевтические занятия, однако сами по себе они не способны улучшить ситуацию:
- Гальванические токи на область патологического очага;
- Электрофорез с актовегином и другими сосудистыми средствами;
- Лечебная физкультура под контролем врача;
- Массаж пораженной области (разрешены все виды массажа, кроме тонизирующего).
СПРАВКА. Врожденный характер патологии обуславливает недостаточную эффективность терапии. При выраженных жалобах применяют глюкокортикостероиды короткими курсами (5-7 дней), которые препятствуют разрушающему действию ионов кальция.
Какой прогноз на выздоровление?
Прогноз для жизни относительно благоприятный. Полное выздоровление невозможно, однако болезнь прогрессирует длительно. У части больных ухудшения не происходит в течение всей жизни. Без лечения трудоспособность снижена.
При проведении полноценной терапии улучшение наступает в 90% случаев, трудоспособность сохраняется пожизненно. Существуют данные о многолетней ремиссии под действием противосудорожных средств.
С возрастом мышечные спазмы ослабевают у всех больных.
Полезное видео:
Возможные осложнения
 Длительное течение заболевания приводит к вовлечению в процесс многих органов и систем.
Длительное течение заболевания приводит к вовлечению в процесс многих органов и систем.
Их поражение происходит опосредованно – вследствие длительного спазма мышц:
- Искривление позвоночника: вперед (лордоз), назад (кифоз), в бок (сколиоз);
- Межпозвоночные грыжи;
- Синдром ночного апноэ (удушье во время сна);
- Кардиомиопатия (поражение сердца развивается потому, что миокард представлен поперечно-полосатой мускулатурой);
- Мышечная атрофия;
- Стойкие изменения мимики, жевания и глотания;
- Бруксизм.
СПРАВКА. Курсовая терапия позволяет избежать осложнений и достичь длительной ремиссии, однако у пациентов часто развивается привыкание к противосудорожному средству. В связи с этим возможность самолечения и длительного приема одного и того же препарата без контроля врача должна быть исключена.
Вывод
Миотония Томсена является редким нервно-мышечным заболеванием. При обнаружении у ребенка характерных симптомов следует обратиться за помощью и придерживаться определенных рекомендаций:
- Исключить провоцирующие факторы (переохлаждение);
- Не заниматься самолечением;
- Не использовать лекарственные средства вне схемы или без врачебных рекомендаций;
- Обеспечить больному покой и длительный сон;
- Оказывать помощь при передвижении, подъеме и спуске по лестнице.
Врожденный характер патологии позволяет выявить ее в раннем возрасте и начать комплексное лечение, которое может требоваться больному в течение всей жизни.
Источник
