Лимфопролиферативный синдром код мкб
Содержание
- Описание
- Дополнительные факты
- Причины
- Классификация
- Симптомы
- Диагностика
- Лечение
- Прогноз
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Аутоиммунный лимфопролиферативный синдром.

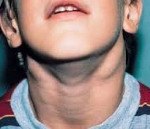
Аутоиммунный лимфопролиферативный синдром
Описание
Аутоиммунный лимфопролиферативный синдром. Группа генетически обусловленных заболеваний, которые возникают по причине наследственных или соматических мутаций в генах, отвечающих за различные этапы FAS — обусловленного апоптоза. Симптоматика может быть вариабельной и наиболее часто включает в себя лимфаденопатию, спленомегалию и разнообразные аутоиммунные поражения системы крови, печени, щитовидной железы. Диагностика аутоиммунного лимфопролиферативного синдрома производится на основании результатов общего и биохимического анализов крови, биопсии лимфатических узлов, генетических исследований. Специфического лечения заболевания в настоящий момент нет, применяют комбинации иммунносупрессивной и цитотоксической терапии.
Дополнительные факты
Аутоиммунный лимфопролиферативный синдром (АЛС, ALPS, синдром Канале-Смит) – группа иммунодефицитных состояний, характеризующихся аутоиммунными цитопениями, лимфаденопатией, спленомегалией. Первые данные о заболевании стали поступать в 1968-м году, после чего вскоре началось бурное изучение патологии. Изначально АЛС был отнесен к первичным иммунодефицитам, однако со временем были обнаружены формы синдрома, обусловленные соматическими мутациями в детском и подростковом организме. Данные о встречаемости у разных исследователей довольно сильно различаются, на сегодняшний момент описано более 500 случаев различных форм аутоиммунного лимфопролиферативного синдрома. Наследственные формы заболевания передаются по аутосомно-доминантному типу, при этом в развитии врожденных форм также довольно велика роль спонтанных мутаций. Среди больных с одинаковой частотой встречаются как мальчики, так и девочки.
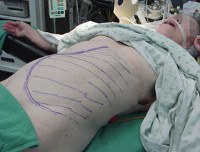
Аутоиммунный лимфопролиферативный синдром
Причины
Выяснено, что причиной любого типа АЛС является нарушение FAS-опосредованного апоптоза лимфоцитов. При образовании Т-лимфоцитов те линии, которые способны атаковать собственные ткани, уничтожаются за счет активизации рецепторов CD-95 (Fas-рецепторов) на поверхности их мембраны. Активация CD-95, относящегося к группе рецепторов фактора некроза опухолей, запускает многостадийную реакцию с участием каспаз, которая оканчивается апоптозом клетки. При аутоиммунном лимфопролиферативном синдроме генетические мутации приводят к блоку этого процесса на определенном этапе, из-за чего устранения потенциально опасных клонов Т-лимфоцитов не происходит, и они начинают накапливаться в лимфатических узлах. Кроме того, создаются условия для аутоиммунного поражения органов и тканей.
Наиболее часто встречаются наследственные и спонтанные мутации в гене TNFRSF6, который кодирует собственно Fas-рецептор. При этом нарушение структуры белка (особенно домена, отвечающего за взаимодействие с FADD-молекулой) приводит к тому, что он становится неспособным выполнять свои рецепторные функции и активизировать апоптоз. Возможны и соматические мутации в гене FAS, которые в полной мере проявляют себя в позднем детском или подростковом периоде, и поэтому их относят к отдельной группе АЛС. Второй по распространенности вариант аутоиммунного лимфопролиферативного синдрома обусловлен мутацией в гене CASP10, кодирующем цистин-аспарагин кислотную протеазу (каспаза-10). Этот белок играет ключевую роль в передаче сигнала об апоптозе с клеточной мембраны в ядро клетки. К этому же варианту относят и мутации гена CASP8.
Третьим по распространенности является аутоиммунный лимфопролиферативный синдром, который вызван мутацией в гене FASLG, кодирующем Fas-лиганд или рецептор CD-178. Он играет вспомогательную роль в распознавании факторов, стимулирующих апоптоз, и участвует в передаче сигнала в клетку. Некоторые формы АЛС обусловлены мутацией гена NRAS, который кодирует «малый G-белок», принимающий участие в качестве вторичного мессенджера в передаче сигналов с мембраны в клетку, в том числе и ядро. Примерно в трети случаев аутоиммунного лимфопролиферативного синдрома врачам-иммунологам не удается установить непосредственную причину заболевания.
Классификация
При помощи методов современной генетики удалось выявить шесть основных форм АЛС:
ALPS 1A. Вызвана мутацией гена TNFRSF6, расположенного на 10 — й хромосоме, чаще всего имеет врожденный характер, наследуется по аутосомно — доминантному типу. По статистике, более 40% АЛС относятся именно к этой разновидности.
ALPS 1В. Обусловлена мутацией гена FASLG, также довольно часто приводит к врожденному аутоиммунному лимфопролиферативному синдрому. К этому типу относят около 10% от всех клинических случаев АЛС.
ALPS 1m Ее причиной являются соматические мутации в гене FAS, возникающие в детском или подростковом возрасте и поэтому приводящие к поздним формам АЛС. При этом повреждение гена должно произойти в полипотентной клетке-предшественнице, которая способна дать начало многим линиям лимфоцитов. При этой форме наиболее часто возникает внезапная самопроизвольная ремиссия заболевания.
ALPS 2. Вызвана мутацией в генах CASP10 и, по некоторым данным, CASP8, которые кодируют белки — каспазы, передающие сигнал об апоптозе от рецептора к ядру клетки. Эта форма аутоиммунного лифопролиферативного синдрома составляет примерно 25% от всех случаев заболевания, может быть как врожденной, так и проявиться в более старшем возрасте.
ALPS 3. Мутация какого гена и характер ее наследования при этой форме неизвестны. Особенностью такого варианта АЛС является нарушение не только FAS-, но и IL2-опосредованного апоптоза, а также более тяжелый характер течения.
ALPS 4. Обусловлена мутацией гена NRAS, также кодирующего белки — передатчики внутриклеточного сигнала. Данный тип аутоиммунного лимфопролиферативного синдрома характеризуется более доброкачественным течением и умеренной выраженностью симптомов.
Симптомы
Симптомы АЛС довольно вариабельны из-за большого количества мутаций, которые могут приводить к такому состоянию. Начало заболевания можно заметить уже на 15-й день после рождения (при врожденных формах), в детском или подростковом возрасте в случае соматических мутаций в генах FAS, CASP10 или NRAS. Обычно первым проявлением заболевания является лимфаденопатия – подмышечные, паховые или шейные лимфатические узлы увеличиваются в размерах, но при этом безболезненны и не спаяны с окружающими тканями. Регистрируется спленомегалия, в некоторых случаях она сопровождается увеличением печени (гепатоспленомегалия).
Аутоиммунные проявления АЛС регистрируются обычно через некоторое время после лимфаденопатии и увеличения селезенки. В основном это поражения кровяных ростков – тромбоцитопения, гемолитическая анемия, приводящая к желтухе, изредка нейтропения. Помимо крови, аутоиммунному поражению могут подвергаться органы ЖКТ (возникают гастрит, панкреатит, колит, аутоиммунный гепатит). На коже могут проявляться признаки васкулита, делая клинику аутоиммунного лимфопролиферативного синдрома схожей с таковой при системной красной волчанке. Кроме того, могут возникать аутоиммунные формы тиреоидита, гломерулонефрита, поражаться суставы, ткани глаза (иридоциклит, увеит). Нередки поражения центральной нервной системы – эпилептические припадки, миелиты, мозжечковая атаксия.
Увеличение паховых лимфоузлов. Увеличение подмышечных лимфоузлов. Увеличение шейных лимфоузлов. Эозинофилия.
Диагностика
Диагностика АЛС производится на основании осмотра, а также лабораторных, иммунологических и генетических исследований. При осмотре выявляют увеличение более чем трех групп лимфатических узлов, спленомегалию, увеличение печени. Анализ крови может показывать уменьшение количества некоторых клеток (анемию, тромбоцитопению), у части больных определяется высокая (до 30%) эозинофилия. Проба Кумбса положительная, в биохимическом анализе крови определяется выраженная гипергаммаглобулинемия. Одним из высокочувствительных методов иммунологической диагностики аутоиммунного лимфопролиферативного синдрома является проточная иммуноцитофлюориметрия, проводимая с целью выявления количества лимфоцитов с атипичным набором рецепторов (CD3+CD4-CD8-). При АЛС количество таких клеток превышает 1% от всех лимфоцитов. В биоптате лимфатических узлов определяется фолликулярная гиперплазия, результатом гистологического исследования селезенки служит лимфоидная гиперплазия.
Врачом-генетиком может быть произведено секвенирование гена FAS с целью выявления мутаций, ставших причиной аутоиммунного лимфопролиферативного синдрома. С учетом значительной величины этого гена для ускорения и удешевления процедуры поиск может быть произведен лишь в отдельных экзонах гена FAS, в которых наиболее часто обнаруживаются нарушения – эти участки называют «горячими точками». Таким образом, при помощи генетической диагностики можно определить АЛС только 1А, 1В и 1m типов. Методики определения остальных форм АЛС генетическими методами на сегодняшний день не разработаны. Изучение наследственного анамнеза в ряде случаев будет неэффективно из-за значительной доли форм заболевания, вызванных соматическими мутациями.
Лечение
Этиотропное лечение аутоиммунного лимфопролиферативного синдрома не разработано, патогенетическая терапия сводится к применению иммуносупрессивных и цитотоксических средств. В качестве средств, подавляющих аутоиммунную активность, наиболее часто используют кортикостероиды (преднизолон, дексаметазон). К специфическим препаратам, ограничивающим скорость пролиферации лимфоцитов, относят микофенолата мофетил, сиролимус. Также при аутоиммунном лимфопролиферативном синдроме активно применяются традиционные цитотоксические средства – метотрексат, циклоспорин А и другие. При значительном увеличении селезенки или отсутствии эффекта от консервативного лечения прибегают к спленэктомии. Пересадка костного мозга и использование стволовых клеток в долгосрочной перспективе давали только временный эффект. При значительно выраженных гематологических нарушениях применяют гемотрансфузии, введение эритроцитарной или тромбоцитарной массы. Больному следует избегать физических нагрузок, использовать высоковитаминную диету.
Прогноз
Прогноз заболевания, ввиду высокой вариабельности и выраженности симптомов, неопределенный или неблагоприятный. У большей части больных проявления заболевания постепенно нарастают, со временем приводя к летальной анемии, тромбоцитопении, билиарному циррозу печени. Также важную роль в прогнозе играют нарушения иммунитета, так как нередко причиной смерти выступают сепсис и другие инфекционные поражения. В прогнозе аутоиммунного лимфопролиферативного синдрома следует учитывать и повышенный риск онкологических заболеваний, примерно пятая часть больных умирает от различных типов лимфом. В некоторых случаях возникает спонтанная и длительная ремиссия патологии.
Основные медуслуги по стандартам лечения | ||
Клиники для лечения с лучшими ценами
|
Источник
Рубрика МКБ-10: D47.9
МКБ-10 / C00-D48 КЛАСС II Новообразования / D37-D48 Новообразования неопределенного или неизвестного характера / D47 Другие новообразования неопределенного или неизвестного характера лимфоидной, кроветворной и родственных им тканей
Определение и общие сведения[править]
Аутоиммунный лимфопролиферативный синдром
Синонимы: синдром Канале-Смита (Canale-Smith)
Аутоиммунный лимфопролиферативный синдром является редким наследственным заболеванием, характеризующееся доброкачественной лимфопролиферацией, мультилинейной цитопенией и повышенным прижизненным риском возникновения ходжкинской и неходжкинской лимфом.
Распространенность аутоиммунного лимфопролиферативного синдрома неизвестна. На сегодняшний день было сообщено о более, чем 500 пациентов во всем мире в различных этнических группах.
Наследование может быть аутосомно-доминантным или аутосомно-рецессивным.
Этиология и патогенез[править]
Аутоиммунный лимфопролиферативный синдром вызван нарушением гомеостаза лимфоцитов. Зародышевые мутации генов FAS (10q24.1), FASLG (1q23) или CASP10 (2q33-q34) лежат в основе патологии. 75% случаев заболевания связаны с гетерозиготными мутациями гена FAS, 10% имеют соматические мутации гена FAS, 2-3% — CASP10 и FASLG <1%. Некоторые пациенты не имеют мутации в любом из этих генов (форма ALPS-U). Совсем недавно сообщалось об одном случае АЛС-подобного расстройства из-за мутации гена PRKCD (3p21.31) без повышения уровня клеток DNT.
Клинические проявления[править]
Аутоиммунный лимфопролиферативный синдром клинически гетерогенное заболевание со следующими первичными клиническими признаками: лимфопролиферация, проявляющаяся лимфаденопатией и гепатоспленомегалией с или без гиперспленизма, которая часто улучшается с возрастом; аутоиммунного нарушениями, в основном с участием клеток крови; а также повышенный риск развития лимфом на протяжении всей жизни.
Многие пациенты демонстрируют незлокачественную лимфопролиферацию в течение первых лет жизни. Клинические симтомы аутоиммунной дисфункции в виде гемолитической анемии, тромбоцитопении, нейтропении или аутоиммунного гепатита имеют различную степень выраженности, но часто эти признаки отсутствуют на момент постановки диагноза. Аутоиммунные заболевания, как сообщается, могут потенциально затрагивать практически любой орган, что приводит к увеиту, фиброзу легких, гастриту, колиту, нефриту, крапивнице, артриту или редко к аутоиммунным неврологическим осложнениям.
Течение заболевания варьирует.
Новообразование неопределенного или неизвестного характера лимфоидной, кроветворной и родственных им тканей неуточненное: Диагностика[править]
Диагноз основывается на клинических, лабораторных и генетических данных. Окончательный диагноз формулируется при наличии двух необходимых диагностических критериев: хроническая доброкачествення неинфекционная лимфаденопатия и/или спленомегалия и повышение уровня TCR альфа/бета-двойных-отрицательных Т-клеток (DNTs) на фоне нормального или повышенного уровня лимфоцитов, наряду с одним первичным дополнительным критерием, включая апоптоз лимфоцитов и наличие каузальной мутаций.
Дифференциальный диагноз[править]
Новообразование неопределенного или неизвестного характера лимфоидной, кроветворной и родственных им тканей неуточненное: Лечение[править]
Некоторым пациентам может потребоваться назначание иммуносупрессивной терапии — сиролимус и микофенолата мофетил.
Прогноз
Пациенты с мутацией FAS имеют значительно повышенный риск развития неходжкинской и ходжкинской лимфом, которые могут возникнуть в любом возрасте и реагирует на традиционную химиотерапию.
Профилактика[править]
Прочее[править]
https://www.orpha.net
Источники (ссылки)[править]
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
МКБ-10: C88.0 Макроглобулинемия Вальденстрема; C88.1 Болезнь альфа-тяжелых цепей; C88.9 Злокачественные иммунопролиферативные болезни неуточненные …
 МКБ 10: Пункт C88 Злокачественные иммунопролиферативные болезни
МКБ 10: Пункт C88 Злокачественные иммунопролиферативные болезниСостав пункта
- C88.0 Макроглобулинемия Вальденстрема
- C88.1 Болезнь альфа-тяжелых цепей
- C88.9 Злокачественные иммунопролиферативные болезни неуточненные
- C88.2 Болезнь гамма-тяжелых цепей
- C88.3 Иммунопролиферативная болезнь тонкого кишечника
- C88.4 Экстранодальная B-клеточная лимфома краевой зоны, ассоциированная с лимфоидной тканью слизистой оболочки
- C88.7 Другие злокачественные иммунопролиферативные болезни
Материалы по лечению заболевания в системе Консилиум
- Клинические рекомендации
- Памятки для пациентов: готовые материалы, чтобы распечатать
- Критерии качества лечения
- Справочники: полезные в повседневной работе документы (шкалы, таблицы, алгоритмы и т.д.).
- Стандарты: материалы для подготовки к проверкам и экспертизам.
Забрать материалы
C88 Злокачественные иммунопролиферативные болезни входит в:
Класс II. C00-D48 Новообразования
Группы новообразований
- C00-C75 Злокачественные новообразования уточненных локализаций, которые обозначены как первичные или предположительно первичные, кроме новообразований лимфоидной, кроветворной и родственных им тканей
- C76-C80 Злокачественные новообразования неточно обозначенные, вторичные и неуточненных локализаций
- C81-C96 Злокачественные новообразования лимфоидной, кроветворной и родственных им тканей, которые обозначены как первичные или предположительно первичные
- C97-C97 Злокачественные новообразования самостоятельных (первичных) множественных локализаций
- D00-D09 In situ новообразования
- D10-D36 Доброкачественные новообразования
- D37-D48 Новообразования неопределенного или неизвестного характера
Примечания
1. Рубрики C76-C80 включают злокачественные новообразования с неточно обозначенной первичной локализацией или те, которые определены как «диссеминированные», «рассеянные» или «распространенные» без указаний на первичную локализацию. В обоих случаях первичная локализация рассматривается как неизвестная.
2. К классу II отнесены как новообразования независимо от наличия/отсутствия у них функциональной активности. Если необходимо уточнить функциональную активность, ассоциирующуюся с тем или иным новообразованием, можно использовать добавочный код из класса IV. Например, катехоламинпродуцирующая злокачественная феохромоцитома надпочечников кодируется рубрикой C74 с добавочным кодом E27.5.
3. Имеется ряд больших морфологических (гистологических) групп злокачественных новообразований: карциномы, включая плоскоклеточные и аденокарциномы; саркомы; другие опухоли мягких тканей, включая мезотелиомы; лимфомы (Ходжкина и неходжкинские); лейкоз; другие уточненные и специфические по локализации типы; неуточненные раки. Термин «рак» является общим и может использоваться для любой из вышеуказанных групп, хотя он редко употребляется по отношению к злокачественным новообразованиям лимфоидной, кроветворной и родственных им тканей. Термин «карцинома» иногда неверно используется как синоним термина «рак». В классе II новообразования классифицируются преимущественно по локализации внутри широких группировок, составленных на основе характера течения. В исключительных случаях морфология указывается в названиях рубрик и подрубрик.
4. Необходимо обратить внимание на особое использование в классе II подрубрики со знаком .8. Там, где необходимо выделить подрубрику для группы «другие», обычно используют подрубрику .7.
5. Рубрики C00-C75 классифицируют первичные злокачественные новообразования в соответствии с местом их возникновения. Многие трехзначные рубрики далее подразделяются на подрубрики в соответствии с различными частями рассматриваемых органов. Новообразование, которое захватывает две или более смежные локализации внутри трехзначной рубрики и место возникновения которого не может быть определено, следует классифицировать подрубрикой с четвертым знаком .8 (поражение, выходящее за пределы одной и более вышеуказанных локализаций), если такая комбинация специально не индексируется в других рубриках. Например, карцинома пищевода и желудка обозначается кодом C16.0 (кардия), в то время как карциному кончика и нижней поверхности языка необходимо кодировать подрубрикой C02.8. С другой стороны, карциному кончика языка с вовлечением нижней его поверхности следует кодировать в подрубрике C02.1, так как место возникновения (в данном случае кончик языка) известно. Понятие «поражение, выходящее за пределы одной и более вышеуказанных локализаций» подразумевает, что вовлеченные области являются смежными. Последовательность нумерации подрубрик часто соответствует анатомическому соседству локализаций, и кодировщик может быть вынужден обратиться к анатомическим справочникам, чтобы определить топографическую взаимосвязь.
Иногда новообразование выходит за пределы локализаций, обозначенных трехзначными рубриками внутри одной системы органов. Для кодирования таких случаев предназначены следующие подрубрики:
- C02.8 Поражение языка, выходящее за пределы одной и более вышеуказанных локализаций
- C08.8 Поражение больших слюнных желез, выходящее за пределы одной и более вышеуказанных локализаций
- C14.8 Поражение губ, полости рта и глотки, выходящее за пределы одной и более вышеуказанных локализаций
- C21.8 Поражение прямой кишки, заднего прохода [ануса] и анального канала, выходящее за пределы одной и более вышеуказанных локализаций
- C24.8 Поражение желчных путей, выходящее за пределы одной и более вышеуказанных локализаций
- C26.8 Поражение органов пищеварения, выходящее за пределы одной и более вышеуказанных локализаций
- C39.8 Поражение органов дыхания и внутригрудных органов, выходящее за пределы одной и более вышеуказанных локализаций
- C41.8 Поражение костей и суставных хрящей, выходящее за пределы одной и более вышеуказанных локализаций
- C49.8 Поражение соединительной и мягких тканей, выходящее за пределы одной и более вышеуказанных локализаций
- C57.8 Поражение женских половых органов, выходящее за пределы одной и более вышеуказанных локализаций
- C63.8 Поражение мужских половых органов, выходящее за пределы одной и более вышеуказанных локализаций
- C68.8 Поражение мочевых органов, выходящее за пределы одной и более вышеуказанных локализаций
- C72.8 Поражение головного мозга и других отделов центральной нервной системы, выходящее за пределы одной и более вышеуказанных локализаций
6. Злокачественные новообразования эктопической ткани следует кодировать в соответствии с упомянутой локализацией, например, эктопическое злокачественное новообразование поджелудочной железы должно кодироваться как относящееся к поджелудочной железе неуточненное (C25.9).
7. Для некоторых морфологических типов класс II предоставляет довольно узкую топографическую классификацию или вовсе не дает таковой. Топографические коды Международной классификации болезней в онкологии (МКБ-0) используются для всех новообразований по существу с помощью тех же трех- и четырехзначных рубрик, которые используются в классе II для злокачественных новообразований (C00-C77, C80), тем самым обеспечивая большую точность локализации для других новообразований [злокачественных вторичных (метастатических), доброкачественных, in situ, неопределенного или неизвестного характера]. Таким образом, учреждениям, заинтересованным в определении локализации и морфологии опухолей, следует пользоваться МКБ-0.
Открыть другие классы
Блок C81-C96 Злокачественные новообразования лимфоидной, кроветворной и родственных им тканей
- C81 Болезнь Ходжкина [лимфогранулематоз]
- C82 Фолликулярная [нодулярная] неходжкинская лимфома
- C83 Диффузная неходжкинская лимфома
- C84 Периферические и кожные T-клеточные лимфомы
- C85 Другие и неуточненные типы неходжкинской лимфомы
- C86 Другие уточненные типы T/NK-клеточной лимфомы
- C88 Злокачественные иммунопролиферативные болезни
- C90 Множественная миелома и злокачественные плазмоклеточные новообразования
- C91 Лимфоидный лейкоз [лимфолейкоз]
- C92 Миелоидный лейкоз [миелолейкоз]
- C93 Моноцитарный лейкоз
- C94 Другой лейкоз уточненного клеточного типа
- C95 Лейкоз неуточненного клеточного типа
- C96 Другие и неуточненные злокачественные новообразования лимфоидной, кроветворной и родственных им тканей
Все блоки
Материал проверен экспертами Актион Медицина
Справочно:
Международная классификация болезней — это:
- А. перечень наименований болезней в определенном порядке.
- Б. перечень диагнозов в определенном порядке.
- В. перечень симптомов, синдромов и отдельных состояний, расположенных по определенному принципу.
- Г. система рубрик, в которые отдельные патологические состояния включены в соответствии с определенными установленными критериями.
- Д. перечень (наименований) болезней, диагнозов и синдромов, расположенных в определенном порядке.
Источник
