Код по мкб гемобластозы
Содержание
- Описание
- Причины
- Симптомы
- Патогенез
- Классификация
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Гемобластозы.

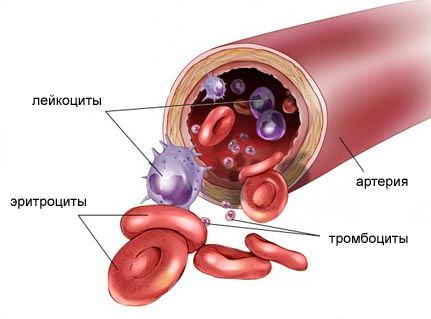
Гемобластозы — опухоли, развивающиеся из клеток кроветворной ткани
Описание
Гемобластозы — группа опухолей, развившихся из клеток кроветворной ткани. Гемобластозы подразделяются на три группы:
Лейкозы — злокачественные опухоли кроветворной тканис первичной локализацией в костном мозге с последующей диссеминацией в периферической крови, селезенке, лимфатических узлах и других тканях.
Гематосаркомы — внекостномозговые, первоначально локальные, опухоли (преимущественно в лимфатических узлах) представленные разрастанием бластных клеток, образующих солидные опухоли и с их возможной генерализацией в кроветворные органы, включая КМ.
Лимфомы — опухоли, состоящие из зрелых лимфоцитов и образованные разрастанием ткани идентичной лимфатическому узлу, но мало или совсем не поражающие КМ.
Причины
Причины гемобластозов окончательно не выяснены, но установлен ряд факторов, влияющих на частоту их развития.
1. ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ.
Доказательствами роли ионизирующего излучения в развитии лейкозов является значительное увеличение через 5-7 лет заболеваемости острым миелобластным лейкозом среди жителей японских городов Хиросима и Нагасаки, подвергшихся атомной бомбардировке, а также увеличение заболеваемости хроническим миелолейкозом среди пациентов, получавших лучевую терапию по поводу злокачественных заболеваний различной локализации. Ионизирующая радиация в основном способствует возникновению острого лейкоза и хронического миелолейкоза (ХМЛ), значительно реже лимфом. Малые дозы излучений, применяемые в медицине с диагностической целью, не влияет начастоту развития лейкозов.
2. ХИМИЧЕСКИЕ СОЕДИНЕНИЯ И ЛЕКАРСТВЕННЫЕ СРЕДСТВА.
Накоплены сведения о возможном лейкозогенном действии некоторых химических веществ: бензол, летучие органические растворители, ряд лекарственных препаратов: хлорамфеникол и особенно цитостатики (лейкеран, миелосан, азотиоприм, циклофосфан).
Хроническое воздействие бензола имеет место при длительном курении, причем не только у активных, но и у пассивных курильщиков. У мужчин, выкуривающих 20 пачек сигарет в год, риск заболеть острым миелоидным лейкозом в течение жизни в 3-4 раза выше по сравнению в некурящими. Считают, что 24% случаев смерти от миелоидного лейкоза связаны с курением сигарет.
Определенную роль в развитии лейкозов могут играть химиотерапевтические вещества, применяемые для лечения злокачественных новообразований. Наиболее лейкозогенными считаются мелфалан, миелосан, азатиоприн, циклофосфамид.
Хлорамфеникол вызывает аплазию КМ с исходом в острый миелоидный лейкоз.
3. ВИРУСЫ.
Подтверждено вирусное происхождение лейкозов и лимфом у крупного рогатого скота, кур, мышей, крыс, кошек, обезьян. Относительно роли вирусов в возникновении лейкозов у человека следует заметить, что доказана лишь роль герпес-вируса Эпштейна-Барра в развитии лимфомы Беркитта и ретровируса HTLV в развитии Т-клеточного лимфолейкоза. Однако до настоящего времени не получено доказательств о том, что инфицирование только этими вирусами без влияния каких-либо дополнительных факторов становится причиной развития опухоли.
4. НАСЛЕДСТВЕННОСТЬ.
Некоторые хромосомные аномалии, в частности синдром Дауна (трисомия по 21-ой хромосоме), синдром Потау (трисомия по 13-ой хромосоме) предрасполагают к развитию миелоидных лейкозов. Заболеваемость возрастает при наследственных заболеваниях, сопровождающихся повышенной ломкостью хромосом — анемии Фанкони, атаксии-телеангиэктазии.
5. ОБМЕННЫЕ НАРУШЕНИЯ.
Некоторые метаболиты триптофана и тирозина, возникающие при нарушении обмена этих аминокислот, способны вызывать хромосомные мутации и оказывать иммуносупрессивное действие.
Симптомы
Гиперкальциемия. Изменение веса. Истощение. Лейкоцитоз. Моноцитоз. Нейтрофилез. Одышка. Потеря веса. Потливость. Тромбоцитоз. Увеличение СОЭ. Увеличение паховых лимфоузлов. Увеличение подмышечных лимфоузлов. Увеличение шейных лимфоузлов.
Патогенез
В настоящее время общепризнанной является клоновая теория патогенеза гемобластозов, согласно которой лейкозные клетки являются потомством одной мутировавшей гемопоэтической клетки-предшественницы. Мутация родоначальной кроветворной клетки происходит под влиянием этиологических факторов и заключается в повреждении генетического аппарата клетки, в результате чего гемопоэтическая клетка приобретает способность к гиперпролиферации и утрачивает способность дифференцироваться.
Лейкозы в своем развитии проходят два этапа: первый — образование доброкачественной моноклоновой опухоли; второй — формирование злокачественной опухоли с признаками поликлоновой трансформации. Первый этап формирования лейкозов начинается с мутации родоначальной кроветворной клетки, она приобретает способность интенсивно пролиферировать и дает потомство клеток — клон. На этом этапе опухоль состоит из клеток, не имеющих признаков атипизма, эти клетки еще сохраняют способность к дифференциации, нет метастазирования в органы и ткани (доброкачественный опухолевый рост). Потомство (клон) мутировавшей клетки характеризуется высокой предрасположенностью к повторным мутациям, что связано с нестабильностью клеточного генома. Поэтому на втором этапе развития лейкозного клона вследствие повторных мутаций опухолевых клеток появляются новые субклоны, характеризующиеся чрезвычайно высокой способностью к мутациям, опухоль становится поликлоновой и приобретает черты злокачественной. Опухолевые клетки по-прежнему интенсивно пролиферируют, но одновременно утрачивают способность к дифференциации. Далее опухолевый клон начинает развиваться по законам опухолевой прогрессии:
Угнетение нормальных ростков кроветворения в костном мозге;
Замена в опухолевой массе дифференцированных клеток бластами, которые теряют способность к дифференциации и нередко вообще становятся морфологически и цитохимически недифференцированными;
Появление способности лейкозных клеток расти и размножаться вне органов кроветворения;
Уход лейкозных клеток из-под контроля цитостатической терапии.
В результате опухолевой прогрессии формируется клиническая картина лейкоза.
Классификация
В настоящее время лейкозы классифицируют, как правило, на основании морфологических и цитохимические особенности субстратных клеток (клеток, составляющих субстрат опухоли).
Прежде всего, лейкозы подразделяются на острые и хронические. Подразделение лейкозов на острые и хронические подразумевает не течение лейкоза, а тот морфологический субстрат, который лежит в основе заболевания. При острых лейкозах — это бластные, недифференцированные клетки, а при хронических лейкозах — это созревающие и морфологически зрелые элементы крови.
Среди множества различных классификаций острых лейкозов наибольшее признание получила классификация франко-американо-британской группы (FAB, 1976), на основе которой выделяют миелоидные и лимфобластные формы острого лейкоза. В свою очередь в группе острых миелоидных лейкозов выделяют 8 их вариантов, а в группе острых лимфобластных лейкозов – 3 типа.
FAB-классификация.
ОМЛ разделяют на восемь классов:
М0 — ОМЛ с минимальным созреванием клеток — 3 %.
М1 — острый миелобластный лейкоз без созревания клеток — 16 %.
М2 — острый миелобластный лейкоз с созреванием клеток — 32 %.
М3 — острый промиелоцитарный лейкоз — 10 %.
М4 — острый миеломоноцитарный лейкоз — 19 %.
М5 — острый моноцитарный лейкоз — 14 %.
М6 — острый эритролейкоз — 6 %.
М7 — острый мегакариобластный лейкоз — менее 1 %.
ОЛЛ разделяется на три класса:
L1- с малыми размерами бластов;
L2 – с крупным размерами бластов;
L3 – с бластными клетками типа клеток при лимфоме Беркитта.
Хронические лейкозы подразделяются на лейкозы миелогенного и лимфогенного происхождения. Основываясь на количестве лейкоцитов в единице объема крови, лейкозы подразделяют на: лейкемические (количество лейкоцитов выше 60 000); сублейкемические (количество лейкоцитов от 6000-60000); алейкемические (количество лейкоцитов ниже нормы).
Лечение
Комплексное лечение первичных злокачественных опухолей костей позволило в последнее время значительно увеличить процент 5-летнего выживания. Помимо ампутации и экзартикуляции пораженной конечности, выполняют органосохраняющие операции: удаление опухоли с резекцией кости. Широко применяют полихимиотерапию: противоопухолевые антибиотики (адреомицин, фармарубицин, блеомицин), соединения платины (платизиам), антиметаболиты (метотрексат) пред- и послеоперационными курсами или как самостоятельное лечение, в том числе при метастазах в кости. Гормональные препараты используются при метастазах рака молочной железы (антиэстрогены), предстательной железы (антиандрогены). Лучевая терапия первичных и метастатических опухолей костей осуществляется гамма-излучением или тормозным излучением на линейном ускорителе электронов в дозе на очаг 40 Гр при комбинированном лечении или 60-70 Гр в качестве самостоятельного лечения статическим методом с 2-3 полей или методом подвижного облучения. При метастазах рака щитовидной железы используется радиоактивный йод, рака молочной и предстательной желез — остеотропный препарат метастрон, содержащий радиоактивный 89Sr.
Лучевые оститы возникают после лучевой терапии злокачественных опухолей, реже других заболеваний. Участки некроза костной ткани с их резорбцией и вяло текущими репаративными процессами сопровождаются изменениями кожи и индуративным отеком подкожной клетчатки. Возможны патологические переломы. Эти изменения нужно отличать от рецидивов и метастазов опухолей.
Основные медуслуги по стандартам лечения | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 января 2020;
проверки требует 1 правка.
Гемобластозы (лат. haemoblastosis; др.-греч. αἷμα «кровь» + βλαστός росток, зародыш + -osis) — опухолевые (неопластические) заболевания кроветворной и лимфатической ткани.
Гемобластозы подразделяют на системные заболевания — лейкозы, а также регионарные — лимфомы.
Отличия между лейкозами и лимфомами заключаются не только в наличии или отсутствии системности поражения. В терминальной стадии лимфомы дают обширные метастазы, в том числе и в костный мозг. Но при лейкозах костный мозг поражается первично, а при лимфомах — вторично в результате метастазирования. При лейкозах опухолевые клетки, как правило, обнаруживаются в крови, поэтому в литературе используется термин для обозначения лейкозов, предложенный ещё Р. Вирховом — «лейкемия».
Эпидемиология[править | править код]
Опухоли кроветворной и лимфоидной ткани в числе пяти самых распространенных опухолей человека. Среди опухолей детей первых 5 лет жизни на их долю приходится 30 % случаев.
Этиология[править | править код]
Факторы, способствующие возникновению гемобластозов.
- Разнообразные мутагенные факторы экзогенного и эндогенного происхождения.
- Наследственность. Её роль подтверждается частым развитием лейкозов у людей с наследственными заболеваниями со спонтанными разрывами хромосом (болезнь Дауна, Блума, анемия Фанкони), с нерасхождением половых хромосом (болезни Клайнфельтера, Тернера), а также существованием «лейкозных семей». Нередко лейкозы развиваются у пациентов с наследственными дефектами иммунитета (атаксия-телеангиэктазия, или синдром Луи-Бар, синдром Вискотта-Олдриджа, болезнь Братона).
- Ионизирующая радиация. Её роль доказывается наблюдениями за пациентами, заболевшими лейкозами и лимфомами через определенное время после атомной бомбардировки Японии, аварий на АЭС, ядерных испытаний. Описаны случаи заболеваний у людей, получавших радиотерапию, а также у врачей-радиологов. Известен цитогенетический маркер радиационного поражения — кольцевидная хромосома. Достоверно установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эритромиелолейкоза и острого лимфобластного лейкоза у детей.
- Химические канцерогены. Их роль доказывается данными экспериментов, наблюдениями за пациентами, работавшими на вредных предприятиях с использованием бензола, а также за больными, получавшими цитостатическую терапию по поводу других онкологических заболеваний. Использование таких цитостатических препаратов, как мелфалан, азатиоприн, лейкеран, миелосан, антибиотика левомицетина, может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобластного лейкоза и эритромиелоза.
- Вирусы. В развитии гемобластозов человека доказано участие двух вирусов: вируса Эпштейна — Барр (африканская лимфома Беркитта) и T-лимфоцитарного вируса лейкоза человека первого типа (T-клеточная лимфома и клеточные лейкозы). Имеются экспериментальные данные, указывающие прямое канцерогенное действие вирусов на гемопоэтические клетки посредством вирусных онкогенов. Однако в большинстве ситуаций внедрение вирусов в клетку вызывает лишь иммортализацию (бессмертие) последней, на фоне которой возникают дополнительные перестройки генома, ведущие к злокачественной трансформации (многоступенчатый канцерогенез).
Патогенез[править | править код]
Всё множество этиологических факторов, воздействуя на стволовые и полустволовые гемопоэтические клетки, приводят к одинаковым результатам — злокачественной трансформации.
Например, при лимфоме Бёркитта происходит реципрокная транслокация между хромосомами 8 и 14q32. Клеточный онкоген c-myc из хромосомы 8 перемещается на хромосому 14 и попадает в зону действия генов, регулирующих синтез тяжёлых цепей иммуноглобулинов. Описанные изменения сочетаются также с точечной мутацией N-ras.
При хроническом миелолейкозе нередко встречается филадельфийская хромосома, образовавшаяся в результате реципрокной транслокации между хромосомами 9 и 22. Образуется новый ген-гибрид c-abl-bcr, белковый продукт которого обладает тирозинкиназной активностью. Онкогены обычно встраиваются в разрывы хромосом. Так, при B-лимфоцитарных лимфомах и лейкозах происходят разрывы в хромосоме 14 в локусе 32q, где локализуются гены тяжёлых цепей иммуноглобулинов. При T-лимфоцитарных лейкозах и лимфомах — в локусе 11q гена α-цепей рецепторов T-лимфоцитов.
Морфогенез[править | править код]
Развитие гемобластозов начинается с малигнизации одной стволовой или полустволовой клетки, дающей пул опухолевых клеток. Это означает, что все гемобластозы имеют моноклоновое происхождение. Моноклоновость происхождения подтверждается экспериментальными и клиническими данными по обнаружению во всех опухолевых клетках одного и того же больного клоновой метки — хромосомной или изоферментной. Например, во всех опухолевых клетках при хроническом миелолейкозе присутствует филадельфийская хромосома.
Стволовые клетки составляют примерно 0,01—0,001 % всей популяции костномозговых клеток. Рост и дифференцировка стволовых и полустволовых клеток-предшественниц управляются факторами роста и стромальным микроокружением. Это подтверждается экспериментами с клеточными культурами, где рост и дифференцировка клеток происходят только в присутствии факторов роста или стромальных клеток.
Многочисленные работы по изучению морфологии и клеточной кинетики гемобластозов (в первую очередь лейкозов) показали, что при их развитии происходит не только малигнизация на уровне стволовых и полустволовых клеток-предшественниц, но также развивается блок дифференцировки в пуле опухолевых клеток.
Литература[править | править код]
- Краткая Медицинская Энциклопедия — Петровский Б.В., 1984
- Патологическая анатомия. Курс лекций. Под ред. В. В. Серова, М. А. Пальцева. — М.: Медицина, 1998
См. также[править | править код]
- Лейкозы
- Лимфомы
- Опухоль
Ссылки[править | править код]
- Гемобластозы, европейская онкологическая школа, видео
Источник
Гемобластозы
— это группа опухолей, возникших из
кроветворных клеток. Опухоль — это плохо
контролируемая организмом плюсткань,
которая возникла из одной мутировавшей
клетки. Она не является следствием
воспаления или накопления неметаболизированных
продуктов. Гемобластозы, при которых
костный мозг повсеместно заселен
опухолевыми клетками, называют лейкозами.
Кроме лейкозов, в группу гемобластозов
входят гематосаркомы, возникшие из
кроветворных клеток, но представляющие
собой внекостномозговые разрастания
бластных клеток; и лимфомы — опухоли,
состоящие из зрелых лимфоцитов, но мало
или совсем не поражающие костный мозг.
Гемобластозы — это
группа опухолей, возникших из кроветворных
клеток. Опухоль — это плохо контролируемая
организмом плюсткань, которая возникла
из одной мутировавшей клетки. Она не
является следствием воспаления или
накопления неметаболизированных
продуктов. Гемобластозы, при которых
костный мозг повсеместно заселен
опухолевыми клетками, называют лейкозами.
Кроме лейкозов, в группу гемобластозов
входят гематосаркомы, возникшие из
кроветворных клеток, но представляющие
собой внекостномозговые разрастания
бластных клеток и лимфомы — опухоли,
состоящие из зрелых лимфоцитов, но мало
или совсем не поражающие костный мозг.
Классификация гемобластозов
(по А. И. Воробьеву
и М. Д. Бриллианту)
ПЕРВИЧНОЕ ПОРАЖЕНИЕ
КОСТНОГО МОЗГА (ЛЕЙКОЗЫ)
I.
Острые лейкозы* (17 – острые нелимфобластные
лейкозы (чаще встречаются у взрослых
больных)
Миелобластный
(ОМЛ)Миеломонобластный
(ОММЛ)Монобластный
(ОмнЛ)Промиелоцитарный
(ОПЛ)Острый эритромиелоз
(ОЭМ)Плазмобластный
(ОпбЛ)Мегакариобластный
(ОмкЛ)Лимфобластный
(ОЛЛ) – чаще встречается у детей.Макрофагальный
Малопроцентный
Недифференцируемый
острый лейкоз.
II.
Хронические лейкозы
Хронический
миелолейкозСублейкемический
миелозЭритремия
(полицитемия, болезнь Вакеза)***Хронический
моноцитарный лейкозХронический
лимфолейкозПарапротеинемические
гемобластозы
а) миеломная болезнь
б) макроглобулинемия
Вальденстрема
в) болезнь тяжелых
цепей
ОПУХОЛЕВЫЙ РОСТ
ВНЕ КОСТНОГО МОЗГА
(ЛИМФОМЫ)
Лимфогранулематоз
(болезнь Ходжкина)****Неходжкинские
лимфомы (Гематосаркомы)**
а) лимфосаркома
б) миелобластная
саркома
в) монобластная
саркома
г) эритробластная
саркома
д) плазмобластная
саркома
е) макрофагальная
саркома
ж) недифференцируемая
гематосаркома
*В основу первых
классификаций острого лейкоза была
заложена клиническая симптоматика. В
соответствии с нею выделяли следующие
формы острых лейкозов: геморрагическую,
язвеннонекротическую, анемическую,
туморозную. В настоящее время в связи
с ранним применением комплекса лечебных
мероприятий, прежде всего цитостатических
средств, такое разделение потеряло
смысл. В то же время возникла насущная
практическая потребность разграничения
стадий процесса, определяющих особенности
лечебной тактики. Клиникогематологически
выделяют первую атаку заболевания (I
стадия), ремиссию (II
стадия), рецидив заболевания (III
стадия), полную клиникогематологическую
ремиссию (IV
стадия) и терминальную стадию острого
лейкоза.
С целью унифицированного
объединения цитохимических и
морфологических основ дифференциации
острых лейкозов в 19761980 гг. гематологами
Франции, США и Великобритании была
создана ФАБ (FAB)классификация,
которая в настоящее время в силу своей
четкости приобретает все большее
распространение. По ФАБклассификации
острые лейкозы разделены на 3 группы:
нелимфобластные
миелогенные (миелоидные) лейкозы (6
типов);лимфобластные (3
типа);миелопоэтические
дисплазии или миелодиспластический
синдром (МДС) – 4 типа.
Нелимфобластные
острые лейкозы включают:
М0острый
недифференцированный лейкоз (около 2%
встречаемость) – редкий вариант лейкоза,
преимущественно лиц молодого возраста.
В настоящее время общепризнано, что
данный вариант заболевания не поддается
дифференциации изза ограниченности
методологических возможностей. Несмотря
на то, что морфологический облик клеток
при этом виде острого лейкоза при
электронной микроскопии идентичен
лимфобластам, биохимические свойства
этих клеток свойственны нелимфобластным
острым лейкозам, что и заставило
предположить миелоидную природу
клеточного субстрата ОНЛ, тем более,
что клиническая симптоматика и характер
клеточного ответа на лечение более
соответствуют ОНЛЛ;
М1острый
миелобластный лейкоз без признаков
вызревания клеток (около 20% встречаемость);
М2острый
миелобластный лейкоз с признаками
вызревания клеток (около 30% встречаемость);
М3острый
промиелоцитарный лейкоз (около 8%
встречаемость);
М3м
(подтип)микрогранулярный промиелоцитарный
лейкоз (может быть идентифицирован
только с помощью электронной микроскопии);
М4острый
миеломонобластный (миеломоноцитарный)
лейкоз (около 28% встречаемость);
М5острый
монобластный (моноцитарный) лейкоз
(около 10% встречаемость);;
М5а
(подтип)без
созревания клеток;
М5б(подтип)с
частичным созреванием клеток;
М6острый
эритромиелоз (эритролейкемия, эритролейкоз)
— (около 4% встречаемость).
М7
(выделяется не всеми авторами)мегакариобластный
острый лейкоз – очень редкая форма.
Лимфобластные
острые лейкозы включают (цитоморфологически):
Л1острый
микролимфобластный лейкоз (чаще
встречается у детей) – преобладают
малые лимфоидные клетки, иногда без
ядрышка и без иммунологических маркеров;
Л2острый
лимфобластный лейкоз с типичными
лимфобластами (чаще встречается у
взрослых);
Л3острый
макро или пролимфобластный лейкоз
(преобладают весьма крупные бластные
клетки (характерные для лимфомы Беркитта)
с нежносетчатым хроматином ядра и
базофильной цитоплазмой).
По иммунологической
классификации вначале выделяли: острый
Тлимфобластный лейкоз, острый
Влимфобластный лейкоз и нульОЛЛ или ни
Т, ни Вострый лимфолейкоз. В настоящее
время иммунологическая классификация
острых лейкозов значительно расширена:
с выделением общего (common)
антигена острого лимфобластного лейкоза
(CALLA),
который свойственен предшественникам
Т и Влимфоцитов и исчезает с появлением
дифференцировки в сторону Т или
Влимфопоэза, в соответствии с наличием
или отсутствием этого антигена на
бластных клетках, не имеющих ни В, ни
Тхарактеристик, из группы нульОЛЛ был
выделен общий ОЛЛ (ООЛЛ); с дальнейшим
изучением ОЛЛ, за счет нульОЛЛ и ООЛЛ
намечается тенденция к расширению
Вклеточных его вариантов. Также сейчас
выделяют преТОЛЛ и преВОЛЛ.
Так как антигены
миелобластных клеток слабее, чем у
лимфобластных, в 20% случаев ОЛ возникают
сложности идентификации его варианта.
Выявление дополнительных клеточных
маркеров обогащает имеющиеся
морфоцитохимические классификации,
что способствует уточнению варианта
ОЛ в сомнительных случаях и позволяет
выявлять новые цитогенетические феномены
(так, например: наличие гибридных форм
ОЛ, при которых бластные клетки могут
нести одновременно маркеры 2 и более
линий гемопоэза: эритроидной и
гранулоцитарной, эритроидной,
гранулоцитарной и мегакариоцитарной,
а главное – миелоидной и лимфоидной
(подобных бластных клеток в нормальном
кроветворении нет!). Таким образом, суть
современной классификации острых
лейкозов в интеграции имеющихся
представлений о цитоморфологических,
метаболических, иммунофенотипических,
кинетических, генетических и
дифференцировочных особенностях
лейкозных клеток.
Миелопоэтические
дисплазии или миелодиспластический
синдром (МДС) подразделяют на первичные
и вторичные. Последние развиваются
вследствие воздействия лучевой или
цитостатической химиотерапии.
ФАБклассификация включает только
первичные миелодисплазии:
Рефрактерная
анемия (РА);РА с избытком
кольцевых сидеробластов или сидеробластная
анемия (СА) с рингформами;РА с избытком
бластов (РАИБ);РАИБ и бластной
трансформацией (РАИБтрансф);Хронический
миеломоноцитарный лейкоз (ХММЛ).
**В классификации
ВОЗ (1976), принятой в России, для обозначения
отдельных вариантов неходжкинских
лимфом (лимфосарком) использована
гематологическая терминология. В
Кильской классификации (1974), принятой
в большинстве стран Европы, и в
классификации Lukes
и Collins
(1974), распространенной в США, которые
близки по сути, дана более подробная
морфологическая (в классификации Lukes
и Collins
также и иммунологическая) расшифровкаотдельных
вариантов неходжкинских лимфом.
В рабочей схеме
(WF,
1982), составленной ведущими
специалистамиэкспертами мира, сделана
попытка объединить все классификации,
при этом выделены 3 прогностические
группы неходжкинских лимфом с указанием
степени злокачественности:
I.
Низкая степень злокачественности:
а) из малых лимфоцитов
б) фолликулярная,
из малых расщепленных клеток
в) фолликулярная,
смешанная из малых расщепленных и
больших клеток
II.
Промежуточная степень злокачественности:
г) фолликулярная,
из больших клеток (расщепленных и
нерасщепленных)
д) диффузная из
малых расщепленных клеток
е) диффузная,
смешанная из малых расщепленных и
больших клеток
ж) диффузная, из
больших клеток
III.
Высокая степень злокачественности:
з) из больших клеток
иммунобластов
и) из лимфобластов
к) из малых
нерасщепленных клеток (тип Беркитта)
Разные (грибовидный
микоз, гистиоцитарная и прочие).
NB!
REAL
– Евроамериканский пересмотр, утверждена
ВОЗ в 1994 году – не выделяют промежуточную
степень злокачественности!
***Клинико-гематологическая
классификация истинной полицитемии
(Коцюбинский Н. Н.
, 1982)
I
стадия. Давность заболевания, как
правило, небольшая. Самочувствие
удовлетворительное. Умеренное повышение
количества эритроцитов и уровня
гемоглобина. Число лейкоцитов и
тромбоцитов нормальное. Очаговая
гиперплазия костного мозга в трепанате.
II
стадия А (стадия развернутых клинических
проявлений без миелоидной метаплазии
селезенки). Характеризуется значительным
нарушением общего состояния, выраженная
плетора, умеренное увеличение селезенки
и печени. Может быть повышено артериальное
давление. Панцитоз при отсутствии сдвига
в лейкоцитарной формуле влево. Тотальная
трехростковая гиперплазия костного
мозга. Нет признаков экстрамедуллярного
кроветворения.
II
стадия В. Характеризуется также
выраженными клиническими проявлениями,
но с миелоидной метаплазией селезенки.
В костном мозге могут быть очаги
миелофиброза.
III
стадия (терминальная, часто анемическая).
Характерно выраженное увеличение
селезенки, печени. Развивается
тромбоцитопения. Может быть исход в
миелофиброз, Ол или хронический
миелолейкоз.
****В настоящее время
общепринятой является международная
классификация (Peters,
1965 с изменениями Ан. Арбор, 1971):
I
стадия – поражение одной группы
лимфоузлов или изолированное (очаговое)
поражение вне лимфатической системы.
II
стадия – поражение двух или более групп
лимфатических узлов по одну сторону
диафрагмы или изолированное поражение
органа вне лимфатической системы с
вовлечением одной или более групп
лимфоузлов на той же стороне диафрагмы.
III
стадия — поражение лимфатических узлов
(органов лимфатической системы) по обе
стороны диафрагмы, которые могут
сочетаться с локализованным поражением
одного из органов вне лимфатической
системы или селезенки.
IV
стадия – диффузные или диссеминированные
поражения одного или нескольких органов
вне лимфатической системы независимо
от того, имеются или нет одновременно
поражения лимфоузлов. Любое поражение
поражение и костного мозга относится
к IV
стадии!
Указывают также:
S
– поражение селезенки; Е – поражение
других экстранодальных органов (печень,
легкие).
Все стадии разделяются
на две группы: без интоксикации (А) и с
явлениями интоксикации (Б). Проявлениями
интоксикации являются: необъяснимая
потеря массы тела >, чем на 10% за 6 месяцев
до обращения к врачу; проливные ночные
поты, лихорадка выше 38С,
не объяснимая другими причинами, в
течение 5и дней; генерализованный кожный
зуд (не изолдированный!).
Количество
лимфатических коллекторов, пораженных
процессом, указывается цифрами.
Биологические
признаки лимфогранулематоза: а –
отсутствуют, в – присутствуют (основные
– СОЭ >30 мм в час, лейкоцитоз > 10х109/л,
гиперглобулинемия, гиперфибриногенемия
и др. )
Символ «Х» —
массивность поражения (это отношение
поперечника грудной клетки к поперечнику
средостения на уровне IV
межреберья (в норме менее 1/3, а если более
– это указывает на массивность поражения).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
