Код мкб постреанимационная болезнь
Содержание
- Описание
- Дополнительные факты
- Причины
- Патогенез
- Классификация
- Симптомы
- Возможные осложнения
- Диагностика
- Лечение
- Список литературы
Названия
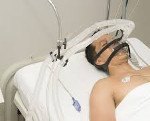
Название: Постреанимационная болезнь.

Постреанимационная болезнь
Описание
Заболевание после реанимации. Специфическое состояние организма, возникающее после успешной реанимации. Это вызвано временной ишемией общей ткани и синдромом восстановления кровотока. Это проявляется в выраженном повышении концентрации ферментов крови, гипоперфузии, снижении ОЦК, развитии диссеминированного внутрисосудистого свертывания и недостаточности нескольких органов. Это диагностируется наличием соответствующих симптомов и остановки сердца в недавнем прошлом. Конкретные методы лечения включают гормоны, кардиотоники, инфузии солевого раствора и компонентов крови, противоишемические и ноотропные препараты.
Дополнительные факты
Впервые постреанимационная болезнь (PRD) как самостоятельная нозологическая единица была описана советским ученым, членом Академии медицинских наук им. В. А. Неговского в 1979 году. Работы других специалистов расширили и укрепили знания о патологии, тем самым укрепляя позиции реаниматологии как науки в медицинском мире. Согласно статистическим данным, более половины пациентов, перенесших сердечно-легочную смерть (СЛР), умирают от острой недостаточности кровообращения или изменений в головном мозге, вызванных глобальной ишемией. Выживание после успешных событий CPR, согласно различным источникам, колеблется от 29 до 40%. Постэкзитативное заболевание возникает в первые часы после восстановления перфузии, оно занимает 7-10 дней. Прогноз на жизнь ухудшается пропорционально времени, прошедшему от остановки сердца до начала реанимации.
Постреанимационная болезнь
Причины
PSR развивается под влиянием нескольких патогенетических факторов, которые влияют на пациента, который перенес клиническую смерть. Комплексное негативное воздействие на ослабленный болезнью организм приводит к значительным изменениям функций органов и ферментных систем, что может привести к смерти пациента. Основными этиологическими факторами формирования PRB являются: Длительный недостаточный запас O2 усиливает гибель части клеток. Во-первых, повреждение мозга (постреанимационная энцефалопатия) происходит как структура, наиболее чувствительная к гипоксии. Появляется спазм сосудов, компенсаторная тахикардия, уменьшается сердечный выброс, что усугубляет недостаток кислорода. Есть изменения в ткани миокарда, скелетных мышцах. Процессы миолиза начинаются с выброса продуктов распада мышц в кровь.
• Синдром реперфузии. В условиях гипоксии ткани переходят в режим анаэробного гликолиза, и клетки перестраиваются на этот путь производства энергии. Резкое восстановление кровотока и поступление большого количества кислорода приводит к чрезмерному накоплению его токсических форм, активации апоптоза и некрозу клеток.
• ЛЕД. Выявляется при шоковых состояниях, что проявляется образованием микротромбов в сосудистом русле. Последние блокируют просвет капилляров, ухудшают микроциркуляцию в тканях и вызывают образование множества мелких ишемических очагов. В будущем это в сочетании с другими факторами провоцирует полиорганную недостаточность. Они возникают как запаздывающий результат ДВС в тот момент, когда возможности системы гемостаза истощаются, концентрация факторов свертывания уменьшается. Состояние характеризуется практически полным отсутствием в плазме веществ, ответственных за образование сгустка крови. Это сопровождается развитием геморрагического синдрома.
• Метаболический шторм. После восстановления кровотока у пациентов отмечаются массовые изменения регуляторных механизмов гомеостаза. Подкисление внутренней среды происходит при снижении рН ≤ 7,34, уровень электролитов, в том числе калия, кальция и , Снижается. При активной инфузии бикарбоната натрия на стадии СЛР вместо ацидоза можно определить ятрогенный алкалоз. Снижение ОЦК обусловлено отложением части крови в печени, скелетных мышцах, селезенке.
Патогенез
Патогенез основан на изменениях, которые происходят в результате остановки сердца. У пациента развивается острая почечная недостаточность, вторичный септический шок, дыхательная недостаточность и сердечно-сосудистые заболевания, а также нарушение работы рецепторных структур. Вскрытие определяет дистрофические изменения в почках, и легкие часто показывают признаки двусторонней мультифокальной пневмонии. Большое количество миоглобина также обнаружено здесь. Ткани различной степени тяжести обнаруживаются в тканях. Мозг может содержать мертвые зоны, что свидетельствует о ишемическом инсульте. Со смертью мозга (декортация) наблюдаются необратимые изменения в туловище, шейных сегментах и коре.
Классификация
Посттравматическое заболевание систематизируется поэтапно, каждый из которых соответствует времени, прошедшему с момента восстановления кровотока. Согласно классификации Е. С. Златокрилин с 1999 года, существует 5 основных этапов развития PWB. Все они характеризуются определенными изменениями состояния пациента. Различают следующие этапы развития патологических изменений: Длится 6-8 часов после реанимации. Произошло явное снижение перфузии тканей (в 4-5 раз меньше нормы). Существуют явления гипоксии кровообращения — состояния, которое возникает при недостаточном давлении в капиллярах. Доходит до 10-12 часов болезни. Относительная стабилизация функций организма и временное улучшение состояния не отмечено. Наблюдается дефицит объема циркулирующей крови, кровоток в тканях уменьшается в 2-3 раза. Потери электролита, в основном К +, растут. Стадия имеет важное прогностическое значение, она позволяет с большой вероятностью определить дальнейшее течение и результат патологического состояния. Это наблюдается со второго дня заболевания. Плазменная фибринолитическая активность замедляется, образуется смешанная гипоксия, обусловленная изменением свойств гемоглобина и развитием респираторного дистресс-синдрома. Появляются первые признаки микротромбоза капиллярной сети внутренних органов. Нарушения носят функциональный характер, нет необратимых процессов. Переломный момент в развитии болезни. Это приходит через 3-4 дня. Может характеризоваться общим улучшением состояния или дальнейшим прогрессированием патологических изменений. При неблагоприятном результате усиливаются явления катаболизма, возникает интерстициальный отек легких, происходит гидрогенизация головного мозга. Начинается общий воспалительный ответ, выявляются признаки недостаточности внутренних органов. Это происходит в течение 5-7 дней. Диагностированы объемные септические процессы: пневмония, сепсис, внутренние абсцессы. Антибактериальная терапия малоэффективна. Причиной инфекции является подавление иммунитета из-за длительной гипоксии. Токсическая энцефалопатия проявляется в максимальной степени, обостряется полиорганная недостаточность, в крови накапливаются продукты обмена. Смерть больного наступает через 1-5 дней. Причиной смерти является поражение нескольких жизненно важных систем, токсический токсический шок, сепсис.
Симптомы
Есть много клинических симптомов PSD, которые указывают на негативные изменения. На начальном этапе у больного наблюдаются симптомы шока: мраморность кожного тона, резкое снижение артериального давления до неопределяемых значений, компенсаторная тахикардия, расширение зрачков. Обычно пациент находится в глубокой коме. Недостаток осознанности, физическая активность. Рефлексы резко подавлены или полностью выключены. Мышечный тонус снижен.
В будущем, изменения в частоте сердечных сокращений из-за недостатка электролитов и ишемических изменений в CVS обнаружены. Проводниковые блокады, аритмия проявляются в виде нерегулярного, фрагментарного пульса. Артериальное давление может оставаться низким или возвращаться к норме. Часто гемодинамика поддерживается лекарственными методами. Симптомы сердечной недостаточности и дыхательной системы видны — цианоз, цианоз и акоцианоз, которые сохраняются даже при искусственной вентиляции легких.
При обследовании пациента иногда обнаруживается небольшая петехиальная сыпь, что указывает на развитие геморрагического синдрома. Могут быть признаки внутреннего или внешнего скрытого кровотечения, включая рвоту «кофейной гущи», стул типа «мелена», прогрессирующую гипотензию, тахиаритмию, снижение уровня гемоглобина, гемоглобина и бледность кожи. При наличии изменений в печени слизистые оболочки и кожные покровы организма становятся желтоватыми. Поражение почек характеризуется резким снижением мочеиспускания или полным отсутствием мочи. При тяжелых изменениях в центральной нервной системе сохраняется бессознательное состояние, кома, сохраняется.
Рвота. Рвота с кровью.
Возможные осложнения
Осложнения PRB включают смерть мозга, при которой соматические функции поддерживаются, но центральная нервная система претерпевает необратимые изменения. Такие пациенты становятся вегетативными без надежды на выздоровление. Диагноз подтверждается результатами электроэнцефалографии. Серьезным следствием прерывания кровотока является отказ нескольких органов, при котором две или более систем организма выходят из строя. В большинстве случаев происходит разрушение почек, гепатобилиарной системы, легких, сердца, мозга. Возможно массивное кровотечение, при котором смерть пациента наступает из-за острой кровопотери.
Диагностика
Диагноз ставится на основании клинического, лабораторного и аппаратного исследования жизненно важных органов пациента. Реаниматолог-анестезиолог определяет состояние вместе со специалистами другого профиля (невролог, кардиолог, нефролог и ), Представителями лаборатории и службы функциональной диагностики. Как правило, нет никаких диагностических трудностей. Используйте такие методы, как:
• Физическое обследование. Он позволяет выявить внешние признаки PRB, выявить явные нарушения, связанные с изменениями сердечного ритма, снижением артериального давления и ухудшением дыхания в легких. Терапевтические меры начинаются по результатам первого медицинского заключения. Параллельно с интенсивной терапией применяются другие методы обследования ретроспективно. Повышение концентрации определенных ферментов (LDH, щелочная фосфатаза, CPK) обнаруживается в крови пациента. Имеются изменения в составе электролита и газа, увеличение гематокрита более 36-48%. По мере развития почечной недостаточности уровень мочевины, креатинина повышается. Содержание белка снижается.
• Аппаратные методы. Свидетельством смерти мозга является изоэлектрическая линия на ЭЭГ. Повреждение сердца приводит к появлению на пленке кардиографа признаков ишемии миокарда и аритмий различных типов: необычайно деформированных желудочковых комплексов, неравных интервалов RR, фибрилляции малой или большой волны, депрессии или повышения « ST ». При проведении сонографии можно обнаружить некротические участки внутренних органов.
Лечение
PSR требует ряда медицинских процедур, направленных на восстановление жизненно важных функций и функций мозга. Меры общего режима имеют важное значение, которые становятся особенно важными при длительном пребывании пациента в бессознательном состоянии. Ремонтные меры включают в себя: Актуален для оживших пациентов любого профиля. Требуется тщательный уход с ежедневным мытьем и сменой положения тела каждые 2 часа. Участки мацерации кожи обрабатывают камфорным спиртом или специализированными дерматозащитными средствами. При отсутствии острой почечной недостаточности указывается качественное белковое питание и чрезмерное употребление алкоголя. Невыполнение этих требований приводит к развитию пролежней, основательной интоксикации, увеличению нагрузки на иммунную систему и повышенному риску сепсиса.
• Медикаментозная терапия. Он направлен на защиту тканей от гипоксии, улучшение перфузии и стимулирование работы сердца и мозга. Такие группы препаратов используются как кардиотоники, амины давления, антигипоксические, микроциркуляторные, улучшающие микроциркуляцию, спазмолитики, ноотропы. Обязательна инфузионная терапия с использованием коллоидных и кристаллоидных растворов.
• Методы работы. Условно им может быть назначен гемодиализ, необходимый для удаления токсичных отходов. При почечной недостаточности плазмаферез проводится для устранения избыточного объема воды, содержащей продукты метаболизма. Полноценная операция PRB не разработана.
Список литературы
1. Постреанимационная болезнь / Неговский В. А. , Гурвич А. М. , Золотокрылина Е. С. – 1987.
2. Руководство по интенсивной терапии / Трещинский А. И. , Глумчера Ф. С. – 2004.
3. Сердечно-легочная реанимация, пособие для студентов, ординаторов, аспирантов и врачей / НИИ общей реаниматологии им. В. А. Неговского – 2017.
Источник
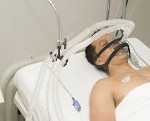
Постреанимационная болезнь – специфическое состояние организма, возникающее после успешных реанимационных мероприятий. Вызывается временной тотальной ишемией тканей и синдромом восстановления кровотока. Проявляется выраженным увеличением концентрации ферментов крови, гипоперфузией, уменьшением ОЦК, развитием диссеминированного внутрисосудистого свертывания, полиорганной недостаточностью. Диагностируется по наличию соответствующей симптоматики и остановки кровообращения в недавнем прошлом. Специфическое лечение включает гормоны, кардиотоники, инфузии солевых растворов и компонентов крови, противоишемические и ноотропные лекарственные средства.
Общие сведения
Впервые постреанимационная болезнь (ПРБ) как самостоятельная нозологическая единица была описана советским ученым, членом АМН В. А. Неговским в 1979 году. Труды других специалистов расширили и укрепили знания о патологии, тем самым упрочив в медицинском мире позиции реаниматологии как науки. Согласно статистической информации, более половины больных, перенесших сердечно-легочную смерть (СЛР), умирает от острой недостаточности кровообращения или изменений в головном мозге, вызванных глобальной ишемией. Выживаемость после успешных СЛР-мероприятий, по данным разных источников, составляет от 29 до 40%. Постреанимационная болезнь возникает в первые часы после восстановления перфузии, протекает 7-10 дней. Прогноз для жизни ухудшается пропорционально времени от остановки сердца до начала реанимационных мероприятий.
Постреанимационная болезнь
Причины
ПРБ развивается под действием нескольких патогенетических факторов, воздействующих на пациента, подвергшегося клинической смерти. Комплексное негативное влияние на ослабленный болезнью организм приводит к значительным изменениям в работе органов и ферментативных систем, что может послужить причиной гибели больного. К числу наиболее важных этиофакторов формирования ПРБ относятся:
- Тотальная ишемия. Длительное недостаточное поступление O2 потенцирует отмирание части клеток. В первую очередь происходит поражение головного мозга (постреанимационная энцефалопатия) как структуры, наиболее чувствительной к гипоксии. Наблюдается спазм сосудов, компенсаторная тахикардия, уменьшается сердечный выброс, что усугубляет кислородное голодание. Происходят изменения в тканях миокарда, скелетной мускулатуре. Начинаются процессы миолиза с выделением в кровь продуктов распада мышц.
- Синдром реперфузии. В условиях гипоксии ткани выходят на анаэробный режим гликолиза, клетки перенастраиваются на данный путь получения энергии. Резкое восстановление кровотока и поступление большого количества кислорода ведет к избыточному накоплению его токсичных форм, активации процессов апоптоза и некроза клеток.
- ДВС. Выявляется при шоковых состояниях, проявляется образованием в сосудистом русле микротромбов. Последние блокируют просвет капилляров, ухудшают микроциркуляцию в тканях, становятся причиной образования множественных мелких ишемических очагов. В дальнейшем это в сочетании с другими факторами провоцирует полиорганную недостаточности.
- Кровотечения. Возникают как отсроченный результат ДВС в момент, когда возможности системы гемостаза истощаются, концентрация факторов свертывания уменьшается. Состояние характеризуется практически полным отсутствием в плазме субстанций, ответственных за формирование тромба. Сопровождается развитием геморрагического синдрома.
- Метаболическая буря. После восстановления кровотока у больных отмечаются массивные изменения механизмов регуляции гомеостаза. Происходит закисливание внутренней среды со снижением pH ≤ 7,34, падает уровень электролитов, в том числе калия, кальция и прочих. При активном вливании натрия гидрокарбоната на этапе СЛР вместо ацидоза может определяться ятрогенный алкалоз. Выявляется уменьшение ОЦК за счет депонирования части крови в печени, скелетных мышцах, селезенке.
Патогенез
Патогенез основывается на изменениях, наступающих в результате остановки кровообращения. У больного развивается ОПН, вторичный септический шок, недостаточность дыхания и ССС, сбои в работе рецепторных структур. На вскрытии определяют дистрофические изменения в почках, в легких часто присутствуют признаки двухсторонней многоочаговой пневмонии. Здесь же выявляют большое количество миоглобина. В тканях обнаруживают кровоизлияния различной степени тяжести. Головной мозг может содержать отмершие участки, что свидетельствует о возникновении ишемического инсульта. При церебральной смерти (декортикация) отмечаются необратимые изменения ствола, шейных сегментов, коры больших полушарий.
Классификация
Постреанимационная болезнь систематизируется по стадиям, каждая из которых соответствует времени, прошедшему с момента восстановления кровотока. Согласно классификации Е.С. Златокрылиной от 1999 года, существует 5 основных этапов прогрессирования ПРБ. Все они характеризуются определенными трансформациями в состоянии пациента. Различают следующие фазы развития патологических изменений:
- Этап №1. Протекает на протяжении 6-8 часов со времени реанимационных мероприятий. Отмечается выраженное снижение тканевой перфузии (в 4-5 раз меньше нормы). Присутствуют явления циркуляторной гипоксии – состояния, возникающего при недостаточном давлении в капиллярах.
- Этап №2. Наступает к 10-12 часу болезни. Отмечается относительная стабилизация функций организма, временное улучшение состояния. Имеет место дефицит объема циркулирующей крови, тканевый кровоток снижен в 2-3 раза. Увеличиваются потери электролитов, преимущественно K+. Стадия имеет важное прогностическое значение, позволяет с высокой долей вероятности определить дальнейшее течение и исход патологического состояния.
- Этап №3. Наблюдается со вторых суток болезни. Замедляется фибринолитическая активность плазмы, формируется смешанная гипоксия, обусловленная изменением свойств гемоглобина и развитием респираторного дистресс-синдрома. Возникают первые признаки микротромбоза капиллярной сети внутренних органов. Нарушения носят функциональный характер, необратимые процессы отсутствуют.
- Этап №4. Переломный момент в течении болезни. Наступает к 3-4 дню. Может характеризоваться общим улучшением состояния или дальнейшим прогрессированием патологических изменений. При неблагоприятном исходе усиливаются явления катаболизма, возникает интерстициальный отек легких, гидрогенизация головного мозга. Начинается генерализованный воспалительный ответ, обнаруживаются признаки недостаточности внутренних органов.
- Этап №5. Манифестирует к 5-7 суткам. Диагностируются объемные септические процессы: пневмонии, сепсис, внутренние абсцессы. Антибактериальная терапия неэффективна. Причина инфекции – угнетение иммунитета из-за длительной гипоксии. Максимально проявляется энцефалопатия токсического происхождения, усугубляется полиорганная недостаточность, в крови накапливаются продукты обмена веществ. Гибель пациента наступает спустя 1-5 дней. Причиной смерти становится поражение нескольких жизненно важных систем, инфекционно-токсический шок, сепсис.
Симптомы постреанимационной болезни
Существует множество клинических признаков ПРБ, свидетельствующих о негативных изменениях. На начальном этапе у больного присутствует симптоматика шока: мраморный оттенок кожи, резкое снижение АД вплоть до неопределяемых значений, компенсаторная тахикардия, расширение зрачков. Как правило, пациент находится в глубокой коме. Отсутствует сознание, двигательная активность. Рефлексы резко угнетены или полностью выключены. Мышечный тонус снижен.
В дальнейшем выявляются изменения сердечного темпа по причине недостатка электролитов и ишемического поражения ССС. Возможны блокады проводимости, аритмии, что проявляется в виде неритмичного, отрывочного пульса. Артериальное давление может оставаться сниженным или приходить в норму. Часто гемодинамику поддерживают медикаментозными методами. Визуально различимы признаки сердечной и дыхательной недостаточности – диффузный цианоз и акроцианоз, сохраняющиеся даже при проведении искусственной вентиляции легких.
При осмотре больного иногда обнаруживается мелкая петехиальная сыпь, которая говорит о развитии геморрагического синдрома. Могут отмечаться признаки внутреннего или наружного скрытого кровотечения, в т. ч. рвота «кофейной гущей», стул по типу «мелены», прогрессирующая гипотония, тахиаритмия, уменьшение показателей Hb, Ht, бледность кожи. При наличии изменений со стороны печени слизистые оболочки и покровы тела приобретают желтоватую окраску. Поражение почек характеризуется резким уменьшением диуреза или полным отсутствием мочи. При тяжелых изменениях ЦНС сохраняется бессознательное состояние, кома.
Осложнения
К числу осложнений ПРБ относится смерть мозга, при которой соматические функции сохраняются, однако ЦНС подвергается необратимым изменениям. Такие пациенты переходят в вегетативное состояние без надежды на восстановление. Диагноз подтверждается по результатам электроэнцефалографии. Тяжелое последствие остановки кровотока – полиорганная недостаточность, при которой происходит отказ двух и более систем организма. В большинстве случаев деструкции подвергаются почки, гепатобилиарный аппарат, легкие, сердце, головной мозг. Возможно появление массивных геморрагий, при которых гибель больного наступает от острой кровопотери.
Диагностика
Диагноз устанавливают на основании клинического, лабораторного и аппаратного изучения работы жизненно важных органов пациента. Определением состояния занимается врач анестезиолог-реаниматолог в тандеме со специалистами другого профиля (неврологом, кардиологом, нефрологом и пр.), представителями службы лабораторной и функциональной диагностики. Обычно диагностические затруднения отсутствуют. Используют такие методы, как:
- Физикальный осмотр. Позволяет выявить внешние признаки ПРБ, определить очевидные нарушения, связанные с изменением сердечного ритма, снижением артериального давления, ухудшением дыхания в легких. Лечебные мероприятия начинают по результатам первичного врачебного заключения. Другие способы обследования применяют постфактум, параллельно с интенсивной терапией.
- Лаборатория. В крови больного обнаруживается рост концентрации некоторых ферментов (ЛДГ, ЩФ, КФК). Присутствуют изменения со стороны электролитного и газового состава, увеличение гематокрита более 36-48%. При развитии почечной недостаточности повышается уровень мочевины, креатинина. Уменьшается содержание белка.
- Аппаратные способы. Свидетельством смерти мозга является изоэлектрическая линия на ЭЭГ. Поражение сердца приводит к появлению на пленке кардиографа признаков ишемии миокарда и аритмий различного типа: внеочередных деформированных желудочковых комплексов, неодинаковых интервалов «R-R», мелковолновой или крупноволновой фибрилляции, депрессии или подъему сегмента «ST». При выполнении сонографии могут выявляться некротизированные участки во внутренних органах.
Лечение постреанимационной болезни
ПРБ требует проведения ряда лечебных процедур, направленных на восстановление жизненных функций и работы головного мозга. Существенное значение имеют общережимные мероприятия, которые становятся особенно важными при долговременном пребывании больного в бессознательном состоянии. К числу восстановительных мер относятся:
- Общие способы. Актуальны в отношении реанимационных пациентов любого профиля. Требуется тщательный уход с ежедневным мытьем и изменением положения тела каждые 2 часа. Участки мацерации кожи обрабатывают камфарным спиртом или специализированными дерматопротекторными средствами. При отсутствии ОПН показано полноценное белковое питание, обильное питье. Несоблюдение этих требований влечет за собой развитие пролежней, углубление интоксикации, усиление нагрузки на иммунную систему, повышение риска сепсиса.
- Медикаментозная терапия. Направлена на защиту тканей от гипоксии, улучшение перфузии, стимуляцию работы сердца, головного мозга. Применяются такие группы препаратов, как кардиотоники, прессорные амины, антигипоксанты, средства, улучшающие микроциркуляцию, спазмолитики, ноотропы. Показана обязательная инфузионная терапия с использованием коллоидных и кристаллоидных растворов.
- Оперативные методы. К их числу условно можно отнести проведение гемодиализа, необходимого для удаления токсичных продуктов обмена веществ. При почечной недостаточности осуществляется плазмаферез для устранения излишних объемов воды, содержащей продукты обмена. Полноценные операции, предназначенные для лечения ПРБ, не разработаны.
Прогноз и профилактика
Постреанимационная болезнь имеет неблагоприятный для жизни пациента прогноз. В течение первого полугодия погибает около 80% людей, подвергшихся длительной гипоксии. Среди больных, получивших помощь немедленно после остановки сердца, этот показатель значительно ниже. Причиной смерти становятся неврологические и сердечные заболевания, хроническая дыхательная недостаточность. Часть выживших подвергается постгипоксической энцефалопатии, при которой ухудшаются умственные способности. Профилактика заключается в своевременном начале СЛР, минимизации периода отсутствия кровотока, полноценной медикаментозной поддержке на всех этапах восстановительного процесса, начиная с первых его минут.
Источник
