История болезни системная склеродермия диффузная форма синдром рейно
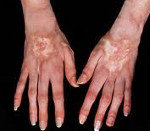

Системная склеродермия — диффузная патология соединительной ткани, для которой характерны фиброзно-склеротические изменения кожи, суставно-мышечного аппарата, внутренних органов и сосудов. Типичными признаками системной склеродермии служат синдром Рейно, уплотнение кожи, маскообразное лицо, телеангиэктазии, полимиозит, суставные контрактуры, изменения со стороны пищевода, сердца, легких, почек. Диагностика системной склеродермии основана на комплексе клинических данных, определении склеродермических аутоантител, биопсии кожи. Лечение включает антифиброзные, противовоспалительные, иммуносупрессивные, сосудистые средства, симптоматическую терапию.
Общие сведения
Системная склеродермия – коллагеноз с полисиндромными проявлениями, в основе которого лежит прогрессирующий фибросклероз кожных покровов, опорно-двигательного аппарата, висцеральных органов и сосудов. Среди болезней соединительной ткани занимает второе место по частоте встречаемости после системной красной волчанки. Патология детально описана еще в ХVII в., однако общепринятый термин «склеродермия» был введен в употребление лишь в середине ХIХ столетия, а детальное изучение заболевания в рамках ревматологии началось с 40-50-х г.г. прошлого века. Распространенность системной склеродермии колеблется от 6 до 20 случаев на 1 млн. человек. Женское население заболевает в 3-6 раз чаще, чем мужское; основную долю пациентов составляют лица в возрасте 30-60 лет. Системная склеродермия имеет медленно прогрессирующее течение, со временем приводящее к утрате трудоспособности.
Причины
Точные представления о причинах системной склеродермии отсутствуют. Накопленные наблюдения позволяют лишь высказывать отдельные этиологические гипотезы. В пользу генетической детерминированности свидетельствуют факты семейной истории системной склеродермии, а также наличие у ближайших родственников других склеродермических болезней, коллагенозов (СКВ, ревматоидного артрита, синдрома Шегрена), микроангиопатий, кардиопатий и нефропатий неизвестного генеза. Выявлена ассоциация склеродермии с определенными антигенами и аллелями HLA-системы, определяющими иммунный ответ, что также свидетельствует о наличии генетического следа в генезе патологии.
Наряду с наследственной теорией, широко обсуждается роль инфекции, в первую очередь цитомегаловирусной. Некоторые пациенты связывают дебют заболевания с перенесенным гриппом или стрептококковой ангиной. Ряд наблюдений указывает на триггерную роль химических агентов: кварцевой и угольной пыли, растворителей, лекарственных средств (в частности, блеомицина и других цитостатиков). Доказано участие вибрационного воздействия, стресса, охлаждения и обморожения, травм в запуске иммунопатологических сдвигов при системной склеродермии. Фоном для развития системного склероза может служить гормональная перестройка, обусловленная пубертатом, родами, абортом, климаксом. У отдельных пациентов началу заболевания предшествуют операции (удаление зуба, тонзиллэктомия и др.) и вакцинация. Т. о., на основании имеющихся данных можно сделать вывод о мультифакториальном генезе системной склеродермии, сочетающем в себе сложное взаимодействие эндо- и экзогенных факторов с наследственной предрасположенностью.
Патогенетические механизмы системной склеродермии изучены лучше этиологии. Ключевую роль в них играют нарушения клеточного и гуморального иммунитета, приводящие к повышению числа CD4+ и В-лимфоцитов, и реакция гиперчувствительности, обусловливающая образование широкого спектра аутоантител (антинуклеарных, антицентромерных, анти-Scl-70, антинейтрофильных, антиэндотелиальных, цитоплазматических, АТ к соединительной ткани и др.) и циркулирующих иммунных комплексов. Подобная иммунная активация способствует гиперактивности фибробластов и повреждению сосудистого эндотелия. Специфика заболевания определяется генерализованным склерозом органов и тканей (кожи, костно-суставной и мышечной системы, ЖКТ, сердца, легких, почек) и развитием облитерирующей микроангиопатии. Рассмотренный механизм позволяет отнести системную склеродермию к аутоиммунным заболеваниям.
Классификация
На сегодняшний день термином «склеродермия» обозначается группа заболеваний со сходными патогенетическими механизмами, протекающих с локальным или генерализованным фиброзом соединительной ткани. С позиций международной клинической классификации выделяют следующие формы склеродермических болезней: системная склеродермия, очаговая склеродермия, отечная склеродермия (склередема Бушке), эозинофильный фасциит, индуцированная склеродермия, мультифокальный фиброз, псевдосклеродермия.
Системная склеродермия (диффузная или генерализованная склеродермия, прогрессирующий системный склероз) может протекать в нескольких клинических формах:
- Пресклеродермия не имеет дерматологических проявлений и сопровождается только феноменом Рейно.
- Для диффузной склеродермии патогномонично стремительное развитие, поражение кожи, сосудов, мышечно-суставного аппарата и внутренних органов в течение первого года заболевания.
- Лимитированная форма протекает с медленно развивающимися фиброзными изменениями, преимущественным поражением кожных покровов и поздним вовлечением внутренних органов.
- При склеродермии без склеродермы отмечаются только висцеральные и сосудистые синдромы без типичных кожных проявлений.
- Перекрестная форма может проявляться сочетанием системной склеродермии с дерматомиозитом, полимиозитом, СКВ, РА, васкулитами.
Системная склеродермия может протекать в хронической, подострой и острой форме. При хроническом течении на протяжении многих лет единственным указанием на заболевание служит синдром Рейно; другие типичные поражения развиваются постепенно и длительно. При подостром варианте системной склеродермии преобладает кожно-суставной (склеродермия, полиартрит, полимиозит) и висцеральный синдром (сердечно-легочный) при незначительных вазомоторных нарушениях. Острая форма патологии отличается стремительным (в течение 12 мес.) формированием системного фиброза и микрососудистых нарушений. Различают три степени активности системной склеродермии: I – минимальную, типичную для хронического варианта; II – умеренную, обычно встречающуюся при подостром процессе; III – максимальную, сопровождающую течение острой и иногда подострой форм.
Симптомы системной склеродермии
Клиническая специфика системной склеродермии заключается в полиморфности и полисиндромности проявлений. Варианты развития болезни могут варьировать от маловыраженных форм с относительно благоприятным прогнозом до быстропрогрессирующих диффузных поражений с ранним фатальным исходом. В дебюте системной склеродермии, еще до появления специфических поражений, отмечается потеря веса, слабость, субфебрилитет.
Наиболее ранним признаком заболевания служит синдром Рейно, характерный для 99% пациентов и протекающий с преходящими пароксизмами вазоспазма. Под воздействием стресса или охлаждения пальцы рук резко бледнеют, затем кожа приобретает синевато-фиолетовую окраску. Сосудистый спазм может сопровождаться чувством зябкости и онемения кистей. После разрешения вазоконстрикции наступает стадия реактивной гиперемии: кожа становится ярко-розовой, появляется ощущение ломоты и боли в пальцах. Феномена Рейно при склеродермии может носить системный характер, т. е. распространяться на сосуды кожи лица, языка, почек, сердца и др. органов.
Кожный синдром присутствует у большинства больных системной склеродермией. В своей эволюции он проходит 3 фазы: воспалительного отека, уплотнения (индурации) и атрофии кожи. Начальную стадию характеризует появление плотного отека кожи рук и ног, сопровождающегося зудом. В дальнейшем развивается склеродактилия (утолщение кожи пальцев), образуются трофические язвы, деформируются ногти. Лобные и носогубные складки сглаживаются, в результате чего лицо приобретает маскообразное выражение. Вследствие атрофии сальных и потовых желез кожа становится сухой и грубой, лишенной волосяного покрова. Часто обнаруживаются телеангиэктазии, депигментация или гиперпигментация кожи, подкожные кальцинаты.
Мышечно-суставной синдром также часто сопутствует системной склеродермии. Типичны отечность и скованность суставов, артралгии – данный симптомокомплекс носит название склеродермического полиартрита. Вследствие уплотнения кожи формируются сгибательные контрактуры суставов, развиваются теносиновиты. Возможен остеолиз ногтевых фаланг, приводящий к укорочению пальцев. Поражение мышц при системной склеродермии протекает по типу полимиозита или невоспалительной миопатии.
Висцеральные поражения могут затрагивать ЖКТ (90% случаев), легкие (70%), сердце (10%), почки (5%). Со стороны органов пищеварения отмечается дисфагия, изжога, тошнота и рвота. Развивается рефлюкс-эзофагит, усугубляющийся образованием язв и стриктур пищевода. На этом фоне у больных системной склеродермией повышен риск формирования пищевода Барретта и аденокарциномы. При поражении тонкого кишечника возникает диарея, метеоризм, похудание; при вовлечении толстого кишечника – запоры и кишечная непроходимость.
Поражение легких при системной склеродермии может выражаться в виде пневмофиброза и легочной гипертензии. Оба синдрома проявляются непродуктивным кашлем, прогрессирующей экспираторной одышкой и дыхательной недостаточностью. Поражение легких служит ведущей причиной летальных исходов у больных системной склеродермией, поэтому расценивается как прогностически неблагоприятный фактор. При вовлечении сердца могут развиваться аритмии, перикардит (адгезивный или экссудативный), эндокардит, сердечная недостаточность.
Почечный синдром при системной склеродермии чаще протекает в форме латентной нефропатии с умеренными функциональными нарушениями. Однако у ряда больных в первое пятилетие от дебюта заболевания развивается грозное, потенциально летальное осложнение — острая склеродермическая почка, которая протекает с гиперренинемией, злокачественной артериальной гипертензией, тромбоцитопенией и гемолитической анемией, стремительно нарастающей почечной недостаточность. В числе прочих синдромальных проявлений системной склеродермии встречаются полиневропатия, синдром Шегрена, аутоиммунный тиреоидит, первичный билиарный цирроз печени и др.
Диагностика
Американской коллегией ревматологов разработаны критерии, на основании которых может быть выставлен диагноз системной склеродермии. Среди них выделяют большой критерий (проксимальная склеродермия — уплотнение кожи кистей рук, лица и туловища) и малые (склеродактилия, дигитальные рубчики, двусторонний пневмофиброз). При выявлении двух малых или одного большого признака клинический диагноз можно считать подтвержденным. Дифференциально-диагностические мероприятия проводятся как внутри группы склеродермических болезней, так и среди других системных заболеваний: синдрома Шегрена, полимиозита, дерматомиозита, облитерирующего тромбангиита и мн. др.
Общеклинические анализы малоинформативны, а выявляемые в них изменения – неспецифичны. Со стороны крови отмечается гипохромная анемия, лейкоцитопения или лейкоцитоз, умеренное увеличение СОЭ. В общем анализе мочи может выявляться протеинурия, лейкоцитурия, микрогематурия. Биохимические показатели указывают на признаки воспаления (повышение уровня серомукоида и фибриногена, СРБ, РФ). Наибольшее значение имеют результаты иммунологического обследования. При системной склеродермии в крови обнаруживаются склеродермические аутоантитела-маркеры: АТ к Scl-70 и антицентромерные АТ.
Среди инструментальных методик для ранней диагностики системной склеродермии наибольшую ценность представляет капилляроскопия ногтевого ложа, позволяющая выявить начальные признаки болезни. Для оценки состояния костной системы проводится рентгенография кистей. С целью выявления интерстициального пневмофиброза целесообразно выполнение рентгенографии и КТ легких. Для исследования ЖКТ назначают рентгенографию пищевода, рентгенографию пассажа бария по кишечнику. Электрокардиография и ЭхоКГ необходимы для выявления кардиогенных поражений и легочной гипертензии. Электромиография позволяет подтвердить миопатические изменения. Для гистологической верификации системной склеродермии проводится биопсия кожи, мышц, почек, легких, перикарда.
Лечение системной склеродермии
Лицам, страдающим системной склеродермией, следует избегать стрессовых факторов, вибрации, переохлаждения, инсоляции, контакта с бытовыми и производственными химическими агентами, отказаться от курения и употребления кофеина, приема сосудосуживающих средств. Фармакотерапия, ее дозировки и длительность зависят от клинической формы, активности и скорости прогрессирования заболевания, тяжести висцеральных поражений.
Патогенетическая терапия системной склеродермии проводится с использованием сосудистых, антифиброзных и иммуносупрессивных препаратов. Для предупреждения эпизодов сосудистого спазма и профилактики ишемических осложнений назначаются вазодилататоры (нифедипин, верапамил, дилтиазем, циннаризин и др.), антиагреганты (ацетилсалициловую кислоту, пентоксифиллин) и антикоагулянты (гепарин, варфарин). С целью подавления развития системного фиброза используется D-пеницилламин. Противовоспалительная терапия при системной склеродермии включает прием НПВП (ибупрофен, диклофенак, нимесулид) и глюкокортикоидов. Препараты данной группы помогают уменьшить признаки воспаления (миозита, артрита, тендосиновита) и иммунологическую активность. Для замедления прогрессирования системного фиброза может применяться метотрексат, циклоспорин, пульс-терапия циклофосфаном.
Симптоматическая терапия при системной склеродермии направлена на уменьшение расстройств пищеварения, сердечной недостаточности, легочной гипертензии. При развитии склеродермического почечного криза назначается каптоприл, эналаприл; в некоторых случаях может потребоваться проведение гемодиализа. Хирургическое лечение – грудная симпатэктомия — показано при осложненной форме синдрома Рейно.
Прогноз
Прогноз при системной склеродермии в целом неблагоприятный. Самая низкая пятилетняя выживаемость (30-70%) ассоциируется с диффузной формой. Предикторами неблагополучного прогноза выступают легочный и почечный синдромы, дебют болезни у пациентов старше 45 лет. Лимитированная форма и хроническое течение болезни имеют более благоприятный прогноз и лучшую выживаемость, при них возможно планирование беременности и благополучное родоразрешение. Пациенты с системной склеродермией подлежат диспансерному учету и наблюдению каждые 3–6 месяцев.
Источник
В отделение пульмонологии университетской клинической больницы № 1 Первого МГМУ имени И.М. Сеченова 24 февраля 2013 г. поступил больной С., 63 лет, с жалобами на постоянный кашель с выделением светлой мокроты, одышку при минимальной физической нагрузке (ходьба на 100 м), цианоз кончиков пальцев рук и ног, усиливающийся холод, цианоз губ.
История заболевания. Отмечает частые острые респираторные вирусные инфекции, бронхиты с детства. Вышеуказанные жалобы беспокоят около 1,5–2 лет. Был обследован в Звенигородской больнице (выписки на руках нет). После обследования был поставлен диагноза «хронический бронхит (не курит, профвредности отрицает), инфекционный бронхиолит». После лечения с небольшим положительным эффектом был выписан домой. Кашель самостоятельно проходил и вновь появлялся, одышка беспокоит постоянно. Эпизодически принимал симптоматическую терапию без эффекта. В апреле 2012 г. был обследован в ГКБ № 11, где при Эхо-КГ обнаружено умеренное расширение правых камер сердца. Трикуспидальная (2 степень), митральная (1 степень) регургитация. Признаки среднетяжелой легочной гипертензии.
Функция внешнего дыхания. Умеренное снижение вентиляционной способности легких по смешанному типу. Умеренная обструкция мелких и средних бронхов. Проба с вентолином отрицательная. При компьютерной томографии (КТ) грудной клетки наблюдается картина фиброзирующего альвеолита, лимфоаденопатии.
Заключение кардиолога: ишемическая болезнь сердца (ИБС): атеросклеротический кардиосклероз, нарушение ритма сердца по типу желудочковой экстрасистолии (бигимения), наджелудочковой тахикардии. Хроническая сердечная недостаточность (ХСН) I степени II функционального класса (ФК) NYНА.
Был поставлен диагноз: «фиброзирующий альвеолит (идиопатический?). Хронический обструктивный бронхит вне обострения. Дыхательная недостаточность I степени. ИБС: атеросклеротический кардиосклероз, нарушение ритма сердца по типу желудочковой экстрасистолии (бигимения), наджелудочковой тахикардии, ХСН I степени ФК II NYНА». Рекомендована терапия: ипратропия бромид 2 дозы 4 р./сут, фенотерол 1–2 дозы по потребности, небиволол, оротовая кислота. Однако данная терапия не дала положительного эффекта.
В анамнезе с 1983 г. наблюдалось резкое посинение пальцев рук, особенно в зимний период, которое трактовалось как синдром Рейно.
При поступлении общее состояние относительно удовлетворительное. Телосложение нормостеническое. Кожные покровы бледные, цианоз губ, кистей и стоп. Уплотнение кожи фаланг пальцев рук. Дыхание через нос свободное. Частота дыхания 18/мин. Перкуторный звук легочный. Аускультативно дыхание жесткое, на форсированном выдохе единичные сухие свистящие хрипы. Тоны сердца приглушены, ритм правильный. Частота сердечных сокращений (ЧСС) = Ps = 68 уд./мин. АД 135/80 мм рт. ст. Живот пальпаторно мягкий, безболезненный. Нижний край печени у края правой реберной дуги. Дизурии нет. Поколачивание по поясничной области безболезненно. Очаговой симптоматики нет. Щитовидная железа не увеличена.
При обследовании в общем анализе крови: гемоглобин – 155,6 г/л, эритроциты – 5,331 млн, цветовой показатель – 0,87, тромбоциты – 145,0 тыс., лейкоциты – 6,68 тыс., нейтрофилы – 32,07%, базофилы – 0,29%, моноциты – 10,63%, лимфоциты – 32,07%, СОЭ– 5 мм/ч.
Общий анализ крови в динамике: гемоглобин – 151,6 г/л, эритроциты – 5,100 млн, цветовой показатель – 0,88, тромбоциты – 148,1 тыс., лейкоциты – 6,84 тыс., нейтрофилы – 53,06%, базофилы – 0,35%, моноциты – 13,61%, лимфоциты – 30,48%, СОЭ – 5 мм/ч.
Биохимический анализ крови: кальций – 2,44 ммоль/л (норма – 2,08–2,65), γ-глутамилтранспептидаза – 75 ед./л (норма – 0–55), аспартатаминотрансфераза – 33 ед./л (0–40), аланинаминотрансфераза – 22 ед./л (0–40), общий белок – 72,0 г/л (57–82), альбумин – 43,0 г/л (32–548), креатинин –
1,15 мг/дл (0,7–1,4), глюкоза – 5,1 ммоль/л (3,9–5,5), азот мочевины – 6,9 ммоль/л (3,2–8,2), мочевая кислота – 534,4 мкмоль/л (норма – 148,75–416,5), билирубин общий – 14,5 мкмоль/л (5,0–21,0), натрий – 145 мэкв/л (135–145), калий – 4,3 мэкв/л (3,5–5,0), железо – 12,04 мкмоль/л (9,0–31,3). Триглицериды – 0,91 ммоль/л (0,57–2,28), общий холестерин – 4,26 ммоль/л (3,88–6,47), холестерин липопротеинов очень низкой плотности – 0,18 ммоль/л (0,114–0,342), липопротеины низкой плотности – 3,0 ммоль/л (2,6–4,2), липопротеины высокой плотности – 1,07 ммоль/л ( 0,7–2,3). Белковые фракции: альбумин – 52,4% (54,7–68,7), α-1 – 3,3% (3,7–7,8), α-2 – 11,8% (5,2–10,7), β – 14,0% (8,6–13,7), γ – 18,5% (10,7–19,3). RW, HBsAg, HCV отрицательно, антитела к ВИЧ не выявлены, С-реактивный белок – отрицательный (0–0,8 мг/дл). Ревматоидный фактор – отрицательно.
Иммуноглобулины: IgE – 93,38 МЕ/мл (0–100).
Коагулограмма: активированное частичное тромбопластиновое время – 1,04 (0,75–1,25), протромбиновый индекс – 93% (85–110%), фибриноген – 4,17 г/л (1,8–4,5).
Анализ мокроты: слизистая, полувязкая, серого цвета, запаха не имеет, лейкоциты – 10–30–50 в поле зрения, эритроциты – единичные в поле зрения, макрофаги – много, эпителиальные клетки плоские – значительное количество, эпителий цилиндрический – немного, кристаллов Шарко-Лейдена не найдено, спирали Куршмана не найдено, эозинофилы не найдены.
Общий анализ мочи: цвет соломенно-желтый, рН 5, удельный вес в норме, прозрачность полная, белка, глюкозы нет. Микроскопия осадка: эпителий клетки – немного, лейкоциты – единичные в препарате, слизь – умеренное количество, бактерии – немного.
ЭКГ. Ритм синусовый правильный с ЧСС 80–82/мин. Горизонтальное положение электрической оси сердца с тенденцией к отклонению влево. Перегрузка левого предсердия.
Бодиплетизмография, диффузионная способность легких. Жизненная емкость легких – 4,93 л (103%), объем форсированного выдоха за 1 с (ОФВ1) – 3,45 л (93%). Нарушение вентиляции легких по рестриктивно-обструктивному типу. Общая емкость легких снижена до 76% от должной. Остаточный объем легких снижен до 39%. Обструктивные нарушения – легкой степени тяжести (ОФВ1 – 93%). Снижение скорости воздушного потока в дистальном отделе. Бронхиальное сопротивление не повышено. Положительной пробы с антровентом не получено. Нарушений диффузионной способности не выявлено (DLCO 99%). Сатурация в норме (SpО2 98%).
Эхо-КГ. Полость левого желудочка (ЛЖ): Dd 4,7 (норма – до 5,5 см), конечно-диастолический объем – 90 мл, конечно-систолический объем – 23 мл (по Simpson). Толщина стенок ЛЖ: межжелудочковая перегородка – 1,0 (норма – до 1,0 см), задняя стенка – 1,1 (норма – до 1,1 см). Глобальная сократительная функция ЛЖ: не нарушена, фракция изгнания – 74% (норма – от 55%). Нарушения локальной сократимости: неопределенное движение МПЖ. Диастолическая функция – снижена, Е/А=0,8. Полость правого желудочка (ПЖ) – 2,8 (норма – до 2,6 см). Толщина свободной стенки ПЖ – 0,5 (норма – до 0,5 см), характер движения стенок – не изменен. Левое предсердие – 77 мл. Правое предсердие – 65 мл. Межпредсердная перегородка – без особенностей. Нижняя полая вена коллабирует после глубокого вдоха более чем на 50%. Митральный клапан: уплотнение фиброзного кольца, максимальное давление – 2,3 мм рт. ст., митральной регургитации нет. Аортальный клапан: уплотнение фиброзного кольца, максимальное давление – 4,0 мм рт. ст., аортальная регургитация – нет. Трикуспидальный клапан: не изменен, трикуспидальная регургитация: II степени. Систолическое давление в легочной артерии – 47 мм рт. ст. Клапан легочной артерии: признаков легочной гипертензии, регургитации через клапан нет. Диаметр корня аорты – 3,0 см. Стенки аорты уплотнены. Наличие жидкости в полости перикарда: нет. Заключение: умеренное расширение правых камер, левого предсердия, ствола легочной артерии, легочная гипертензия, уплотнение стенок аорты, снижение диастолической функции ЛЖ.
КТ органов грудной клетки от 19.02.2013. При исследовании грудной клетки в обоих легких, преимущественно субплеврально, определяется неравномерное понижение воздушности легочной ткани, на фоне которого отмечается утолщение легочного интерстиция. В базальных отделах легких определяются участки формирования «сотового легкого». По сравнению с данными исследования от 18.04.2012 отмечается небольшая отрицательная динамика в виде увеличения выраженности данных изменений. В обоих легких сохраняются многочисленные мелкие очаги (в т. ч. кальцинированные в верхушках легких размером до 3 мм). Жидкости в плевральных полостях нет. Трахея и крупные бронхи свободно проходимы, не деформированы. Стенки бронхов утолщены, уплотнены. Визуализируются немногочисленные лимфатические узлы средостения: паратрахеальные размером до 8 мм, парааортальные – до 15 мм, единичный бифуркационный лимфоузел 19 мм (без существенной динамики в сравнении с предыдущим исследованием). Аорта, легочный ствол и их ветви не расширены. Листки перикарда тонкие, жидкости в полости перикарда нет. В стенках аорты и коронарных артерий определяются кальцинаты. Заключение: КТ-картина, вероятнее всего, соответствует фиброзирующему альвеолиту. В сравнении с данными от 18.04.12 – отрицательная динамика.
Рентгенологическое исследование пищевода. Пищевод свободно проходим, не изменен. Стенки его эластичные во всех отделах, рельеф представлен продольными складками слизистой обычного калибра. Кардия смыкается неполностью. Грыжа пищеводного отверстия диафрагмы в положении лежа не определяется. Заключение: рентгенологическая картина недостаточности кардии.
Эзофагогастродуоденоскопия. Премедикация местная. Пищевод проходим. Слизистая пищевода обычной окраски. Слизистая эзофагокардиального перехода ровная, гладкая, перистальтика равномерная и глубокая. Кардия не смыкается. В полости желудка слизь без патологических примесей. Слизистая желудка гиперемирована, отечна, с единичными острыми эрозиями в нижней трети тела желудка и антральном отделе. Складки слизистой желудка средних размеров. Рельеф складок не перестроен. Перистальтика прослеживается по всем стенкам. Луковица двенадцатиперстной кишки также гиперемирована, отечна, с единичными точечными эрозиями. Язв, деформаций нет. В постбульбарном отделе слизистая отечна. Дуоденальный сосок не увеличен. Поверхность его ровная, гладкая. Слизистая над большим дуоденальным сосочком обычной окраски. Заключение: недостаточность кардии. Эрозивный гастродуоденит. Дуоденогастральный рефлюкс.
Рентгенологическое исследование кистей. На обзорной рентгенограмме прямой проекции отмечается регионарный околосуставной остеопороз фаланг пальцев обоих кистей, компактный слой фаланг истончен. Визуализируется сужение суставных щелей лучезапястных суставов и мелких суставов запястья. Отмечаются участки локального остеосклероза, множественные мелкие кисты.
Спироэргометрия. Толерантность к нагрузке низкая – 2,9 МЕТ. При исходной спирометрии – нарушения по рестриктивно-обструктивному типу. Сатурация О2 в покое – 91%. Пиковое потребление О2 – 10,4 мл/кг/мин (39% от должного). Анаэробный порог – 8,3 мл/кг/мин. Кислородный пульс снижен – 6,7 мл/уд. (38% от должного). Диагностически значимой динамики ST-T не зарегистрировано. Нарушения ритма и проводимости не индуцированы. В восстановительном периоде – единичные желудочковые и наджелудочковые экстрасистолы. Дыхательный резерв – в норме (34%). На фоне нагрузки – десатурация до 84%. Исходно признаки гипервентиляции (РетСО2 снижен) с дальнейшим его снижением на фоне нагрузки. Вентиляционный эквивалент по СО2 значительно увеличен – 52,81. Реакция АД на нагрузку умеренно гипертоническая. Проба на ИБС отрицательная. Наиболее вероятная причина – возрастание давления в легочной артерии на фоне нагрузки, что может рассматриваться в рамках основного системного заболевания.
Капилляроскопия. Плотность капилляров равномерно снижена. Большое число умеренно расширенных и мегакапилляров. Геморрагий нет. Заключение: склеродермический тип изменений. Рекомендуется иммунологический анализ крови (АЦА, aScl-70, aRNP-70).
В ЕNA профиле: SS-A (Ro) отрицательно, SS-B (La) отрицательно, Sm отрицательно, RNP/Sm отрицательно, Scl-70 отрицательно, Jo-l отрицательно, антитела к антигену ScL70 4,0 МЕ/мл (норма 0–15). Антицентромерные антитела – 235,5 МЕ/мл (норма 0–10).
При осмотре оториноларингологом диагностирован хронический фарингит. Гайморит в анамнезе. Ревматолог: системная склеродермия (ССД) с преимущественным поражением легких, осложненная легочной гипертензией, синдром Рейно, синдром Шегрена. Окулист: с обеих сторон отмечается снижение базальной секреции при сохранной функции слезных желез, признаки «сухого глаза».
Таким образом, данные обследования и клинического наблюдения позволили нам сформулировать следующий диагноз: ССД, висцеральная форма, хронического течения (синдром Рейно, легочная гипертензия, интерстициальный легочный фиброз, склеродактилия, синдром Шегрена), гастроэзофагеальная рефлюксная болезнь (ГЭРБ). Гиперурикемия.
В клинике проводилась терапия: рабепразол 20 мг 1–2 р./сут, амлодипин 10 мг 1 р./сут.
ССД – прогрессирующее полисиндромное заболевание с характерным изменением кожи, опорно-двигательного аппарата, внутренних органов (легкие, сердце, ЖКТ, почки) и распространенными вазоспастическими нарушениями по типу синдрома Рейно, в основе которых – поражения соединительной ткани с преобладанием фиброза и сосудистая патология в форме облитерирующего эндартериита [1].
В классификации выделяют склеродермические группы болезней:
I. Системный склероз:
1) диффузная (генерализованное поражение кожи и висцеральные поражения);
2) лимитированная (поражение кожи кистей и лица, или CREST-синдром);
3) перекрестный синдром (с дерматомиозитом или ревматоидным артритом);
4) висцеральная (поражение внутренних органов и сосудов, в т. ч. почечных);
5) ювенильная (до 16 лет, преобладают суставной синдром, контрактуры, очаговое поражение кожи).
II. Ограниченная склеродермия.
III. Диффузный эозинофильный фасциит.
IV. Склеродема Бушке.
V. Локализованный системный фиброз.
VI. Индуцированная склеродермия:
1) химическая, лекарственная;
2) вибрационная;
3) метаболическая, наследственная;
4) иммунологическая;
5) паранеопластическая.
Выделяют следующие варианты течения ССД:
- хроническое (преобладание синдрома Рейно и легочной гипертензии по типу «висцерального» варианта синдрома Рейно);
- подострое (преобладание диффузного фиброза и поражения паренхимы легких по типу ИФА);
- острое быстропрогрессирующее.
По стадиям прогрессирования: начальная, генерализация, терминальная.
По степени активности: минимальная, умеренная, высокая.
Среди маркеров системных диффузных заболеваний соединительной ткани так называемого ENA-профиля, всегда рекомендуемого для дифференциального диагноза и выявления различных вариантов перекрестного синдрома, выделяют специфические маркеры, наличие которых более характерно для системного склероза. Более того, выявление определенных сочетаний положительных тестов к различным антителам позволяет предполагать вариант клинического течения системного склероза: антирибонуклеарные антитела (anti-u3RNP – антитела к рибонуклеарному протеину), антитела к топоизомеразе I (Scl 70) и IIа типов и антитела к центромерам (табл. 1).
Многие исследователи рассматривают следующие возможные причины поражения легких при системном склерозе [5–7]:
- непосредственное поражение легких системным склерозом:
- интерстициальные болезни легких (ИБЛ);
- ИБЛ и легочная гипертензия;
- легочная гипертензия;
- поражения бронхиального дерева;
- поражения плевры;
- вторичные поражения легких:
- ГЭРБ и аспирации;
- лекарственное токсическое действие;
- малигнизация;
- слабость респираторных мышц;
- рестриктивные нарушения за счет индурации кожи грудной клетки;
- сердечная недостаточность;
- сочетания непосредственного и вторичных поражений легких, а также другие сочетанные поражения легких, не имеющие непосредственной связи с ССД (хроническая обструктивная болезнь легких / эмфизема, бронхиальная астма, «узловатые» образования легких) [5].
Чаще всего легочная гипертензия при системном склерозе с поражением легких рассматривается как вторичное явление в результате прогрессирования вентиляционных нарушений за счет преобладания интерстициального фиброза [1–3].
Однако имеет место и другая причина развития легочной гипертензии при наличии незначительного прогрессирования фибротических изменений легочной ткани и, как следствие, нетяжелых изменений вентиляционной функции за счет преимущественного вариабельного вазоспазма в артериолярном-капиллярном русле малого круга кровообращения [1, 4–7].
Данный вариант поражения (рис. 1) чаще всего встречают при минимальных склеродермических изменениях на коже и отсутствии положительной реакции к Scl 70, более характерно выявление антицентромерных антител (табл. 1) – так называемый висцеральный вариант течения системного склероза «scleroderma sine derma» («склеродерма без дермы») [1].
Более редкий вариант патологии сосудов малого круга при ССД, но также требующий дифференциального диагноза, протекает по типу вено-окклюзионной болезни за счет поражения посткапиллярного характера, утолщения интимы сосудов, увеличения числа эластических волокон и гладкомышечных клеток, отека и фиброза венул и кальцификации. Чаще всего развитие вено-окклюзионной болезни связано с наличием мутации гена BMRP2. Данный вариант наиболее тяжелого течения с быстрым прогрессированием плохо курируемой одышки и нарастающей гипоксемии за счет преобладания отека легочного интерстиция проявляется КТ-признаками инфильтратов, обширных участков «матового стекла», плевральным выпотом и часто увеличением внутригрудных лимфоузлов [2].
Можно предполагать все известные причины развития легочной гипертензии у пациентов при поражении легких системным склерозом, однако важно выявить преобладающий механизм повреждения для выбора тактики дальнейшей терапии.
Вариант преобладания вазоспастического компонента в капиллярном русле – так называемый «висцеральный» вариант синдрома Рейно при системном склерозе, вероятнее всего, и был ведущим в нашем клиническом наблюдении. Он проявлялся нарастанием одышки у пациента на фоне физической нагрузки со значительным снижением сатурации при отсутствии данных о сердечно-сосудистой патологии и незначимой вентиляционной дисфункции, приводящей к прогрессированию одышки.
Источник
