Генетические синдромы с пороками сердца
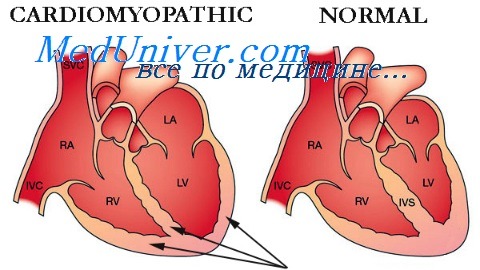
Врожденные пороки сердца у детей с генными синдромами.
Г.Э. СУХАРЕВА, Крымский государственный медицинский университет им. С.И. Георгиевского, кафедра педиатрии с курсом детских инфекционных болезней, Республиканская детская клиническая больница, г. Симферополь
Наследственность — омнибус, в котором нас сопровождают наши предки; то и дело кто-нибудь из них высовывается оттуда, ошеломляя нас своим появлением.
Оливер Холмс
В Украине врожденные сердечно-сосудистые заболевания у детей представляют собой все более серьезную проблему здравоохранения. С начала 90-х годов частота заболеваний органов кровообращения в детском возрасте возросла в 2,5-3 раза [8]. Одной из задач клинициста является поиск этиологического фактора сердечной патологии. За последние годы произошел существенный пересмотр взглядов на природу патологии сердца. Если до недавнего времени в качестве ведущей причины рассматривалось влияние вирусов на кардиогенез с последующим формированием врожденных пороков сердца (ВПС) или развитием воспаления, то научные исследования последних лет свидетельствуют об огромной роли в формировании различной патологии сердца генетических факторов [1, 3, 4, 6, 9, 13, 15, 20]. Врожденные пороки сердца и сосудов представляют с генетической точки зрения весьма гетерогенную группу, встречаясь либо в изолированном виде, либо входя в состав множественных врожденных пороков развития (МВПР), а также моногенных (аутосомно-доминантных или аутосомно-рецессивных) или хромосомных синдромов [2, 7, 11, 12, 14, 16, 17, 19, 23].
Заболевания сердечно-сосудистой системы с учетом влияния генетических факторов Н.А. Белоконь [5] подразделила на следующие группы:
1. Сердечно-сосудистая патология при наследственных синдромах.
2. Сердечно-сосудистая патология при хромосомных аномалиях.
3. Семейные заболевания, при которых сердце является единственной (основной) мишенью поражения.
4. Болезни с наследственным предрасположением, при которых наряду с генетическими большое значение имеют факторы влияния среды.
Сопутствующая патология может иметь различное влияние на состояние ребенка, часто определяя прогноз более существенно, чем сам ВПС: различные наследственные заболевания могут значительно осложнять развитие ребенка, затруднять хирургическое лечение порока сердца и приводить к осложнениям в пред- и послеоперационном периоде, а в некоторых случаях даже могут ставить под сомнение целесообразность хирургической коррекции. В частности, кардиохирург должен знать, что при синдроме Холта — Орама [22] затруднена пункция периферических артерий в связи с патологией лучевой кости и, соответственно, аномальным расположением сосудов. Послеоперационный период синдромов Беквита — Видемана и Ди Джорджи может сопровождаться судорогами гипогликемической и гипокальциемической природы, а также проблемами инфекционного характера и т.д.
Изучение сердечно-сосудистых заболеваний у детей с ассоциированной наследственной патологией является актуальным, так как своевременная диагностика синдромальной патологии, знание этиологии и патогенеза развивающихся специфических осложнений, их профилактика и лечение могут улучшить прогноз и качество жизни пациентов с ВПС.
Цель исследования: выявить особенности течения врожденных пороков сердца и сосудов у больных с генными синдромами.
Нами проведено наблюдение за 56 детьми с ВПС в возрасте 0-18 лет с заболеваниями сердечно-сосудистой системы и ассоциированной наследственной патологией (у 20 из них отмечались генные синдромы), прошедшими стационарное лечение в отделениях реанимации новорожденных, патологии новорожденных, врожденной и наследственной патологии, кардиоревматологии РДКБ и находящимися на диспансерном учете в Крымском республиканском медико-генетическом центре за период 2001-2007 гг.
Методы исследования: клинические; общие лабораторные методы; ЭКГ в покое и при физической нагрузке в 12 стандартных отведениях; холтеровское мониторирование ЭКГ; рентгенография органов грудной клетки в прямой и боковой проекциях; эхокардиография сердца и магистральных сосудов; пульсоксиметрия; кариотипирование; генеалогический метод; генетические биохимические методы.
Среди генетических синдромов, ассоциированных с поражением сердца, преобладали синдром Марфана — у 4 больных (20 %) (рис. 1, 2), синдромы Нунан (рис. 3, 4), Вильямса (рис. 5, 6), Ивемарка (рис. 16) — по 3 случая (по 15 %), синдромы Секкеля и Корнелии де Ланге (рис. 7) — по 2 случая (по 10 %). В единичных случаях (по 5 %) выявлены синдромы Смита — Лемли — Опитца (рис. 8), Холта — Орама (рис. 9), Крузона.
У всех больных с синдромом Марфана имеется расширение восходящей аорты как признак начинающейся аневризмы аорты. Несмотря на то что в настоящее время нет показаний к хирургическому лечению, дети требуют постоянного контроля кардиолога для проведения своевременного оперативного лечения.
Все дети с синдромом Вильямса были прооперированы: устранены КА, надклапанный стеноз аорты. Однако у 1 ребенка во время операции была диагностирована гипоплазия аорты на большом протяжении, что является противопоказанием для ее устранения. Дети находятся под наблюдением кардиолога.
Мы наблюдали 2 детей с редким синдромом Секкеля, описанным в единичных источниках в зарубежной литературе [21, 24, 25]. Так, M.R. MacDonald et al. описали всего 60 наблюдений данного синдрома на протяжении 40 лет, а поражение сердца при синдроме Секкеля в зарубежной литературе описано лишь в нескольких работах. В наших наблюдениях у больных с синдромом Секкеля была диагностирована прогрессирующая митральная недостаточность, у 1 ребенка — в сочетании с митральным стенозом (рис. 10). Больная умерла в возрасте 18 лет, так как родители отказались от хирургического лечения.
У второго ребенка (рис. 11а) в возрасте 3 месяцев диагностирована недостаточность МК (+). При наблюдении в динамике зафиксировано прогрессирование данных изменений до МК (++) (рис. 12) в возрасте 1 год 8 мес. (рис. 11б). Ребенку будет показано оперативное лечение при дальнейшем прогрессировании митральной недостаточности.
В 2 случаях недифференцированных МВПР проводился синдромальный поиск. В первом случае возникла необходимость синдромального поиска у ребенка 2 лет с ВПС (атриовентрикулярная коммуникация).
У ребенка отмечаются аномалия развития шейных и верхнегрудных позвонков («человек без шеи»), задержка роста (синдром Клиппеля — Фейля). Больной был направлен на хирургическое лечение ВПС (рис. 13).
Во втором случае (рис. 14) ребенку с недифференцированным синдромом в возрасте 6 мес. по жизненным показаниям была проведена хирургическая коррекция ВПС (устранена КА). Результат операции удовлетворительный. В настоящее время ребенок находится под наблюдением окулистов.
Синдром Ивемарка (рис. 16), или синдром гетеротаксии [10, 18], часто сочетается с единственным желудочком сердца (ЕЖС), что нашло свое отражение в классификации ВПС: SV, heterotaxia syndrome (синдром Ivemark’s, изометризм, синдром асплении/полисплении).
Все дети с синдромом Ивемарка в наших наблюдениях умерли в неонатальном периоде в связи со сложностью хирургической коррекции ВПС на фоне генетического синдрома.
Таким образом, состояние детей с синдромальной патологией определяется не только тяжестью поражения сердца, различные наследственные заболевания могут приводить к дисфункции других органов и систем, тем самым затруднять терапевтическое и хирургическое лечение порока сердца. Проведенные исследования доказывают необходимость осмотра детей с ВПС врачом-генетиком и обязательного обследования больных с синдромальной патологией для исключения врожденных аномалий развития сердечно-сосудистой системы. Своевременная диагностика наследственного синдрома поможет родителям получить достоверную информацию о прогнозе жизни и развития ребенка, принять адекватное решение о возможности и особенностях его воспитания в семье, узнать генетический риск при повторном деторождении и принять меры дородовой профилактики, а врачам — определить тактику ведения больного, в том числе оценить возможность и, главное, целесообразность проведения кардиохирургической коррекции.
Экономисты и генетики подсчитали, что затраты на проведение своевременной диагностики и коррекции наследственных заболеваний будут в 25 раз меньшими, чем расходы на содержание и лечение людей с наследственной патологией, а также на пособия по инвалидности.
«Если детей с врожденным уродством показать неподготовленным людям, это может произвести страшное впечатление. Подобный прием я бы отнес к числу запрещенных. Но коль есть угроза, лучше показать. Пусть Он и Она знают, что ожидает их потомство», — заметил заведующий отделом Института молекулярной биологии и генетики Национальной академии наук, академик АМН, член-корреспондент НАН Украины, профессор В. Кордюм.
Источник
Генетические причины пороков сердца. Врожденные заболевания сердцаПороки сердца — наиболее распространенная группа заболеваний среди всех врожденных аномалий; они встречаются в 5-7 случаях на 1 тыс. детей, рожденных живыми (более полную информацию об этих нарушениях можно найти в online-версии этой главы). Более высокая распространенность (10%) наблюдается среди мертворожденных или у детей с другой врожденной аномалией. Некоторые факторы, в т.ч. тератогены, инфекции, факторы окружающей среды и наследственность, могут стать причиной ВПС. В последние десятилетия благодаря успехам хирургической коррекции пороков сердца выживаемость и способность к воспроизведению потомства у пациентов с врожденными заболеваниями сердца значительно увеличились. Существенно выросло понимание значимости генетики в диагностике пороков сердца. Хромосомные аберрации свидетельствуют о принципиально важной роли, которую играет генетика в изучении ВПС. Действительно, при спонтанных выкидышах и у детей со значительными нарушениями в количестве и структуре хромосом обнаруживают огромное разнообразие морфологических аномалий сердца. Несмотря на то что исследования с применением методов цитогенетики мало приближают к разгадке наследственных причин заболеваний, изучение наследуемых по Менделю форм ВПС позволяет лучше попять их патогенез. Доминантные, рецессивные и сцепленные с Х-хромосомой генные мутации могут нарушить нормальное развитие сердца и стать причиной появления пороков. В настоящее время доминантные мутации уже распознаны и активно разрабатываются методы идентификации рецессивных мутаций, вызывающих ВПС. Принимая во внимание растущую частоту появления структурных аномалий сердца у детей, родители которых являются единокровными родственниками, можно полагать, что идентификация рецессивных мутаций позволит выявить и другие гены, вносящие вклад в распространенность врожденных заболеваний сердца в популяции в целом. Обнаружение генетических дефектов, ответственных за нарушения развития сердца, позволило пролить свет на механизмы передачи молекулярных сигналов и пути, регулирующие нормальный морфогенез сердца человека, и одновременно понять, почему эти механизмы иногда «выходят из строя». Эти открытия легли в основу трех принципиальных положений. Первое положение: тепы, вовлеченные в патогенез врожденных заболеваний сердца, кодируют факторы транскрипции (GATA4, TBXI, ТВХ5 и NKX2-5) и сигнальные молекулы (PTPN11, KRAS, NOTCH1, JAG1), а также белки, которые в процессе развития сердца направляют и интегрируют взаимодействие клеток и тканей во времени и пространстве. Удивительно, что в отличие от генетических мутаций, которые вызывают развитие заболевания у взрослых (например, КМП), в патогенез ВПС вовлечено всего несколько генов, кодирующих структурные белки (CRELD1, ELN, MYH6).
Вооруженные этими знаниями ученые сосредоточились на изучении организмов-моделей, в которых были обнаружены другие ключевые соединения, регулирующие морфогенез сердца. Так была создана обширная база генов-кандидатов для анализа на наличие потенциальных мутаций у людей. Второе положение связано с типом генных мутаций при врожденных пороках сердца; обычно при таких нарушениях изменена доза гена, что чаще всего приводит к гаплонедостаточности (состояние, когда 50% количества генного продукта недостаточно для нормального функционирования организма) или утрате одной функциональной копии (или аллеля) колируемой этим геном белковой молекулы. Тот факт, что изменение дозы гена приводит к ВПС, означает, что уровень экспрессии этих соединений критичен для нормального морфогенеза сердца. Третье положение касается экспрессивности мутаций (степени фенотипического выражения наследственного признака), ответственных за ВПС. Действительно, у одних членов семьи, пораженной тем или иным генетическим дефектом, возможен некий преобладающий вид аномалии, а у других — с идентичным дефектом — пороки могут иметь иную анатомическую локализацию. Разнообразие врожденных аномалий, обусловленных одной и той же мутацией, свидетельствует о влиянии других факторов. К таким факторам можно отнести, вероятно, генетический фон и окружение плода, которые влияют на фенотипическую экспрессию генетических дефектов. До клинического проявления некоторых мутаций (NKX2-5) могут пройти годы; этим можно объяснить тот факт, что гены, вовлеченные в морфогенез сердца, остаются функционально активными и в миокарде взрослого человека. Выраженное разнообразие клинических проявлений указанных генетических мутаций свидетельствует в пользу концепции — ВПС могут быть обусловлены нарушением различных метаболических путей. В большинстве случаев структурные аномалии сердца возникают спорадически. Результаты исследований вклада генетики в патогенез отдельных структурных аномалий активно используют. Некоторые спорадические случаи отражают вновь возникающие (или спонтанные) доминантные мутации; другие могут быть результатом рецессивных мутаций или изменений во многих генах, что увеличивает риск возникновения аберраций в процессе развития сердца. С появлением технологий, оценивающих вариации генома на уровне популяции, исследователи получили возможность идентифицировать изменения в молекуле ДНК, которые переносят небольшое увеличение риска ВПС на всю популяцию. Эти открытия, вне всякого сомнения, послужат дальнейшему развитию знаний о клинической значимости патогенеза распространенных заболеваний сердца и позволят лучше понять молекулярные основы развития сердца и его функционирования на протяжении всей жизни человека. Врожденные заболевания сердца, наследуемые по законам Менделя, можно разделить па три крупные категории: изолированные нарушения сердечно-сосудистой системы, плейотропные синдромы, к которым часто относят врожденные аномалии сердечно-сосудистой сие темы, и синдромы, при которых сердечно-сосудистая система поражается не всегда. В данной главе рассмотрены типичные примеры заболеваний первых двух категорий, с которыми с наибольшей вероятностью столкнутся кардиологи при лечении взрослых. — Также рекомендуем «Дефекты межпредсердной и межжелудочковой перегородок. Генетические причины дефектов перегородок сердца» Оглавление темы «Генетические поражения сердца»: |
Источник
9 декабря 2017626 тыс.
Содержание
- Врожденные пороки сердца
- Причины врожденных пороков сердца
- Классификация врожденных пороков сердца
- Нарушения гемодинамики при врожденных пороках сердца
- Симптомы врожденных пороков сердца
- Диагностика врожденных пороков сердца
- Лечение врожденных пороков сердца
- Прогноз и профилактика врожденных пороков сердца
Врожденные пороки сердца – группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
Врожденные пороки сердца
Врожденные пороки сердца — весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП – 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).
Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдромы Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
Кроме краснухи беременной, опасность для плода в плане развития врожденных пороков сердца представляют ветряная оспа, простой герпес, аденовирусные инфекции, сывороточный гепатит, цитомегалия, микоплазмоз, токсоплазмоз, листериоз, сифилис, туберкулез и др.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца – болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
В практической кардиологии используется деление врожденных пороков сердца на 3 группы: пороки «синего» (цианотического) типа с веноартериальным шунтом (триада Фалло, тетрада Фалло, транспозиция магистральных сосудов, атрезия трехстворчатого клапана); пороки «бледного» типа с артериовенозным сбросом (септальные дефекты, открытый артериальный проток); пороки с препятствием на пути выброса крови из желудочков (стенозы аорты и легочной артерии, коарктация аорты).
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
Ввиду особенностей антенатальной гемодинамики, кровообращение развивающегося плода при врожденных пороках сердца, как правило, не страдает. Врожденные пороки сердца проявляются у детей сразу после рождения или через какое-то время, что зависит от сроков закрытия сообщения между большим и малым кругами кровообращения, выраженности легочной гипертензии, давления в системе легочной артерии, направления и объема сброса крови, индивидуальных адаптационных и компенсаторных возможностей организма ребенка. Нередко к развитию грубых нарушений гемодинамики при врожденных пороках сердца приводит респираторная инфекция или какое-либо другое заболевание.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой — электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Источник
