Геморрагический синдром при гемофилии а обусловлен дефицитом
Гемофилия – наследственная патология системы гемостаза, в основе которой лежит снижение или нарушение синтеза VIII, IX или XI факторов свертывания крови. Специфическим проявлением гемофилии служит склонность больного к различным кровотечениям: гемартрозам, внутримышечным и забрюшинным гематомам, гематурии, желудочно-кишечным кровотечениям, длительным кровотечениям при операциях и травмах и др. В диагностике гемофилии первостепенное значение имеет генетическое консультирование, определение уровня активности факторов свертываемости, ДНК-исследование, анализ коагулограммы. Лечение гемофилии предполагает проведение заместительной терапии: трансфузии гемоконцентратов с факторами свертывания VIII или IX, свежезамороженной плазмы, антигемофильного глобулина и др.
Общие сведения
Гемофилия – заболевание из группы наследственных коагулопатий, обусловленное дефицитом факторов свертывания плазмы крови и характеризующееся повышенной склонностью к геморрагиям. Распространенность гемофилии А и В составляет 1 случай на 10000-50000 представителей мужского пола. Чаще всего дебют заболевания приходится на ранний детский возраст, поэтому гемофилия у ребенка является актуальной проблемой педиатрии и детской гематологии. Кроме гемофилии, у детей встречаются и другие наследственные геморрагические диатезы: геморрагическая телеангиэктазия, тромбоцитопатия, болезнь Гланцмана т. п.

Гемофилия
Причины гемофилии
Гены, обусловливающие развитие гемофилии, сцеплены с половой Х-хромосомой, поэтому заболевание наследуется по рецессивному признаку по женской линии. Наследственной гемофилией болеют практически исключительно лица мужского пола. Женщины являются проводниками (кондукторами, носителями) гена гемофилии, передающими заболевание части своих сыновей.
У здорового мужчины и женщины-кондуктора с одинаковой вероятностью могут родиться как больные, так и здоровые сыновья. От брака мужчины, больного гемофилией со здоровой женщиной рождаются здоровые сыновья или дочери-кондукторы. Описаны единичные случаи гемофилии у девочек, рожденных от матери-носителя и больного гемофилией отца.
Врожденная гемофилия встречается почти у 70 % пациентов. В этом случае наследуется форма и тяжесть гемофилии. Около 30% наблюдений приходится на спорадические формы гемофилии, связанные с мутацией в локусе, кодирующем синтез плазменных факторов свертывания крови на Х-хромосоме. В дальнейшем такая спонтанная форма гемофилии становится наследственной.
Свертываемость крови, или гемостаз, служит важнейшей защитной реакцией организма. Активизация системы гемостаза происходит в случае повреждения сосудов и начала кровотечения. Свертываемость крови обеспечивается тромбоцитами и особыми веществами – плазменными факторами. При дефиците того или иного фактора свертывания своевременный и адекватный гемостаз становится невозможным. При гемофилии в связи с дефицитом VIII, IX или других факторов нарушается первая фаза свертывания крови — образование тромбопластина. При этом увеличивается время свертывания крови; иногда кровотечение не останавливается в течение нескольких часов.
Классификация гемофилии
В зависимости от дефицита того или иного фактора свертываемости крови, различают гемофилию А (классическую), В (болезнь Кристмаса), С и др.
- Классическая гемофилия составляет подавляющее большинство (около 85%) случаев синдрома и связана с дефицитом VIII фактора свертывания (антигемофильного глобулина), приводящим к нарушению образование активной тромбокиназы.
- При гемофилии В, составляющей 13% случаев заболевания, имеет место недостаток IX фактора (плазменного компонента тромбопластина, фактора Кристмаса), также участвующего в образовании активной тромбокиназы в I фазе свертывания крови.
- Гемофилия С встречается с частотой 1-2% и обусловлена недостаточностью XI фактора свертывания крови (предшественника тромбопластина). На остальные разновидности гемофилии приходится менее 0,5% случаев; при этом может отмечаться дефицит различных плазменных факторов: V (парагемофилия), VII (гипопроконвертинемия), Х (болезнь Стюарта – Прауэр) и др.
Тяжесть клинического течения гемофилии зависит от степени недостаточности коагуляционной активности плазменных факторов свертывания крови.
- При гемофилии тяжелой степени уровень недостающего фактора составляет до 1%, что сопровождается развитием тяжелого геморрагического синдрома уже в раннем детском возрасте. У ребенка с тяжелой гемофилией возникают частые спонтанные и посттравматические кровоизлияния в мышцы, суставы, внутренние органы. Сразу после рождения ребенка могут обнаруживаться кефалогематомы, длительные кровотечения из пуповинного отростка, мелена; позднее — продолжительные кровотечения, связанные с прорезыванием и сменой молочных зубов.
- При среднетяжелой степени гемофилии у ребенка уровень плазменного фактора составляет 1-5%. Заболевание развивается в дошкольном возрасте; геморрагический синдром выражен умеренно, отмечаются кровоизлияния в мышцы и суставы, гематурия. Обострения случаются 2-3 раза в год.
- Легкая форма гемофилии характеризуется уровнем фактора выше 5%. Дебют заболевания возникает в школьном возрасте, часто в связи с травмами или операциями. Кровотечения более редкие и менее интенсивные.
Симптомы гемофилии
У новорожденных детей признаками гемофилии могут служить длительное кровотечение из культи пуповины, подкожные гематомы, кефалогематомы. Кровотечения у детей первого года жизни могут быть связаны с прорезыванием зубов, оперативными вмешательствами (инцизией уздечки языка, циркумцизио). Острые края молочных зубов могут стать причиной прикусывания языка, губ, щек и кровотечений из слизистых оболочек полости рта. Однако в грудном возрасте гемофилия дебютирует редко в связи с тем, что материнском молоке содержится достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений значительно возрастает, когда ребенок с гемофилией начинает вставать и ходить. Для детей после года характерны носовые кровотечения, подкожные и межмышечные гематомы, кровоизлияния в крупные суставы. Обострения геморрагического диатеза случаются после перенесенных инфекций (ОРВИ, ветрянки, краснухи, кори, гриппа и др.) вследствие нарушения проницаемости сосудов. В этом случае нередко возникают самопроизвольные диапедезные геморрагии. Ввиду постоянных и длительных кровотечений у детей с гемофилией имеется анемия различной степени выраженности.
По степени убывания частоты кровоизлияния при гемофилии распределяются следующим образом: гемартрозы (70—80%), гематомы (10-20%), гематурия (14-20%), желудочно-кишечные кровотечения (8%), кровоизлияния в ЦНС (5%).
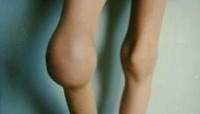
Гемартрозы являются наиболее частым и специфическим проявлением гемофилии. Первые внутрисуставные кровоизлияния у детей с гемофилией случаются в возрасте 1-8 лет после ушибов, травм или спонтанно. При гемартрозе выражен болевой синдром, отмечается увеличение сустава в объеме, гиперемия и гипертермия кожи над ним. Рецидивирующие гемартрозы приводят к развитию хронического синовита, деформирующего остеоартроза и контрактур. Деформирующий остеоартроз приводит к нарушению динамики опорно-двигательного аппарата в целом (искривлению позвоночника и таза, гипотрофии мышц, остеопорозу, вальгусной деформации стопы и др.) и к наступлению инвалидности уже в детском возрасте.
При гемофилии часто возникают кровоизлияния в мягкие ткани – подкожную клетчатку и мышцы. У детей обнаруживаются непроходящие синяки на туловище и конечностях, часто возникают глубокие межмышечные гематомы. Такие гематомы склонны к распространению, поскольку излившаяся кровь не сворачивается и, проникая вдоль фасций, инфильтрирует ткани. Обширные и напряженные гематомы могут сдавливать крупные артерии и периферические нервные стволы, вызывая интенсивные боли, паралич, атрофию мышц или гангрену.
Довольно часто при гемофилии возникают кровотечения из десен, носа, почек, органов ЖКТ. Кровотечение может быть инициировано любыми медицинскими манипуляциями (внутримышечной инъекцией, экстракцией зуба, тонзиллэктомией и др.). Крайне опасными для ребенка с гемофилией являются кровотечения из зева и носоглотки, поскольку могут привести к обструкции дыхательных путей и потребовать экстренной трахеостомии. Кровоизлияния в мозговые оболочки и головной мозг приводят к тяжелым поражениям ЦНС или летальному исходу.
Гематурия при гемофилии может возникать самопроизвольно или вследствие травм поясничной области. При этом отмечаются дизурические явления, при образовании кровяных сгустков в мочевыводящих путях — приступы почечной колики. У больных с гемофилией нередко обнаруживаются пиелоэктазия, гидронефроз, пиелонефрит.
Желудочно-кишечные кровотечения у пациентов с гемофилией могут быть связаны с приемом НПВС и др. лекарств, с обострением латентного течения язвенной болезни желудка и двенадцатиперстной кишки, эрозивным гастритом, геморроем. При кровоизлияниях в брыжейку и сальник развивается картина острого живота, требующая дифференциальной диагностики с острым аппендицитом, кишечной непроходимостью и др.
Характерным признаком гемофилии является отсроченный характер кровотечения, которое обычно развивается не сразу после травмы, а через некоторое время, иногда спустя 6-12 и более часов.
Диагностика гемофилии
Диагностика гемофилии проводится при участии ряда специалистов: неонатолога, педиатра, генетика, гематолога. При наличии у ребенка сопутствующей патологии или осложнений основного заболевания проводятся консультации детского гастроэнтеролога, детского травматолога-ортопеда, детского отоларинголога, детского невролога и др.
Супружеские пары, находящиеся в группе риска по рождению ребенка с гемофилией, должны пройти медико-генетическое консультирование еще на этапе планирования беременности. Выявить носительство дефектного гена позволяет анализ генеалогических данных и молекулярно-генетическое исследование. Возможно проведение пренатальной диагностики гемофилии с помощью биопсии хориона или амниоцентеза и исследования ДНК клеточного материала.
После рождения ребенка диагноз гемофилии подтверждается с помощью лабораторных исследований гемостаза. Основные изменения показателей коагулограммы при гемофилии представлены увеличением времени свертывания крови, АЧТВ, тромбинового времени, МНО, времени рекальцификации; уменьшением ПТИ и др. Решающее значение при диагностике формы гемофилии принадлежит определению снижения прокоагулянтной активности одного из факторов свертывания ниже 50%.
При гемартрозах ребенку с гемофилией проводится рентгенография суставов; при внутренних кровотечениях и забрюшинных гематомах – УЗИ брюшной полости и забрюшинного пространства; при гематурии – общий анализ мочи и УЗИ почек и т. д.
Лечение гемофилии
При гемофилии полное избавление от заболевания невозможно, поэтому основу лечения составляет заместительная гемостатическая терапия концентратами VIII и IX факторов свертывания крови. Необходимая доза концентрата определяется степенью выраженности гемофилии, тяжестью и видом кровотечения.
В лечении гемофилии выделяют два направления – профилактические и «по требованию», в период проявлений геморрагического синдрома. Профилактическое введение концентратов факторов свертывания крови показано пациентам с тяжелой формой гемофилии и проводится 2-3 раза в неделю для предупреждения развития гемофилической артропатии и прочих кровотечений. При развитии геморрагического синдрома требуются повторные трансфузии препарата. Дополнительно используются свежезамороженная плазма, эритромасса, гемостатики. Все инвазивные вмешательства у больных с гемофилией (наложение швов, удаление зубов, любые операции) проводятся под прикрытием гемостатической терапии.
При незначительных наружных кровотечениях (порезах, кровотечениях из полости носа и рта) может использоваться гемостатическая губка, наложение давящей повязки, обработка раны тромбином. При неосложненном кровоизлиянии ребенку необходим полный покой, холод, иммобилизация больного сустава гипсовой лонгетой, в дальнейшем – УВЧ, электрофорез, ЛФК, легкий массаж. Больным с гемофилией рекомендуется диета, обогащенная витаминами А, В, С, D, солями кальция и фосфора.
Прогноз и профилактика гемофилии
Длительная заместительная терапия приводит к изоиммунизации, образованию антител, блокирующих прокоагулянтную активность вводимых факторов, и неэффективности гемостатической терапии в обычных дозах. В таких случаях больному с гемофилией проводится плазмаферез, назначаются иммунодепрессанты. Поскольку больным с гемофилией проводится частое переливание компонентов крови, не исключается риск инфицирования ВИЧ-инфекцией, гепатитами В, С и D, герпесом, цитомегалией.
Легкая степень гемофилии не влияет на продолжительность жизни; при тяжелой гемофилии прогноз ухудшается при массивных кровотечениях, обусловленных операциями, травмами.
Профилактика предполагает проведение медико-генетического консультирования супружеских пар, имеющих отягощенный семейный анамнез по гемофилии. Дети, больные гемофилией, всегда должны иметь при себе специальный паспорт, где указан тип заболевания, группа крови и Rh-принадлежность. Им показан охранительный режим, профилактика травм; диспансерное наблюдение педиатра, гематолога, детского стоматолога и др. специалистов; наблюдение в условиях специализированного гемофильного центра.
Источник
Гемофилия А (классическая гемофилия) — генетически детерминируемое заболевание, вызванное врождённым дефицитом белка фактора свёртывания крови VIII[2]. Наиболее часто встречающаяся форма гемофилии (около 80 % случаев).
Диагностируется путём анализа крови (коагулограмма) на наличие фактора VIII в крови. Возможна пренатальная диагностика гемофилии А у плода в I триместре беременности.
Главным образом для профилактики гемофилии А используется заместительная терапия — регулярное введение препаратов, содержащих недостающий белок — фактор свертывания VIII. Полное излечение от гемофилии А с помощью лекарств невозможно, однако известны случаи, когда при пересадке пациенту донорской печени организм гемофилика в течение нескольких лет вырабатывал фактор VIII, но затем, в процессе обновления клеток печени данный эффект сошел на нет, поэтому эта методика лечения была признана неэффективной.
Наиболее известные препараты для лечения гемофилии А: октанат, иммунат, когенэйт-фс, рекомбинат, гемоктин, коэйт-дви. Все они вводятся только внутривенно. Для профилактики ингибиторных форм гемофилии А используется концентрат фактора свёртывания крови VII активированный (новосэвен, коагил-VII, фейба). Исторически раньше применялось переливание донорской крови, плазмы и криопреципитата (в России вплоть до начала XXI века, в отдельных странах применяется до сих пор).
Генетика[править | править код]
Наиболее частый случай X-сцепленного рецессивного наследования: от матери, которая является носителем, при здоровом отце.
X-сцепленное наследование рецессивного признака от отца, который является больным.
Гемофилия — заболевание, связанное с рецессивной мутацией в X-хромосоме. Встречается у мужчин и у гомозиготных женщин. Тем не менее, легкая форма гемофилии А (и В) встречается у гетерозиготных женщин из-за инактивации X-хромосомы, поэтому рекомендовано определять уровень фактора VIII и IX у всех носителей и потенциальных носителей перед хирургическим вмешательством и в случае клинически значимых кровотечений[3].
Гемофилия встречается примерно у 1 из 5000 мужчин[3]. Из них 85 % имеют гемофилию А и 15 % — гемофилию B[3].
У 5-10 % пациентов с гемофилией проблема с дисфункцией белка фактора VIII (качественная недостаточность), а у остальных — с недостаточным количеством производимого фактора VIII (количественный дефицит)[3]. Среди тех, кто имеет серьезный дефицит (определяемый как <1 % активности фактора VIII), 45-50 % имеют те же мутации, инверсии внутри гена фактора VIII, что приводит к полной ликвидации производства белка. Тем не менее, обе формы гемофилии могут быть вызваны различными мутациями, и первоначальный диагноз и классификация производится путём измерения активности белка, а не с помощью генетических тестов, хотя генетические тесты рекомендованы для однократной проверки членов семьи, имеющей один известный случай гемофилии B[3].
Примерно 30 % больных не имеют семейной истории болезни, их болезнь предположительно вызвана новой мутацией[4].
Тяжесть заболевания[править | править код]
Есть множество различных мутаций, которые приводят к гемофилии А. В связи с различиями в изменениях участвующих генов (и как следствие — в результирующем белке), у пациентов с гемофилией может наблюдаться различный уровень активного фактора свертываемости крови. Случаи с менее чем 1 % активного фактора классифицируются как тяжелая форма гемофилии, 1-5 % активного фактора относится к умеренной гемофилии, а легкая форма гемофилии характеризуется диапазоном 5-40 % от нормального уровня активного фактора свертывания крови[5].
Признаки и симптомы[править | править код]
Характерные симптомы зависят от тяжести заболевания. В целом характерны случаи внутренних или внешних кровотечений, которые называются «кровоточивостью»[6][7]. Пациенты с более тяжелой формой гемофилии страдают более тяжелыми и более частыми кровотечениями, в то время как для пациентов с легкой формой гемофилии характерны более мелкие симптомы, за исключением послеоперационного периода или серьезных травм. Больные умеренной формой гемофилии имеют переменные симптомы, которые проявляются в диапазоне между тяжелой и легкой формой.
Если при вагинальных родах используются щипцы или вакуум-экстракция, первым признаком гемофилии могут быть тяжелые синяки или гематомы головы, или даже внутричерепное кровоизлияние[8]. Длительное кровотечение из раны обрезания или после прокола вены или пробы их пятки новорожденного является ещё одним распространенным ранним признаком гемофилии. Эти признаки могут побудить сделать анализы крови, которые укажут на гемофилию. У других пациентов, особенно в случаях умеренной или легкой формы гемофилии, первое серьезное кровотечение возникнет в случае первой серьезной травмы.
Гемофилия сильно повышает риск длительного кровотечения при распространенных травмах, а в тяжелых случаях кровотечения могут быть спонтанными и не иметь очевидной причины. Кровотечение может возникнуть в любой части тела. Поверхностные кровотечения, например в результате ссадины, мелкой или рваной раны, могут продолжаться долго, а образующаяся корочка может быть легко повреждена из-за отсутствия фибрина, что приведет к повторному кровотечению. В то время как поверхностные кровотечения могут доставлять определенные неудобства, наиболее серьезными на сегодняшний день являются следующие группы опасных кровоизлияний:
- в суставах
- в мышцах
- желудочно-кишечном тракте
- в мозге
Кровоизлияния в мышцы и суставы свидетельствуют о гемофилии, в то время как кровоизлияния в пищеварительный тракт наблюдаются и при других нарушениях свертывания крови. Кровоизлияния в суставы являются одним из самых серьезных симптомов гемофилии, хотя обычно не угрожают жизни. Повторные кровотечения в суставную капсулу могут привести к необратимому повреждению суставов, хроническому артриту и инвалидности. Повреждение сустава не является результатом кровоизлияния в капсулу, а происходит в процессе заживления. Когда кровь в суставе расщепляется ферментами, кости в этой области также ухудшаются. Это в свою очередь приводит к сильным болям.
Диагностика[править | править код]
Стандартные анализы крови (общий и биохимический) не позволяют судить о количестве факторов свёртываемости крови.
Для диагностики гемофилии используют различные лабораторные методы. Диагноз гемофилия может быть заподозрен, если коагулологические тесты показывают повышение Активированного частичного тромбопластинового времени (АЧТВ), протромбинового времени и времени кровотечения. АЧТВ тест — это первый анализ крови, который показан при подозрении на гемофилию. Диагноз ставится при наличии очень низкого (<10 МЕ) уровня фактора VIII.
Данные о семейном анамнезе часто учитываются, хотя и не являются решающими. В последнее время доступным для определения вероятности наличия или передачи гемофилии стало генетическое тестирование.
Диагностика гемофилии А также включает в себя определение тяжести заболевания, которая может варьироваться от легкой до тяжелой в зависимости от количества и активности фактора VIII, обнаруженного в крови. Уровень фактора VIII в крови обычно не меняется в течение жизни человека.
Дифференциальная диагностика[править | править код]
Дифференциальной диагностики чаще всего требуют два наиболее распространенных диагноза: гемофилия B (известная также как болезнь Кристмаса), которая характеризуется дефицитом фактора IX, и болезнь Виллебранда, которая характеризуется дефицитом фактора Виллебранда, необходимого для надлежащего функционирования фактора VIII. Гемофилия С также иногда требует дифференциальной диагностики.
Терапия[править | править код]
Пациенты с наиболее тяжелой формой гемофилии требуют регулярного внутривенного введения плазменного или рекомбинантного концентрата фактора VIII.
Режим профилактического лечения определяется индивидуально. Помимо «обычных» пищевых добавок, дополнительный концентрат фактора дается в период хирургических процедур и после травмы.
Осложнения[править | править код]
Особой терапевтической проблемой является развитие антител «ингибиторов» фактора VIII, вызванных его частым вливанием. Это проявляется тем, что организм принимает «нормальный» фактор VIII как чужеродный, так как не имеет его собственной «копии». У таких пациентов вливание фактора VIII становится малоэффективным. Недавно активированный фактор VII (NovoSeven) стал доступен для лечения кровотечений у пациентов с гемофилией и ингибиторами фактора.
См. также[править | править код]
- Гемофилия
Коагулологические тесты:
- Тромбоэластография
- Тест генерации тромбина (тромбиновый потенциал, эндогенный тромбиновый потенциал)
- Тест протромбинового времени (или Протромбиновый тест, МНО, ПВ)
- Активированное частичное тромбопластиновое время (АЧТВ)
- Тромбодинамика
Примечания[править | править код]
Источник
