Галстян г р синдром диабетической стопы
 Для цитирования. Кисляков В.А., Оболенский В.Н., Юсупов И.А. Синдром диабетической стопы: комплексный подход к лечению // РМЖ. 2015. No 12. С. 768–770.
Для цитирования. Кисляков В.А., Оболенский В.Н., Юсупов И.А. Синдром диабетической стопы: комплексный подход к лечению // РМЖ. 2015. No 12. С. 768–770.
Распространенность и экономические аспекты
В XXI в. сахарный диабет (СД) стал ведущим неинфекционным заболеванием. Каждые 10 с в мире становится на 2 больных СД больше – это 7 млн в год. По мнению экспертов Всемирной организации здравоохранения, СД занимает 1-е место среди заболеваний, приводящих к инвалидности, и 3-е – по смертности [1–4].
Согласно исследованиям Эндокринологического научного центра (ЭНЦ), в России распространенность СД достигает 10–12 млн человек (7–8% населения страны). Наиболее высокая распространенность СД среди взрослого населения крупных городов. При этом соотношение мужчин и женщин – 1:3. В половине случаев СД 2-го типа выявляется на 5–7-м году от начала заболевания, и у 20–30% выявляются специфические осложнения: катаракта, ретинопатия, нефропатия, нейропатия, синдром диабетической стопы (СДС), ишемическая болезнь сердца, артериальная гипертония и др. [5–8].
СДС приводит к гнойно-некротическим поражениям стоп с последующей потерей нижних конечностей – к самой высокой инвалидизации. Окончательные цифры распространенности СДС в настоящее время неизвестны. Тем не менее установлено, что у 15% больных СД развиваются патологические изменения в стопах или голеностопном суставе [9–13].
В последние годы широко обсуждаются не только клинические, но и экономические, социальные аспекты профилактики и лечения СДС, методы клинико-экономического анализа и, прежде всего, учет всех затрат, связанных с лечением СДС [1, 14].
На 18-м конгрессе Международной федерации диабета (МФД) были представлены, в частности, данные о распространенности язвенных дефектов при СДС в странах Балканского региона – 7,5%. Диагноз СД впервые ставится во время хирургического вмешательства у 15–19% больных, подвергающихся ампутации. Специалисты МФД считают, что вероятная частота ампутаций при СД составляет 5–24 на 100 000 населения в год, или 6–8 на 1000 больных в год, а в эпидемиологически неблагоприятных регионах достигает 24 на 1000 больных в год. В России, согласно данным государственного регистра, эти показатели колеблются от 0,76 до 18,2 и в среднем составляют 6,4 случая на 1000 больных [3, 4, 11, 15].
Расходы на лечение СДС в развитых странах составляют около 12–15% от всех затрат на лечение СД, в развивающихся странах они могут составлять до 40% от общего объема финансовых ресурсов, выделяемых на СД. Подсчитано, что на проведение одной ампутации в зарубежных странах тратится более 10 000 долл. Общие затраты на лечение СДС в среднем составляют 13 179 долл. и меняются в зависимости от степени тяжести по классификации Wagner в пределах от 1892 долл. при I степени до 27 721 долл. при IV–V степени тяжести. Лечение СДС на фоне хронической артериальной недостаточности нижних конечностей обходится в 4,5 раза дороже, чем при сохранном периферическом кровотоке. Ежегодная стоимость лечения язвенных поражений стоп при СДС в США составляет 5 млрд долл. прямых медицинских затрат и 400 млн долл. косвенных медицинских затрат. Кроме того, в США зафиксировали, что 77% людей старше 75 лет после ампутации не способны вернуться в собственный дом и им нужна дополнительная помощь и поддержка социальных групп [8, 16–18].
Анализ работы отделения диабетической стопы ЭНЦ показал, что при своевременно начатой адекватной терапии СДС понижается риск хирургических вмешательств и тяжелых осложнений: у 98% больных с нейропатической инфицированной формой СДС можно избежать хирургического вмешательства; у 60% с нейроишемической формой – проведения ампутаций на уровне голени и бедра; у 25% с критической ишемией – предотвратить высокие ампутации на уровне бедра; на 50% уменьшить частоту образования язв стоп в группе высокого риска [4, 5, 13].
Летальность среди больных СД, перенесших высокую ампутацию конечности по поводу гангрены, в течение последующих 5 лет достигает 68%, в ближайшие 3 нед. – 22%, в течение года – 11–41%, через 3 года – 20–50%, через 5 лет – от 39–68%. Частота ипсилатеральных ампутаций через год после первой ампутации – до 24%, через 2 года – 30%, через 5 лет – 49% и контралатеральных ампутаций через год после первой ампутации – до 12%, через 2 года – 23%, через 5 лет – 28-51%. Рецидивы язв на стопах через 1, 3, 5 лет составили 44, 61, 70% соответственно. Рецидивирующие деструктивные поражения ухудшают проблемы лечения, реабилитации, социальной помощи, увеличивая экономические затраты [19–23].
Если распространенность СД, а соответственно и СДС будет увеличиваться с той же скоростью, что и сейчас, то к 2025 г. экономический ущерб составит от 213 до 396 млрд долл. в год. 75% прироста заболевания придутся на развивающиеся страны. По данным немецких исследователей, общая стоимость лечения больных СД в Германии составляет приблизительно 5 млрд. евро, а средняя стоимость лечения 1 пациента – 5000 евро в год. Ежегодные общие затраты в России на лечение нейроишемической формы СДС составляют 56,2 млн долл., при этом затраты на ампутации достигают 14,4 млн долл. [2, 5, 17].
По оценке главного экономиста Morgan Stanley Эльги Бартш, сочетание двух факторов – СД и ожирения – снизит среднегодовые темпы роста валового внутреннего продукта (ВВП) в странах Организации экономического сотрудничества и развития (ОЭСР) в 2015–2035 гг. с 2,3 до 1,8%, в странах БРИКС (Бразилия, Россия, Индия, Китай, Южно-Африканская Республика) – с 4,5 до 4,2%. Согласно прогнозам ОЭСР, среднегодовые темпы роста ВВП России составят 2,8%. При сохранении нынешнего уровня потребления сахара гражданами страны этот показатель снизится до 2%. Согласно результатам исследования, проведенного фармацевтической компанией «Ново Нордиск», «Инвестиции в лечение сахарного диабета в России», ежегодные прямые затраты, связанные с СД в России, составляют 12,5 млрд долл. США. При этом 42% объема этих средств расходуется на лечение осложнений, которые выявляются у 40–50% людей в момент постановки диагноза. Соответственно диагностика заболевания на ранних стадиях позволит российскому обществу сэкономить более 1,5 млрд долл. США из средств, выделяемых на здравоохранение [13].
Принципы терапии
По мнению большинства авторов, в лечении пациентов с синдромом диабетической стопы должны участвовать квалифицированные эндокринолог, гнойный хирург, сосудистый хирург, ортопед, специально обученный средний медицинский персонал, а комплексное лечение должно включать общие и местные методы (рис. 1) [24–26].
Тактика комплексного лечения зависит от формы заболевания [14, 15, 18, 19, 21, 27]. Мы, как и ряд специалистов, выделяем следующие клинические формы СДС.
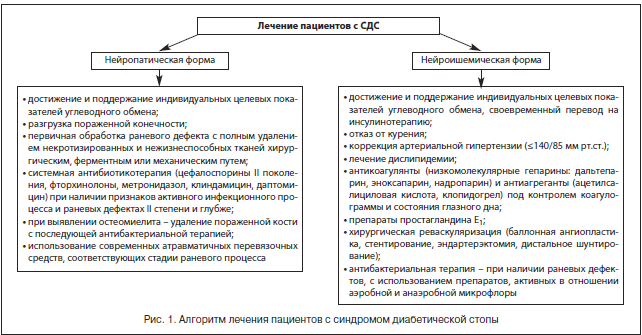
1. Нейропатическая форма:
– без остеоартропатии;
– с остеоартропатией – «сустав Шарко».
2. Нейроишемическая форма с учетом других характеристик.
К общим принципам терапии пациентов с СДС относятся коррекция факторов риска, компенсация углеводного обмена и поддержание целевых показателей углеводного обмена, компенсация сопутствующих заболеваний, системная антибактериальная, антитромботическая, вазопротекторная терапия в сочетании с адекватным обезболиванием.
К местным принципам лечения относятся: обеспечение полной разгрузки пораженной области с помощью разгрузочного полубашмака, индивидуальной разгрузочной повязки, костыля, сложной ортопедической обуви, кресла-каталки; контроль раневой инфекции, заключающийся в первичной обработке раны и местном лечении раны с правильным выбором повязки в зависимости от фазы течения раневого процесса; хирургическое лечение гнойно-некротического очага стопы с закрытием ран и/или формированием культи пораженной стопы при помощи реконструктивных и пластических операций; восстановление магистрального артериального кровотока в сосудах нижних конечностей.
Перспективным является применение L-лизина эсцината в комплексном лечении язвенных и гнойно-некротических поражений при СДС. Эффективность препарата объясняется его противоотечным действием, связанным со снижением проницаемости сосудистой стенки и улучшением венозного оттока. L-лизина эсцинат обладает стабилизирующим действием на мембраны клеток, снижает активность лизосомальных ферментов, принимающих непосредственное участие в воспалительном процессе. Кроме того, препарат блокирует эффекты фосфолипазы А2, которая является ключевым веществом в развитии воспалительной реакции, связанной с повреждением мембран клеток различными факторами при ишемии, инфекции и травме. Стабилизация фосфолипазы А2 способствует снижению активности простагландинов, что также приводит к уменьшению воспалительного ответа. Доказано также влияние L-лизина эсцината на такие медиаторы воспаления, как гистамин, серотонин, которые выделяются из тромбоцитов, тучных клеток и создают основу для классической воспалительной реакции. Комплексный эффект препарата L-лизина эсцината апробирован в нейрохирургической, неврологической, травматологической практике, ангиологии и флебологии [26–31].
Мы регулярно применяем L-лизина эсцинат по 10 мл в разведении на 50 мл физиологического (0,9%) раствора внутривенно капельно в течение 10 дней у пациентов с нейропатической формой СДС в послеоперационном периоде, с трофическими язвами на фоне нейропатических отеков и у больных с язвами на фоне венозной недостаточности (СЕАР 2-3). Отмечаем благоприятное течение послеоперационного периода, более раннее уменьшение отеков, снижение болевого синдрома, нейропатических болей, заживление язв. Рекомендуем применение L-лизина эсцината для лечения язвенных и гнойно-некротических поражений при СДС в амбулаторной и стационарной практике.
Заключение
СД является серьезным заболеванием, способным привести к тяжелым социально-экономическим и демографическим последствиям. Вопрос о влиянии СДС на качество жизни остается малоизученным. Неизвестны долговременные затраты, связанные с лечением рецидивов язв, проведением повторных ампутаций и увеличением расходов на социальное обслуживание. Кроме того, неучтенными остаются непрямые затраты вследствие утраты человеком из-за болезни профессиональных и социальных функций, что наносит обществу материальный и духовный ущерб.
Опыт других стран, например США, показал, что мультидисциплинарный подход, ранняя диагностика и обучение больных позволяют снизить количество язв стопы и ампутаций на 49–85% и существенно уменьшить расходы государства. Использование программ по профилактике осложнений и обучению больных СД приводит к уменьшению количества ампутаций почти в 2 раза, а экономический эффект от внедрения программ обучения составил 10 млн долл. [2, 5, 9, 11, 13, 21].
Учитывая вышеизложенное, 20 апреля 2015 г. в Кремле Президент РФ Владимир Путин подписал Закон о ратификации соглашения о сотрудничестве стран СНГ в борьбе с ростом заболеваемости сахарным диабетом [18], что в сочетании с грамотным ведением пациентов с СДС может улучшить прогноз как для этих пациентов, так и для больных СД в целом.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 28 августа 2017;
проверки требуют 11 правок.
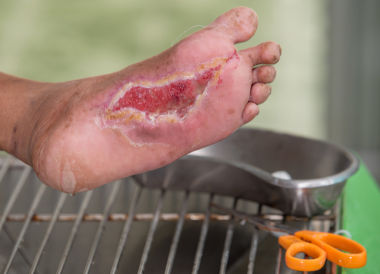
Синдро́м диабети́ческой стопы́ (диабети́ческая стопа́, англ. diabetic foot) — комплекс анатомо-функциональных изменений, развивающихся на фоне диабетической нейропатии, микро- и макроангиопатии, остеоартропатии, способствующих повышенной травматизации и инфицированию мягких тканей стопы, развитию гнойно-некротического процесса и в запущенных случаях ведущий к ампутации[1]. Синдром диабетической стопы собирательное понятие, объединяющее группу поздних осложнений сахарного диабета, при которых развиваются патологические изменения стоп больного в виде гнойно-некротических процессов, язв и костно-суставных поражений, возникающие на фоне специфических изменений периферических нервов, сосудов, кожи и мягких тканей, костей и суставов. В ряде случаев понятие «диабетическая стопа» как самостоятельная нозологическая форма не используется, а указываются составляющие её заболевания (абсцесс, флегмона, гангрена и другие).
Актуальность[править | править код]
Синдром диабетической стопы является основной причиной ампутаций конечностей при сахарном диабете. Поражены около 8-10 % больных сахарным диабетом, а 40-50 % из них могут быть отнесены в группы риска. В 10 раз чаще синдром диабетической стопы развивается у лиц со вторым типом сахарного диабета. По меньшей мере, у 47 % больных лечение начинается позднее возможного. Результатом являются ампутации конечностей, увеличивающие смертность больных в 2 раза и повышающие дальнейшую стоимость лечения и реабилитации больных в 3 раза. Совершенствование тактики диагностики, диспансеризации, лечения больных позволяют снизить частоту ампутаций у больных на 43-85 %.
Синдром диабетической стопы развивается у большинства больных сахарным диабетом 1 типа к 7-10 годам с начала болезни[источник не указан 2834 дня], у больных сахарным диабетом 2 типа может иметь место с начала заболевания. В 85 % случаев представлен язвами стоп разной тяжести. По оценкам исследований, частота проявления патологии в сообществе больных диабетом, в течение жизни составляет около 15% и может достигать пикового значения в 25%.[2]
Классификация[править | править код]
По форме
- Нейропатическая форма. Проявляется деструктивным процессом на стопе на фоне диабетической полиневропатии
- Нейроишемическая форма. Имеет место на фоне диабетической ангиопатии
- Остеоартропатическая форма
- Острая стадия
- рентген-негативный период
- рентген-позитивный период
- Подострая стадия
- Хроническая стадия
- Острая стадия
По наличию осложнений
- Хроническая критическая ишемия конечности
- Язва, локализация, степень по Вагнеру (1-5)
- Синдром Менкеберга
- Патологический перелом
- Деформация стопы
Группы риска[править | править код]
Примерно 40-50 % больных сахарным диабетом относятся к группам риска. Критериями отнесения больного в группу риска по синдрому диабетической стопы являются:
- явления периферической нейропатии,
- отсутствие пульса на артериях стоп,
- деформация стопы,
- выраженные гиперкератозы стопы,
- наличие язв, гнойно-некротических процессов, ампутаций в анамнезе.
Принято выделять три группы риска:
- I. Чувствительность сохранена во всех точках, пульсация на артериях стопы хорошая. Обследуются ежегодно.
- II. Чувствительность снижена, отсутствует дистальный пульс, имеются деформации. Обследуются раз в ½ года.
- III. В анамнезе — язвы и/или ампутации на стопе, значительная нейропатия. Обследуются раз в 3 месяца.
Обследование[править | править код]
В обследовании больных с диабетической стопой применяется мультидисциплинарный подход.
Примерная программа обследования:
1. Выполняется всем больным при каждой консультации
- осмотр специалистов центра диабетической стопы: эндокринолога, хирурга c обязательной оценкой неврологического дефицита по шкале НДС, измерения порога вибрационной чувствительности (камертон, биотензиометр);
- консультация невропатолога;
- консультация офтальмолога (осмотр глазного дна);
- измерение лодыжечно-плечевого индекса (допплеровский аппарат);
- измерение транскутанного напряжения по кислороду;
- гликемический профиль и определение уровня гликозилированного гемоглобина;
- липиды крови: уровень холестерина, ЛПНП, триглицериды, ЛПВП.
2. У больных с отсутствием пульса на артериях стопы, снижением ЛПИ ниже 0,9, снижением ТсРО2 ниже 60, клиникой перемежающейся хромоты
- ультразвуковая допплерография и цветное дуплексное картирование артерий нижних конечностей;
- консультация ангиохирурга.
3. У больных с деформациями на стопе, выраженным гиперкератозом
- рентгенография стоп;
- консультация ортопеда.
4. У больных с язвенными дефектами стоп
- микробиологическое исследование раневого отделяемого (посев);
- рентгенография стоп (при язвенных дефектах 2 и выше степени по Вагнеру);
- общий анализ крови.
Лечение[править | править код]
Консервативное[править | править код]
Диабетическая стопа, требующая проведения консервативной терапии
Терапия диабетической стопы включает базовые (обязательные для всех больных) и дополнительные (применяемые по показаниям) мероприятия
К базовым относятся:
- профилактика полинейропатии: контроль глюкозы, давления, гиперлипидемии;
- подиатрический уход за стопой;
- разгрузка стопы.
К дополнительным:
- антимикробная терапия (антибиотики широкого спектра действия, по результатам взятого материала из язв; дозировка индивидуальна);
- лечение болевого синдрома (обезболивающие препараты);
- лечение нейропатии;
- лечебная разгрузка и иммобилизация стопы;
- лечение ангиопатии путём улучшения кровотока;
- местное лечение язв и ран (местные антисептические и антибактериальные препараты).
Антибактериальная терапия инфицированной диабетической стопы[править | править код]
На начальном этапе лечения выбор схемы антибиотикотерапии включает оценку спектра возможных микроорганизмов-возбудителей инфекции и степени выраженности ишемии конечности, и, кроме того, определение пути введения препарата.
При инфекциях легкой степени и неосложненных инфекциях средней степени тяжести рекомендуется пероральное назначение антибиотиков, активных в отношении аэробных грамположительных кокков и характеризующихся высокой биодоступностью при приеме внутрь (цефалексин, клиндамицин, линкомицин, ко-тримоксазол).
Для лечения тяжелых инфекций, а также распространенных, хронических инфекций средней степени тяжести для эмпирической терапии используют антибиотики с широким спектром действия. Схема лечения должна включать в себя препараты, активные как в отношении грамположительных кокков (в том числе и метициллинорезиистентного золотистого стафилококка), так и грамотрицательных бактерий и облигатных анаэробов (левофлоксацин, ципрофлоксацин, клиндамицин, имипенем, цефтазидим в комбинации с метронидазолом). Путь введения антибиотика должен быть парентеральным, в особенности на начальном этапе лечения, с целью быстрого достижения эффективной концентрации препарата в зоне язвенного дефекта.[3]
Оперативное[править | править код]
Запущенный случай диабетической стопы (гангрена пальцев), требующий хирургического вмешательства
Понятие хирургическое лечение диабетической стопы объединяет:
- вскрытие абсцессов, флегмон, некрэктомии;
- оперативные вмешательства с целью восстановления артериального кровоснабжения стопы — ангиопластика и стентирование артерий нижних конечностей, аутовенозное шунтирование, эндартерэктомия;
- ампутации и экономные резекции.
Новые методы лечения[править | править код]
В мире постоянно исследуются новые методики терапии синдром диабетической стопы. Главными целями исследований является получение более эффективных и быстрых методов заживление ран, которые появляются как результат заболевания. Новые методы значительно снижают необходимость ампутаций конечностей, которая так велика при этом заболевании.
В Германии уже изучены и внедрены в практику целый ряд методов лечения диабетической стопы. На основании различных клинических исследований и апробаций новые методы терапии оценены мировым медицинским сообществом как очень перспективные.[4]
К ним относятся:
- Метод экстракорпоральной ударно-волновой терапии;
- Терапия факторами роста;
- Лечение с помощью применения стволовых клеток[5];
- Терапия методом плазменной струи;
- Био-механический способ;
Рекомендации больным[править | править код]
Основные рекомендации больным содержат ответы на следующие вопросы:
Что делать всегда?
- строго контролировать уровень глюкозы в крови, вовремя консультироваться у своего эндокринолога;
- отказаться от курения;
- носить хлопчатобумажные или шерстяные носки (не синтетические), свободную кожаную обувь;
- ежедневно проводить гимнастику для стоп, ходить не менее 2 часов;
- лечить у дерматолога грибковые поражения ногтей (потемнение, расслоение ногтя);
- не реже 1 раза в год (а при наличии изменений — 1 раз в месяц) обследоваться в отделении диабетической стопы.
Что делать каждым вечером?
- внимательно осмотреть стопы, используя зеркало для осмотра плохо доступных участков (при плохом зрении нужно воспользоваться помощью родных);
- вымыть ноги теплой (ни в коем случае не горячей) водой с детским мылом или слаборозовым раствором перманганата калия;
- тщательно высушить кожу личным полотенцем, особенно межпальцевые промежутки (промокать, а не тереть);
- смазать кожу смягчающим (витаминизированным, бактерицидным) кремом тонким слоем;
- межпальцевые промежутки обработать водкой;
- если нужно, очень аккуратно постричь ногти, оставляя их не очень короткими, состригая ноготь прямо (при плохом зрении самостоятельно стричь ногти запрещено).
Чего не делать?
- не ходить босиком, особенно на улице, в местах общего пользования;
- не парить ноги, не мыть их горячей водой;
- не пользоваться грелками;
- не делать солевых ванночек;
- не пользоваться мазевыми повязками без назначения врача;
- не применять средства для размягчения мозолей;
- не пользоваться чужими носками, обувью, не посещать общую баню;
- не подходить близко к открытому огню и нагревательным приборам;
- не обрабатывать ноги, не стричь ногти самостоятельно при плохом зрении;
- не заниматься самостоятельным лечением. Самостоятельно не лечить мозоли, потертости, натоптыши, гиперкератозы, трещины.
Когда обращаться к специалисту?
- при развитии вросшего ногтя;
- при ушибах, потертостях, ожогах;
- при потемнении пальцев, появлении болей в икрах при ходьбе и в покое;
- при потере чувствительности стоп;
- при ранах любого размера и любой причины;
- при язвах и нагноениях;
- когда подошел срок, назначенный врачом отделения диабетической стопы, или возникли любые вопросы, касающиеся стоп.
Прогноз[править | править код]
Развитие диабетической стопы (и тем более гангрены) очень опасно для здоровья человека. Несложные принципы профилактики, своевременно проводимые пациентами, в большинстве случаев позволяют избежать появления диабетических язв[1].
Сахарный диабет и его последствия, такие как диабетическая стопа — основная причина ампутаций ног.
Профилактика[править | править код]
Основополагающие принципы профилактики развития диабетических язв[1]:
- ежедневно мыть и тщательно промакивать кожу ног, избегать воздействия высоких температур (горячая вода, небезопасная близость ног к отопительным приборам), в случае развития диабетической нейропатии (особенно в стадии потери болевой и температурной чувствительности) температуру воды в ванной перед мытьём определять термометром, а не «пробовать ногой»;
- регулярно осматривать кожу стоп с целью раннего выявления потёртостей, волдырей-водянок, порезов и трещин, пользоваться зеркалом для осмотра подошвы;
- не пользоваться грелками (особенно электрическими) и не держать ноги в горячей воде (выше рекомендованной врачом температуры);
- не ходить босиком;
- не использовать мозольные пластыри;
- каждый день проверять обувь руками на наличие посторонних предметов и внутренних повреждений, способствующих появлению мозолей;
- не носить носки (чулки) со швами;
- никогда не надевать обувь без стелек и на босую ногу;
- правильно выбирать обувь: подбирать и носить только мягкую и просторную (широкую) обувь;
- не срезать появившиеся мозоли самостоятельно — при их появлении обращаться в отделение диабетической стопы, доверяя лечение специально подготовленному персоналу;
- срезать ногти на ногах только прямо (не полукругом!);
- в случае возникновения вросшего ногтя или выявления других травматических повреждений стопы немедленно обратиться к врачу.
Примечания[править | править код]
- ↑ 1 2 3 Малая энциклопедия врача-эндокринолога / Ефимов А. С. — 1-е изд. — Киев: Медкнига, ДСГ Лтд, Киев, 2007. — С. 170-181. — 360 с. — («Библиотечка практикующего врача»). — 5000 экз. — ISBN 966-7013-23-5.
- ↑ Benjamin A. Lipsky, David G. Armstrong, Nalini Singh. Preventing Foot Ulcers in Patients With Diabetes (англ.) // JAMA. — 2005-01-12. — Vol. 293, iss. 2. — P. 217–228. — ISSN 0098-7484. — doi:10.1001/jama.293.2.217.
- ↑ Французов В. Н., Хайкина Е. В., Решедько Г. К. Диагностика и лечение хирургических инфекций стопы при сахарном диабете // Клин. Микробиол. Антимикроб. Химиотер. — 2005. — Т. 7, № 3. — С. 235—244.
- ↑ «Новые методы лечения диабетической стопы» Серия статей © 2013 Deutsche Medizinmanagement Zentrum «Deutsche Arzt»
- ↑ Maksimova N., Krasheninnikov M., Zhang Y., Ponomarev E., Pomytkin I., Melnichenko G., Lyundup A. Early passage autologous mesenchymal stromal cells accelerate diabetic wound re-epithelialization: A clinical case study // Cytotherapy. — 2017. — doi:10.1016/j.jcyt.2017.08.017.
Литература[править | править код]
- International Consensus and Guidelines on the Diabetic Foot, December 15, 1997; May, 1999
- Гурьева И. В., Кузина И. В., Воронин А. В. и др. Синдром диабетической стопы. Методические рекомендации. Москва, 2000
- Гурьева И. В., Комелягина Е. Ю., Кузина И. В. Диабетическая периферическая сенсомоторная нейропатия. Патогенез, клиника и диагностика. Методические рекомендации. Москва, 2000
- Приказ МЗ РФ № 267 от 16.07.2001 «О развитии диабетологической помощи населению Российской Федерации»
- Клинико-функциональные особенности и медико-социальная реабилитация больных сахарным диабетом, осложненным синдромом диабетической стопы. Министерство социальной защиты населения РФ. Москва, 1994
- Стандарты диагностики и обследования больных с синдромом диабетической стопы и групп риска. Сост. Б. И. Яремин, Самара, 2006
- Применение новых технологий в лечении синдрома диабетической стопы: клинический случай. О. В. Удовиченко Г. Р. Галстян И. А. Ерошкин А. А. Ефимов О. В. Носов Ю. Г. Васильев. Лечащий врач. — 2003.- № 10.
- Гнойно-некротические поражения нейроишемической формы синдрома диабетической стопы. Новые возможности комплексного хирургического лечения. В. А. Митиш, И. А. Ерошкин, А. В. Ерошенко [и др.]. Эндокринная хирургия. −2008. — № 1.
- Роль рентгеноэндоваскулярного восстановления артерий нижних конечностей в лечении синдрома диабетической стопы. И. А. Ерошкин [и др.]. Медицинская визуализация. — 2009. — № 11.
Ссылки[править | править код]
- Новые методы лечения диабетической стопы — серия статей, © 2013 Deutsche Medizinmanagement Zentrum «Deutsche Arzt»
- Как правильно ухаживать за ногами при диабете — WebMedInfo.ru
- Антибактериальная терапия инфицированной диабетической стопы
- Эберпрот П (Heberprot P 75) при лечении диабетической стопы.
Источник
