Цитокины и синдром сухого глаза
Содержание | Следующая статья
Н.М. Калинина, В.Ю. Попов, В.В. Бржеский
В последние годы синдром «сухого глаза» представляет собой одно из самых распространенных заболеваний органа зрения. Ксерозом эпителия глазной поверхности страдают до 12 % больных офтальмологического профиля в возрасте до 40 лет и свыше 67 % пациентов — старше 50 лет. В основе патофизиологических механизмов развития ксероза эпителия глазной поверхности ключевую роль играют воспалительные процессы, опосредованные Т-лимфоцитами. Эти клетки и запускают каскад воспалительных цитокинов, вызывающих повреждение и апоптоз бокаловидных клеток, продуцирующих муцины слезной жидкости. В силу этих обстоятельств возникающий дефицит муцинов способствует снижению стабильности слезной пленки, поддерживая тем самым порочный круг. Уровень концентрации провоспалительных цитокинов в слезной жидкости может служить маркером активности воспаления глазной поверхности. В силу этого иммунопатологические процессы определяют клиническое течение ксероза и его возможный прогноз. (Цитокины и воспаление. 2015. Т. 14. № 1. С. 5–10.)
Ключевые слова: синдром «сухого глаза», воспаление, цитокины, глазная поверхность, слезная жидкость.
Синдром «сухого глаза» (ССГ) является одним из самых распространенных заболеваний органа зрения, диагностируемых офтальмологами в настоящее время во всем мире. При этом частота его возникновения значительна и продолжает увеличиваться. Так, по данным Marquardt R. и Wenz F.N., в 1980 г. ССГ можно было обнаружить у 30 % пациентов, впервые обратившихся к офтальмологу, в 1995 г. ССГ был выявлен у 2 % населения мира, а уже в 2004 г. Schirra F.и Ruprecht K.W. приводят данные распространенности ССГ от 5,2 до 63 % [31, 41, 47]. При этом частота встречаемости ССГ в популяции коррелирует с увеличением возраста пациентов [25]. По данным Бржеского В.В. и Сомова Е.Е. (2009), у 30–40 % больных офтальмологического профиля можно обнаружить признаки, присущие ССГ. Причем до 12 % из них находятся в возрасте до 40 лет, а 67 % — старше 50[1].
Наряду с известными причинами (синдромом Съегрена, перименопаузой, другой эндокринной патологией, дисфункцией мейбомиевых желез и многими другими), в настоящее время развитию ССГ способствует увеличение спектра экзогенных факторов: работа с компьютерными мониторами, использование в офисных помещениях и в автомобилях кондиционеров, внедрение и широкое распространение кераторефракционной хирургии, косметические процедуры, применение средств контактной коррекции зрения, современных медикаментозных препаратов различной направленности и других «составляющих» жизни современного цивилизованного общества.
В целом, ССГ можно определить как комплекс признаков ксероза поверхности глазного яблока вследствие длительного нарушения стабильности слезной пленки (СП) [1]. В силу этого рядом авторов выделяются три этиологических типа роговично-конъюнктивального ксероза: 1) в результате дефицита слезопродукции, 2) при повышенной испаряемости СП и 3) в связи с одновременным воздействием на передний сегмент глазного яблока первых двух факторов [1, 3, 55].
Первый патогенетический тип ССГ связан с сокращением продукции слезной жидкости, что приводит к истончению СП. В силу этого обстоятельства повышается испаряемость водной составляющей слезной пленки, а ее липидный и муциновый слои «слипаются». Это приводит к образованию на поверхности роговицы несмачиваемых слезной жидкостью участков. Как показали исследования Tsubota при снижении слезопродукции с 1,2 до 0,12 мкл/мин даже нормальная испаряемость влаги сопровождается потерей до 78 % ее объема [54]. К этому же патогенетическому типу ССГ относятся и те клинические формы патологии органа зрения, течение которых сопровождается дисфункцией желез, продуцирующих липиды и/или муцины.
Второй патогенетический тип ССГ обусловлен нарушением стабильности СП вследствие различных причин, но, прежде всего, из-за ее активного испарения. Такой механизм развития патологического процесса характерен для тех случаев, когда в силу разных причин увеличивается экспонируемая площадь глазной поверхности и продолжительность ее обнажения (лагофтальм, экзофтальм, сокращение числа мигательных движений век или их анатомические аномалии). Функциональная недостаточность СП может возникать и в силу негативного воздействия на нее экзогенных факторов или недостаточной конгруэнтности век.
Третий патогенетический тип ССГ обусловлен одновременным воздействием на передний сегмент глазного яблока первых двух этиологических факторов.
Уже более двух десятилетий известно, что в патофизиологических механизмах развития ССГ ключевую роль играет воспаление, опосредованное Т-лимфоцитами, которое в ряде случаев носит аутоиммунный характер [2, 18, 19, 23, 24, 38, 40, 42, 52].
Воспалительный генез ССГ, хроническая иммунная стимуляция конъюнктивального эпителия и железистых структур подтверждается рядом авторов обнаружением в слезе высоких концентраций провоспалительных цитокинов [40, 42–44, 49, 53]. Патологическое усиление продукции провоспалительных цитокинов дестабилизирует равновесие глазной поверхности, поддерживает длительное воспаление, вызывает апоптоз бокаловидных клеток, снижает содержание муцина в слезной пленке. Возникающий в силу изложенных обстоятельств дефицит муцина еще больше снижает стабильность СП, что поддерживает порочный круг [17, 22, 23, 34–38, 48].
При возникновении ССГ дисфункция прероговичной слезной пленки и развивающийся в эпителии глазной поверхности ксеротический процесс стимулируют продукцию провоспалительных цитокинов, что приводит к созреванию незрелых антиген-презентирующих клеток (iAPC) с выраженной иммуностимулирующей активностью. Зрелые APC мигрируют в регионарные лимфатические узлы, контактируя с «наивными» (не дифференцированными) Т-хелперами (Th0), способствуя образованию Т-хелперов 1 (Th1) и Т-хелперов 17 (Тh17). Th17 являются антагонистами регуляторных Т-клеток (Treg) и приводят к потере функций подавления цитотоксических Т-клеток Treg-клетками. Затем активированные Т-клетки мигрируют к эпителию глазной поверхности, где запускают каскад провоспалительных цитокинов, приводящий в дальнейшем к апоптозу клеток эпителия глазной поверхности.
Молекулярные механизмы воспалительного процесса, протекающие при ССГ, выглядят следующим образом: дисфункция СП приводит к активации митоген-активированных протеинкиназ (МАРК), основная функция которых заключается в запуске системы передачи и усиления сигнала работающей по каскадному принципу активации белков в определенной последовательности. Это происходит при воздействии на клетку цитокинов и факторов роста). К МАРК относятся с-junN-терминальные киназы (cJNK), внеклеточные киназы (ERK) и протиеинкиназы р38 [29]. Они, в свою очередь, инициируют фосфорилирование белков. Этот процесс вызывает активацию факторов ядерной транскрипции: ядерный фактор каппа β (NF-κB), активатор белка-1 (AP-1) и фактор активации транскрипции (ATF). Они и инициируют продукцию провоспалительных медиаторов клетками эпителия глазной поверхности [13, 28]. Основными из провоспалительных медиаторов, продуцируемых клетками эпителия глазной поверхности, являются интерлейкин1 (IL-1), интерлейкин 6 (IL-6), фактор некроза опухоли α (TNFα), хемокины и матриксные металлопротеиназы (MMP) [5, 11, 26, 27, 29, 40, 58]. Провоспалительные медиаторы обеспечивают активацию APC, состоящих из дендритных клеток и макрофагов. APC мигрируют по афферентным лимфатическим сосудам в регионарную лимфоидную ткань, где происходит их дальнейшая дифференцировка в тканевые Th1 (CD4+Т-клетки) и Th17. Затем они мигрируют по эфферентным кровеносным сосудам к глазной поверхности, где приводят к дальнейшему освобождению провоспалительных цитокинов. Th1 секретируют интерферон γ (IFNγ), активирующий выработку хемокинов, и молекулы клеточной адгезии (САМ), которые способствуют дальнейшей миграции Th17 к глазной поверхности. Кроме того, Th1 способствуют созреванию макрофагов собственно глазной поверхности, а Th17 вырабатывают IL-17, который стимулирует выработку MMP, что приводит к повреждению эпителиальных клеток [9]. Следует отметить также, что IL-17 усиливает продукцию фактора роста эндотелия сосудов (VEGF), вызывая лимфоангиогенез и дальнейшую миграцию иммунокомпетентных клеток. Так формируется в тканях, формирующих глазную поверхность, хроническое воспаление, лежащее в основе ССГ [23, 51].
В настоящее время в патогенезе ССГ в наибольшей степени исследована роль интерлейкинов, фактора некроза опухоли и интерферонов [2, 4, 10, 30, 38, 57]. Провоспалительный цитокин IL-1 является одним из наиболее изученных медиаторов воспаления и иммунитета, определяющихся в слезной жидкости, в том числе, и при ССГ [15, 39]. В настоящее время под названием IL-1 известны 2 полипептида: IL-1α и IL-1β. Обе молекулы активируют один и тот же рецептор и вызывают сходные биологические эффекты. Кроме того, есть и третий белок со сходной структурой и обладающий способностью специфически связываться с рецепторами IL-1: рецепторный антагонист IL-1 (IL-1Ra).
IL-1 является пусковым провоспалительным цитокином, который активирует каскад других провоспалительных цитокинов. А именно, IL-1 активирует продукцию IL-6 и TNFα. Это было доказано работами Narayanan S. et al. при моделировании ССГ на мышах: при блокировании рецепторов IL-1 происходит снижение содержания уровней IL-6 и TNFα в слезной жидкости [39]. При этом взаимодействие IL-1 и TNFα увеличивает выработку хемокинов, необходимых для хемотаксиса и продукции MMP [8, 13, 20, 45].
Содержание | Следующая статья
Источник
Дата публикации 11 ноября 2019Обновлено 11 ноября 2019
Определение болезни. Причины заболевания
Синдром сухого глаза (сухой кератоконъюнктивит) — это воспалительное состояние глаза, при котором слёзная плёнка изменяется по своему химическому и количественному составу. Проявляется комплексом симптомов, таких как жжение, чувство рези и инородного тела в глазу.
По данным различных авторов, сухость глаза встречается примерно у 15-17 % взрослых, проживающих в развитых странах. Этот показатель каждый год увеличивается. За последние 30 лет синдром сухого глаза стал встречаться в 4,5 раза чаще [1].
Одна из причин такого увеличения распространённости синдрома связана с развитием рефракционных хирургических вмешательств — лазерного кератомилёза, фоторефракционной кератэктомии, передней радиальной кератотомии и других. Во время этих операций нарушается иннервация роговицы.
На рост данной патологии также оказывают влияние:
- повсеместное использование смартфонов, планшетов, компьютеров, другого офисного оборудования, а также кондиционеров, так как они высушивают воздух;
- ношение мягких контактных линз;
- регулярный приём лекарств — мочегонных, противоаллергических препаратов, антидепрессантов, средств для снижения холестерина, бета-блокаторов, противозачаточных таблеток [1].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы синдрома сухого глаза
Часто встречаемые симптомы [11]:
- раздражение (покраснение) глаз;
- ощущение инородного тела в глазах;
- чувство жжения;
- слизистое отделяемое в виде нитей;
- периодические «затуманивание».
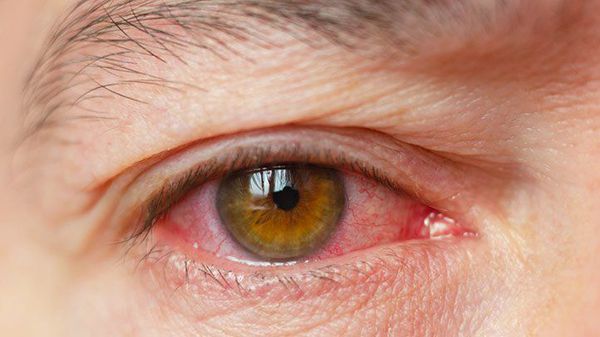
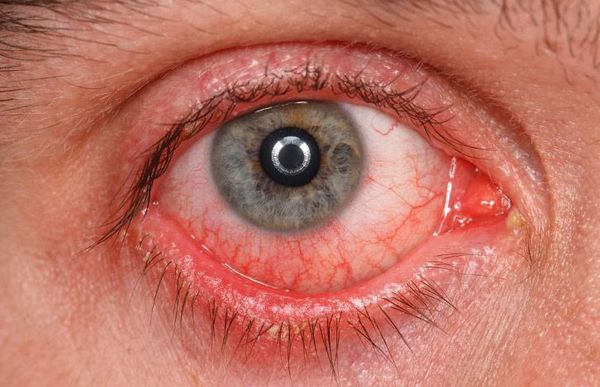
Реже наблюдается зуд в глазу, светобоязнь, утомление или чувство тяжести в глазах. При этом чувства стянутости и давления за глазами не возникают.
Как правило, все перечисленные симптомы проявляются на обоих глазах, но иногда они возникают только в одном глазном яблоке.
Любопытно, что пациенты с синдромом сухого глаза редко жалуются на сухость глаз, хотя иногда они отмечают нехватку эмоциональных слёз или отсутствие слезотечения в ответ на раздражитель, например, лук. В некоторых случаях пациентов беспокоит слезотечение, особенно на улице, так как там много раздражающих факторов — яркое солнце, ветер, холод. От возникающего слезотечения они испытывают дискомфорт.
Признаки сухого кератоконъюнктивита часто усиливаются из-за воздействия внешних факторов, связанных с повышенным испарением слезы от ветра, кондиционера, отопления или при длительном чтении, так как человек начинает реже моргать. При закрытых веках симптомы уменьшаются [5].
Патогенез синдрома сухого глаза
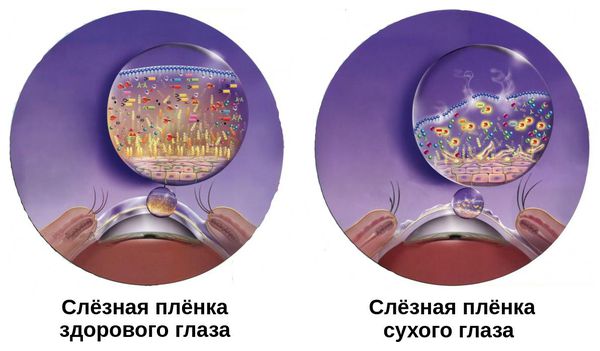
Патогенез сухого кератоконъюнктивита связан с нарушением стабильности слёзной плёнки. Она покрывает переднюю поверхность глаза. В норме её толщина составляет около 10 мкм. При развитии синдрома она становится тоньше.
Распределение слёзной плёнки поверхности глаза происходит благодаря рефлекторному морганию. Для её эффективного распределения должны сочетаться несколько факторов:
- нормальный моргательный рефлекс;
- контакт век и глазной поверхности;
- нормальный эпителий (внешний слой) роговицы.
Слёзная плёнка неоднородна. Она имеет три слоя:
- первый (внешний) слой — липидный — вырабатывается мейбомиевыми железами;
- второй слой — водный — вырабатывается слёзными железами;
- третий слой — муциновый — вырабатывается бокаловидными клетками роговицы.
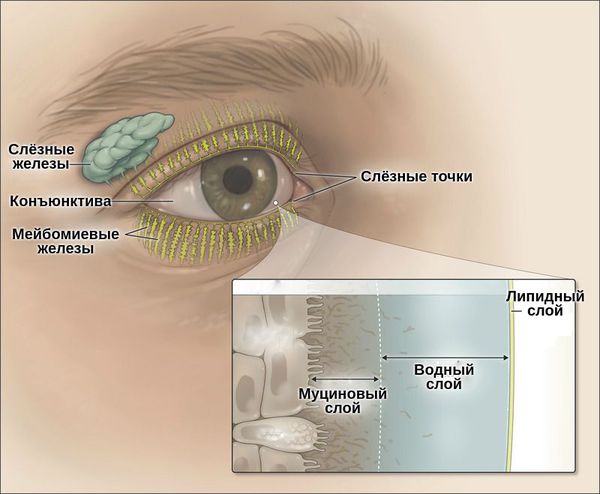
Липидный слой — самый тонкий. Его основная задача — задерживать испарения водного слоя и поддерживать слёзную плёнку. При его нехватке увеличивается испаряемость слезы, что приводит к «сухому глазу».
Водный слой является основой слёзной плёнки. Он состоит из воды, электролитов и белков. За счёт непрерывного обновления он выполняет своё предназначение — доставляет кислород к эпителию роговицы, защищает от бактерий, вымывает инородные тела, обеспечивает гладкость и ровность оптической поверхности.
Муциновый слой состоит из муцинов, которые помогают слёзной плёнке удерживаться на роговице. Он увлажняет и смазывает роговичный эпителий. Его дефицит может быть вызван как нехваткой водного слоя, так и высокой испаряемостью слёзной жидкости. Другой причиной нарушения муцинового слоя может стать повреждение бокаловидных клеток, которые его продуцируют. Это происходит при рубцующемся конъюнктивите, нехватке витамина А, химических ожогах, токсическом воздействии медикаментов [3].
Исходя из особенностей строения слёзной плёнки, патогенез сухого кератоконъюнктивита затрагивает несколько звеньев образования и функционирования слёзной плёнки [1]:
- выработка слезы, муцинов и липидов;
- скорость испарения слёзной плёнки;
- образование слёзной плёнки на поверхности эпителия роговицы.
Классификация и стадии развития синдрома сухого глаза
Единой классификации данного синдрома пока нет, но существует несколько авторских классификаций. Вот некоторые из них.
Национальный глазной институт Америки выделяет две основные категории синдрома:
- Снижение выработки слезы:
- синдром Шегрена — нарушение работы слюнных и слёзных желёз, которое приводит к развитию синдрома сухого глаза;
- снижение выработки слезы, не связанное с синдромом Шегрена.
- Увеличение испарения слезы:
- воспалительное заболевание мейбомиевой железы;
- атрофия мейбомиевых желёз.
Доктор B. Dohlman классифицирует синдром в зависимости от причин снижения слезопродукции слёзным железами:
- Дефицит слезопродукции — обычно связан со скоплением лимфоцитов в ткани слёзной железы:
- синдром Шегрена;
- коллагеноз (синдром Райли — Дея) — редкое наследственное заболевание, которое поражает периферическую нервную систему.
- Дефицит муцина:
- синдром Стивенса Джонсона — тяжёлая системная аллергия, которая снижает защитные свойства муцина;
- глазной пемфигоид — хроническое заболевание глаз аутоиммунного генеза, приводит к недостатку муцина;
- авитаминоз витамина А, который входит в состав муцина.
- Изменённая поверхность роговицы — наблюдается при трахоме (хроническом конъюнктивите, вызванном хламидиями), простом герпесе, роговичных дистрофиях. Повреждённые места уязвимы для инфекций и появления язв.
- Недостаточность увлажнения. Связана с нейропаралитическим кератитом — воспалительно-дистрофическим изменением роговицы на фоне поражения тройничного нерва. Проявляется снижением или отсутствием чувствительности роговицы, невралгическими болями, помутнением и язвой роговицы.
Азиатское общества сухих глаз (ADES) также классифицирует синдром по причинам его возникновения [2]:
- дефицит воды;
- снижение смачиваемости;
- увеличение испарения.
По клиническим проявлениям — жжению, зуду, рези, ощущению тяжести и инородного тела в глазах, слезотечению, светобоязни, уменьшению симптомов после закрытия глаз — синдром сухого глаза бывает:
- слабым — 1-2 симптома;
- умеренным — 3-5 симптомов;
- тяжёлым — более 5 симптомов.
Осложнения синдрома сухого глаза
В зависимости от стадии синдрома у человека может временно ухудшаться зрение, которое восстанавливается при моргании.
Сухость глаза повышает вероятность возникновения бактериального кератита и частого изъязвления, которые могут стать причиной появления перфорации роговицы [5]. Клинически бактериальный кератит проявляется:
- острой болью в глазу;
- отёком;
- корнеальным синдромом — светобоязнью, слезотечением, непроизвольным «зажмуриванием»;
- выраженной воспалительной инъекцией глазного яблока;
- слизисто-гнойными выделениями;
- помутнениями роговицы;
- поверхностными или глубокими изъязвлениями роговицы.
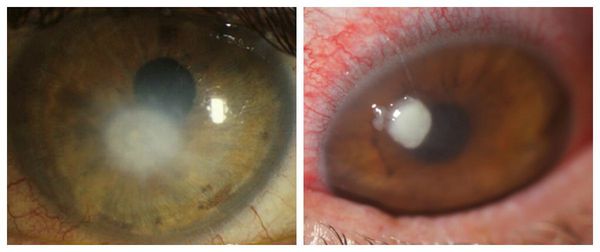
Перфорация роговицы опасна серьёзным снижением зрения, которое может потребовать пересадку роговицы.
Диагностика синдрома сухого глаза
При проведении биомикроскопии врач-офтальмолог может разглядеть признаки нарушения слёзной плёнки и роговицы.
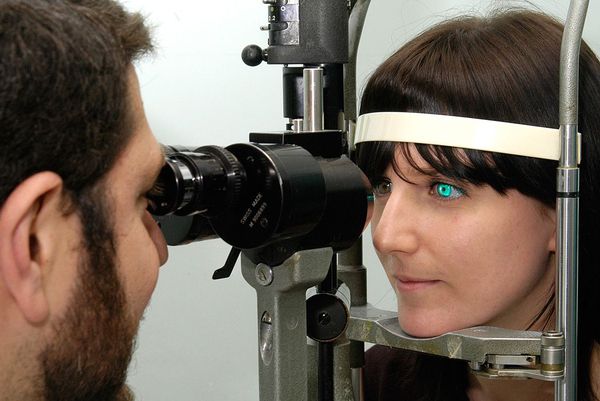
Нарушения слёзной плёнки:
- Появление нитей муцина — признак раннего сухого кератоконъюнктивита. В здоровом глазу после разрыва слёзной плёнки муциновый и липидный слои смешиваются и быстро смываются. При синдроме сухого глаза муцин также смешивается с липидным слоем, но не вымывается, а скапливается в слёзной плёнке и смещается при мигании.
- Уменьшение слёзного мениска — объёма водного слоя слёзной плёнки. В норме он представляет собой выпуклую полосу с правильным верхним краем. При сухом кератоконъюнктивите слёзный мениск становится вогнутым, неравномерным, тонким, а иногда вовсе исчезает.
- Отделяемое в виде пены — возникает в слёзной плёнке или по краю века при нарушении работы мейбомиевых желёз.
Нарушения роговицы:
- Точечная эрозия роговицы — возникает в нижней половине роговицы.
- Появление роговичных нитей. Они состоят из небольших комочков слизи в форме запятой. Одни концы нитей прикрепляются к поверхности роговицы, другие свободно двигаются при мигании.
- Наличие нитчатых инфильтратов — полупрозрачные бело-серые немного выпуклые образования. Как правило, их обнаруживают одновременно с нитями слизи во время окрашивания бенгальским розовым красителем [5].
Для подтверждения и постановки диагноза сухости глаз также проводят различные тесты. Чем выраженнее синдром, тем они надёжнее. Во время тестов измеряют следующие параметры [3]:
- стабильность слёзной плёнки и время её разрыва;
- выработка слезы — тест ширмера, осмолярность слезы;
- заболевание глазной поверхности — окрашивание поверхности глаза.
Тест на время разрыва слёзной плёнки
Время разрыва слёзной пленки — показатель её стабильности. Его измеряют следующим образом:
- в нижний свод конъюнктивы закапывают флуоресцеин;
- просят пациента мигнуть несколько раз, а затем не моргать;
- через щелевую лампу с кобальтовым синим фильтром исследуют срез слёзной плёнки.
Через некоторое время в окрашенной плёнке возникают чёрные линии или пятна, которые указывают на появление сухих участков. Важно зафиксировать время между последним миганием и появлением первых сухих участков. Если данный промежуток длится менее 10 секунд, то это отклонение от нормы.
Тест Ширмера
Данный тест проводят для оценки слезопродукции. С его помощью измеряют увлажнённую часть специальными бумажными фильтрами. Тест проводят следующим образом:
- осторожно убирают имеющуюся слезу;
- согнутый бумажный фильтр помещают в полость конъюнктивы, не касаясь роговицы;
- просят пациента не закрывать глаз и моргать как обычно;
- через пять минут фильтры убирают и оценивают уровень увлажнения: 6-10 мм — это норма, диапазон менее 6 мм указывает на снижение выработки слезы.
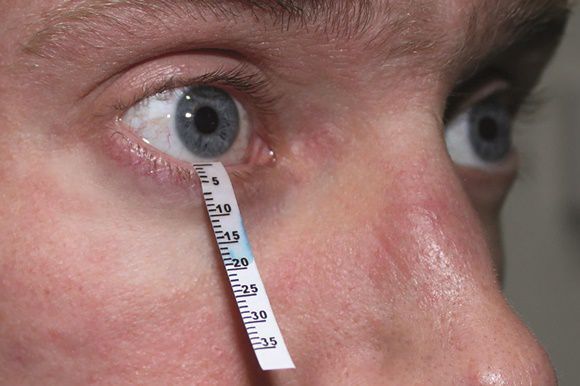
Тест с окрашиванием глазной поверхности
Специальные красители используют для окрашивания нежизнеспособных клеток муцина. Бенгальский розовый краситель прокрашивает изменённую поверхность роговицы в виде двух треугольников. Роговичные нити и инфильтраты также окрашиваются, но ещё интенсивнее. Минусом бенгальского розового в том, что он может вызвать гиперемию (покраснение) глаз, особенно при выраженном синдроме [5]. Тест с лиссаминовым зелёным вызывает меньше раздражения.
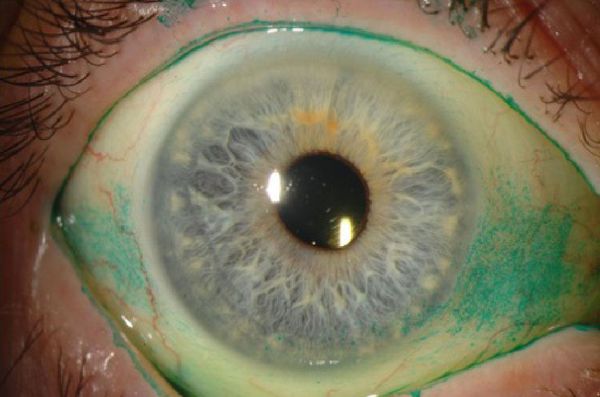
Другие способы диагностики
Помимо основных перечисленных методов диагностики иногда используют следующие тесты [3]:
- осмолярность слёзной плёнки;
- измерение состава слезы;
- слёзная менискометрия;
- импрессионная цитология;
- тест на лактоферрин;
- тест красной нити фенола;
- клиренс-флюоресцииновый тест.
Также применяется мейбография — бесконтактная визуальная оценка структуры мейбомиевых желёз. Она проводится независимо от возраста и пола пациента [9]. Данный метод диагностики используется редко, так как он достаточно новый и не везде есть нужное оборудование.
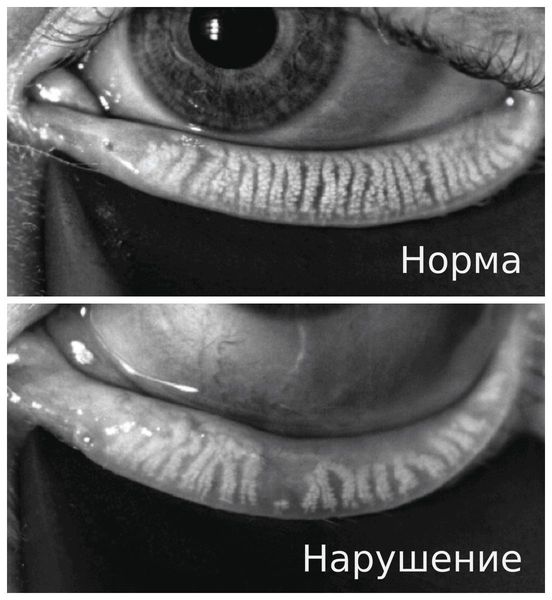
Лечение синдрома сухого глаза
Главная задача при лечении «сухого глаза» — уменьшить неприятные ощущения, сохранить оптическую поверхность роговицы и не допустить повреждения её структур. Одновременно можно применять сразу несколько способов лечения [5].
Сохранение вырабатываемой слезы:
- Уменьшение комнатной температуры — позволяет минимизировать испарения слёзной плёнки.
- В помещении можно использовать увлажнители воздуха, но чаще всего это не даёт результатов. Аппарат не способен значительно увеличить относительную влажность воздуха. Местно повысить влажность можно при помощи специальных очков. У них есть съёмная прокладка, которая защищает глаза от ветра и других раздражающих факторов.

- Частичная боковая тарзорафия — операция, которая заключается в полном или частичном ушивании краёв век. Она уменьшает расстояние между веками глаза, чем может благотворно повлиять на состояние пациента.
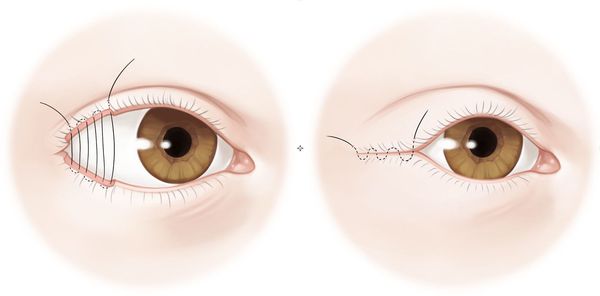
Заместители слезы:
- Капли используются довольно часто. Их главный недостаток — короткий период действия и развитие чувствительности к консерванту.
- Гели состоят из карбомеров — заместителей слезы. Их приходится наносить не так часто, как капли, поэтому использование гелей предпочтительней.
- Также используют мази, которые содержат вазелин и минеральные липиды.
- Спреи для век обычно содержат средство на основе липосома. Они позволяют уменьшить испарение и стабилизировать слёзную плёнку.
Муколитические препараты
Ацетилцистеин 5 % в форме капель можно использовать для лечения пациентов с нитчатым кератитом и инфильтратами. Капли применяют четыре раза в день. Они могут вызвать покраснение после закапывания.
Уменьшение оттока слезы
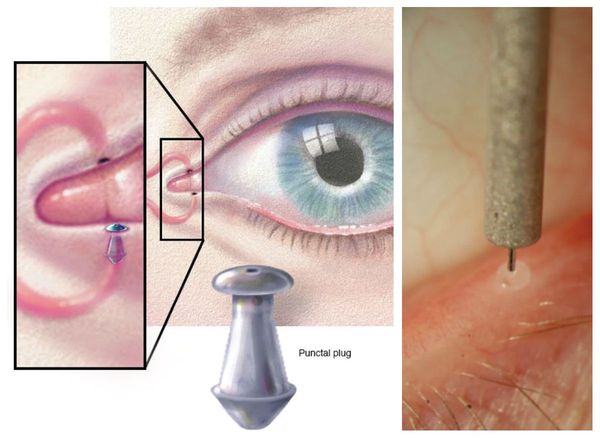
Окклюзия (закупорка) слёзной точки сохраняет отток слезы и продлевает эффект воздействия искусственных слёз. Это процедура показана пациентам с выраженным синдромом, особенно из-за токсичности консервантов.
Временная закупорка слёзной точки происходит при помещении коллагеновой заглушки в слёзные канальцы. Самая важная задача временной окклюзии — убедиться в том, что после неё не возникнет обильное слезотечение. Для временной окклюзии на несколько месяцев используются силиконовые заглушки. Постоянная окклюзия проводится пациентам с выраженным сухим кератоконъюнктивитом.

Другие варианты лечения:
- Местное использование циклоспорина 0,05 % или 0,1 % — безопасный, хорошо переносимый и эффективный препарат. Он позволяет уменьшить воспаление слёзной плёнки на уровне клеток.
- Системный приём холинергических препаратов типа пилокарпина — весьма эффективен в лечении ксеростомии — сухости во рту. У 40 % пациентов с сухим кератоконъюнктивитом наблюдается положительный эффект.
Лечение мейбомиевых желёз
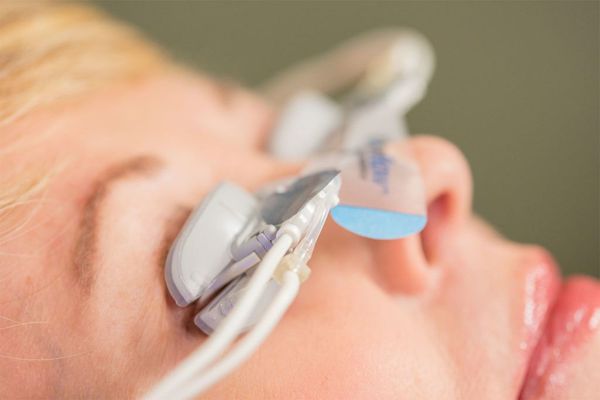
Нарушение работы данных желёз является основной причиной появления синдрома сухого глаза. Существует множество вариантов его лечения. Консервативные меры включают тёплые компрессы и гигиену век — наложение тёплых ватных дисков на пять минут, использование специальных гелей для век. Потенциальные медицинские методы лечения включают в себя антибиотики, нестероидные и стероидные противовоспалительные средства, добавки незаменимых жирных кислот, гормональную терапию и контроль инвазии демодекса — распространения клеща Demodex. Процедуры включают внутрипротоковое исследование мейбомиевых желёз, использование электронных нагревательных приборов, интенсивную импульсную световую терапию и интраназальную нейростимуляцию — электростимуляция нервных окончаний увеличивают производство слезы [7].
Прогноз. Профилактика
Причинные процессы, вызывающие сухость глаза, как правило, необратимы, поэтому лечение строится вокруг контроля симптомов и предотвращения повреждения поверхности.
Пациенту необходимо пересмотреть свой образа жизни:
- не носить контактные линзы дольше, чем рекомендует производитель;
- прекратить использование препаратов с потенциально токсическим воздействием (капли с консервантами);
- следить, чтобы уровень влажности в помещении был достаточным;
- чаще моргать во время чтения, просмотра телевизора или работы за компьютером;
- располагать экран так, чтобы он был ниже уровня глаз.
Интересно, что при ношении гарнитуры виртуальной реальности толщина липидного слоя и стабильность слёзной плёнки становится лучше, чем при использовании обычного настольного компьютера [8].
Выраженная сухость глаза у курильщиков электронных сигарет и вейперов указывают на потенциальный вред паров электронных сигарет и вейпов по отношению к глазам. Они ухудшают качество слёзной плёнки, из-за чего синдром сухого глаза становится умеренным или тяжёлым. Помимо пара на слёзную плёнку воздействуют опасные побочные продукты вейпа [4].
На качество слёз также влияет индекс массы тела. Как показало недавнее исследование, качество слезы у людей с высоким индексом массы тела было ниже, чем у людей с нормальным весом [10]. Поэтому правильно питание может снизить риск развития нарушений обмена веществ в организме, а следовательно и синдрома сухого глаза.
Хирургическое вмешательство является наиболее эффективным средством для повышения остроты зрения при катаракте. И хотя современные способы лечения катаракты безопасны и эффективны, после операции может развиться несколько осложнений, таких как кистозный макулярный отёк, а также сухость глаза. Причины послеоперационного «сухого глаза» пока не установлены. Поэтому если пациент планирует лазерную рефракционную операцию, то врач должен предупредить его, что эта процедура может привести к синдрому сухого глаза или усугубить его [3].
Препаратов, предназначенных для профилактики послеоперационного сухого глаза, пока не разработано. И хотя использование нестероидных противовоспалительных средств эффективно снижает частоту и степень послеоперационного кистозного макулярного отёка, они могут вызывать побочные эффекты, включая аномалии поверхности и сухость глаз. В связи с этим послеоперационные лекарства должны тщательно отбираться, чтобы улучшить результаты лечения и не допустить развитие сухого кератоконъюнктивита [6].
Источник
