Бругада синдром и его типы
Синдром Бругада — наследственное заболевание[1], обусловленное мутацией гена SCN5A, расположенного в плече p 3-й хромосомы, кодирующего биосинтез белковых субъединиц натриевого канала кардиомиоцитов.
Впервые это понятие, позже ставшее эпонимом, предложили испано-бельгийские кардиологи — братья Педро и Хосеп Бругада[2].
Мутации генов[править | править код]
На сегодняшний день известны, по крайней мере, 5 генов, ответственных за развитие этого состояния. В зависимости от мутации гена выделяют следующие варианты:
Патогенез[править | править код]
Заболевание имеет аутосомно-доминантный тип наследования в 25 % семей. Клинические проявления синдрома Бругада развиваются обычно в молодом возрасте (до 35-40 лет), реже — наблюдаются даже в пожилом и старческом возрасте. При исследовании статистических данных, накопленных в странах Юго-Восточной Азии и Дальнего Востока, было отмечено, что в данном регионе значительно распространены случаи внезапной ночной смерти в молодом возрасте (в год от 4 до 10 случаев на 10 000 жителей, в том числе в Лаосе — 1 случай на 10 000 жителей; в Таиланде — 26-38 на 100 000).
[7]
Описаны также случаи приобретенного синдрома Бругада[2].
Синдром Бругада характеризуется наличием преходящей полной или неполной блокады правой ножки пучка Гиса, косонисходящим подъёмом сегмента S-T в правых грудных отведениях (V1-V3), рецидивирующей пароксизмальной полиморфной желудочковой тахикардией и высоким риском внезапной сердечной смерти.
Симптомокомплекс[править | править код]
Полная форма синдрома Бругада включает следующие клинико-электрокардиографические проявления:
- Типичная электрокардиографическая картина (косонисходящее повышение сегмента S-T над изолинией на 1 мм и больше в отведениях V1—V3, на некоторых ЭКГ напоминает морду бультерьера, поэтому данное изменение иногда называют «типом бультерьера»[2], спонтанное или индуцированное введением антиаритмических препаратов I класса (блокаторов натриевых каналов, например, аймалина (гилуритмала) в дозе 1 мг/кг или новокаинамида в дозе 10 мг/кг, флекаинида 2 мг/кг); полная или неполная блокада правой ножки пучка Гиса); возможно укорочение интервала Q-T и удлинение P-Q (P-R);
- Пароксизмы полиморфной желудочковой тахикардии, часто рецидивирующие;
- синкопальные (обморочные) состояния;
- высокий риск внезапной сердечной смерти вследствие полиморфной желудочковой тахикардии или фибрилляции желудочков.
Примечания[править | править код]
- ↑ Окороков А. Н., Диагностика болезней внутренних органов: Т. 10. Диагностика болезней сердца и сосудов.: — М.: Мед. лит., 2005. — 384 с.: ил. ISBN 5-89677-091-X; — ст. 239—241.
- ↑ 1 2 3 Л. А. Бокерия, О. Л. Бокерия, Л. Н. Киртбая. СИНДРОМ БРУГАДА: КЛЕТОЧНЫЕ МЕХАНИЗМЫ И ПОДХОДЫ К ЛЕЧЕНИЮ. Анналы аритмологии, № 3, 2010.
- ↑ 1 2 Antzelevitch C; Pollevick GD; Cordeiro JM; Casis, O.; Sanguinetti, M. C.; Aizawa, Y.; Guerchicoff, A.; Pfeiffer, R.; Oliva, A. Loss-of-Function Mutations in the Cardiac Calcium Channel Underlie a New Clinical Entity Characterized by ST-Segment Elevation, Short QT Intervals, and Sudden Cardiac Death (англ.) // Circulation (англ.)русск. : journal. — Lippincott Williams & Wilkins (англ.)русск., 2007. — Vol. 115, no. 4. — P. 442—229. — doi:10.1161/CIRCULATIONAHA.106.668392. — PMID 17224476.
- ↑ Delpon E; Cordeiro JM; Núñez L; Thomsen, P. E. B.; Guerchicoff, A.; Pollevick, G. D.; Wu, Y.; Kanters, J. K.; Larsen, C. T. Functional Effects of KCNE3 Mutation and its Role in the Development of Brugada Syndrome (англ.) // Circulation Arrhythmia and Electrophysiology : journal. — 2008. — Vol. 1, no. 3. — P. 209—218. — doi:10.1161/CIRCEP.107.748103. — PMID 19122847.
- ↑ Watanabe H; Koopmann TT; Le Scouarnec S; Yang, Tao; Ingram, Christiana R.; Schott, Jean-Jacques; Demolombe, Sophie; Probst, Vincent; Anselme, Frédéric. Sodium channel β1 subunit mutations associated with Brugada syndrome and cardiac conduction disease in humans (англ.) // Journal of Clinical Investigation (англ.)русск. : journal. — 2008. — June (vol. 118, no. 6). — P. 2260—2268. — doi:10.1172/JCI33891. — PMID 18464934.
- ↑ 1 2 Bezzina, Connie R; Barc, Julien; Mizusawa, Yuka; Remme, Carol Ann; Gourraud, Jean-Baptiste; Simonet, Floriane; Verkerk, Arie O; Schwartz, Peter J; Crotti, Lia; Dagradi, Federica; Guicheney, Pascale; Fressart, Véronique; Leenhardt, Antoine; Antzelevitch, Charles; Bartkowiak, Susan; Schulze-Bahr, Eric; Zumhagen, Sven; Behr, Elijah R; Bastiaenen, Rachel; Tfelt-Hansen, Jacob; Olesen, Morten Salling; Kääb, Stefan; Beckmann, Britt M; Weeke, Peter; Watanabe, Hiroshi; Endo, Naoto; Minamino, Tohru; Horie, Minoru; Ohno, Seiko; Hasegawa, Kanae; Makita, Naomasa; Nogami, Akihiko; Shimizu, Wataru; Aiba, Takeshi; Froguel, Philippe; Balkau, Beverley; Lantieri, Olivier; Torchio, Margherita; Wiese, Cornelia; Weber, David; Wolswinkel, Rianne; Coronel, Ruben; Boukens, Bas J; Bézieau, Stéphane; Charpentier, Eric; Chatel, Stéphanie; Despres, Aurore; Gros, Françoise; Kyndt, Florence; Lecointe, Simon; Lindenbaum, Pierre; Portero, Vincent; Violleau, Jade; Gessler, Manfred; Tan, Hanno L; Roden, Dan M; Christoffels, Vincent M; Marec, Hervé Le; Wilde, Arthur A; Probst, Vincent; Schott, Jean-Jacques; Dina, Christian; Redon, Richard. Common variants at SCN5A-SCN10A and HEY2 are associated with Brugada syndrome, a rare disease with high risk of sudden cardiac death (англ.) // Nature Genetics : journal. — 2013. — ISSN 1061-4036. — doi:10.1038/ng.2712.
- ↑ Л. М. Макаров. Синдром Бругада. журнал «Лечащий врач».
Источник

Синдром Бругада – генетически обусловленное кардиологическое состояние, характеризующееся различными нарушениями работы сердца, которые приводят к резкому повышению риска развития внезапной сердечной смерти. Симптомами этого состояния являются приступы пароксизмальной тахикардии, обмороки, фибрилляции предсердий и жизнеугрожающие фибрилляции желудочков, чаще всего возникающие во время сна. Диагностика синдрома Бругада производится на основании характерного симптомокомплекса, электрокардиографических данных и изучения наследственного анамнеза, некоторые формы патологии определяются молекулярно-генетическими методами. Специфического лечения заболевания не существует, применяют антиаритмическую терапию, используют разнообразные кардиостимуляторы.
Общие сведения
Синдром Бругада – группа генетических нарушений, приводящих к изменению ионной проницаемости мембран кардиомиоцитов, вследствие чего возникают патологии ритма и проводимости, создающие повышенный риск внезапной сердечной смерти. Впервые такое состояние было описано в 1992 году двумя братьями – бельгийскими кардиологами испанского происхождения Хосе и Педро Бругада, обратившими внимание на взаимосвязь определенных электрокардиологических проявлений и нарушений сердечного ритма. В настоящее время установлено, что синдром Бругада является наследственным состоянием с предположительно аутосомно-доминантным механизмом передачи, удалось выявить несколько генов, мутации которых способны вызывать это заболевание. По некоторым данным, практически половина всех случаев внезапной сердечной смерти в мире обусловлены именно этой патологией. Распространенность синдрома Бругада различается в разных регионах планеты – в странах Америки и Европы она составляет примерно 1:10 000, тогда как в африканских и азиатских государствах это заболевание встречается чаще – 5-8 случаев на 10 000 населения. Синдром Бругада примерно в 8 раз чаще поражает мужчин, чем женщин, проявления патологии возникают в разном возрасте, но чаще всего выраженная симптоматика наблюдается в 30-45 лет.
Синдром Бругада
Причины и классификация синдрома Бругада
Причина развития нарушений при синдроме Бругада заключается в патологической работе ионных каналов кардиомиоцитов, в основном натриевых и кальциевых. Их дефект, в свою очередь, обусловлен мутациями генов, кодирующих белки ионных каналов. Методами современной генетики удалось достоверно идентифицировать 6 основных генов, поражение которых приводит к развитию синдрома Бругада, в отношении еще нескольких существует подозрение, но отсутствует необходимая доказательная база. На этой основе построена классификация данного состояния, включающая в себя 6 форм заболевания (BrS):
- BrS-1 – наиболее распространенный и хорошо изученный вариант синдрома Бругада. Обусловлен мутацией гена SCN5A, расположенного на 3 хромосоме. Продуктом экспрессии данного гена является альфа-субъединица натриевого канала 5 типа, широко представленного в миокарде. Помимо синдрома Бругада мутации данного гена становятся причиной большого количества наследственных кардиологических патологий – семейной фибрилляции предсердий, синдрома слабости синусового узла 1 типа и ряда других.
- BrS-2 – данная разновидность синдрома Бругада вызывается дефектами гена GPD1L, который локализован на 3 хромосоме. Он кодирует один из компонентов глицерол-3-фосфат дегидрогеназы, принимающей активное участие в работе натриевых каналов кардиомиоцитов.
- BrS-3 – этот тип синдрома Бругада обусловлен дефектом гена CACNA1C, расположенного на 12 хромосоме. Продуктом его экспрессии является альфа-субъединица кальциевого канала L-типа, также присутствующего в кардиомиоцитах.
- BrS-4 – как и в предыдущем случае, причиной развития синдрома Бругада 4 типа является поражение потенциал-зависимых кальциевых каналов L-типа. Оно обусловлено мутацией гена CACNB2, расположенного на 10 хромосоме и кодирующего бета-2-субъединицу вышеуказанных ионных каналов.
- BrS-5 – распространенная разновидность синдрома Бругада, обусловленная мутацией гена SCN4B, локализованного на 11 хромосоме. Он кодирует белок одного из малых натриевых каналов кардиомиоцитов.
- BrS-6 – вызывается дефектом гена SCN1B, расположенного на 19 хромосоме. Во многом этот вариант синдрома Бругада схож с первым типом заболевания, поскольку в этом случае тоже поражаются натриевые каналы 5 типа. Ген SCN1B кодирует бета-1-субъединицу этого ионного канала.
Кроме того, в развитии синдрома Бругада подозреваются мутации генов KCNE3, SCN10A, HEY2 и некоторых других. Однако на сегодняшний день достоверно доказать их роль в возникновении данного заболевания не удается, поэтому пока количество генетических вариантов синдрома Бругада ограничено шестью. Наследование всех форм данной патологии неясно, лишь у 25% больных определяются признаки аутосомно-доминантной передачи. Предположительно имеет место доминантный тип наследования с неполной пенетрантностью либо влияние спонтанных мутаций. Также непонятны причины того, почему синдром Бругада чаше поражает мужчин, нежели женщин – возможно, выраженность проявлений заболевания находится в зависимости от гормонального фона больного.
Патогенез нарушений при любой форме синдрома Бругада примерно одинаков – из-за изменения проницаемости мембраны кардиомиоцитов для ионов натрия происходит нарушение трансмембранного потенциала и взаимосвязанных с ним характеристик возбудимых тканей: возбудимости, сократимости, передачи возбуждения окружающим клеткам. В результате возникают блокады проводящих путей сердца (пучков Гиса), тахиаритмии, усиливающиеся при повышении вагусных воздействий (во время сна). Степень выраженности симптомов при синдроме Бругада зависит от доли пораженных натриевых каналов. Усиливать проявления болезни могут некоторые лекарственные вещества, способны ингибировать ионные каналы сердца.
Симптомы синдрома Бругада
Возраст появления первых признаков синдрома Бругада сильно отличается у разных больных – были зарегистрированы случаи этой патологии как у детей 3-4 лет, так и у лиц старческого возраста. Одним из первых проявлений патологии становятся изменения на электрокардиограмме при полном отсутствии других клинических симптомов, поэтому данное заболевание нередко выявляется случайно. В большинстве случаев выраженная клиника синдрома Бругада возникает в возрасте 30-45 лет, этому предшествует бессимптомный период продолжительностью 10-12 лет, в течение которого единственным признаком патологии являются изменения на ЭКГ.
Обычно больные синдромом Бругада жалуются на беспричинное головокружение, обмороки, частые приступы тахикардии, особенно в ночное время или в период дневного отдыха. Иногда отмечается аномальная реакция на прием некоторых лекарственных средств – антигистаминных препаратов первого поколения, бета-адреноблокаторов, ваготонических средств. Их применение при синдроме Бругада может сопровождаться усилением побочных явлений, а также сердцебиениями, обмороками, падением артериального давления и другими негативными проявлениями. Никаких других симптомов при этом заболевании не выявляется, чем объясняется редкое обращение пациентов к кардиологу или другим специалистам – в ряде случаев проявления синдрома Бругада достаточно редкие и слабовыраженные. Тем не менее, это не снижает риск внезапной сердечной смерти, обусловленной данной патологией.
Диагностика синдрома Бругада
Для определения синдрома Бругада используют электрокардиографические методики, изучение наследственного анамнеза пациента, молекулярно-генетический анализ. Заподозрить наличие этого заболевания можно при наличии синкопальных явлений (головокружений, обмороков) неясного происхождения, жалоб на внезапные приступы тахиаритмий. Изменения на электрокардиограмме при синдроме Бругада могут определяться на фоне полного отсутствия клинических симптомов заболевания. При этом кардиологи выделяют три основных типа изменений на ЭКГ, незначительно отличающихся между собой. Типичная картина электрокардиограммы при синдроме Бругада сводится к элевации (подъему) сегмента ST над изоэлектрической линией и отрицательному зубцу Т на правых грудных отведениях (V1-V3). Также могут определяться признаки блокады правой ножки пучка Гиса, при холтеровском мониторировании выявляются приступы пароксизмальной тахикардии или фибрилляции предсердий.
Как правило, наследственный анамнез больных синдромом Бругада отягощен – среди родственников или предков имеются случаи летальных исходов от сердечной недостаточности, смерти во сне или внезапной сердечной смерти. Этот факт, а также наличие вышеперечисленных симптомов и изменений на ЭКГ дает основания для проведения молекулярно-генетической диагностики. В настоящее время врачи-генетики в подавляющем большинстве клиник и лабораторий производят определение синдрома Бругада, вызванного только мутациями генов SCN5A и SCN4B (1 и 5 типы патологии), в отношении остальных форм методы генетической диагностики пока не разработаны. Дифференцировать это состояние следует с реакцией организма на прием некоторых лекарственных средств, хроническим миокардитом и другими кардиологическими патологиями.
Лечение и профилактика синдрома Бругада
Специфических методов лечения синдрома Бругада на сегодняшний момент не существует, поэтому ограничиваются только борьбой с проявлениями этого заболевания, а также профилактикой жизнеугрожающих приступов тахиаритмии и фибрилляций. Наиболее широко при этом состоянии применяется амиодарон, несколько реже используются дизопирамид и хинидин. Однако медикаментозная терапия при синдроме Бругада в ряде случаев является малоэффективной, единственным надежным средством профилактики аритмии и внезапной сердечной смерти в этом случае становится имплантация кардиовертера-дефибриллятора. Только этот прибор способен оценивать работу миокарда больного и при патологических и жизнеугрожающих изменениях сердечного ритма приводить ее в норму посредством электрического разряда.
Многие традиционные антиаритмические препараты при синдроме Бругада противопоказаны, так как они угнетают деятельность натриевых каналов кардиомиоцитов и усиливают проявления патологии. К средствам, запрещенным при этом заболевании, относят аймалин, пропафенон, прокаинамид. Поэтому больным синдромом Бругада следует обязательно сообщать специалистам об имеющемся диагнозе, чтобы избежать назначения неверного антиаритмического средства. При наличии подобного заболевания у родственников или случаях внезапной сердечной смерти в роду следует регулярно производить ЭКГ-исследование для как можно более ранней диагностики этого состояния.
Прогноз синдрома Бругада
Прогноз синдрома Бругада неопределенный, так как степень выраженности симптомов заболевания очень вариабельна и находится в зависимости от ряда факторов. При наличии только электрокардиографических проявлений патологии без выраженных клинических симптомов прогноз относительно благоприятный. Если синдром Бругада сопровождается потерями сознания и приступами аритмии – без установки кардиовертера-дефибриллятора риск внезапной сердечной смерти возрастает во много раз. При применении данного прибора прогноз несколько улучшается, поскольку устройство может круглосуточно корректировать патологические изменения сердечного ритма.
Источник
- 1 Синдром Бругада
- 1.1 Введение
- 1.1.1 Эпидемиология
- 1.1.2 Этиология
- 1.2 Классификация
- 1.3 Диагностика
- 1.4 Дифференциальная диагностика
Синдром Бругада
Введение
Синдром, характеризующийся ЭКГ признаками блокады правой ножки пучка Гиса с элевацией точки J и сегмента ST в правых прекордиальных отведениях и проявляющийся клинически рецидивирующими синкопальными состояниями, а также случаями внезапной сердечной смерти, которая наступает чаще у лиц мужского пола в возрасте 30–40 лет, описан P. Brugada и J. Brugada в 1992 г. Заболевание наследуется по аутосомно-доминантному типу, при этом характерна неполная пенетрантность генетических изменений.
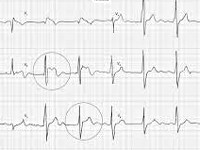
Желудочковые тахикардии, (преимущественно полиморфная, крайне редко — мономорфная) характеризующиеся высоким риском трансформации в фибрилляцию желудочков, являются основным клиническим проявлением синдрома Бругада. Характерно их возникновение в покое, во время ночного сна (рис. 1), что делает более вероятным их выявление с помощью ХМ ЭКГ, а не при стандартной записи ЭКГ. Одним из клинических проявлений, сопровождающих эти аритмические события, могут быть эпизоды хриплого (агонального) дыхания во сне. Желудочковые тахикардии могут провоцироваться лихорадочными состояниями, а также рядом лекарственных препаратов (см. табл. 1). Симптомы заболевания проявляются обычно у взрослых, а средний возраст возникновения случаев внезапной сердечной смерти составляет 41±15 лет. Кроме того, при синдроме Бругада чаще чем в общей популяции регистрируют случаи суправентрикулярных тахиаритмий.
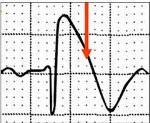
Рис. 1. Неустойчивый пароксизм (выделен рамкой) полиморфной желудочковой тахикардии (частота сердечных сокращений 160–180 уд./мин.). Холтеровская мониторная запись ЭКГ в 12 отведениях у больной синдромом Бругада. Время возникновения пароксизма — 23 часа. Стрелками в отведении V1 указана элевация точки J в сокращениях синусового ритма.
Эпидемиология
Распространённость заболевания в общей популяции в настоящее время неизвестна. Существенно чаще оно встречается в странах Юго-Восточной Азии (Азиатско-Тихоокеанский регион), где его распространённость достигает 0,5–1:1000. Синдром Бругада (Brugada Syndrome, BrS) выявляется у лиц, не имеющих признаков органического заболевания сердца, у мужчин встречается в 8–10 раз чаще, чем у женщин, что, предположительно, обусловлено большей силой кратковременного выходящего тока ионов калия Ito (одного из токов, участвующих в формировании синдрома) и действием более высоких концентраций тестостерона.
Этиология
Синдром Бругада вызывают генетические мутации, приводящие к уменьшению силы входящих натриевого (INa) и кальциевого (ICa,L) токов или увеличению силы выходящих калиевых токов (Ito,f, IKs, IK,ATP).
Классификация
В настоящее время известны 12 генетических вариантов синдрома, они представлены в табл. 1. Молекулярно-генетические методы позволяют обнаружить мутации приблизительно у 1/3 больных с явными клинико-инструментальными проявлениями синдрома Бругада, что указывает на генетическую гетерогенность заболевания и позволяет предполагать открытие большого числа новых, не известных в настоящее время мутаций, в будущем. Наиболее распространены мутации гена SCN5A, которые обнаруживают почти у 30% пациентов.
Таблица 1. Молекулярно-генетические типы синдрома Бругада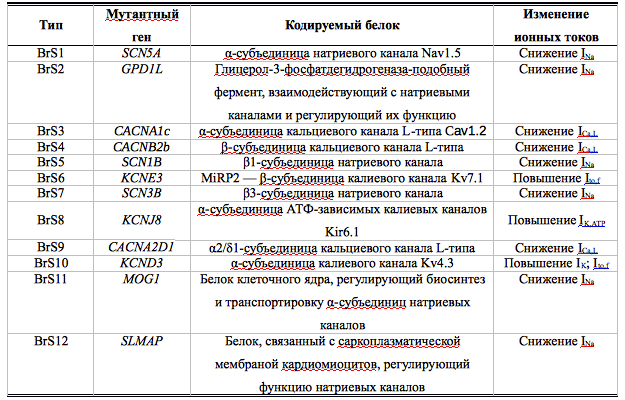
Диагностика
Основой диагностики синдрома Бругада является регистрация патогномоничных данному заболеванию изменений сегмента ST на ЭКГ при отсутствии структурного заболевания сердца и других состояний, при которых могут быть зарегистрированы подобные изменения ЭКГ (указаны далее). На основании характера изменений конечной части желудочкового комплекса выделяют три ЭКГ-типа феномена Бругада (табл. 2, рис 2).
Таблица 2. ЭКГ-типы феномена Бругада

Рис. 2. ЭКГ–типы Синдрома Бругада. Стрелками указана точка J. Элевация более 2 мм.
Регистрацию ЭКГ следует также проводить, располагая электроды правых прекордиальных отведений (V1–V2) выше стандартной позиции, вплоть до II межреберья. Выявление патогномоничных изменений ЭКГ в этих позициях имеет такую же диагностическую значимость, как и при стандартном расположении электродов. Изменения конечной части желудочкового комплекса, характерные для синдрома Бругада, могут иметь преходящий характер. Поэтому в тех случаях, когда имеющиеся записи ЭКГ не несут в себе признаков, в полной мере укладывающихся в диагностические критерии, но есть основание предполагать наличие синдрома Бругада, целесообразно проведение диагностических провокационных лекарственных проб с использованием блокаторов натриевых каналов, вводимых внутривенно, — аймалина (в дозе 1 мг/кг; в России не зарегистрирован) или прокаинамида (в дозе 10 мг/кг), позволяющих в части случаев «обнажить» признаки этого синдрома. Фармакологические провокационные пробы должны проводиться опытным медицинским персоналом при мониторировании ЭКГ больного и обязательной возможности организации реанимационных мероприятий в случае индукции опасных для жизни желудочковых аритмий под влиянием вводимых препаратов.
В соответствии с изменёнными диагностическими критериями, для постановки диагноза синдрома Бругада необходима регистрация на ЭКГ спонтанной или индуцированной лекарственными препаратами элевации сегмента ST по типу «свода» (тип 1) хотя бы в одном из правых прекордиальных отведений (V1–V2) при расположении электродов в типичном месте или установке их во II межреберье.
Методы молекулярно-генетической диагностики также имеют значение для диагностики заболевания, однако генетические мутации у больных синдромом Бругада удаётся обнаружить лишь приблизительно в 30% случаев, поэтому отрицательный результат генетического анализа не позволяет полностью исключить диагноз синдрома Бругада. В случае обнаружения у больного синдромом Бругада генетической мутации проведение скрининга, направленного на выявление этой мутации, рекомендовано всем близким родственникам, даже при отсутствии у них характерных этому заболеванию изменений ЭКГ. Проведение молекулярно-генетических исследований лицам, имеющим ЭКГ-изменения 2 и 3 типов, при отсутствии у них клинических проявлений синдрома Бругада и отягощённого по ВСС семейного анамнеза в настоящее время не рекомендовано.
Дифференциальная диагностика
Синдром Бругада следует дифференцировать от других возможных причин синкопальных состояний, учитывая относительно молодой возраст больных, прежде всего, от эпилепсии и вазо-вагальных обмороков, а также от других врождённых желудочковых нарушений ритма сердца.
Необходимо также отметить, что схожие с синдромом Бругада изменения ЭКГ могут быть выявлены при целом ряде патологических состояний. Причинами «бругадоподобных» изменений ЭКГ могут быть:
- атипичная блокада правой ножки пучка Гиса;
- гипертрофия левого желудочка;
- феномен ранней реполяризации желудочков;
- острый коронарный синдром;
- аневризма левого желудочка;
- стенокардия Принцметала;
- острый перикардит;
- гемоперикард;
- тромбоэмболия лёгочной артерии;
- расслаивающая аневризма аорты;
- электролитные нарушения (гиперкалиемия, гиперкальциемия);
- гипотермия/гипертермия;
- аритмогенная дисплазия-кардиомиопатия правого желудочка;
- механическая компрессия выносящего тракта правого желудочка (например, опухоль органов средостения);
- передозировка трициклических антидепрессантов;
- кокаиновая интоксикация;
- различные заболевания центральной и вегетативной нервной системы (субарахноидальное кровоизлияние; геморрагический инсульт; атаксия Фридриха);
- мышечная дистрофия Дюшена–Беккера.
Источник
