Болезнь фара код мкб
Содержание
- Описание
- Дополнительные факты
- Причины
- Патогенез
- Классификация
- Симптомы
- Диагностика
- Дифференциальная диагностика
- Лечение
- Прогноз
- Профилактика
Названия
Название: Болезнь Фара.

Болезнь Фара
Описание
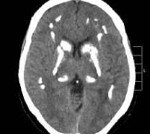
Болезнь Фара. Идиопатическая симметричная кальцификация церебральных структур — подкорковых ганглиев, коры полушарий, мозжечка. Может протекать бессимптомно, клинически проявляется экстрапирамидными расстройствами (гиперкинезами, паркинсонизмом), мозжечковыми нарушениями, интеллектуальным снижением. Диагностируется по данным церебральной КТ при исключении вторичного характера кальцинированных очагов по результатам биохимических, ультразвуковых, ПЦР исследований. Лечение симптоматическое с применением средств, улучшающих тканевый обмен, цитопротекторов, препаратов леводопы, антиконвульсантов.
Дополнительные факты
Болезнь Фара включает случаи первичного идиопатического отложения кальция в мозговых структурах, вторичные формы церебрального кальциноза в рамках данной патологии не рассматриваются. Первые подробные описания заболевания сделаны в 1930 году немецким невропатологом К. Т. Фаром. Болезнь Фара является редкой нозологией, распространённость составляет менее 1 случая на 1 млн. Населения. Гендерные различия в заболеваемости выражаются соотношением мужчин и женщин 2:1. Патология проявляется в любом возрастном периоде, чаще в 30-60 лет. Прижизненно выявляется лишь в 1-2% случаев, что объясняется наличием бессимптомных вариантов течения, диагностикой заболевания под видом иных нейродегенеративных процессов (болезни Паркинсона, сенильной хореи).
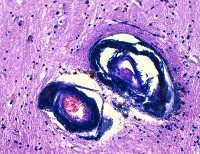
Болезнь Фара
Причины
Приводящие к возникновению заболевания этиологические факторы точно не установлены. Предполагают генетический характер патологии с локализацией нарушений в четырнадцатой (локус 14q13), второй (локус 2q37) хромосомах, хромосомном участке q21. 1-q11. 23 восьмой хромосомы. При исследовании семейных случаев выявлена генетическая гетерогенность. Установлены варианты, когда болезнь наследовалась аутосомно-доминантным и Х-сцепленным путём. Описаны спорадические случаи, при которых семейный характер патологии не прослеживается. Известно, что клиническая манифестация происходит, когда общий объём кальцификатов достигает критической величины — 3,9 см³.
Патогенез
Формирующие болезнь патогенетические механизмы окончательно не определены. Предполагаются генетически детерминированные сдвиги церебрального метаболизма, становящиеся причиной отложения в мозговых тканях избытков кальция. Выраженная кальцификация подкорковых образований становится причиной дезорганизации лобно-субкортикальной системы, регулирующей произвольные движения и обеспечивающей когнитивные функции (память, мышление, внимание).
Морфологически кальцификаты обнаруживаются симметрично в различных структурах: коре мозга, белом веществе, подкорковых ганглиях, внутренней капсуле, мозжечке, стенках мелких артерий, реже вен. Характерно наличие периваскулярных мелких кальциевых конгломератов. Наиболее массивная кальцификация выявляется в подкорковых отделах. Микроскопически кальцификаты отличаются типичной структурой, представленной нитями толщиной 140-400 мкм. Они зачастую содержат минеральные комплексы с включениями железа, меди, алюминия, фосфора, свинца, цинка, кобальта.
Классификация
В практической неврологии болезнь Фара подразделяется на две клинические формы, отличающиеся возрастом манифестации, типом преобладающей симптоматики:
• Ювенильная форма. Дебют заболевания происходит в детском или подростковом периоде. Характерны экстрапирамидные нарушения в виде атетоза, хореи, мышечной дистонии. Патология может сопровождаться олигофренией. По мере взросления отмечается смена гиперкинезов паркинсонической симптоматикой.
• Сенильная форма. Манифестирует в пожилом и среднем возрасте. Клиническая картина характеризуется доминированием симптомов паркинсонизма в сочетании с когнитивными расстройствами. Типична прогрессирующая деменция.
Симптомы
В типичных случаях болезнь дебютирует появлением утомляемости, неуклюжести движений, шаткости ходьбы, изменений речи, непроизвольных двигательных актов или ночных мышечных спазмов. Основу клинических проявлений составляют экстрапирамидные нарушения. В молодом возрасте это различные гиперкинезы: атетоз — непроизвольные червеобразные движения в пальцах кистей, хореоатетоз — сочетание атетоза с быстрыми насильственными движениями в конечностях, торсионная дистония — тонические мышечные спазмы, придающие телу неестественные позы. У взрослых наблюдается вторичный паркинсонизм: амимия лица, брадикинезия, замедленные скованные движения, шаркающая походка, постуральный тремор.
Симптоматика паркинсонизма зачастую сочетается с мозжечковой атаксией (дискоординация, несоразмерность движений, нистагм), пирамидной недостаточностью (слабость в конечностях, повышенные сухожильные рефлексы, патологические стопные знаки). Возможна дизартрия, дисфагия, недержание мочи. Эпилептические пароксизмы более характерны для ювенильной формы заболевания, могут отмечаться у взрослых.
Тремор.
Диагностика
Основным диагностическим методом, позволяющим неврологу достоверно установить наличие очагов кальциноза в мозговых тканях, является КТ головного мозга. Интенсивность очагов на томограммах отражает уровень концентрации кальция. МРТ головного мозга значительно хуже визуализирует кальцификаты, но позволяет оценить сопутствующие дегенеративные процессы. С целью подтверждения идиопатического характера патологии проводится целый ряд дополнительных обследований:
• Биохимический анализ крови. Производится определение электролитов крови: кальция, фосфора, железа, натрия. Отсутствие существенных отклонений позволяет исключить общие обменные нарушения в организме, приводящие к отложению кальция.
• Определение уровня паратгормона Нормальные показатели концентрации гормона в крови исключают наличие гипопаратиреоза, псевдогипопаратиреоза, как наиболее распространённых причин кальцификации.
• УЗИ щитовидной и паращитовидных желёз. У пациентов с болезнью Фара эхоскопическая картина остается в пределах нормы, что исключает связанные с поражением этих желёз гормонально-обменные нарушения.
• ТКДГ церебральных сосудов. Необходима для оценки мозговой гемодинамики, выявления хронической церебральной ишемии как первопричины дегенеративных изменений, сопровождающихся кальцификацией.
• ПЦР. Исследования. Направлены на выявление токсоплазмы, цитомегаловируса и других инфекционных агентов, способных вызывать воспалительные изменения мозговых тканей с образованием кальцификатов.
Диагноз болезнь Фара правомочен после исключения вторичного характера церебральной кальцификации, наблюдающейся при эндокринных (гипопаратиреоз, псевдогипопаратиреоз, гипотиреоз), сосудистых (атеросклероз, амилоидоз сосудов), инфекционных (краснуха, цистицеркоз, токсоплазмоз, цитомегалия) заболеваниях.
Дифференциальная диагностика
Дифференциальная диагностика проводится также с болезнью Галлервордена-Шпатца, туберозным склерозом.
Лечение
Поскольку патогенез заболевания остаётся неясным, терапия имеет преимущественно симптоматический характер. С целью улучшения обменных процессов применяются стимуляторы тканевого метаболизма (ацетилкарнитин, глютаминовая кислота, комплекс L-цитруллин+малат, никотинамид), цитопротекторы (рибофлавин, янтарная кислота, мельдоний). При симптомах паркинсонизма предпочтительно назначение фармпрепаратов леводопы, при гиперкинезах — холинолитиков, бензодиазепинов. Наличие эпилептических приступов служит показанием к лечению современными антиконвульсантами (леветирацетамом). В комплексной терапии применяется лечебная физкультура, водолечение, когнитивные тренинги.
Прогноз
Клинически проявленная болезнь Фара рассматривается как хроническое нейродегенеративное заболевание. Прогноз выздоровления неблагоприятный, однако, при должном уровне поддерживающей симптоматической терапии состояние пациентов длительное время остаётся удовлетворительным. Субклинический вариант не сказывается на здоровье и когнитивных способностях больного, может быть случайной находкой при проведении компьютерной томографии.
Профилактика
Специфические меры, позволяющие предупредить развитие болезни, не разработаны.
Источник
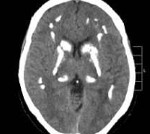
Болезнь Фара — идиопатическая симметричная кальцификация церебральных структур: подкорковых ганглиев, коры полушарий, мозжечка. Может протекать бессимптомно, клинически проявляется экстрапирамидными расстройствами (гиперкинезами, паркинсонизмом), мозжечковыми нарушениями, интеллектуальным снижением. Диагностируется по данным церебральной КТ при исключении вторичного характера кальцинированных очагов по результатам биохимических, ультразвуковых, ПЦР исследований. Лечение симптоматическое с применением средств, улучшающих тканевый обмен, цитопротекторов, препаратов леводопы, антиконвульсантов.
Общие сведения
Болезнь Фара включает случаи первичного идиопатического отложения кальция в мозговых структурах, вторичные формы церебрального кальциноза в рамках данной патологии не рассматриваются. Первые подробные описания заболевания сделаны в 1930 году немецким невропатологом К.Т. Фаром. Болезнь Фара является редкой нозологией, распространённость составляет менее 1 случая на 1 млн. населения. Гендерные различия в заболеваемости выражаются соотношением мужчин и женщин 2:1. Патология проявляется в любом возрастном периоде, чаще в 30-60 лет. Прижизненно выявляется лишь в 1-2% случаев, что объясняется наличием бессимптомных вариантов течения, диагностикой заболевания под видом иных нейродегенеративных процессов (болезни Паркинсона, сенильной хореи).
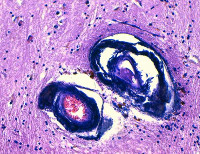
Болезнь Фара
Причины болезни Фара
Приводящие к возникновению заболевания этиологические факторы точно не установлены. Предполагают генетический характер патологии с локализацией нарушений в четырнадцатой (локус 14q13), второй (локус 2q37) хромосомах, хромосомном участке q21.1-q11.23 восьмой хромосомы. При исследовании семейных случаев выявлена генетическая гетерогенность. Установлены варианты, когда болезнь наследовалась аутосомно-доминантным и Х-сцепленным путём. Описаны спорадические случаи, при которых семейный характер патологии не прослеживается. Известно, что клиническая манифестация происходит, когда общий объём кальцификатов достигает критической величины — 3,9 см³.
Патогенез
Формирующие болезнь патогенетические механизмы окончательно не определены. Предполагаются генетически детерминированные сдвиги церебрального метаболизма, становящиеся причиной отложения в мозговых тканях избытков кальция. Выраженная кальцификация подкорковых образований становится причиной дезорганизации лобно-субкортикальной системы, регулирующей произвольные движения и обеспечивающей когнитивные функции (память, мышление, внимание).
Морфологически кальцификаты обнаруживаются симметрично в различных структурах: коре мозга, белом веществе, подкорковых ганглиях, внутренней капсуле, мозжечке, стенках мелких артерий, реже вен. Характерно наличие периваскулярных мелких кальциевых конгломератов. Наиболее массивная кальцификация выявляется в подкорковых отделах. Микроскопически кальцификаты отличаются типичной структурой, представленной нитями толщиной 140-400 мкм. Они зачастую содержат минеральные комплексы с включениями железа, меди, алюминия, фосфора, свинца, цинка, кобальта.
Классификация
В практической неврологии болезнь Фара подразделяется на две клинические формы, отличающиеся возрастом манифестации, типом преобладающей симптоматики:
- Ювенильная форма — дебют заболевания происходит в детском или подростковом периоде. Характерны экстрапирамидные нарушения в виде атетоза, хореи, мышечной дистонии. Патология может сопровождаться олигофренией. По мере взросления отмечается смена гиперкинезов паркинсонической симптоматикой.
- Сенильная форма — манифестирует в пожилом и среднем возрасте. Клиническая картина характеризуется доминированием симптомов паркинсонизма в сочетании с когнитивными расстройствами. Типична прогрессирующая деменция.
Симптомы болезни Фара
В типичных случаях болезнь дебютирует появлением утомляемости, неуклюжести движений, шаткости ходьбы, изменений речи, непроизвольных двигательных актов или ночных мышечных спазмов. Основу клинических проявлений составляют экстрапирамидные нарушения. В молодом возрасте это различные гиперкинезы: атетоз — непроизвольные червеобразные движения в пальцах кистей, хореоатетоз — сочетание атетоза с быстрыми насильственными движениями в конечностях, торсионная дистония — тонические мышечные спазмы, придающие телу неестественные позы. У взрослых наблюдается вторичный паркинсонизм: амимия лица, брадикинезия, замедленные скованные движения, шаркающая походка, постуральный тремор.
Симптоматика паркинсонизма зачастую сочетается с мозжечковой атаксией (дискоординация, несоразмерность движений, нистагм), пирамидной недостаточностью (слабость в конечностях, повышенные сухожильные рефлексы, патологические стопные знаки). Возможна дизартрия, дисфагия, недержание мочи. Эпилептические пароксизмы более характерны для ювенильной формы заболевания, могут отмечаться у взрослых.
Сопровождающие болезнь Фара когнитивные нарушения характеризуются снижением памяти на текущие и прошлые события, замедленным мышлением, неустойчивым вниманием, угасанием способности к аналитической и синтетической интеллектуальной деятельности. Прогрессирование расстройств когнитивной сферы у детей приводит к олигофрении, во взрослом возрасте — к развитию корково-подкорковой деменции с элементами агнозии, апраксии, алексии. Однако часть больных ювенильной формой остаются интеллектуально сохранными.
Диагностика
Основным диагностическим методом, позволяющим неврологу достоверно установить наличие очагов кальциноза в мозговых тканях, является КТ головного мозга. Интенсивность очагов на томограммах отражает уровень концентрации кальция. МРТ головного мозга значительно хуже визуализирует кальцификаты, но позволяет оценить сопутствующие дегенеративные процессы. С целью подтверждения идиопатического характера патологии проводится целый ряд дополнительных обследований:
- Биохимический анализ крови. Производится определение электролитов крови: кальция, фосфора, железа, натрия. Отсутствие существенных отклонений позволяет исключить общие обменные нарушения в организме, приводящие к отложению кальция.
- Определение уровня паратгормона . Нормальные показатели концентрации гормона в крови исключают наличие гипопаратиреоза, псевдогипопаратиреоза, как наиболее распространённых причин кальцификации.
- УЗИ щитовидной и паращитовидных желёз. У пациентов с болезнью Фара эхоскопическая картина остается в пределах нормы, что исключает связанные с поражением этих желёз гормонально-обменные нарушения.
- ТКДГ церебральных сосудов. Необходима для оценки мозговой гемодинамики, выявления хронической церебральной ишемии как первопричины дегенеративных изменений, сопровождающихся кальцификацией.
- ПЦР-исследования. Направлены на выявление токсоплазмы, цитомегаловируса и других инфекционных агентов, способных вызывать воспалительные изменения мозговых тканей с образованием кальцификатов.
Диагноз болезнь Фара правомочен после исключения вторичного характера церебральной кальцификации, наблюдающейся при эндокринных (гипопаратиреоз, псевдогипопаратиреоз, гипотиреоз), сосудистых (атеросклероз, амилоидоз сосудов), инфекционных (краснуха, цистицеркоз, токсоплазмоз, цитомегалия) заболеваниях. Дифференциальная диагностика проводится также с болезнью Галлервордена-Шпатца, туберозным склерозом.
Лечение болезни Фара
Поскольку патогенез заболевания остаётся неясным, терапия имеет преимущественно симптоматический характер. С целью улучшения обменных процессов применяются стимуляторы тканевого метаболизма (ацетилкарнитин, глютаминовая кислота, комплекс L-цитруллин+малат, никотинамид), цитопротекторы (рибофлавин, янтарная кислота, мельдоний). При симптомах паркинсонизма предпочтительно назначение фармпрепаратов леводопы, при гиперкинезах — холинолитиков, бензодиазепинов. Наличие эпилептических приступов служит показанием к лечению современными антиконвульсантами (леветирацетамом). В комплексной терапии применяется лечебная физкультура, водолечение, когнитивные тренинги.
Прогноз и профилактика
Клинически проявленная болезнь Фара рассматривается как хроническое нейродегенеративное заболевание. Прогноз выздоровления неблагоприятный, однако, при должном уровне поддерживающей симптоматической терапии состояние пациентов длительное время остаётся удовлетворительным. Субклинический вариант не сказывается на здоровье и когнитивных способностях больного, может быть случайной находкой при проведении компьютерной томографии. Специфические меры, позволяющие предупредить развитие болезни, не разработаны.
Источник
Рубрика МКБ-10: G23.8
МКБ-10 / G00-G99 КЛАСС VI Болезни нервной системы / G20-G26 Экстрапирамидные и другие двигательные нарушения / G23 Другие дегенеративные болезни базальных ганглиев
Определение и общие сведения[править]
Двусторонний стриопаллидодентатный кальциноз
Синонимы: феррокальциноз сосудов головного мозга, идиопатический кальциноз базальных ганглиев.
Идиопатический кальциноз базальных ганглиев, его также ошибочно называют болезнью Фара, характеризуется накоплением отложений кальция в различных областях мозга, особенно в базальных ганглиях и зубчатом ядре, часто ассоциируется с нейродегенерацией.
Распространенность неизвестна, менее 200 случаев заболевания были зарегистрированы на сегодняшний день. Чаще встречается у мужчин (соотношение мужчин и женщин 2: 1).
Патология носит семейный или спорадический характеро. Известно более 30 семей с наследственной формой патологии, которая наследуется аутосомно-доминантно.
Этиология и патогенез[править]
Идиопатический кальциноз базальных ганглиев является генетически гетерогенной патологией. С возникновением заболевания связывают локусы генов IBGC1 (14q11.2–21.3.), IBGC2 (2q37), IBGC3 (8p21.1-q11.13) и IBGC4 (5q32). Мутация гена SLC20A2 (локус IBGC3) была обнаружена у 218 пациентов из 29 семей. Еще один локус был идентифицирован в 2013 году и связан с геном PDGFRB, кодирующем тромбоцитарный бета фактор роста (PDGFB).
Клинические проявления[править]
Идиопатический кальциноз базальных ганглиев может протекать бессимптомно. Симптоматические формы, как правило, манифестируют на четвертом десятилетии жизни, хотя кальцификации могут быть найдены во втором десятилетии. У пациентов наблюдаются двигательные расстройства, в том числе паркинсонизм, хорея, тремор, дистония, атетоз, орофациальная дискинезия и атаксия. Кроме того пациенты демонстрируют психоневрологические расстройства — затруднение концентрации внимание, нарушения памяти и/или изменения личности и поведения, а также признаки деменции.
Часто первыми симптомами заболевания являются моторная неуклюжесть, утомляемость, неустойчивая походка, медленная или невнятная речь, дисфагия, непроизвольные движения или судороги. Может возникнуть недержание мочи .
Другие уточненные дегенеративные болезни базальных ганглиев: Диагностика[править]
Диагноз основывается на данных КТ или МРТ, демонстрирующих двусторонние, почти симметричные кальцификации одной или нескольких из следующих областей: базальных ганглиев, зубчатых ядер, таламуса и коры головного мозга. Электроэнцефалограмма, исследование нервной проводимости, зрительные вызванные потенциалы и слуховые вызванные потенциалы, как правило, нормальные или с незначительными отклонениями.
Дифференциальный диагноз[править]
Дифференциальный диагноз включает гипопаратиреоз и псевдогипопаратиреодизм, синдром Кенни-Каффи 1-го типа, нейродегенерации с накоплением железа, синдром Коккейна и синдром Айкарди-Гутьерреса.
Другие уточненные дегенеративные болезни базальных ганглиев: Лечение[править]
Специфического лечения на сегодняшний день нет. Лечение основано на купировании симптомов тревоги, депрессии, обсессивно-компульсивное поведения и дистонии.
Профилактика[править]
Прочее[править]
Обызвествление базальных ядер и зубчатого ядра может сопутствовать некоторым другим состояниям (см. табл. 15.7), нередко оно выявляется у пожилых и может быть одной из причин легких двигательных нарушений, часто встречающихся в этой возрастной группе. При выраженном обызвествлении бывают тяжелые прогрессирующие двигательные расстройства в виде паркинсонизма или хореоатетоза.
В случае гипокальциемии (при послеоперационном или идиопатическом гипопаратиреозе либо при псевдогипопаратиреозе) прогрессирование двигательных расстройств можно остановить, если нормализовать концентрацию кальция в крови с помощью витамина D (50 000—100 000 МЕ/сут) и препаратов кальция. Для предупреждения передозировки витамина D необходимо регулярное биохимическое исследование крови. Регресс двигательных нарушений наблюдается редко, за исключением, возможно, случаев идиопатического гипопаратиреоза. Реже обызвествление возникает при гиперпаратиреозе и псевдопсевдогипопаратиреозе (нормокальциемическом псевдогипопаратиреозе).
Источники (ссылки)[править]
https://www.orpha.net
https://www.dovepress.com
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
