Аутоиммунный полигландулярный синдром 1 типа фото

Аутоиммунный полигландулярный синдром – эндокринопатия аутоиммунного генеза, протекающая с одновременным первичным множественным поражением желез внутренней секреции и других органов. При аутоиммунном полигландулярном синдроме 1 типа отмечается надпочечниковая недостаточность, кандидоз кожи и слизистых, гипопаратиреоз; аутоиммунный полигландулярный синдром 2 типа протекает с развитием надпочечниковой недостаточности, гипер- или гипотиреоза, инсулинозависимого сахарного диабета, первичного гипогонадизма, миастении, стеатореи и др. нарушений. Диагностика включает определение комплекса лабораторных показателей (биохимического анализа, гормонов крови и мочи), УЗИ и КТ надпочечников, УЗИ щитовидной железы. Лечение аутоиммунного полигландулярного синдрома требует назначения заместительной терапии гормонами (кортикостероидами и минералокортикоидами, L-тироксином).
Общие сведения
Аутоиммунный полигландулярный синдром (АПГС) – иммуноэндокринное нарушение, характеризующееся первичной функциональной недостаточностью нескольких желез внутренней секреции, а также неэндокринными органоспецифическими заболеваниями. В эндокринологии различают аутоиммунный полигландулярный синдром 1 и 2 типов (АПГС-1, 2), которые имеют свои генетические, иммунологические и клинические особенности.
Аутоиммунный полигландулярный синдром 1 типа обычно манифестирует в детском возрасте (10-12 лет) и иногда обозначается в литературе термином «ювенильная семейная полиэндокринопатия». В целом распространенность АПГС-1 невелика, однако заболевание несколько чаще встречается в мужской популяции, преимущественно у жителей Финляндии, Сардинии, Ирана, что объясняется длительной генетической обособленностью этих народов. Аутоиммунный полигландулярный синдром 1 типа включает триаду признаков: надпочечниковую недостаточность, гипопаратироз и кандидамикоз.
Наиболее частым вариантом множественной эндокринопатии аутоиммунной природы является аутоиммунный полигландулярный синдром 2 типа, который развивается у взрослых (старше 20-30 лет); среди заболевших преобладают женщины. Компонентами АПГС-2 являются надпочечниковая недостаточность, сахарный диабет 1-го типа, аутоиммунное поражение щитовидной железы по типу первичного гипотиреоза или тиреотоксикоза. Кроме эндокринных нарушений, аутоиммунному полигландулярному синдрому 1 и 2 типов сопутствуют другие органоспецифические проявления.
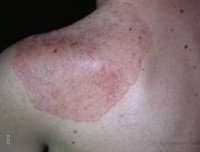
Аутоиммунный полигландулярный синдром
Причины аутоиммунного полигландулярного синдрома
Оба типа аутоиммунного полигландулярного синдрома являются генетически детерминированными, на что указывает семейно-наследственный характер заболевания. При этом АПГС-1 поражаются братья и сестры одного поколения; аутоиммунным полигландулярным синдромом 2 типа – представители одной семьи на протяжении нескольких поколений.
Аутоиммунный полигландулярный синдром 1 типа – единственное известное аутоиммунное заболевание, имеющее моногенную природу. К развитию АПГС-1 приводит мутация гена аутоиммунного регулятора (AIRE), расположенного на длинном плече 21 хромосомы (21q22.3). Аутоиммунный полигландулярный синдром-1 наследуется по аутосомно-рецессивному типу и не связан с гаплотипами HLA.
Аутоиммунный полигландулярный синдром 2 типа ассоциирован с HLA-гаплотипом (антигенами DR3, DR4, DR5, В8, Dw3). Вероятно, что механизм развития АПГС-2 связан с аномальной экспрессией антигенов HLA-системы на клеточных мембранах желез внутренней секреции, которая запускается под воздействием каких-либо внешних факторов.
Симптомы аутоиммунного полигландулярного синдрома 1 типа
Аутоиммунный полигландулярный синдром 1 типа обычно впервые заявляет о себе в первые 10 лет жизни развитием гранулематозного кандидоза (кандидамикоза кожи и слизистых) и гипопаратиреоза. В дальнейшем (часто спустя десятилетия) присоединяется хроническая надпочечниковая недостаточность (аддисонова болезнь). Клиническими критериями установления диагноза синдрома служит сочетание двух из трех упомянутых эндокринных нарушений.
Кандидоз при АПГС-1 носит генерализованный характер и поражает слизистые оболочки полости рта, гениталий, дыхательных путей и желудочно-кишечного тракта, а также кожу, ногтевые валики, ногти. Гипопаратиреоз проявляется судорогами мышц конечностей, парестезией кожи, ларингоспазмом, судорожными припадками, напоминающими эпилепсию. Надпочечниковая недостаточность при аутоиммунном полигландулярном синдроме нарастает скрыто и может впервые проявится аддисоническим кризом на фоне стрессового состояния.
Классическая триада при аутоиммунном полигландулярном синдроме часто сочетается с первичным гипогонадизмом (45%), алопецией (30%), синдромом мальабсорбции (23%), пернициозной анемией (14%), хроническим аутоиммунным гепатитом (12%), аутоиммунным тиреоидитом (10%), инсулинозависимым сахарным диабетом (4%), витилиго (4%). Реже встречается дистрофия ногтевых пластин, гипоплазия зубной эмали, гломерулонефрит, бронхиальная астма, катаракта.
На фоне аутоиммунного полигландулярного синдрома 1 типа у женщин отмечается гипоплазия яичников (аутоиммунный оофорит), сопровождающийся первичной или вторичной аменореей. Мужской гипогонадизм проявляется снижением либидо, импотенцией, бесплодием.
Симптомы аутоиммунного полигландулярного синдрома 2 типа
Манифестация аутоиммунного полигландулярного синдрома 2 типа приходится на зрелый возраст (около 30 лет). Первым проявлением эндокринопатии обычно служит хроническая надпочечниковая недостаточность. Другие аутоиммунные компоненты (сахарный диабет 1-го типа, аутоиммунный тиреоидит), как правило, присоединяются через 7-10 и более лет.
У пациентов с аутоиммунным полигландулярным синдромом 2 типа часто развивается первичный гипогонадизм, миастения, витилиго, дерматит, алопеция, аутоиммунный гастрит, целиакия, стеаторея, полисерозиты (плеврит, перикардит, асцит), тимома. При аутоиммунном полигландулярном синдроме могут наблюдаться атрофия зрительных нервов, опухоли гипофиза, аутоиммунная тромбоцитопеническая пурпура и т. д.
Наиболее часто в клинической практике встречается вариант аутоиммунного полигландулярного синдрома 2-го типа, сочетающий первичную хроническую надпочечниковую недостаточность с аутоиммунным поражением щитовидной железы: аутоиммунным тиреоидитом, реже — диффузным токсическим зобом (синдром Шмидта). Множественные эндокринопатии взаимно отягощают друг друга и утяжеляют течение заболевания.
Диагностика аутоиммунного полигландулярного синдрома
Критериями для постановки клинического диагноза служат подтвержденные лабораторным и инструментальным путем изолированные компоненты аутоиммунного полигландулярного синдрома (кожно-слизистый кандидоз, гипопаратиреоз и ХНН при АПГС-1; ХНН, аутоиммунный тиреоидит и сахарный диабет при АПГС-2). При АПГС 1 типа наиболее показательно проведение молекулярно-генетического анализа, позволяющего выявить характерную генную мутацию.
Лабораторное обследование при аутоиммунном полигландулярном синдроме включает определение биохимических показателей крови (уровня общего и ионизированного кальция, фосфора, калия, натрия, билирубина, трансаминаз, щелочной фосфатазы, общего белка, мочевины, креатинина, глюкозы), КОС крови и др. Важные диагностические сведения дают результаты исследований гормонов: ТТГ, свободного тироксина, паратгормона, АКТГ, инсулина, С-пептида, кортизола, ренина, альдостерона, соматомедина С, АТ-ТПО, АТ к бета-клеткам поджелудочной железы и GAD, тестостерона, ЛГ, ФСГ и др.
Инструментальные исследования включают УЗИ брюшной полости, щитовидной железы, органов малого таза (у женщин) и мошонки у мужчин, ЭхоКГ, КТ надпочечников. При наличии показаний проводятся консультации узких специалистов – диабетолога, гастроэнтеролога, гепатолога, дерматолога, миколога, невролога, гематолога, офтальмолога, гинеколога-эндокринолога, андролога, ревматолога.
Лечение аутоиммунного полигландулярного синдрома
Терапия аутоиммунного полигландулярного синдрома представляет сложную задачу и складывается из лечения его отдельных компонентов. Основу патогенетической терапии составляет постоянная заместительная гормонотерапия при функциональной недостаточной пораженных эндокринных желез. При надпочечниковой недостаточности назначаются глюкокортикоиды (гидрокортизон, дексаметазон, преднизолон, триамцинолон), минералокортикоиды (ДОКСА, триметилацетат дезоксикортикостерона и др.), при гипотиреозе — L-тироксин.
При кандидамикозе, сопровождающем аутоиммунный полигландулярный синдром 1 типа, используются противогрибковые препараты. При сахарном диабете на фоне аутоиммунного полигландулярного синдрома 2 типа может потребоваться иммуносупрессивная терапия циклоспорином. Пациентам рекомендуется употребление повышенного количества аскорбиновой кислоты и соли. Запрещается прием алкоголя, некоторых лекарственных препаратов.
Прогноз аутоиммунного полигландулярного синдрома
Раннее выявление аутоиммунного полигландулярного синдрома и проведение адекватной заместительной терапии позволяют контролировать течение заболевания. Однако трудоспособность, как правило, снижается – пациентам присваивается II-III группа инвалидности.
Пациенты с аутоиммунным полигландулярным синдромом подлежат диспансерному наблюдению эндокринолога и других специалистов. При стрессовых состояниях, интеркуррентных инфекциях, физическом или умственном перенапряжении больным необходимо увеличение дозы гормонов. Необходимо немедленное обращение к врачу при любом ухудшении самочувствия. Летальный исход при аутоиммунном полигландулярном синдроме может наступать от ларингоспазма, висцерального кандидамикоза, острой надпочечниковой недостаточности.
Источник
Так называют заболевания, протекающие с аутоиммунным поражением двух или более эндокринных желез и других органов. Различают три аутоиммунных полигландулярных синдрома. Аутоиммунный полигландулярный синдром типа I проявляется в детстве; главные его компоненты — хронический генерализованный гранулематозный кандидоз, гипопаратиреоз и первичная надпочечниковая недостаточность.

Аутоиммунный полигландулярный синдром типа II чаще проявляется в зрелом возрасте и характеризуется аутоиммунными заболеваниями щитовидной железы, инсулинозависимым сахарным диабетом, первичной надпочечниковой недостаточностью и первичным гипогонадизмом. Аутоиммунный полигландулярный синдром типа III — это сочетание аутоиммунного заболевания щитовидной железы с каким-либо другим аутоиммунным эндокринным заболеванием.
Аутоиммунные полигландулярные синдромы
Тип I
Хронический генерализованный гранулематозный кандидоз. Гипопаратиреоз.
Первичная надпочечниковая недостаточность.
Первичный гипогонадизм.
Алопеция.
Первичный гипотиреоз.
Нарушения всасывания.
Хронический аутоиммунный гепатит.
Витилиго.
Болезнь Аддисона—Бирмера
Тип II
Аутоиммунное заболевание щитовидной железы (хронический лимфоцитарный тиреоидит, реже диффузный токсический зоб).
Инсулинозависимый сахарный диабет.
Первичная надпочечниковая недостаточность.
Первичный гипогонадизм.
Миастения.
Витилиго.
Алопеция.
Болезнь Аддисона—Бирмера.
Целиакия
Тип III
Аутоиммунное заболевание щитовидной железы в сочетании с инсулинозависимым сахарным диабетом либо с первичной надпочечниковой недостаточностью
Этиология и патогенез
Происхождение аутоиммунных полигландулярных синдромов до сих пор неизвестно. Полагают, что в их развитии участвуют и генетические, и негенетические факторы. Аутоиммунный полигландулярный синдром типа I наследуется аутосомно-рецессивно; связь с аллелями HLA не прослеживается.
Почти у всех больных имеются мутации гена AIRE (Autoimmune REgulator — регулятор аутоиммунитета), расположенного в локусе 21q22.3. Этот ген кодирует белок, регулирующий аутоиммунитет.
У больных аутоиммунными полигландулярными синдромами типов II и III с повышенной частотой встречаются аллели HLA-DR3 и HLA-DR4. Эти синдромы наследуются аутосомно-доминантно с вариабельной экспрессивностью. Конкордантность однояйцовых близнецов по инсулинозависимому сахарному диабету и по диффузному токсическому зобу составляет всего около 50%. Следовательно, для проявления генетических дефектов требуются какие-то пусковые факторы.
В случае инсулинозависимого сахарного диабета и хронического лимфоцитарного тиреоидита такими факторами могут служить вирусные инфекции (вирусы краснухи, эпидемического паротита, Коксаки В, цитомегаловирус) и пищевые антигены, например белки молока.
У больных аутоиммунными полигландулярными синдромами порой обнаруживают разнообразные органоспецифические аутоантитела. Некоторые из них распознают ферменты эндокринных клеток (например, йодидпероксидазу тироцитов, 20,22-десмолазу надпочечников, глутаматдекар-боксилазу р-клеток) и являются маркерами аутоиммунных заболеваний.
Другие аутоантитела связываются с мембранными рецепторами (например, с рецепторами ТТГ, АКТГ, инсулина), нарушая функцию эндокринных клеток. Третьи связывают комплемент, вызывая цитотоксические реакции. Роль цитокинов, в частности интерферона, и нарушений клеточного иммунитета в патогенезе аутоиммунных полигландулярных синдромов неясна.
Аутоиммунный полигландулярный синдром типа I
Другие названия синдрома: аутоиммунный полигландулярный синдром, ювенильный тип; APECED (Autoimmune Ро-lyEndocrinopathy, Candidiasis, Ectodermal Dystrophy — аутоиммунная полиэндокринопатия, кандидоз, дистрофия эктодермы). Синдром обычно проявляется в первые 10 лет жизни.
Для диагноза требуется наличие двух из трех главных компонентов — хронического генерализованного гранулематозного кандидоза, гипопаратиреоза, первичной надпочечниковой недостаточности. Дефицит минералокортикои-дов и дефицит глюкокортикоидов развиваются одновременно или последовательно.
Из других гормональных нарушений возможны первичный гипогонадизм, первичный гипотиреоз, реже — разрушение β-клеток островков поджелудочной железы с развитием инсулинозависимого сахарного диабета. Наблюдаются также гипоплазия зубной эмали, дистрофия ногтей, тимпаносклероз, витилиго, кератопатия, болезнь Аддисона—Бирмера.
У некоторых больных развиваются хронический аутоиммунный гепатит, нарушения всасывания (возможные причины: идиопатическая кишечная лимфангиэктазия, дефицит IgA, синдром слепой петли, гипопаратиреоз), функциональный аспленизм, ахалазия кардии, желчнокаменная болезнь. В начале заболевания может быть поражен только один орган. Со временем число их увеличивается, так что у каждого больного, как правило, имеется от двух до пяти компонентов синдрома. У иранских евреев встречается вариант синдрома, проявляющийся только гипопаратиреозом.
Исследования, проведенные в Финляндии, показали, что у 78% больных имеется какой-либо неэндокринный компонент синдрома. Чаще всего это кандидозный стоматит. Кандидозом страдает большинство больных, он часто рецидивирует, однако протекает легко, и при обследовании его часто не замечают. Поражение паращитовидных желез обычно предшествует развитию надпочечниковой недостаточности.
Гипогонадизм развивается у 60% женщин детородного возраста. Гипопаратиреоз, надпочечниковая недостаточность и другие гормональные нарушения иногда проявляются только после 30 лет, что диктует необходимость пожизненного наблюдения.
Аутоиммунный полигландулярный синдром типа II (синдром Шмидта)
Главный компонент синдрома — аутоиммунное заболевание щитовидной железы, другие наиболее частые эндокринные нарушения: инсулинозависимый сахарный диабет, первичная надпочечниковая недостаточность и первичный гипогонадизм. Патоморфологическим признаком синдрома служит лимфоцитарная инфильтрация щитовидной железы и коры надпочечников. Патология щитовидной железы — это чаще всего хронический лимфоцитарный тиреоидит (проявляется гипотиреозом), реже — диффузный токсический зоб (проявляется тиреотоксикозом).
У многих больных с антителами к микросомальным антигенам и к тиреоглобулину функция щитовидной железы никогда не нарушается, поэтому прогнозировать течение болезни только на основании определения антител нельзя. Инсулинозависимый сахарный диабет встречается примерно в половине семей с этим синдромом.
Поражение кожи встречается реже, чем при аутоиммунном полигландулярном синдроме типа I, и включает витилиго, обусловленное аутоиммунной реакцией против меланоцитов, и алопецию. Хронический генерализованный гранулематозный кандидоз нехарактерен.
У небольшого числа больных на поздних стадиях заболевания возникает гипопаратиреоз, который обычно имеет преходящий характер и обусловлен аутоантителами, конкурирующими с ПТГ за связывание с рецептором ПТГ. Аутоиммунный полигландулярный синдром типа II выявляют почти у 25% больных миастенией. При сочетании миастении с тимомой этот синдром еще более вероятен.
Аутоиммунный полигландулярный синдром типа III
В небольшом числе семей из поколения в поколение сочетаются поражения щитовидной железы и коры надпочечников или щитовидной железы и островков поджелудочной железы в отсутствие иных аутоиммунных заболеваний. Больные страдают хроническим лимфоцитарным тиреоидитом (или другим аутоиммунным заболеванием щитовидной железы) и инсулинозависимым сахарным диабетом либо первичной надпочечниковой недостаточностью.
Диагностика
Надпочечниковая недостаточность, если ее вовремя не выявить и не назначить лечение, может стать причиной смерти. Поскольку симптомы надпочечниковой недостаточности нарастают постепенно и не всегда очевидны, всех больных из группы риска и всех родственников больных аутоиммунными полигландулярными синдромами нужно регулярно обследовать.
Для выявления надпочечниковой недостаточности лучше всего подходит проба с АКТГ. Для выявления гипергликемии измеряют глюкозу в плазме натощак. Кроме того, измеряют уровни ТТГ, ЛГ, ФСГ, а у мужчин — еще и тестостерона. Если подозревается аутоиммунный полигландулярный синдром типа I, определяют также уровни кальция и фосфора.
Обследование проводят каждые 1—2 года, начиная с детства и до 50 лет (в случае аутоиммунных полигландулярных синдромов типов II и III) или 40 лет (в случае аутоиммунного полигландулярного синдрома типа I). Прогностическая ценность определения органоспецифических аутоантител неясна. Дифференциальный диагноз включает синдром Ди Джорджи (гипопаратиреоз, обусловленный аплазией или дисгенезией паращитовидных желез, и хронический генерализованный гранулематозный кандидоз); синдром Кирнса—Сейра (гипопаратиреоз, первичный гипогонадизм, инсулинозависимый сахарный диабет, гипопитуитаризм); синдром Вольфрама, или DIDMOAD (Diabetes Insipidus, Diabetes Mellitus, Optic Atrophy, Deafness — несахарный диабет, инсулинозависимый сахарный диабет, атрофия зрительных нервов, глухота); врожденную краснуху (инсулинозависимый сахарный диабет и первичный гипотиреоз).
Лечение
За исключением диффузного токсического зоба, лечение эндокринных патологий включает заместительную гормональную терапию и подробно описывается в главах, посвященных болезням надпочечников, щитовидной и паращитовидных желез, яичников и яичек. Особого внимания заслуживает лечение первичного гипотиреоза, который может маскировать проявления надпочечниковой недостаточности за счет увеличения Т1/2 кортизола.
Введение тиреоидных гормонов больным со скрытой надпочечниковой недостаточностью способно спровоцировать гипоадреналовый криз. В связи с этим у каждого больного с аутоиммунным полигландулярным синдромом до начала лечения гипотиреоза следует исключить надпочечниковую недостаточность. Если же таковая обнаружена, заместительную глюкокортикоидную терапию начинают одновременно или перед началом лечения тиреоидными гормонами.
Другие аутоиммунные синдромы
Антитела к рецептору инсулина
Инсулинорезистентностъ, под которой понимают пониженную чувствительность тканей-мишеней к инсулину, часто встречается при ожирении, тяжелых инфекционных заболеваниях, травмах, после хирургических вмешательств, а также у больных акромегалией и синдромом Кушинга. В последних двух случаях действию инсулина на ткани-мишени препятствует избыток СТГ или кортизола. Изредка инсулинорезистентность бывает обусловлена аутоантителами к рецептору инсулина, которые препятствуют связыванию гормона со своим рецептором. Другие антитела к рецептору инсулина способны сами активировать рецептор и провоцировать приступы гипогликемии. Это нарушение надо иметь в виду при дифференциальной диагностике гипогликемии голодания.
Под синдромом инсулинорезистентности и acanthosis nigricans типа Б понимают сочетание антител к рецептору инсулина с acanthosis nigricans. Синдром часто встречается у женщин средних лет; инсулинорезистентность носит приобретенный характер и развивается на фоне других аутоиммунных заболеваний, например СКВ или синдрома Шегрена.
Больные страдают также витилиго, алопецией, синдромом Рейно, артритом, изредка — тиреотоксикозом, гипотиреозом, гипогонадизмом. Acanthosis nigricans — ворсинчато-бородавчатое разрастание и гиперпигментация кожи задней поверхности шеи, подмышечных впадин, паховых и других крупных складок — нередко позволяет заподозрить диагноз. Однако сам по себе acanthosis nigricans не указывает на аутоиммунную природу инсулинорезистентности. Он наблюдается также у больных, страдающих ожирением и синдромом поликистозных яичников.
В этом случае инсулинорезистентность носит наследственный характер и, по-видимому, обусловлена мутациями гена рецептора инсулина, приводящими к внутриклеточным нарушениям передачи сигнала, а заболевание называют синдромом инсулинорезистентности и acanthosis nigricans типа А.
Степень нарушений, которые вызывают антитела, блокирующие рецептор инсулина, бывает разной. Антитела, активирующие рецептор инсулина, могут стать причиной снижения числа рецепторов и их десенситизации. Степень инсулинорезистентности при этом колеблется в широких пределах. У одних больных, страдающих acanthosis nigricans, толерантность к глюкозе либо не нарушена, либо слегка снижена, что влечет за собой компенсаторную гиперинсулинемию, выявляемую лишь лабораторными методами. У других больных развивается тяжелейший сахарный диабет, требующий ежедневного введения огромных доз инсулина (до тысяч единиц).
Клиническая картина во многом определяется природой антител. Более характерна инсулинорезистент-ность, но и гипогликемия голодания — не редкость: она может быть первым проявлением болезни или развиться впоследствии. Приступы гипогликемии связывают с действием антител, активирующих рецепторы инсулина.
Антитела к рецептору инсулина появляются также при атаксии-телеангиэктазии. Заболевание наследуется аутосомно-рецессивно и характеризуется инсулинорезистентным сахарным диабетом, атаксией, телеангиэктазиями, аутоиммунными нарушениями, склонностью к гемобластозам.
Аутоантитела к инсулину
При аутоиммунных заболеваниях иногда появляются поликлональные аутоантитела к эндогенному инсулину. Диссоциация комплексов инсулин-антитело через несколько часов после приема пищи может вызвать приступ гипогликемии. Большинство таких больных описано в Японии, что наводит на мысль о генетической детерминированности синдрома. Аутоантитела к инсулину служат причиной завышенных результатов измерения уровня инсулина в сыворотке.
Исключить ошибку позволяет определение уровня С-пептида: если он в норме, уровень инсулина завышен. При моноклональных гаммапатиях, в частности при миеломной болезни, плазматические клетки иногда продуцируют моноклональные аутоантитела к инсулину, что также сопровождается гипогликемией.
Антитела к тиреоидным гормонам
У больных с сочетанием аутоиммунной патологии щитовидной железы и моноклональной гаммапатии, например макроглобулинемии Вальденстрема, антитела к тиреоидным гормонам снижают биологическую активность Т4 и Т3, что может привести к первичному гипотиреозу. В остальных случаях эти антитела просто искажают результаты измерения уровней Т4 и Т3 и затрудняют оценку функции щитовидной железы.
Синдром POEMS
Компоненты синдрома перечислены в его названии: Polyneuropathy — полинейропатия, Organomegaly — спланхномегалия, Endocrinopathy — эндокринопатии, Monoclonal gammopathy — моноклональная гаммапатия, Skin lesions — поражение кожи. Важнейшими из них являются тяжелая, прогрессирующая сенсорно-моторная полинейропатия и миеломная болезнь.
Скопления плазматических клеток (плазмоцитомы) вызывают остеосклероз и продуцируют моноклональные IgG и IgA. Эндокринные проявления синдрома включают аменорею у женщин, импотенцию и гинекомастию у мужчин, первичный гипогонадизм, гиперпролактинемию, инсулинонезависимый сахарный диабет, первичный гипотиреоз и надпочечниковую недостаточность.
Поражение кожи проявляется гиперпигментацией, утолщением кожи, гирсутизмом и потливостью. У двух третей больных отмечаются гепатомегалия и увеличение лимфоузлов, у трети — спленомегалия. Кроме того, возможны внутричерепная гипертензия с отеком диска зрительного нерва, асцит, плевральный выпот, отеки, гломерулонефрит, лихорадка.
Из-за полиорганных нарушений заболевание нередко принимают за коллагеноз. Свойственные синдрому эндокринные нарушения наводят на мысль о его аутоиммунной природе, однако антител к эндокринным клеткам у больных не обнаруживают. В крови и других тканях повышено содержание ИЛ-6, однако роль этого цитокина в патогенезе синдрома неясна. Лечение миеломной болезни (облучение плазмоцитом, химиотерапия) способно сгладить эндокринные нарушения.
ДРУГИЕ ПОЛИЭНДОКРИНОПАТИИ
Множественные эндокринные нарушения наблюдаются при многих наследственных и приобретенных заболеваниях. Генетические дефекты, лежащие в основе некоторых из них, до сих пор неизвестны. Синдром Мак-Кьюна—Олбрайта обусловлен дефектом αs-субъединицы G-белка, сопрягающего рецепторы многих гормонов с аденилатциклазой. Дефектный белок постоянно активирует аденилатциклазу, что приводит к гиперфункции эндокринных желез. У больных наблюдаются преждевременное половое развитие, акромегалия, тиреотоксикоз, синдром Кушинга и гиперпигментированные пятна.
Источник
