Абдоминальный компартмент синдром клинические рекомендации

Интраабдоминальная гипертензия (ИАГ) (Intra-abdominal Hypertension (IAH)) и абдоминальный компартмент-синдром (АКС) (Abdominal Compartment Syndrome (ACS)) являются тяжелыми осложнениями заболеваний, как у хирургических, так и у нехирургических больных. Однако эти два сопутствующих явления, при своей высокой распространенности, часто остаются непризнанными или не диагностированными. ИАГ воздействует на региональную и общую перфузии, что может привести к полиорганной недостаточности и летальному исходу.
Наиболее ранним проявлением, даже при относительно низком уровне ИАГ, является олигурия и острое повреждение почек (ОПП). Профилактика ИАГ путем раннего выявления и мониторинга пациентов группы риска может полностью исключить развитие АКС. Понимание этиологии и патофизиологии ИАГ и AКС имеет важное значение для выявления патологии и может быть использовано в качестве руководства при его профилактике и осуществлении соответствующей терапии.
Определение и руководящие принципы ИАГ и АКС установлены Всемирным обществом абдоминального компартмент-синдрома (WSACS).
Интраабдоминальное давление (ИАД) — давление внутри брюшной полости.
В среднем у взрослого человека нормальный уровень ИАД находится в пределах 0–5 мм рт.ст., в то время как у тяжелобольных взрослых он обычно составляет 5–7 мм рт. ст.
Интраабдоминальная гипертензия (ИАГ) — постоянное или рецидивирующее патологическое повышение ИАД больше ≥ 12 мм рт.
Абдоминальный компартмент синдром (АКС) — устойчивая ИАГ (более 20 мм рт.ст.), при абдоминальном перфузионном давлении (АПД) < 60 мм рт. ст., связанная с новой дисфункцией/недостаточностью органов.
Абдоминальное перфузионное давление — это разница между средним артериальным давлением (САД) и ИАГ.
АПД является индикатором висцеральной перфузии, понятие которой уподобляется церебральному перфузионному давлению. WSACS определил нормальное АПД на уровне 60 мм рт.ст. или выше.
АПД менее 60 мм рт. ст. — надежный индикатор необходимости хирургической декомпрессии, что делает его полезным как в диагностике, так и в лечении.
Система классификации была разработана WSACS для ИАГ. Классификация ИАГ по степеням выглядит следующим образом:
- I степень: ИАД 12–15 мм рт. ст.;
- II степень: ИАД 16–20 мм рт. ст.;
- III степень: ИАД 21–25 мм рт. ст.;
- IV степень: ИАД > 25 мм рт.
С другой стороны, АКС дополнительно классифицируется в зависимости от причины и продолжительности ИАГ на первичную, вторичную и рецидивирующую.
- Первичный АКС — это состояние, ассоциированное с травмой или заболеванием в области брюшной полости, которое часто требует раннего хирургического или интервенционного рентгенологического вмешательства.
- Вторичный АКС относится к состояниям, которые не исходят из брюшной полости. Рецидивирующий АКС относится к состоянию, возникшему после предыдущего хирургического или медицинского лечения первичного или вторичного АКС.
Эти системы классификационных групп, разработанные WSACS, облегчают последующее управление ИАГ и АКС в рамках организации поэтапного подхода к ведению больных.
Наиболее распространенные факторы риска развития ИАГ и/или АКС в соответствии WSACS:
- снижение эластичности брюшной стенки;
- увеличение содержимого внутри просвета кишечника;
- увеличение внепросветного/внутрибрюшного содержимого;
- синдром капиллярной утечки и агрессивная инфузионная терапия.
Примечание. Некоторые из этих факторов риска далеки от патофизиологического обоснования и клинического суждения.
Развитие ИАГ у пациентов, которым проводится интенсивная терапия, связано с ухудшением клинического исхода, и это может наблюдаться у пациентов с тяжелым острым панкреатитом, распространенность интраабдоминальной гипертензии у этого типа пациентов составляет около 40–50 %, что обычно является осложнением ранней и агрессивной инфузионной терапии.
Помимо серьезных ожогов и сепсиса, которые являются одними из причин вторичного ИАГ/АКС, травмы и хирургические манипуляции в области живота являются предрасполагающими условиями, влияющими на развитие первичного ИАГ/АКС и, следовательно, послеоперационной почечной недостаточности. В проспективном наблюдательном исследовании, которое включало 263 пациента, ИАГ (определяемая как ИАП, превышающая или равная 18 мм рт.ст.) была независимой причиной нарушения функции почек после абдоминальной операции.
Чтобы понять основные принципы ИАГ и АКС, мы можем сравнить его в целом с компартмент-синдромом, когда повышение давления ухудшает капиллярный кровоток, в конечном итоге уменьшая приток в артериолы и уменьшая венозный отток. В дальнейшем это вызывает клеточную гипоксию, которая, в свою очередь, предшествует анаэробному дыханию и молочнокислому ацидозу.
Человеческое тело можно рассматривать как сочетания различных анатомических отделов, взаимодействующие друг с другом, по этой причине патофизиология внутриполостной гипертензии и компартмент-синдрома является многофакторной и может наблюдаться почти во всех системах органов.
ИАГ, очевидно, не только вызывает снижение перфузии во всех органах брюшной полости, но и оказывает влияние на внебрюшинные органы, а в некоторых случаях даже оказывает влияние на внутричерепное давление. Проще говоря, когда внутрибрюшное давление повышается, многие органы постепенно начинают отказывать. Было установлено, что ИАГ вызывает ряд патофизиологических изменений, начиная с региональных нарушений кровотока и заканчивая явной недостаточностью систем органов и развитием АКС.
Помимо уровня ИАД и этиологии ИАГ у пациента, схожую по значимости роль играет коморбидность, которую следует принимать во внимание, поскольку это снижает порог ИАД, вызывающий клинические проявления (изображение 1).
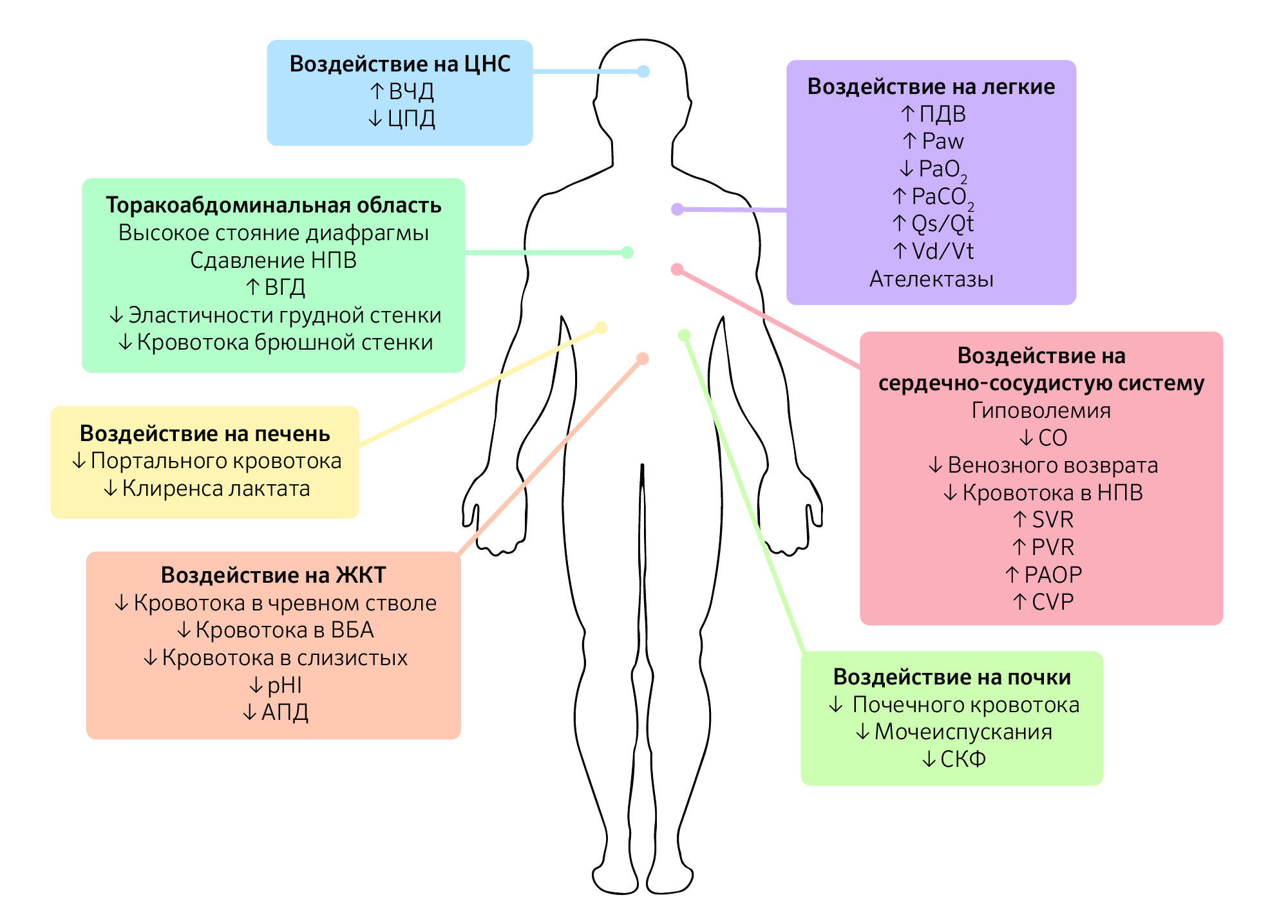
Изображение 1 | Патофизиологические последствия интраабдоминальной гипертензии.
Последствия интраабдоминальной гипертензии не ограничиваются только органами брюшной полости, а, скорее, оказывают прямое или косвенное воздействие на каждую систему органов в организме. Схема влияния ИАГ на системы органов.
Сокращения: ВЧД — внутричерепное давление; ЦПД — церебральное перфузионное давление; ВГД — внутригрудное давление; НПВ — нижняя полая вена; ВБА — верхняя брыжеечная артерия; pHI — pH слизистой желудка ; АПД — абдоминальное перфузионное давление; ПДВ — пиковое давление вдоха; Paw, mean airway pressure —среднее давление в дыхательных путях; PaО2 — парциальное давление кислорода в артериальной крови; PaCO2 — парциальное давление углекислого газа в артериальной крови; Qs/Qt — внутрилегочный шунт; Vd/Vt — легочное мертвое пространство; CO, cardiac output — сердечный выброс; SVR — системное сосудистое сопротивление; PVR — легочное сосудистое сопротивление; PAOP — окклюзионное давление в легочной артерии; CVP — центральное венозное давление; СКФ — скорость клубочковой фильтрации.
Повышение ИАГ увеличивает внутригрудное давление путем брюшно-грудной передачи через краниальное смещение диафрагмы. Это явление создает прямое сжатие внутригрудных органов. Прямая компрессия сердца вызывает снижение сократительной способности, наполнения сердца и эластичности правого желудочка. ИАГ также приводит к нарушению венозного возврата, поскольку давление нижней полой вены увеличивается параллельно увеличению ИАГ, это отмечается даже при ИАД 10 мм рт. ст. Кроме того, отклонение диафрагмы вызывает анатомическое сужение полой вены, что приводит к дальнейшему снижению венозного возврата к сердцу и, в конечном счете, сердечного выброса. С другой стороны, сдавление легочной паренхимы приводит к сдавлению сосудистой сети, тем самым увеличивая легочное, аортальное и системное сосудистое сопротивление. Потому, несмотря на снижение венозного возврата и сердечного выброса, среднее артериальное давление остается стабильным, что делает его неточным гемодинамическим маркером.
Измерение давления на основе внутрисердечного или внутрисосудистого объема также имеет тенденцию быть недостоверным. Это объясняется тем, что, как окклюзионное давление легочной артерии (pulmonary artery occlusion pressure, PAOP), так и центральное венозное давление (central venous pressure, CVP) измеряются пропорционально барометрическому давлению, когда на самом деле эти показатели — сумма внутрисосудистого и внутригрудного давления.
Параметрами, которые более точно отражают состояние внутрисосудистого объема, являются следующие: конечный диастолический объем правого желудочка (right ventricular end-diastolic volume, RVEDV), общий конечный диастолический объем (global end-diastolic volume, GEDV) и ударный объем, поскольку они остаются незатронутыми изменениями внутригрудного давления.
Аналогичным образом повышенное ИАД передается в грудную клетку главным образом через отклонение диафрагмы, вызывающее сдавление легочной паренхимы. Паренхиматозное сжатие при ИАД 16 мм рт. ст. снижает эластичность легочной ткани на 50 %. Паренхиматозное давление также вызывает снижение емкости вдоха и функциональной остаточной емкости, в то время как пиковое инспираторное, экспираторное и среднее давление в дыхательных путях увеличиваются. В результате возникает альвеолярный ателектаз, увеличивается альвеолярное мертвое пространство, снижается легочный капиллярный кровоток, что приводит к снижению транспорта кислорода и снижению экскреции углекислого газа, а также увеличению фракции внутрилегочного шунта (Qsp/Qt) и рассогласованию вентиляции и перфузии (VQ) и, в конечном счете, к гипоксемии и гиперкапнии.
Несколько механизмов были предложены в качестве этиологии для ИАГ-индуцированной почечной дисфункции и недостаточности. Компрессия почечных артерий и вен в сочетании с компрессией почечных канальцев — вероятный механизм, лежащий в основе ИАГ/АКС-индуцированной почечной дисфункции и недостаточности, сопровождающейся снижением сердечного выброса. Различные авторы предположили, что прямое сдавление паренхимы провоцирует развитие «синдрома почечного компартмента», при котором почечный артериальный кровоток уменьшается, а почечное венозное давление и почечное сосудистое сопротивление повышается. Это приводит к тому, что кровь шунтируется от коры почек и клубочков, что приводит к нарушению функции клубочков и канальцев, вызывая ишемию почек и последующую почечную недостаточность.
При ИАД более 15 мм рт.ст. отмечается олигурия, в то время как анурия проявляется при ИАД более 30 мм рт. ст. Клинически наблюдаются изменения в функции почек, такие как снижение СКФ, повышение содержания азота мочевины в крови (BUN) и креатинина в сыворотке крови, увеличение фракционной экскреции натрия, снижение концентрации натрия и хлорида в моче и увеличение концентрации калия в моче. Однако все эти изменения, по-видимому, могут быть устранены, если ИАГ диагностируется и успешно управляется до того, как произойдет существенная дисфункция органа.
Высокое давление в брюшной полости вызывает мальперфузию кишечника из-за нарушения артериального и венозного кровотока. Было показано, что повышение ИАД на 10 мм рт. ст. снижает брыжеечный кровоток. Снижение перфузии кишечника вызывает ишемию кишечника и даже отек кишечника и кишечную непроходимость. Перфузия слизистой оболочки кишечника также нарушается, вызывая снижение рН и молочнокислый ацидоз, который в конечном итоге повреждает слизистый барьер кишечника. Потеря слизистого барьера приводит к внутрипросветной бактериальной транслокации, приводящей к сепсису или септическому шоку и последующему ухудшению исхода.
Повышенный ИАД существенно влияет на функцию печени. Прямое сжатие печени нарушает печеночный венозный и портальный кровоток. Кроме того, сужение печеночных вен на уровне диафрагмы ослабляет печеночный венозный кровоток, в то время как печеночный артериальный поток нарушается из-за снижения сердечного выброса.
На клеточном уровне микроциркуляторный кровоток также снижается, нарушая метаболизм глюкозы, вызывая увеличение производства лактата и одновременно нарушая механизм его утилизации.
Устойчивое и длительное повышение внутрибрюшного и внутригрудного давлений вызывает повышение внутричерепного давления (ВЧД) и снижение церебрального перфузионного давления (ЦПД). Bloomfield и соавторами в ходе двух различных исследований было установлено, что при повышении внутригрудного давления снижается мозговой венозный поток, что, в свою очередь, вызывает внутримозговой отек.
Раннее выявление пациентов группы риска является первым шагом в диагностике ИАГ и АКС. WSACS рекомендует проводить скрининг на ИАГ/АКС при наличии двух или более факторов риска. Рекомендация состоит в том, чтобы оценить ИАД на исходном уровне, и, если оно повышено, то ИАД необходимо продолжать контролировать каждые 4-6 часов.
Клиническое обследование, такое как пальпация и измерение окружности живота, оказалось крайне неточным и ненадежным в диагностике ИАГ и/или АКС. Радиографический ввод, такой как обычная рентгенография грудной клетки и/или живота, УЗИ брюшной полости, компьютерная томография и МРТ брюшной полости, также оказался ограниченным, поскольку результаты не являются ни чувствительными, ни специфичными для ИАГ и АКС. Тем не менее они могут продемонстрировать наличие возможной причины ИАГ, а также могут выявить воздействие ИАД (высокий уровень стояния диафрагмы, уплощение нижней полой вены, сжатие почечных вен и повышенное усиление стенки кишечника).
Когда комбинация рентгенологических данных сочетается с клинической картиной, тогда рентгенолог и врач-клиницист должны поднять вопрос о возможной ИАГ и/или АКС в качестве дифференциального диагноза.
Лучшим методом установления или исключения факта ИАГ является измерение внутрибрюшного давления. Существуют прямые и косвенные способы определения ИАД. Прямое измерение внутрибрюшного давления может быть выполнено с помощью внутрибрюшинного катетера с датчиком давления. Методы косвенного измерения включают определение любого из следующих давлений:
- давление в нижней полой вене;
- внутрижелудочное давление;
- внутрикишечное давление;
- внутриматочное давление;
- внутрипузырное давление.
В связи с положением мочевого пузыря в брюшной полости, внутрипузырный метод считается простым, точным и минимально инвазивным; следовательно, это надежный и воспроизводимый способ измерения ИАД.
При выполнении измерения, необходимо соблюдать несколько рекомендаций:
- Сообщать о ИАД в мм рт.ст. (1 мм рт. ст. = 1,36 см H2O),
- Пациент должен находиться в положении лежа на спине, чтобы избежать ложного повышения ИАД,
- Измерения должны проводиться в конце выдоха во время расслабления мышц живота,
- Датчик должен быть обнулен в середине подмышечной линии на уровне подвздошного гребня.
Необходимое оборудование
- Катетер Фолея с мочеприемником
- Система контроля давления
- Физиологический раствор изотонический с инфузионной системой.
- Кабель датчика/преобразователя
- Шприц 30 мл
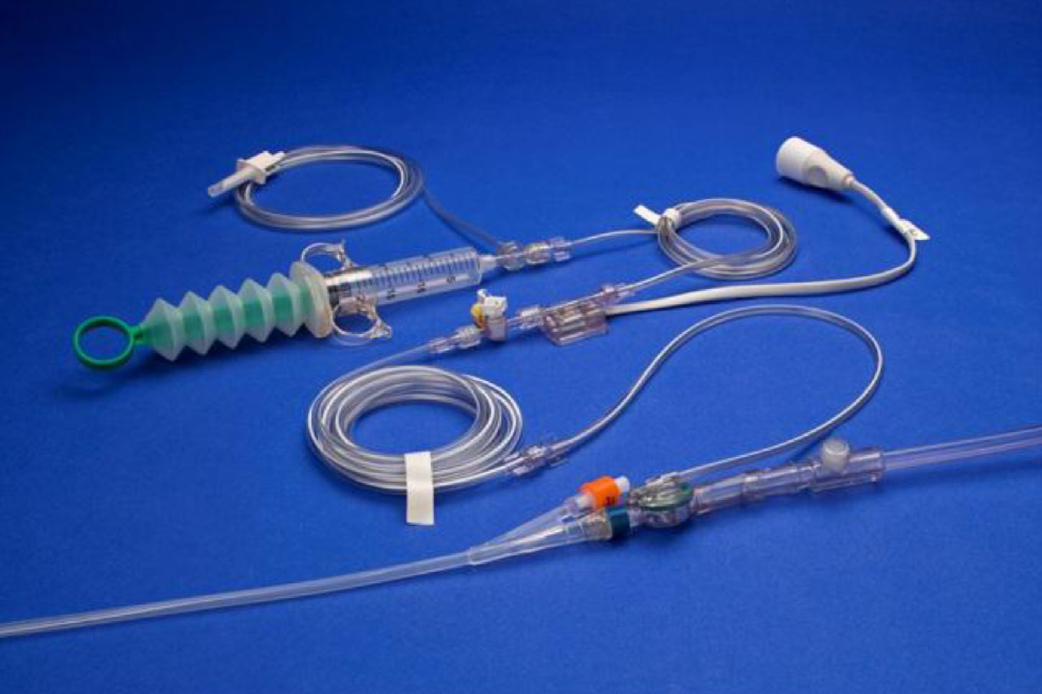
Изображение 2 | Система мониторинга ИАД ABVISER IPA
Шаги для измерения внутрипузырного давления:
- Подсоедините кабель датчика к монитору и настройте систему контроля давления.
- Расположите пациента в положении лежа на спине, чтобы избежать более высокого ИАД. Мочевой катетер устанавливается в полость мочевого пузыря.
- Отрегулируйте датчик и обнулите его так, чтобы атмосферный порт находился на уровне средней подмышечной линии, гребне подвздошной кости.
- Зафиксируйте катетер на расстоянии от порта, очистите порт спиртовым тампоном, затем подсоедините трубку датчика к порту отбора проб.
- Поверните кран на пациента и дайте шприцу заполнить максимум 25 мл по 0,9 % из пакета для внутривенного вливания.
- Поверните кран и введите 25 мл 0,9% физиологического раствора в мочевой пузырь.
- Освободите зажим на дренажной трубке для мочеиспускания, чтобы весь воздух удалялся из мочевого катетера.
- Подождите 30–60 с после установки для релаксации и стабилизации мышц детрузора мочевого пузыря.
- Измерьте ИАД в фазе выдоха, запишите показания давления на мониторе.
Установлено, что измерение ИАП имеет существенное прогностическое значение для тяжелобольных пациентов, так как ИАГ и АКС часто ассоциируются с неблагоприятными исходами. По этой причине ранняя и постоянная оценка, включая серийные измерения ИАД, должна контролироваться у любого пациента, у которого есть подозрение на ИАП/АКС.
Раннее распознавание имеет важное значение в управлении и благоприятном для пациента исходе. Необходимо понять патофизиологию ИАГ и АКС, исходить из более высокой настороженности и проверить наличие ИАГ у всех пациентов, имеющих факторы риска. В идеале хотелось бы иметь возможность диагностировать развивающийся ИАГ и АКС и вмешиваться до начала дисфункции и отказа органов и систем.
Предпочтительно, чтобы раннее терапевтическое вмешательство, будь то медицинские или хирургические попытки уменьшить ИАГ, рассматривалось как можно раньше. Руководящие принципы и рекомендации WSACS дают врачам полезное понимание ИАГ и АКС и их клинического управления для улучшения выживаемости пациентов.
Список литературы
- Meldrum D, Moore F, Franciose R, Sauaia A, Burch J. Prospective characterization and selective management of the abdominal compartment syndrome. Am J Surg . 1997;174(6):667–673. https://www.sciencedirect.com/… pii/S0 0 029610970 02018 . Accessed September 26, 2018.
- Eddy V, Nunn C, Morris J. Abdominal compartment syndrome: the Nashville experience. Surg Clin . 1997;77(4):801–812. https://www.surgical.theclinics.com/article/S0039- 6109(05)70585- 5/abstract . Accessed September 26, 2018.
- Tiwari A, Jenkins M, Amin A, Cheng K, Hamilton G. Regarding “Abdominal compartment syndrome after mesenteric revascularization. J Vasc Surg . 2002;35(4):831. https://www.jvascsurg.org/article/S0741- 5214(02)70067- 0/abstract . Ac- cessed September 26, 2018.
- Vidal, M., Weisser, J., Gonzalez, F., …MT-C care, 2008 undefined. Incidence and clinical effects of intra-abdominal hypertension in critically ill patients. https://journals.lww.com/ccmjo… 08/060 0 0/Incidence _ and _ clinical _ effects _ of _ intra _ abdominal.20.aspx . Accessed September 26, 2018.
- Holodinsky JK, Roberts DJ, Ball CG, et al. Risk factors for intra-abdominal hypertension and abdominal compartment syndrome among adult intensive care unit patients : a systematic review and meta-analysis. Crit Care . 2013;17(5):1. doi: 10.1186/cc13075.
- Hunt L, Frost SA, Hillman K, Newton PJ, Davidson PM. Management of intra-abdominal hypertension and abdominal compartment syndrome : a review. J Trauma Manag Outcomes . 2014;8(1):1–8. doi: 10.1186/1752- 2897- 8- 2 .
- Patel, A., Lall, C., …SJ-AJ of, 2007 undefined. Abdominal compartment syndrome. Am Roentgen Ray Soc . https://www. ajronline.org/doi/abs/10.2214/AJR.07.2092 . Accessed September 26, 2018.
Источник
Определения:
• Интраабдоминальное давление (ИАД): постоянное давление, имеющееся в брюшной полости. В норме в брюшной полости имеется давление в диапазоне от нуля до небольшого положительного значения. Нормальные средние значения интраабдоминального давления у здоровых собак: ≤ 10 см вод. ст. (< 7,5 мм рт. ст.). Нормальные средние значения интраабдоминального давления у здоровых кошек: ≤ 9 см вод. ст. (< 7,3 мм рт. ст.).
Примечание: значения интраабдоминального давления указывают в см вод. ст. и в мм рт. ст. Для преобразования значения, выраженного в мм рт. ст., в см вод. ст. необходимо умножить это значение на 1,34.
• Интраабдоминальная гипертензия (ИАГ): повышение ИАД выше нормального диапазона значений. Наличие абдоминальной гипертензии может приводить или не приводить к патологии (например, интраабдоминальное давление повышается во время беременности и приводит к интраабдоминальной гипертензии, но без неблагоприятных эффектов).
• Абдоминальный компартмент-синдром (АКС): стойкое повышение ИАД, которое приводит к дисфункции/недостаточности органов. Это тяжелое состояние!
Введение
Увеличение содержимого брюшной полости является фактором риска для развития ИАГ, и АКС можно рассматривать как конечную стадию ИАГ, которая может быть фатальной. Хотя животных использовали в моделях ИАГ, распространенность этого состояния у ветеринарных пациентов в критическом состоянии не исследована, и оно может быть упущено из виду врачом.
Патофизиология
Хотя факторы, способствующие развитию ИАГ и АКС у людей, могут отличаться от таковых у животных, конечный результат АКС, по-видимому, одинаков у различных видов.
В тяжелых случаях повышенное интраабдоминальное давление может приводить к нарушению не только регионального кровотока, но и перфузии тканей; если оставить это состояние без лечения, оно может стать причиной системной воспалительной реакции и последующей мультиорганной недостаточности. ИАГ и АКС поражают многие системы органов как внутри, так и вне брюшной полости. Отек стенки кишечника, который вносит основной вклад в ИАГ у людей, может развиваться из-за снижения лимфооттока и капиллярной утечки. Повреждение стенки кишечника может предрасполагать пациентов к бактериальной транслокации и повышению продукции медиаторов воспаления. У людей отек стенки кишечника усиливается в случае агрессивной/реанимационной инфузионной терапии. К счастью, у мелких животных отек стенки кишечника после агрессивной инфузионной терапии возникает редко. При повышении интраабдоминального давления может нарушаться кровоснабжение печени, что может способствовать острой печеночной недостаточности. Олигурия и анурия являются хорошо известными последствиями АКС и могут возникать из-за прямой компрессии собирательных протоков почек или нарушения кровоснабжения почек из-за компрессии почечных сосудов. АКС может приводить к компрессии абдоминальной каудальной полой вены, что способствует уменьшению сердечного выброса вследствие снижения венозного возврата и преднагрузки (ПН). При повышении интраабдоминального давления возможно повышенное давление на диафрагму, способное привести к возрастающему усилию при дыхании и сочетанному повышению интраторакального давления; это может снижать податливость левого желудочка и способствовать уменьшению сердечного выброса. Переданное повышение интраторакального давления может привести к компрессии краниальной полой вены и снижению церебрального венозного оттока, повышению внутричерепного давления и снижению церебрального перфузионного давления (ЦПД). Хотя эффекты повышенного интраабдоминального давления могут быть безвредными для здоровых людей (например, во время беременности), у пациентов в критическом состоянии с предсуществующими заболеваниями или у пациентов, уже находящихся в группе риска органной недостаточности, АКС может играть значительную роль, способствуя органной недостаточности за счет повреждения в соответствии с «теорией множественных поражений».
Факторы риска
Аналогично тому, что ИАГ и АКС могут влиять на органы, расположенные внутри и вне брюшной полости, факторы, способствующие развитию ИАГ и АКС, могут возникать внутри (первичные) и вне (вторичные) брюшной полости. Первичные причины включают увеличение содержимого брюшной полости (органомегалия, кровотечение, асцит, опухоли, общий гнойный перитонит и т.п.), увеличение содержимого полых органов (содержимого желудка, дилатация/заворот кишечника, пиометра и т.п.) и снижение податливости брюшной стенки (резекция больших участков брюшной стенки во время хирургических операций, шинирование или наложение абдоминальных повязок).
Методы измерения интраабдоминального давления (ИАД)
ИАД можно измерять непрерывно или периодически прямыми или непрямыми методами.
У людей «золотым стандартом» для измерения ИАД является прямое измерение интраабдоминального давления посредством прикрепления датчика давления или водяного манометра к катетеру, конец которого расположен в перитонеальной полости. Разработано много приборов для этого метода, хотя он редко используется в клинике, поскольку доказана надежность других, более дешевых и менее инвазивных методов, сопровождающихся меньшим количеством осложнений.
Наиболее распространенным методом, используемым в ветеринарной медицине, является трансвезикулярное измерение давления посредством размещения мочевого катетера. Техника проведения данного измерения сводится к следующему: после установки постоянного катетера (используется стерильная техника) мочевой пузырь полностью опорожняют с помощью шприца, соединенного с 3-канальным запорным краном; шприц удаляют, а 3-канальный запорный кран соединяют с мешком, содержащим 250 мл 0,9%-ного раствора хлорида натрия, и водяным манометром. Во время всей процедуры следует соблюдать стерильность. Водяной манометр фиксируют на уровне лобкового симфиза, при этом пациент лежит на левом или правом боку. Затем в мочевой пузырь вводят объем 0,9%-ного раствора хлорида натрия, равный 1,0 мл/кг, открывая запорный кран между мешком с солевым раствором и мочевым катетером. После этого манометр заполняют 0,9%-ным раствором хлорида натрия, открывая запорный кран между мешком с солевым раствором и водяным манометром. В заключение открывают запорный кран между водяным манометром и мочевым катетером и обеспечивают измерение ИАД как разности между нулевым уровнем и мениском жидкости в манометре.
Животное должно быть спокойным и расслабленным, поскольку измерения ИАД, производимые в момент, когда животное вырывается и/или испытывает боль, могут привести к повышенным значением ИАД. Поэтому измерения следует производить после введения животному анксиолитиков и анальгетиков. Кашель и рвота также могут влиять на ИАД, и если эти события произошли во время измерения, то его следует повторить. Известно, что ожирение повышает ИАД у людей, и проведенное ранее ветеринарное исследование документировало прогрессивное повышение ИАД с увеличением балльной оценки упитанности (BCS) у кошек. С учетом этих результатов может быть полезным вмешательство при меньших уровнях ИАГ у животных с избыточной массой тела или ожирением из-за потенциальной вероятности уже имеющейся дисфункции органов. Инстилляция слишком большого объема солевого раствора может привести к сокращению детрузора и ложно повышенным значениям ИАД. Это было показано у собак при введении объемов, равных всего 2 мл/кг. Поэтому рекомендуется инстиллировать в мочевой пузырь всего 1 мл/кг после его полного опорожнения. Положение тела влияет на измерения ИАД, поскольку органы смещаются в брюшной полости в зависимости от положения тела, что может повлиять на давление в мочевом пузыре. Большинство измерений ИАД у собак и кошек проводят в положении лежа на боку.
Наконец, существуют колебания показаний, полученных через короткие промежутки времени, что подчеркивает важность анализа тенденций изменения значений ИАД, а не измерения отдельных значений. Было предложено производить измерения непрерывно или по меньшей мере через каждые 4 часа.
Рекомендации
Для людей имеются четкие рекомендации, сформулированные Всемирным обществом абдоминального компартмент-синдрома (WSACS), в которых определены ИАД, ИАГ и АКС. У людей ИАГ определена как ИАД, превышающее 12 мм рт. ст., тогда как АКС существует, если ИАД устойчиво держится на уровнях, превышающих 20 мм рт. ст., при наличии признаков впервые выявленной дисфункции органов.
Были даны рекомендации по определению нормальных значений ИАД и ИАГ у собак. ИАД в диапазоне от 0 до 10 см вод. ст. следует считать нормальным; ИАД в диапазоне от 10 до 20 см вод. ст. соответствует легкой ИАГ, тогда как ИАД в диапазоне от 20 до 35 см вод. ст. соответствует ИАГ средней тяжести или тяжелой ИАГ, а значения, превышающие 35 см вод. ст., означают тяжелую ИАГ. Менее четкими являются рекомендации для кошек: в одном исследовании был определен нормальный диапазон от 0 до 9 см вод. ст. у седированных кошек и от 0 до 18 см вод. ст. у бодрствующих кошек. Специфическая система градации ИАГ для кошек еще не разработана, однако существует вероятность того, что для них может быть пригодна система, сходная с системой, предложенной для собак.
Лечение
Декомпрессионная абдоминальная хирургическая операция рекомендована в качестве способа лечения абдоминального компартмент-синдрома у людей, если интраабдоминальное давление превышает 20 мм рт. ст. (26,7 см вод. ст.). Это часто связано с манипуляциями в открытой брюшной полости и нередко является следствием выраженного отека кишечника, обусловленного агрессивной инфузионной терапией. У ветеринарных пациентов нет четких рекомендаций, указывающих, когда нужно начинать лечение ИАГ, и, по-видимому, этот момент будет разным в зависимости от первопричины. Пациентам, не имеющим симптомов, может не потребоваться вмешательство, хотя их состояние следует тщательно контролировать. У пациентов с основными заболеваниями, требующими хирургической коррекции (кишечная непроходимость, пиометра, сепсис), в кратчайшие сроки должна быть выполнена хирургическая операция, обеспечивающая декомпрессию брюшной полости после устранения исходной причины. В случае асцита без других четких показаний к хирургической операции следует проанализировать возможность абдоминоцентеза для удаления жидкости и снижения интраабдоминального давления у следующих групп пациентов:
– со средней или тяжелой ИАГ;
– с сопутствующим отеком мозга/повышенным внутричерепным давлением;
– с повышенным дыхательным усилием;
– с признаками недостаточности/нарушения функций органов.
Источник
