Впс единственный желудочек код мкб

Врожденные пороки сердца – аномалии его строения, формирующиеся еще во внутриутробном периоде.
 Врожденным пороком сердца называют дефект в строении миокарда или его крупных сосудов, формирующийся внутриутробно.
Врожденным пороком сердца называют дефект в строении миокарда или его крупных сосудов, формирующийся внутриутробно.
Большинство врожденных пороков сердца приводят к грубым нарушениям кровотока внутри этого органа или по большому и/или малому кругам кровообращения.
↯
Больше статей в журнале
«Заместитель главного врача»
Активировать доступ
Из рекомендации вы узнаете
Рассмотрим понятие и классификацию ВПС по МКБ-10, опишем причины их развития, симптомы, методы диагностики и лечения, а также возможные осложнения и прогноз.
Классификация МКБ 10 ВПС
- Q20 Врожденные аномалии [пороки развития] сердечных камер и соединений: коды болезней по МКБ-10
- Q21 Врожденные аномалии [пороки развития] сердечной перегородки: классификация по МКБ-10
- Q22 Врожденные аномалии [пороки развития] легочного и трехстворчатого клапанов: коды болезней по МКБ-10
- Q23 Врожденные аномалии [пороки развития] аортального и митрального клапанов: коды болезней по МКБ-10
- Q24 Другие врожденные аномалии [пороки развития] сердца: классификация по МКБ-10
- Q25 Врожденные аномалии [пороки развития] крупных артерий: классификация по МКБ-10
- Q26 Врожденные аномалии [пороки развития] крупных вен: классификация по МКБ-10
- Q27 Другие врожденные аномалии [пороки развития] системы периферических сосудов: коды болезней по МКБ-10
- Q28 Другие врожденные аномалии [пороки развития] системы кровообращения: коды болезней по МКБ-10
Причины врожденных пороков сердца
Классификация врождённых пороков сердца выделяет наследственные и ненаследственные причины их возникновения.
К ненаследственным факторам относятся различные внешние отрицательные воздействия, а также факторы, напрямую относящиеся к состоянию здоровья матери. Однако часто бывает, что в формировании ВПС участвуют обе эти группы факторов одновременно.
Кроме того, врожденные пороки могут сочетаться с другими дефектами развития – например, аномалиями лицевого скелета, внутренних органов, рук и ног, нарушениями развития и роста плода.
Дополнительным фактором риска развития врожденного порока сердца (код по МКБ-10 – Q20-Q26) является недоношенность. Так, среди новорожденных с диагностированными пороками сердца доля недоношенных детей превышает долю здоровых младенцев в два раза.
Риск ВПС гораздо выше у младенцев, появившихся на свет в результате спонтанных преждевременных родов. Этот риск высок, в первую очередь, в отношении сердечных аномалий, после исключения хромосомных патологий и множественных дефектов внутриутробного развития.
Скорее всего, это связано с воздействием различных тератогенных факторов, основную роль среди которых играют внутриутробные инфекции, которые считаются также одной из главных причин начала преждевременной родовой деятельности.
Современные методы генетических исследований при ВПС
Врожденный порок сердца (код по МКБ 10 ВПС- Q20-Q26) очень часто является лишь одним из отклонений в развитии плода и, как правило, сочетается с дефектами строения лицевого скелета, рук и/или ног, аномалиями строения внутренних органов и систем.
На сегодняшний день существует ряд генетических исследований, позволяющих выявить ВПС у детей.
К ним относятся:
- цитогенетические исследования;
- флуоресцентная гибридизация in situ;
- ДНК-анализ на предмет выявления генетических мутаций.
Ненаследственные факторы риска ВПС
Доказано, что многие негативные воздействия в период беременности способны повышать риск развития врожденного порока сердца (код по МКБ-10 — Q20-Q26) у плода.
Однако сведений о факторах ненаследственного риска, на основании которых возможна профилактика данной патологии, не так много. В первую очередь речь идет о заболеваниях беременной женщины.
Фенилкетонурия
Данное заболевание при недостаточном контроле резко (до 6 раз) повышает риски возникновения врожденных пороков сердца у плода.
Речь идет о таких дефектах, как тетрада Фалло, дефекты межжелудочковой перегородки, открытый артериальный проток, единый желудочек сердца. При соблюдении диеты и ограничений в питании в период зачатия и беременности этот риск можно значительно снизить.
Прегестационный диабет
ВПС (МКБ-10, код Q20-Q26) могут возникнуть в результате прегестационного или, реже, гестационного диабета у матери.
Речь идет о таких дефектах, как:
- Дефекты латерализации.
- Транспозиции магистральных сосудов.
- Открытый антриовентрикулярный канал.
- Дефекты межжелудочковой перегородки.
- Синдром гипоплазии левых отделов сердца.
- Конотрункальные дефекты.
- Дефекты путей оттока.
- Открытый артериальный проток.
- Различные кардиомиопатии.
При диабете у матери ВПС формируются до 7 недели гестации. Доказана связь между постоянным контролем уровня глюкозы в крови во время закладки органов плода и врожденными пороками сердца.
Строгий гликемический контроль в период зачатия и во время беременности позволяет снизить риски развития ВПС, однако достичь и поддерживать эугликемию на ранних сроках вынашивания ребенка достаточно сложно, так как большая часть женщин, страдающих сахарным диабетом, не планируют заранее свое материнство и не контролируют уровень глюкозы в крови перед зачатием.
Диабет у матери существенно повышает риск развития врожденного порока сердца у ребенка, поэтому важно хорошо понимать реальное влияние этого ненаследственного фактора на аномалии развития плода.
В статье вы найдете только несколько готовых образцов и шаблонов.
В Системе «Консилиум» их более 5000.
Успеете скачать всё, что нужно, по демодоступу за 3 дня?
Активировать
Краснуха
Женщинам во время подготовки к беременности рекомендуется вакцинация против краснухи, так как данное заболевание в период вынашивания ребенка (тем более на ранних сроках) является абсолютным показанием к прерыванию.
Вирус краснухи проникает через плацентарный барьер и оказывает тератогенное воздействие на эмбрион и плод, провоцируя множественные грубые пороки развития, в том числе и пороки развития сердца, несовместимые с жизнью.
Развернуть клиническую рекомендацию «Тетрада Фалло»
Симптомы врожденных пороков сердца
Симптомы ВПС (код по МКБ-10 — Q20-Q26), которые требуют неотложного врачебного вмешательства:
- синюшный, серый или бледный оттенок кожи;
- отсутствие или резкое ослабление пульса;
- снижение артериального давления на ногах на 10 мм рт.ст и больше по сравнению с правой рукой;
- снижение сатурации или насыщение крови кислородом на правой руке выше на 5% и более по сравнению с ногой;
- одышка – более 60 в минуту;
- ЧСС более 180 или менее 100 ударов в минуту, сердечная аритмия;
- гепатомегалия;
- олигурия у новорожденных;
- шумы в сердце (наименее специфический симптом).
Диагностика критического ВПС
Порок сердца, который сопровождается развитием жизнеугрожающих состояний в первые часы или сутки после появления ребенка на свет, называются критическими.
Без соответствующего хирургического лечения они приводят к смерти в первые месяцы жизни ребенка.
Пороки сердца делятся на «синие» и «белые». К первым, проявляющимся цианозом кожных покровов, относятся:
- тетрада Фалло;
- различные атрезии (легочной артерии, трехстворчатого клапана и др.).
К «белым» порокам развития относятся:
- гипоплазия левых отделов миокарда;
- транспозиция магистральных сосудов;
- общий артериальный ствол;
- выраженный стеноз легочной артерии;
- полный аномальный дренаж легочных вен;
- резкая коарктация аорты;
- критический стеноз клапанов аорты.
Диагноз «критический ВПС» ставится в родильном доме в первые часы жизни младенца. Ребенок с такой патологией требует немедленной госпитализации в кардиохирургический центр, а скорейшее оперативное вмешательство позволит сохранить ему жизнь, в то время как поздняя диагностика и отсутствие хирургического лечения приводят к гибели ребенка еще в периоде новорожденности.
Причины неустановленного диагноза или позднего диагностирования ВПС:
- Патологии плода, ВСП не выявлен в ходе проявления скрининга в период беременности или информация об этом отсутствует.
- Некорректная оценка состояния новорожденного.
- Ориентир на отсутствие шумов в сердце, которым могут отсутствовать даже при самых грубых врожденных пороках сердца.
- Неверная оценка показателей сатурации кислорода в крови у новорожденного.
- Отсутствие повторного осмотра младенца через несколько часов после рождения.
- Отсутствие проведения ЭХО-КГ-скрининга в роддоме.
- Врачебные ошибки, отсутствие у врача ультразвуковой диагностики навыков проведения ЭХО-КГ-скрининга.
Нужно помнить, что в подавляющем числе случаев не диагностированный вовремя врожденный порок сердца приводит к летальному исходу.
Клинические рекомендации по врожденным порокам сердца описывают алгоритм оценки состояния новорожденного для того, чтобы не пропустить опасную для жизни патологию.
Он включает в себя:
- оценку оттенка кожи;
- оценку пульса на периферических артериях;
- измерение артериального давления на правой руке и любой ноге (одновременно);
- аускультацию легких и сердца;
- оценка локализации сердца в грудной, а печени — в брюшной полости;
- оценка наличия синдромальной патологии или других ВПР.
Для того, чтобы избежать несвоевременной постановки диагноза, нужно помнить, что многие критические пороки сердца афоничны, то есть не дают шумов в этом органе. Иными словами, отсутствие шумов не гарантирует того, что пороков нет, а их наличие необязательно говорит о врожденном пороке сердца.
В то же время многие их них являются дуктус-зависимыми, когда открытый артериальный проток (ОАП) представляет собой единственный источник поступления крови в легочную артерию или аорту.
Закрытие дуктуса в этих случаях значительно ухудшает состояние пациента, часто приводя к летальному исходу. Для поддержания функции открытого артериального протока пациенту инфузионно вводится вазопростан.
При гипоплазии левых отделов сердца, транспозиции магистральных сосудов, атрезии легочной артерии категорически противопоказана кислородотерапия. Очень важно при критических ВПС обеспечить необходимый объем циркулирующей крови в соответствии с потребностями младенца.
В свою очередь, рождение ребенка с трисомией (синдром Дауна, Эдвардса и др.), другими синдромальными патологиями и множественными пороками развития требует тщательного обследования на предмет врожденной кардиопатологии, так как их вероятность при данных заболеваниях очень высока.

Лечение врожденных пороков сердца
Врожденные пороки сердца лечатся хирургическими или (реже) консервативными методами. Новорожденным детям с грубыми ВПС показаны операции на сухом сердце в условиях гипотермии, проводимые в специальных клиниках кардиологического профиля.
Нередко сначала проводится паллиативное вмешательство, позволяющее добиться относительной компенсации порока, после чего проводится радикальная коррекция дефекта.
Консервативное лечение включает в себя несколько этапов:
- при острой декомпенсации;
- при гипоксемических кризах;
- при септических осложнениях;
- при осложнениях иного характера.
В вышеперечисленных случаях ребенок проходит терапевтический курс в специализированном стационаре, а долечивание показано в санаторно-курортном учреждении кардиологического профиля.
Такие больные находятся на диспансерном учете у врача-ревматолога, назначающего поддерживающее лечение.
Также консервативная терапия показана в период подготовки к операции и реабилитации после нее.
Больным показан:
- постельный режим;
- умеренная физическая нагрузка;
- полноценный рацион, дробные приемы пищи;
- кислородотерапия – при явных признаках кислородного голодания.
Стандарты специализированной медпомощи при врожденных аномалиях, пороках развития сердечной перегородки, скачайте в Системе Консилиум
Лекарственная терапия включает в себя прием следующих препаратов:
- Аспаркам, панагин, рибоксин, кокарбоксилаза, витамин В – улучшают обменные процессы в тканях сердца.
- Ксантинола никотинат, витамин Е – улучшают микроциркуляцию и реологические свойства крови.
- Бета-адреноблокаторы – предупреждают гипоксические кризы, выступают в качестве стабилизаторов мембраны при различных нарушениях сердечного ритма.
- Диуретики, сердечные гликозиды – показаны при острой и подострой сердечной недостаточности.
В кардиологическом стационаре пациента наблюдают ревматолог и кардиохирург. Все очаги хронической инфекции перед операцией должны быть санированы – все подобные манипуляции (включая удаление зубов) проводятся под прикрытием антимикробных препаратов.
Хирургическое лечение ВПС показано при неэффективности или невозможности консервативной терапии. У детей в большинстве случаев показана именно операция.
Очень распространена ранняя коррекция пороков сердца, однако некоторые негрубые дефекты (такие, например, как низко расположенный дефект межжелудочковой перегородки) не требуют оперативного лечения, а открытый артериальный проток и некоторые дефекты перегородок исчезают по мере взросления ребенка.
Операции проводятся тогда, когда порок находится в стадии относительной компенсации. Сегодня распространены не только большие операции на открытом сердце в условиях гипотермии, но и щадящие методики, которые могут быть достойной альтернативной масштабным полостным операциям.
Осложнения
Возможны следующие осложнения ВПС (код по МКБ-10 — Q20-Q26):
- Задержка роста и развития, трудности в учебной деятельности.
- Аритмии.
- Хроническая сердечная недостаточность.
- Инфаркт, инсульт.
- Эндокардит, миокардит – бактериальные поражения сердца.
- Эмоциональные проблемы, депрессивные расстройства.
Часто врожденные пороки сердца требует пожизненного наблюдения у врача-кардиолога, а также особого отношения к своему здоровью и лечению любых сопутствующих болезней.
Прогноз
Врожденные пороки сердца – одна из основных причин инвалидности детей раннего возраста.
Однако при своевременно установленном диагнозе и скорейшем квалифицированном оперативном лечении прогноз является благоприятным, а смертность не превышает 2%.
При сложных комбинированных пороках развития сердца и сосудов (к ним относится, например, тетрада Фалло) летальность достигает 25%, но даже в этом случае своевременное поэтапное хирургическое вмешательство по абсолютным показаниям дает ребенку шанс полноценно развиваться и вести обычную жизнь.
Материал проверен экспертами Актион Медицина
Источник
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Дополнительные факты
- Причины
- Классификация
- Симптомы
- Диагностика
- Дифференциальная диагностика
- Лечение
- Течение и стадии
- Прогноз
- Основные медицинские услуги
- Клиники для лечения
Названия
Q21,0 Дефект межжелудочковой перегородки.
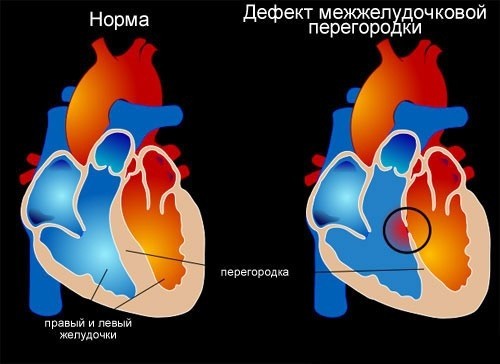
Наличие дефекта между правым и левым желудочками сердца.
Описание
Дефект межжелудочковой перегородки. Врожденная внутрисердечная аномалия, характеризующаяся наличием сообщения между правым и левым желудочками. Дефект межжелудочковой перегородки проявляется одышкой, отставанием в физическом развитии, быстрой утомляемостью, учащенным сердцебиением, наличием «сердечного горба». Инструментальная диагностика дефекта межжелудочковой перегородки включает проведение ЭКГ, ЭхоКГ, рентгенографии органов грудной клетки, вентрикулографии, аортографии, катетеризации камер сердца, МРТ. При дефектах межжелудочковой перегородки проводят радикальные (закрытие дефекта) и паллиативные (сужение легочной артерии) вмешательства.
Дополнительные факты
Дефект межжелудочковой перегородки (ДМЖП) – отверстие в перегородке, разделяющей полости левого и правого желудочка, наличие которого приводит к патологическому шунтированию крови. В кардиологии дефект межжелудочковой перегородки – наиболее часто встречающийся врожденный порок сердца (9–25% от всех ВПС). Частота критических состояний при дефекте межжелудочковой перегородки составляет около 21%. С одинаковой частотой порок обнаруживается у новорожденных мальчиков и девочек.
Дефект межжелудочковой перегородки может быть единственной внутрисердечной аномалией (изолированный ДМЖП) или входить в структуру сложных пороков (тетрады Фалло, общего артериального ствола, транспозиции магистральных сосудов, атрезии трехстворчатого клапана и тд ). В ряде случаев межжелудочковая перегородка может отсутствовать полностью — такое состояние характеризуется как единственный желудочек сердца.
Особенности гемодинамики при дефекте межжелудочковой перегородки.
Межжелудочковая перегородка образует внутренние стенки обоих желудочков и составляет примерно 1/3 площади каждого из них. Межжелудочковая перегородка представлена мембранозным и мышечным компонентами. В свою очередь, мышечный отдел состоит из 3-х частей — приточной, трабекулярной и отточной (инфундибулярной).
Межжелудочковая перегородка, наряду с другими стенками желудочков, принимает участие в сокращении и расслаблении сердца. У плода она полностью формируется к 4-5-ой неделе эмбрионального развития. Если этого по каким-либо причинам не происходит, в межжелудочковой перегородке остается дефект. Нарушения гемодинамики при дефекте межжелудочковой перегородки обусловлены сообщением левого желудочка с высоким давлением и правого желудочка с низким давлением (в норме в период систолы давление в левом желудочке в 4 — 5 раз выше, чем в правом).
После рождения и установления кровотока в большом и малом кругах кровообращения из-за дефекта межжелудочковой перегородки возникает лево-правый сброс крови, объем которого зависит от размеров отверстия. При небольшом объеме шунтируемой крови давление в правом желудочке и легочных артериях остается нормальным либо незначительно повышается. Однако при большом поступлении крови через дефект в малый круг кровообращения и ее возврате в левые отделы сердца, развивается объемная и систолическая перегрузка желудочков.
Значительное повышение давления в малом круге кровообращения при больших дефектах межжелудочковой перегородки способствует возникновению легочной гипертензии. Повышение легочно-сосудистого сопротивления взывает развитие сброса крови из правого желудочка в левый (обратного или перекрестного шунтирования), что приводит к артериальной гипоксемии (синдром Эйзенменгера).
Многолетняя практика кардиохиругов показывает, что наилучших результатов закрытия дефекта межжелудочковой перегородки можно добиться при сбросе крови слева направо. Поэтому при планировании операции тщательно учитываются гемодинамические параметры (давление, сопротивление и объем сброса).
Причины
Чаще всего дефект межжелудочковой перегородки является следствием нарушения эмбрионального развития и формируется у плода при нарушениях закладки органов. Поэтому дефекту межжелудочковой перегородки часто сопутствуют другие сердечные пороки: открытый артериальный проток (20%), дефект межпредсердной перегородки (20%), коарктация аорты (12%), стеноз устья аорты (5%), аортальная недостаточность (2,5—4,5%), недостаточность митрального клапана (2%), реже — аномальный дренаж легочных вен, стеноз легочной артерии и тд.
В 25-50% случаев дефект межжелудочковой перегородки сочетается с пороками развития внесердечной локализации — болезнью Дауна, аномалиями развития почек, расщелиной твердого неба и заячьей губой.
Непосредственными факторами, вызывающими нарушение эмбриогенеза, выступают вредные воздействия на плод в I триместре гестации: заболевания беременной (вирусные инфекции, эндокринные нарушения), алкогольная и лекарственная интоксикации, ионизирующая радиация, патологическое течение беременности (выраженные токсикозы, угроза самопроизвольного прерывания беременности и пр. ). Имеются данные о наследственной этиологии дефекта межжелудочковой перегородки. Приобретенные дефекты межжелудочковой перегородки могут являться осложнением инфаркта миокарда.
Классификация
Размер дефекта межжелудочковой перегородки оценивается, исходя из его абсолютной величины и сопоставления с диаметром аортального отверстия: маленький дефект составляет 1-3 мм (болезнь Толочинова–Роже), средний – равен примерно 1/2 диаметра аортального отверстия, большой – равен или превышает его диаметр.
С учетом анатомического расположения дефекта выделяют:
• перимембранозные дефекты межжелудочковой перегородки — 75% (приточные, трабекулярные, инфундибулярные) расположены в верхней части перегородки под аортальным клапаном, могут закрываться самопроизвольно;
• мышечные дефекты межжелудочковой перегородки – 10% (приточные, трабекулярные) — расположены в мышечном отделе перегородки, на значительном удалении от клапанной и проводящей систем;
• надгребневые дефекты межжелудочковой перегородки — 5% — расположены выше наджелудочкового гребня (мышечного пучка, отделяющего полость правого желудочка от его выносящего тракта), самопроизвольно не закрываются.
Симптомы
Клинические проявления больших и малых изолированных дефектов межжелудочковой перегородки различны. Малые дефекты межжелудочковой перегородки (болезнь Толочинова—Роже) имеют диаметр менее 1 см и встречаются в 25-40% от числа всех ДМЖП. Проявляются нерезко выраженной утомляемостью и одышкой при нагрузке. Физическое развитие детей, как правило, не нарушено. Иногда у них определяется слабо выраженное куполообразное выпячивание грудной клетки в области сердца — «сердечный горб». Характерным клиническим признаком малых дефектов межжелудочковой перегородки служит аускультативно выявляемое наличие грубого систолического шума над областью сердца, который фиксируется уже на первой неделе жизни.
Большие дефекты межжелудочковой перегородки, имеющие размеры более 1/2 диаметра устья аорты или более 1 см, проявляются симптоматически уже в первые 3 месяца жизни новорожденных, приводя в 25-30% случаев к развитию критического состояния. При больших дефектах межжелудочковой перегородки отмечается гипотрофия, одышка при физической нагрузке или в покое, повышенная утомляемость. Характерны затруднения при кормлении: прерывистое сосание, частые отрывы от груди, одышка и бледность, потливость, пероральный цианоз. В анамнезе у большинства детей с дефектом межжелудочковой перегородки — частые респираторные инфекции, затяжные и рецидивирующие бронхиты и пневмонии.
В возрасте 3-4-лет, по мере нарастания сердечной недостаточности, у таких детей появляются жалобы на сердцебиение и боли в области сердца, склонность к носовым кровотечениям и обморокам. Транзиторный цианоз сменяется постоянным пероральным и акроцианозом; беспокоит постоянная одышка в покое, ортопноэ, кашель (синдром Эйзенменгера). На наличие хронической гипоксии указывают деформация фаланг пальцев и ногтей («барабанные палочки», «часовые стекла»).
Диагностика
К методам инструментальной диагностики дефекта межжелудочковой перегородки относятся ЭКГ, ФКГ, рентгенография грудной клетки, ЭхоКС, катетеризация камер сердца, ангиокардиография, вентрикулография.
Электрокардиограмма при дефекте межжелудочковой перегородки отражает перегрузку желудочков, наличие и степень выраженности легочной гипертензии. У взрослых больных могут регистрироваться аритмии (экстрасистолия, мерцание предсердий), нарушения проводимости (блокада правой ножки пучка Гиса, синдром WPW). Фонокардиография фиксирует высокочастотный систолический шум с максимумом в III-IV межреберье слева от грудины.
Эхокардиография позволяет выявить дефект межжелудочковой перегородки или заподозрить его по характерным нарушениям гемодинамики. Рентгенография органов грудной клетки при больших дефектах межжелудочковой перегородки обнаруживает усиление легочного рисунка, усиленную пульсацию корней легких, увеличение размеров сердца. Зондирование правых полостей сердца выявляет повышение давления в легочной артерии и правом желудочке, возможность проведения катетера в аорту, повышенную оксигенацию венозной крови в правом желудочке. Аортография проводится для исключения сопутствующих ВПС.
Дифференциальная диагностика
Дифференциальная диагностика дефекта межжелудочковой перегородки проводится с открытым атриовентрикулярным каналом, общим артериальным стволом, дефектом аортолегочной перегородки, изолированным стенозом легочной артерии, стенозом аорты, врожденной митральной недостаточностью, тромбоэмболией.
Лечение
Асимптомное течение дефекта межелудочковой перегородки при его небольших размерах позволяет воздержаться от хирургического вмешательства и осуществлять динамическое наблюдение за ребенком. В ряде случаев возможно спонтанное закрытие дефекта межжелудочковой перегородки к 1-4 годам жизни или в более позднем возрасте. В остальных случаях показано хирургическое закрытие дефекта межжелудочковой перегородки, как правило, после достижения ребенком 3-х лет.
При развитии сердечной недостаточности и легочной гипертензии проводится консервативное лечение с помощью сердечных гликозидов, мочегонных препаратов, ингибиторов ангиотензинпревращающего фермента, кардиотрофиков, антиоксидантов.
Кардиохирургическое лечение дефекта межжелудочковой перегородки может быть радикальным и паллиативным. К радикальным операциям относятся ушивание малых дефектов межжелудочковой перегородки П-образными швами; пластика больших дефектов синтетической (тефлон, дакрон и тд ) заплатой или биологической (консервированный ксеноперикард, аутоперикард) тканью; рентгенэндоваскулярная окклюзия дефекта межжелудочковой перегородки.
У грудных детей с выраженной гипотрофией, большим лево-правым шунтированием крови и множественными дефектами предпочтение отдается паллиативной операции, направленной на создание искусственного стеноза легочной артерии с помощью манжетки. Данный этап позволяет подготовить ребенка к радикальной операции по устранению дефекта межжелудочковой перегородки в более старшем возрасте.
Течение и стадии
Женщины с небольшим дефектом межжелудочковой перегородки, как правило, в состоянии нормально выносить и родить ребенка. Однако, при больших размерах дефекта, аритмии, сердечной недостаточности или легочной гипертензии риск осложнений во время беременности значительно повышается. Наличие синдрома Эйзенменгера является показанием для искусственного прерывания беременности. У женщин с дефектом межжелудочковой перегородки имеется повышенная вероятность рождения ребенка с аналогичным или другим врожденным пороком сердца.
Перед планированием беременности пациентке с пороком сердца (оперированным или нет) необходимо проконсультироваться с акушером-гинекологом, кардиологом, генетиком. Ведение беременности у категории женщин с дефектом межжелудочковой перегородки требует повышенного внимания.
Прогноз
Естественное течение дефекта межжелудочковой перегородки в целом не позволяет надеяться на благоприятный прогноз. Продолжительность жизни при данном пороке зависит от величины дефекта и составляет в среднем около 25 лет. При больших и средних дефектах 50-80% детей умирают в возрасте до 6 мес. Или 1 года от сердечной недостаточности, застойной пневмонии, бактериального эндокардита, нарушений ритма сердца, тромбоэмболических осложнений.
В редких случаях ДМЖП не оказывает существенного влияния на продолжительность и качество жизни. Спонтанное закрытие дефекта межжелудочковой перегородки наблюдается в 25-40% случаев, преимущественно при его малом размере. Однако даже в этом случае больные должны находиться под наблюдением кардиолога в связи с возможными осложнениями со стороны проводящей системы сердца и высоким риском возникновения инфекционного эндокардита.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
