Волчаночный нефрит с нефротическим синдромом

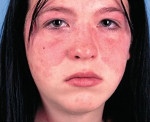
Волчаночный нефрит — это деструкция гломерулярного аппарата почек вследствие аутоиммунного воспаления при системной красной волчанке. Проявляется отеками, уменьшением диуреза, макрогематурией, повышением АД, нарастающей интоксикацией, которые обычно усугубляют основную симптоматику СКВ, реже являются самостоятельными симптомами волчанки. Диагностируется с помощью общего анализа мочи, определения уровней сывороточного креатинина, аутоантител, волчаночного антикоагулянта, пункционной биопсии почек с гистологическим исследованием биоптата. Для лечения применяют цитостатики, кортикостероиды, ингибиторы рецепторов ангиотензина, проводят ЗПТ, трансплантацию почки.
Общие сведения
Клинические признаки волчаночного гломерулонефрита определяются почти у половины больных с установленным диагнозом СКВ. Судя по результатам биопсий, распространенность почечной патологии при волчанке может превышать 90%. Заболевание одинаково часто поражает женщин и мужчин, страдающих волчанкой, однако у пациентов мужского пола волчаночный нефрит отличается более ранним началом, тяжелым и агрессивным течением. При возникновении в возрасте старше 40 лет гломерулонефрит имеет меньшую активность и протекает благоприятнее. Актуальность своевременной диагностики нефрологической патологии у больных СКВ обусловлена ухудшением общего прогноза при аутоиммунном поражении почек. Активный люпус-нефрит остается второй по частоте причиной смерти от волчанки и составляет до 23% в структуре летальности при этом заболевании.
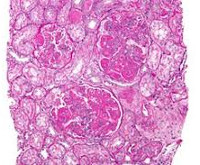
Волчаночный нефрит
Причины
Поражение почек при СКВ обусловлено характерными нарушениями иммунитета. Непосредственной причиной нефрита становится повреждение паренхимы и интерстиция вследствие специфической аутоиммунной деструкции тканей. Специалистами в сфере клинической урологии, нефрологии и ревматологии выявлено два этиологических фактора развития почечной патологии у пациентов, страдающих системной красной волчанкой:
- Иммунные комплексы. При СКВ неконтролируемо усиливается образование антител к собственным клеткам организма. Осаждение циркулирующих иммунных комплексов (ЦИК) в почках потенцирует возникновение специфического воспалительного процесса (гломерулонефрита).
- Волчаночный антикоагулянт. Антифосфолипидные антитела, вытесняя фосфолипид-связывающие протеины, провоцируют усиление коагуляции. Возникающие артериальные и венозные микротромбозы приводят к ишемии и атрофии почечной паренхимы, усугубляя течение нефрита.
Патогенез
Ключевым звеном в развитии волчаночного нефрита является повреждение почечных тканей вследствие аутоиммунной деструкции. В результате поликлональной активации B-лимфоцитов, недостаточной активности T-супрессоров, низкой толерантности к аутоантигенам в организме больного в большом количестве образуются антитела к ДНК, нуклеосомам, кардиолипину, некоторым фракциям комплемента. Первыми в гломерулах обычно осаждаются иммунные комплексы, антигеном в которых являются нуклеосомы, тропные к анионным участкам базальных мембран. В дальнейшем происходит осаждение ЦИК с другими антигенами.
Накопление иммунных комплексов под эндотелием, эпителием, в базальных мембранах, межуточной ткани нарушает мембранную проницаемость, активирует нейтрофилы, цитокины, систему комплемента и другие эффекторные механизмы воспалительного ответа. В конечном итоге пролиферируют клетки клубочков, расширяются мезангиальные пространства, в виде «проволочных петель» утолщаются базальные мембраны капилляров, подвергаются фибриноидному некрозу и склерозируются капиллярные петли. Ситуация усугубляется повреждениями эндотелия и ишемией тканей из-за микротромбозов ренальных сосудов, вызванных развитием волчаночного варианта антифосфолипидного синдрома.
Классификация
В качестве основного критерия систематизации вариантов люпус-нефрита использованы морфологические изменения почечных структур, их распространенность и клинические проявления. Такой подход позволяет максимально точно спрогнозировать течение заболевания и подобрать оптимальную схему лечения. Эксперты ВОЗ различают 6 классов волчаночного нефрита:
- Класс I – мезангиальный нефрит с нормальными клубочками. Морфологические изменения мезангия не выражены, при электронной или иммунофлуоресцентной микроскопии в нем определяются иммунные комплексы. Клиническая симптоматика отсутствует. Наиболее прогностически благоприятный вариант патологии. Пациенты нуждаются в динамическом наблюдении и скрининговых исследованиях для контроля над состоянием почек.
- Класс II – пролиферативный мезангиальный нефрит. Отмечается расширение мезангия, увеличение количества мезангиальных клеток, наличие осажденных ЦИК. В осадке мочи могут выявляться эритроциты, суточная протеинурия не превышает 500 мг. Клинические симптомы поражения почек отсутствуют. Прогноз благоприятный. Базисная терапия предполагает прием блокаторов ангиотензиновых рецепторов, глюкокортикостероидов в низких и средних дозировках.
- Класс III – пролиферативный очаговый гломерулонефрит. До половины гломерул подверглись эндо- и экстракапиллярной клеточной пролиферации. Участки воспаления сегментарно распределены в паренхиме. Определяется протеинурия и гематурия. Гипертензия, нефротический синдром, повышение концентрации сывороточного креатинина наблюдаются редко. Кроме кортикостероидов назначают цитостатические препараты. Прогноз различный.
- Класс IV – пролиферативный диффузный гломерулонефрит. Иммуновоспалительному некрозу и склерозированию подверглось больше половины гломерул. В клинической картине кроме лабораторных изменений часто выявляется повышение давления, нефротический синдром. Уровень сывороточного креатинина обычно увеличен. Необходима комплексная терапия цитостатиками и стероидами. Прогноз серьезный.
- Класс V – мембранозный гломерулонефрит. Гломерулярная мембрана утолщена. Обнаруживается субэпителиальное и интрамембранозное отложение иммунных комплексов. Преобладает клиника нефротического синдрома, у некоторых больных возможно увеличение АД, появление эритроцитов в моче, изредка повышается уровень креатинина. Рекомендована иммуносупрессорная терапия разными препаратами и ЗПТ. Прогноз сомнительный.
- Класс VI – склерозирующий гломерулонефрит. Склерозировано более 90% клубочковых капилляров. Быстро возникает и нарастает хроническая почечная недостаточность при минимальных изменениях мочевого осадка. Прогноз неблагоприятный. Пациентам требуется раннее назначение заместительной почечной терапии и пересадка почек. Без радикального лечения заболевание переходит в терминальную стадию.
Отечественными специалистами предложена классификация люпус-нефрита с учетом тяжести, особенностей течения и исходов патологического процесса. Быстропрогрессирующую форму аутоиммунного воспаления почек с нефротическим синдромом, злокачественной гипертензией, ранним возникновением ХПН, плохим прогнозом выявляют у 10-12% больных СКВ. Активный нефрит с признаками волчаночного нефротического синдрома обнаруживают у 30-40% пациентов. В 30-33% случаев определяется активный гломерулонефрит, в картине которого преобладает мочевой синдром. У 15-30% больных нефрит протекает латентно и диагностируется только лабораторно.
Симптомы волчаночного нефрита
Заболевание развивается в среднем через год после постановки диагноза СКВ, хотя может быть и единственным висцеральным проявлением волчанки. В 40% люпус-нефрит имеет бессимптомное течение и выявляется лабораторно. В клинике обычно преобладают признаки основной патологии (поражения суставов, характерная эритема, серозиты), к которым присоединяются отеки, локализованные на лице и наиболее выраженные по утрам, уменьшение суточного количества мочи. 2-5% больных отмечают появление видимой примеси крови в моче. При прогрессировании процесса у 60-70% пациентов возникает стойкая артериальная гипертензия с высокими значениями диастолического давления, рефрактерная к традиционным гипотензивным препаратам. Общее состояние зависит от выраженности морфологических изменений, при нефрите легкой степени нарушения отсутствуют, при тяжелом течении нарастают симптомы интоксикации, появляется кожный зуд, сильные головные боли.
Осложнения
Заболевание часто приводит к формированию или обострению сердечно-сосудистой патологии. Наиболее распространенными осложнениями волчаночного нефрита, развивающимися вследствие поражения сосудов при симптоматической артериальной гипертензии с дислипидемией, являются ишемическая болезнь сердца, инсульты. У пациентов могут возникать тяжелые инфекционные процессы (сепсис, некурабельные пневмонии, туберкулез), связанные с резким снижением иммунитета при длительном лечении кортикостероидами и цитостатиками. Нефрит при волчанке повышает риск злокачественной трансформации клеток, в частности – лейкоцитов с развитием В-клеточных лимфом. Почечная недостаточность как исход волчаночного гломерулонефрита обнаруживается у 10-15% больных. У 36% пациентов с быстропрогрессирующим заболеванием наблюдается ДВС-синдром.
Диагностика
Постановка диагноза волчаночного нефрита обычно не представляет сложностей при наличии характерной симптоматики заболевания. Диагностика может быть затруднена, если гломерулонефрит является единственным органным проявлением СКВ. При подозрении на волчаночный генез поражения почек рекомендованы следующие методы исследований:
- Общий анализ мочи. Соответственно клиническому варианту люпус-нефрита в осадке могут определяться эритроциты, лейкоциты, цилиндры. Для всех форм волчаночного гломерулонефрита кроме I класса характерна протеинурия от 200 до 3000-3500 мг белка/сут и более.
- Содержание креатинина в крови. Обычно показатель повышен у пациентов с диффузным пролиферативным люпус-нефритом, реже — при очаговом, мембранозном поражении, склерозирующей форме заболевания. Высокий креатинин служит прогностически неблагоприятным признаком.
- Исследование крови на антитела. Обнаруживается наличие антинуклеарного фактора, антинуклеарных антител, антител к ds-ДНК, нуклеосомам, гистонам. С1q. При проведении анализа применяют иммунофлуоресцентные и иммуногистохимические методы.
- Волчаночный антикоагулянт (LA). Умеренные и высокие показатели теста характерны для сочетания нефрита с антифосфолипидным синдромом. Положительные результаты свидетельствуют о повышенном риске усугубления аутоиммунного воспаления тромботическими процессами.
- Пункционная биопсия почек. Гистологическое исследование биоптата позволяет выявить патогномоничные морфологические изменения тканей. Проводится всем больным с подозрением на люпус-нефрит при измененном общем анализе мочи или повышенном сывороточном креатинине.
В общем анализе крови часто определяется снижение уровня лейкоцитов, эритроцитов, тромбоцитов, ускорение СОЭ. В качестве вспомогательных методов, позволяющих оценить выраженность структурных изменений и функциональную состоятельность почечной паренхимы, могут выполняться УЗИ, КТ, МСКТ, МРТ почек, экскреторная урография, нефросцинтиграфия, комплексное биохимическое исследование крови, нефрологический комплекс, оценка системы гемостаза. Дифференциальная диагностика люпус-нефрита проводится с быстропрогрессирующим и хроническим гломерулонефритом, лекарственной нефропатией, поражениями почек при ревматоидном артрите, других системных заболеваниях соединительной ткани, миеломной болезни, аутоиммунном гепатите, геморрагическом васкулите, первичном и наследственном амилоидозе. По показаниям пациента кроме уролога, нефролога и ревматолога консультирует терапевт, гепатолог, гематолог, онколог, онкогематолог, токсиколог.
Лечение волчаночного нефрита
Основными терапевтическими задачами при ведении пациентов с СКВ, у которых диагностирован специфический гломерулонефрит, являются индукция ремиссии, максимально долгое сохранение функциональной состоятельности паренхимы, профилактика рецидивов и осложнений, улучшение качества жизни и показателей выживаемости. При выборе схемы лечения учитывают активность аутоиммунного процесса, потенциальную обратимость деструктивных изменений, выраженность почечной недостаточности. Больным с неактивным процессом (I класс люпус-нефрита) рекомендован периодический скрининг состояния почек и назначение препаратов для коррекции других клинических проявлений СКВ.
При волчаночном гломерулонефрите II класса терапию начинают с ингибиторов АПФ, оказывающих антигипертензивный и нефропротективный эффекты за счет снижения системного артериального давления без ущерба ренальному кровотоку. Терапевтическая резистентность состояния, нарастание протеинурии, появление признаков гематурии является основанием для дополнительного применения глюкокортикостероидов и имидазольных цитостатиков. Больным с активным люпусным воспалением гломерул III-V класса в качестве базисных назначают иммуносупрессивные лекарственные средства:
- Цитостатические препараты. Являются обязательным элементом индукционного и поддерживающего лечения. При агрессивном течении заболевания предпочтительна пульс-терапия сверхвысокими дозами алкилирующих производных диамидофосфата, которые ингибируют активность B-лимфоцитов. В последующем больных переводят на поддерживающие дозировки имидазольных цитостатиков или селективных производных микофеноловой кислоты.
- Глюкокортикостероиды. В качестве монопрепаратов в настоящее время практически не используются. Эффективно дополняют цитостатическую терапию, обеспечивая более длительное сохранение почечных функций и лучшие показатели выживаемости. Обычно назначаются в низких дозировках и альтернирующих режимах приема. На начальных этапах лечения возможно проведение активной пульс-терапии высокими дозами.
Альтернативными методами ведения больных с терапевтически резистентными вариантами волчаночного гломерулонефрита являются применение ингибиторов кальциневрина, синтетических моноклональных антител к CD20 и CD22-антигенам мембран B-лимфоцитов, антицитокиновых препаратов, молекулярных блокаторов иммунной реакции. Апробируются и внедряются технологии тотального облучения лимфоидной ткани, костного мозга с последующей трансплантацией стволовых клеток.
Симптоматическая терапия люпус-нефрита направлена на коррекцию отдельных клинических проявлений заболевания. При развитии артериальной гипертензии и значительной протеинурии рекомендован прием ингибиторов АПФ или селективных блокаторов рецепторов ангиотензина II. Для устранения возможной дислипидемии используются статины. Пациентам с признаками антифосфолипидного синдрома показаны антикоагулянты и антиагреганты. Нарастание признаков почечной недостаточности, особенно при волчаночных гломерулонефритах V-VI класса, служит основанием для проведения ЗПТ (гемодиализа, перитонеального диализа, гемофильтрации, гемодиафильтрации и др.), а затем трансплантации почки после 3-6-месячного снижения активности аутоиммунного воспаления.
Прогноз и профилактика
Хотя развитие почечной патологии в целом ухудшает прогноз СКВ, при своевременной диагностике и адекватной терапии пятилетняя выживаемость наблюдается у 80-85% больных с тяжелыми формами гломерулонефрита и у 95% с процессами средней тяжести. Первичная профилактика волчаночного нефрита заключается в скрининговых обследованиях пациентов из группы риска по СКВ с целью раннего выявления и назначения комплексного лечения основной патологии, что позволяет снизить вероятность развития поражения почек. Для предупреждения прогрессирования уже имеющегося нефрита необходимо проведение длительной поддерживающей терапии.
Источник
Содержание статьи:
Волчаночный нефрит имеет клинические проявления у 50-60% пациентов с системной красной волчанкой (СКВ), морфологические изменения диагностируются у большинства больных СКВ, даже без развития почечной недостаточности. Оценка функции почек у пациентов в этой ситуации важна, потому что раннее выявление и лечение поражения почек значительно улучшает жизненный прогноз. Люпус-нефрит в большинстве наблюдений присоединяется в течение 5 лет после постановки диагноза, но иногда является первичным и единственным симптомом СКВ. Патологию почек регистрируют чаще у мужчин молодого возраста, а саму СКВ – у женщин (9:1). Дети с СКВ подвержены более высокому риску ренальных повреждений, что связывают с высокой агрессивностью процесса и токсичностью терапии.
Этиология
Этиология до настоящего времени неизвестна, специалисты отмечают, что первым симптомам СКВ предшествуют признаки вирусоподобного заболевания.
• Генетические факторы
Как и при многих аутоиммунных заболеваниях, данные свидетельствуют о том, что генетическая предрасположенность играет роль в развитии как СКВ, так и волчаночного нефрита. Гены, многие из которых еще не идентифицированы, опосредуют эту генетическую предрасположенность.
СКВ чаще встречается у родственников первой степени (мать, отец, братья и сестры), семейная распространенность составляет 10-12%, для монозиготных близнецов – 24-58%, дизиготных – 2-5%. Это подтверждает влияние генетических факторов в развитии СКВ, но то, что из монозиготной пары не в 100% случаев заболеют оба близнеца, позволяет предположить, что факторы окружающей среды также следует учитывать.
• Иммунологические факторы
Начальный ответ аутоантитела потенциально направлен против нуклеосомы, которая возникает из апоптотических клеток. У пациентов с СКВ нарушены механизмы очистки от «клеточного мусора», который способствует плазмоцитоидные дендритные клетки продуцированию интерферон-α – мощного индуктора иммунной системы и аутоиммунитета.
В-лимфоциты активизируются при СКВ из-за сбоя гомеостатических механизмов, что приводит к срыву толерантности и способствует выработке антител. Обнаружены и другие аутоантитела, которые появляются с течением времени, от нескольких месяцев до нескольких лет до начала клинических проявлений.
Патофизиология
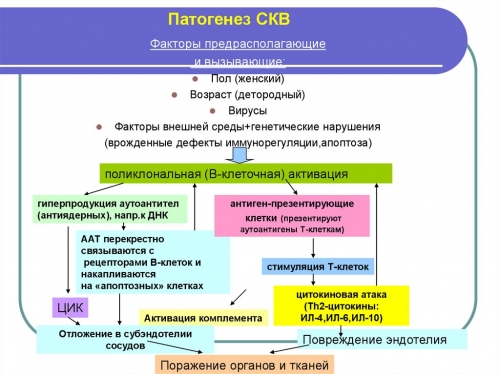
Основная причина – поражение гломерулярного аппарата почек. Иммунитет играет ведущую роль в патогенезе волчаночного нефрита. Иммунологические механизмы включают продукцию нефритогенных аутоантител с образованием внутрисосудистых иммунных комплексов, которые откладываются в клубочках. Антитела могут связываться с антигенами гломерулярной базальной мембраны, формируя иммунные комплексы in situ, способствующие воспалительному ответу. Происходит привлечение воспалительных клеток с активацией лимфоцитов, макрофагов и нейтрофилов.
Гистологический тип волчаночного нефрита зависит от множества факторов, включая антигенную специфичность и другие свойства аутоантител, тип воспалительного ответа, который определяется другими факторами организма. При более тяжелых формах патологии пролиферация эндотелиальных, мезангиальных и эпителиальных клеток и продукция матриксных белков приводят к фиброзу.
Гломерулярный тромбоз – еще один механизм, который может играть роль в патогенезе волчаночного нефрита, главным образом у пациентов с антифосфолипидным синдромом, что является ответом на взаимодействие антител и отрицательно заряженных фосфолипидных белковых комплексов. Некоторые исследования продемонстрировали влияние типа кишечной микрофлоры Ruminococcus gnavus в патогензе волчаночного нефрита. У пациентов с СКВ и почечной недостаточностью было выявлено пятикратное их увеличение.
Классификация
Таблица. Нефрологическая и патоморфологическая классификация волчаночного нефрита
| Класс I | Минимальный мезангиальиый ВН |
| Класс II | Мезангиальиый пролиферативный ВН |
| Класс III | Фокальный ВНа Активный или неактивный фокальный, сегментарный или глобальный эндо- и экстракапиллярный гломеруломефрит с вовлечением менее 50% клубочков обычно с фокальными субэндотелиальными депозитами, наличием или отсутствием мезангиальной альтерации |
| Класс III(A) | Активные повреждения: фокальный пролиферативный ВН |
| Класс III(A/C) | Активные и хронические повреждения: фокальный пролиферативный и склерозирующий ВН |
| Класс III(C) | Хронические неактивные повреждения с гломерулярньм склерозом: фокальный склерозирующий ВН |
| Класс IV | Диффузный ВНб Активный или неактивный фокальный, сегментарный или глобальный эндо- и экстракапилляриый гломерулонефрит с вовлечением 50% клубочков и более обычно с фокальными субэндотелиальными депозитами, наличием или отсутствием мезангиальной альтерации. Данный класс подразделяется на диффузный сегментарный (IV-S) ВН, когда 50% вовлеченных в процесс клубочков и более имеет сегментарные повреждения и диффузный глобальный (IV-G) ВН, когда 50% вовлеченных клубочков и более имеет глобальные повреждения. Сегментарным обозначают как гломерулярные повреждения с вовлечением менее половины петель капилляров. Данный класс включает случаи с диффузными отложениями в виде проволочных петель, но с незначительной или отсутствием пролиферации |
| Класс IV-S (A) | Активные повреждения: диффузный сегментарный пролиферативный ВН |
| Класс IV-G (A) | Активные повреждения: диффузный глобальный пролиферативный ВН |
| Класс IV-S (A/C) | Активные и хронические повреждения: диффузный сегментарный активный и склерозирующий пролиферативный ВН |
| Класс IV-G (A/C) | Активные и хронические повреждения диффузный глобальный активный и склерозирующий пролиферативный ВН |
| Класс IV-S (C) | Активные и хронические повреждения: диффузный сегментарный склерозирующий ВН |
| Класс IV-G (C) | Хронические неактивные повреждения с рубцами: диффузный глобальный склерозирующий ВН |
| Класс V | Мембранозный ВН Глобальные или сегментарные субэпителиальные иммунные депозиты при световой микроскопии и при ИФ или ЭМ с или без альтерации мезангия Класс V ВН может быть в комбинации с III или IV классом. В этом случае в диагнозе необходимо указать оба класса Класс V ВН может быть представлен далеко зашедшим склерозом паренхимы |
| Класс VI | Далеко зашедший склерозирующий ВН 90% клубочков и более глобально склерозировано без признаков активности |
Симптомы волчаночного нефрита
Пациенты с активным волчаночным нефритом часто имеют экстраренальные (не связанные с почками) симптомы активной системной красной волчанки, включая усталость, повышение температуры, сыпь, артрит, серозит. Клинические проявления чаще встречаются при очаговом пролиферативном и диффузном пролиферативном волчаночном нефрите. Иногда выраженная симптоматика отсутствует, но о патологии можно заподозрить по изменениям в лабораторных анализах: повышенному уровню креатинина, низкому уровню альбуминов, протеинурии, цилиндрурии.
Симптомы могут включать периферические отеки, вторичные к гипертонии или гипоальбуминурии. Массивное накопление жидкости чаще встречается у людей с диффузным или мембранозным волчаночным нефритом, так как при данных формах типична выраженная потеря белка с мочой из-за вовлечения в процесс большого количества клубочков. К прочим симптомам СКВ относят головную боль, головокружение, нарушение зрения и признаки сердечной декомпенсации.
Диагностика
Диагностические мероприятия начинают с анализа истории заболевания и физикального осмотра, при котором обращают внимание на сыпь (эритематозный дерматит на лице, напоминающий бабочку), язвенные поражения в носовой или ротовой полости, симметричные изменения суставов (проявления СКВ). Для мембранозного волчаночного нефрита характерны признаки изолированного нефротического синдрома. К ним относят: периферические отеки, асцит, выпот в плевральной полости и перикарде.
Дифференциальная диагностика включает:
• Хронический гломерулонефрит;
• Диффузный пролиферативный гломерулонефрит;
• Мембранозный гломерулонефрит не волчаночной этиологии;
• Быстропрогрессирующий гломерулонефрит;
• Полиартериит Нодоса;
• Гранулематоз с полиангиитом (Вагнера).
Для окончательной верификации диагноза рассматривают вопрос о проведении нефробиопсии у пациента с системной красной волчанкой с клиническими или лабораторными признаками волчаночного нефрита.
Лабораторная диагностика
Лабораторные исследования включают:
• общий анализ мочи (лейкоциты, эритроциты повышены, протеинурия от незначительной до выраженной, цилиндры);
• биохимию крови (повышение уровня креатинина, мочевины);
• анализ мочи на концентрацию креатинина и белка (норма: экскреция креатинина составляет 1000 мг / 24 ч / 1,75 м 2 ; экскреция белка составляет 150-200 мг / 24 ч / 1,75 м 2 ; соотношение белка и креатинина в моче составляет • суточный анализ мочи на клиренс креатинина и выведение белка.
Определена группа новых биомаркеров, помогающая в диагностике волчаночного нефрита:
• альфа-1-кислый гликопротеин;
• церулоплазмин;
• липокалинподобная синтаза простагландина D;
• трансферрин.
К лабораторным тестам на активность СКВ относят:
• определение антител к уровням двухцепочечной ДНК (дцДНК),
• комплемента (С3, С4 и СН 50 );
• скорости оседания эритроцитов (СОЭ);
• уровня С-реактивного белка (СРБ).
Повышенный уровень СОЭ и анти-дцДНК, а также пониженный уровень С3 и С4 связаны с активным процессом в почках, особенно при очаговом и диффузном волчаночном нефрите. Клинически значимый люпус-нефрит подтверждает снижение клиренса креатинина на 30%, протеинурия более 1000 мг / сутки и результаты биопсии почки, свидетельствующие об активном заболевании.
Лечение

Лечение волчаночного нефрита зависит от патоморфологических изменений. Мезангиальный процесс (класс I, минимальная активность процесса) не подразумевает активной терапии, за пациентами наблюдают в динамике. При мезангиальном пролиферативном нефрите (класс II) терапию проводят, если протеинурия превышает 1000 мг / сутки. Назначают преднизон от низких до умеренных доз, длительность приема индивидуальна.
Пациенты с фокальным (класс III) или диффузным (класс IV) волчаночным нефритом имеют высокий риск прогрессирования и развития терминальной стадии хронической почечной недостаточности, поэтому нуждаются в агрессивной терапии. Используют более высокие дозы преднизона, длительность курса не менее 4 недель, в дальнейшем пациента переводят на поддерживающую дозу в течение 24 месяцев. При острой форме вводят метилпреднизолон внутривенно в дозе 1000 мг/сутки в течение 3 дней (перед началом основного лечения кортикостероидами, пульсовая терапия).
Пациентов с мембранозной формой волчаночного нефрита (V класс) лечат преднизоном в течение 1-3 месяцев с переводом на поддерживающую дозу с последующим уменьшением в течении 1-2 лет, при условии адекватного ответа на препарат. Течение доброкачественное при чистой форме.
Показания к дополнительному назначению иммунодепрессантов:
• отсутствие ответа на кортикостероидную терапию;
• непереносимость;
• ухудшение функциональной способности почек;
• серьезные пролиферативные изменения;
• признаки склероза в нефробиоптатах.
К данной группе препаратов относят циклофосфамид, циклоспорин А, азатиоприн, микофентолат мофетил.
Все пациенты с волчаночным нефритом должны получать фоновую терапию гидроксихлорохином, если нет противопоказаний. Ингибиторы ангиотензин-превращающего фермента или блокаторы ангиотензин-рецепторов следует вводить, если протеинурия достигает или превышает 0,5 г / день. Целевое АД – на уровне или ниже 13080 мм. рт. ст.
Экспериментальная терапия

Применение анти-CD 20 моноклональных антител у пациентов с активным волчаночным нефритом, устойчивом к традиционной терапии, возможно позволит добиться обнадеживающих результатов. Ритуксимаб, вызывающий гибель В-клеток, не подтвердил выраженной эффективности для лечения СКВ. Клинические испытания по Ритуксимабу полностью не завершены, одобрение получено для терапии больных, страдающих ревматоидным артритом и неходжкинской лимфомой.
Другие анти-CD20 моноклональные антитела были использованы экспериментально для волчаночного нефрита; например, у пациентов, которые отвечают на терапию ритуксимабом, но продолжение лечения невозможно из-за выраженных побочных эффектов. К препаратам относят:
• Окрелизумаб;
• Офатумумаб;
• TRU-015.
Белимумаб является моноклональным антителом против B-лимфоцитарного стимулятора (BLyS). Было обнаружено, что он оказывает положительное влияние на клинические и лабораторные показатели у пациентов с активной формой СКВ. Кроме того, количество В-клеток и сывороточного IgM со временем снижалось. Белимумаб был одобрен FDA для применения у пациентов с активной аутоантителпозитивной СКВ на фоне стандартной терапии.
Атацицепт ингибирует BLyS и пролиферативный лиганд (APRIL]). В ранних исследованиях было показано, что атацицепт обладает биологическим эффектом у пациентов с СКВ, что приводит к дозозависимому снижению уровня В-клеток и уровня иммуноглобулинов.
Учеными разрабатывается антицитокиновая терапия. Были предложены различные ее виды, включая моноклональные антитела, направленные против:
• Интерферона-α;
• Интерлейкина (ИЛ) -1;
• IL-6;
• IL-10;
• Факторов некроза опухоли альфа (TNF-α).
Т-клеточная терапия химерным рецептором антигена (CAR) была признана важным достижением при лечении рака, и в настоящее время исследователи тестируют использование этих продуктов в других терапевтических областях, включая аутоиммунные заболевания. Ученые сообщают, что в экспериментах с грызунами в двух моделях СКВ лечение Т-клетками CAR удлиняло продолжительность жизни и облегчало клинические проявления.
CD19-нацеленные CAR T-клетки блокировали CD19 + B-клетки, устраняли продукцию аутоантител и задерживали или обращали вспять процесс заболевания.
Волчаночный нефрит и ХПН
Пациенты с терминальной стадией почечной недостаточности требуют диализной терапии и являются хорошими кандидатами для трансплантации почки . Больные с волчаночным нефритом и ХПН составляют 1,5% от всех пациентов, находящихся на гемодиализе. Пятилетняя выживаемость при волчаночном нефрите и уремии при заместительной почечной терапии – 60-70%, сопоставима с таковой для прочих больных, без СКВ.
Исследования показали, что гемодиализ предпочтительнее перитонеального диализа: задокументированы более высокие уровни антител к двухцепочечной ДНК (дцДНК), выраженная тромбоцитопения и необходимость принимать более высокие дозы кортикостероидов у пациентов с СКВ и ХПН, находящихся на перитонеальном диализе. Доказано, что гемодиализ также оказывает противовоспалительное действие с уменьшеним количества Т-хелперов в лимфоцитах. СКВ обычно не прогрессирует у пациентов, находящихся на гемодиализе, вспышки возникают редко и проявляются сыпью, артритом, серозитом, лихорадкой и лейкопенией, что в каждом случае требует специального лечения.
Прогноз
За последние 4 десятилетия изменения в лечении волчаночного нефрита и общей медицинской помощи значительно улучшили общую выживаемость и уменьшили риск прогрессирования почечной недостаточности. В течение 1950-х годов 5-летняя выживаемость среди пациентов с волчаночным нефритом была близка к 0%. Последующее добавление иммунодепрессантов привело к документированной 5- и 10-летней выживаемости, достигающей 85% и 73% соответственно.
Автор
Виктория Мишина
Дата публикации
01.04.2019
Источник
