Тромболитическая терапия при остром коронарном синдроме

Библиографическое описание:
Спиридонова, А. В. Тромболитическая терапия на догоспитальном этапе оказания медицинской помощи при остром коронарном синдроме с подъемом сегмента ST / А. В. Спиридонова. — Текст : непосредственный // Молодой ученый. — 2020. — № 25 (315). — С. 453-456. — URL: https://moluch.ru/archive/315/71759/ (дата обращения: 13.07.2020).
Сердечно-сосудистые заболевания являются основной причиной смерти во всем мире. По уровню смертности от ишемической болезни сердца (ИБС) наша страна занимает одно из лидирующих позиций. Ежегодно от сердечно-сосудистых заболеваний (ССЗ) в мире умирают около 17 млн. человек и в первую очередь — от осложнений ишемической болезни сердца (ИБС). Согласно данным отчета Росстата за 2019 год, всего за 2018 год зарегистрировано 161 300 случаев острого инфаркта миокарда, что превышает показатели 2017 года — 158 600 случаев. В процентном соотношении рост заболеваемости острым инфарктом миокарда составил 1,9 %, за период с 2010 г. по 2018 г. рост показателей по острому ИМ составил 3,73 %.
Одним из основных факторов, определяющих прогноз пациентов с острым коронарным синдромом (ОКС), является своевременное оказание медицинской помощи в первые часы заболевания, поскольку именно в этот период показатели летальности наиболее высокие. Именно правильно разработанная схема оказания помощи на догоспитальном этапе в ранние сроки при ОКС с последующей госпитализацией пациента в профильный стационар позволяет избежать сосудистой катастрофы.
Основная часть
ИБС-заболевание, обусловленное нарушением равновесия между коронарным кровотоком и метаболическими потребностями миокарда.
Термин “ОКС” используют для обозначения обострения ИБС. Этим термином объединяют такие клинические состояния, как инфаркт миокарда(ИМ) и нестабильная стенокардия. Эксперты Всероссийского научного общества кардиологов приняли следующее определение ОКС и нестабильной стенокардии (2001 г.): “ОКС — термин, обозначающий любую группу клинических признаков или симптомов, позволяющих подозревать ОИМ или нестабильную стенокардию. Включает в себя понятия ОИМ, инфаркт миокарда со стойким подъемом сегмента ST ЭКГ (ИМпST), инфаркт миокарда без подъема сегмента ST ЭКГ(ИМбпST ЭКГ), ИМ, диагностированный по изменениям ферментов, по другим биомаркерам, по поздним ЭКГ признакам, и нестабильную стенокардию”
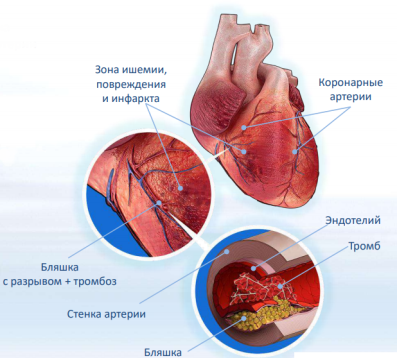
Непосредственной причиной развития ИМпST является окклюзия КА, как правило, тромботического происхождения, соответствующей области поражения миокарда. Поэтому основой лечения этих больных является восстановление коронарного кровотока — коронарная реперфузия. Разрушение тромба и восстановление перфузии миокарда приводят к ограничению размеров его повреждения и, в конечном итоге, к улучшению ближайшего и отдаленного прогноза. Поэтому все больные ИМпST должны быть безотлагательно обследованы для уточнения показаний и противопоказаний к восстановлению коронарного кровотока. На догоспитальном этапе оказания медицинской помощи при ИМпST методом коронарной реперфузии непосредственно является тромболитическая терапия(ТЛТ).
Основным показанием для назначения ТЛТ считается ОКС с подъемом сегмента ST в 2-х и более смежных отведениях или появление блокады левой ножки пучка Гиса в первые 6 часов от начала симптомов [3]
Противопоказания к тромболитической терапии
Абсолютные:
– Геморрагический инсульт или инсульт неизвестного происхождения любой давности
– Ишемический инсульт в предыдущие 6 мес.
– Травма или опухоли головного мозга, артериовенозная мальфармация
– Большая травма/операция/травма головы в течение предыдущего мес.
– Желудочно-кишечное кровотечение в течение предыдущего мес.
– Периодические кровотечения (исключая месячные)
– Диссекция аорты
– Пункции в течении суток (биопсия печени, люмбарная пункция)
Относительные:
– Транзиторная ишемическая атака в течение предыдущих 6 мес.
– Оральная антикоагулянтная терапия
– Беременность или 1 неделя после родов
– Резистентная гипертония (САД >180 мм рт.ст. и/или диастолическое АД>110 мм рт.ст.)
– Тяжелое заболевание печени
– Инфекционный эндокардит
– Обострение язвенной болезни
– Продолжительная или травматичная реанимация
Важным преимуществом ТЛТ является возможность искусственно расширить терапевтическое окно острого инфаркта миокарда за счёт догоспитального тромболизиса.
Известно, что эффективность ТЛТ снижается со временем в параболической зависимости: чем раньше удается провести лечение, тем больше шансов на спасение жизни пациента. В случае выбора тромболизиса в качестве стратегии реперфузии, максимально допустимое время задержки от постановки диагноза ИМпST до тромболизиса должно быть не более 10 мин. [1]
Повреждение миокарда в результате окклюзии КА развивается быстро, и уже через 4–6 ч от начала первых симптомов болезни большая часть ишемизированного миокарда некротизируется. Поэтому очень важно провести реперфузионную терапию как можно раньше. [2]
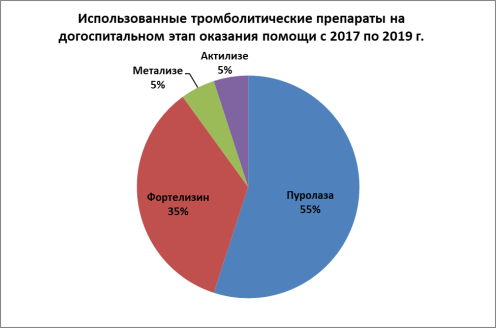
На примере исследования больных с ИМпST двух районов Чувашской Республики с численностью населения в 57 тысяч человек представлена статистика по распределению больных с ОИМ, получавших ТЛТ на догоспитальном этапе оказания скорой медицинской помощи, за 2 года. При анализе карт вызовов скорой медицинской помощи на одной из подстанций скорой медицинской помощи Чувашии выявлены следующие данные:
За период 2017–2019 года диагноз ИМпST был выставлен 28 больным.
72 % из которых была успешна проведена ТЛТ c последующей госпитализацией в специализированное учреждение.
Пациенты должны быть транспортированы в ЧКВ (чрескожное коронарное вмешательство)-центр как можно быстрее после начала тромболизиса. Спасительное ЧКВ показано пациентам, у которых тромболизис был неэффективен (снижение сегмента ST менее чем на 50 % от исходного уровня через 60–90 мин после начала тромболизиса) или имеются нарушения гемодинамики, электрической нестабильности сердца, усугубление ишемии, и персистирующие ангинозные боли, в то время как рутинное ЧКВ показано пациентам с ИМпST после успешного тромболизиса в течение 2–24 ч. [1]
Заключение
Оказание помощи больному с ОКС представляет собой единый процесс. В настоящее время наиболее эффективными, патогенетически обоснованными методом лечения острого коронарного синдрома с подъемом сегмента ST на догоспитальном этапе оказания медицинской помощи является тромболитическая терапия. Именно ранний догоспитальный тромболизис позволяет восстановить кровоток в инфаркт-зависимой артерии, прервать («абортировать») развитие некроза в миокарде, снизить риск развития фатальных осложнений (фибрилляция желудочков, кардиогенный шок, острая застойная сердечная недостаточность) на догоспитальном этапе оказания помощи.
Литература:
- Российский кардиологический журнал 2018; 23 (5): 103–158
- Оганов Р. Г.. Всероссийское научное общество кардиологов Национальные клинические рекомендации.Москва 2009
- Джанашия, П. Х. Неотложная кардиология. Руководство для врачей / П. Х. Джанашия. — Москва: БИНОМ, 2016 г.с 206
Основные термины (генерируются автоматически): нестабильная стенокардия, коронарный кровоток, медицинская помощь, скорая медицинская помощь, догоспитальный этап оказания, острый инфаркт миокарда, инфаркт миокарда, подъем сегмента, острый коронарный синдром, ишемическая болезнь сердца.
Источник
Острый коронарный синдром (ОКС)— любая группа клинических признаков или симптомов, позволяющих подозревать острый инфаркт миокарда (ОИМ) или нестабильную стенокардию (НС). Этот термин включает всебя инфаркт миокарда сподъемом сегмента ST(ИМпST) или без подъема сегмента ST(ИМб/пST); инфаркт миокарда, диагностированный поизменениям ферментов, побиомаркерам, поздним ЭКГ-признакам иНС[1, 2]. Онпоявился всвязи снеобходимостью выбирать лечебную тактику доокончательной диагностики перечисленных состояний ииспользуется при первом контакте сбольными, преимущественно надогоспитальном этапе. Диагноз ОКС ставится наосновании клинических симптомов ишемической болезни сердца (ИБС): появление, учащение и/или утяжеление ангинозных приступов. Морфологической основой ОКС является повреждение атеросклеротической бляшки сформированием тромба вкоронарной артерии (рис.1).
При этом может окклюзироваться крупная коронарная артерия (рис. 2), и тогда развивается обширный трансмуральный некроз миокарда, что находит отражение на ЭКГ в виде подъема сегмента ST. При неполной окклюзии артерии могут быть ЭКГ-изменения в виде депрессии сегмента ST, формирования отрицательных зубцов Т, или ЭКГ-изменения могут отсутствовать.
ОКС с подъемом или без подъема сегмента ST — это диагноз, который ставит врач при первом контакте с пациентом. Далее на основании результатов, в т. ч. повторного исследования крови на содержание маркеров некроза миокарда, динамики ЭКГ, уточняется, имеет ли место развитие ИМпST или ИМб/пSТ, или у больного отсутствует некроз миокардиоцитов, и речь идет о НС.
Современный стандарт оказания помощи больным с ИМпST включает проведение экстренного чрескожного коронарного вмешательства (ЧКВ) со стентированием инфаркт-связанной артерии в течение первых 120 мин от начала ангинозного приступа. Это позволяет восстановить коронарный кровоток более чем у 90% больных [1, 2].
В то же время действующими рекомендациями предусматривается, что у больных, госпитализация которых в специализированный центр по каким-либо причинам откладывается, возможно применение фармакологического метода реваскуляризации миокарда — тромболитической терапии (ТЛТ) (рис. 3).
В результате системного тромболизиса (внутривенного введения тромболитического препарата) происходит лизис тромба и восстанавливается проходимость окклюзированной коронарной артерии. Восстановление коронарного кровотока приводит к сохранению жизнеспособности и электрической стабильности кардиомиоцитов, ограничению зоны некроза, нормализации функции миокарда, снижению смертности у больных с ИМпST [3]. Тромболизис считается эффективным, если через 90 мин отмечается значительное уменьшение интенсивности либо исчезновение болевого синдрома, снижение сегмента ST более 50%, появление реперфузионных аритмий [2].
Эффективность тромболизиса ограничена временными параметрами и резко снижается с увеличением времени от начала болевого приступа (т. е. от начала формирования коронарного тромба). Наиболее эффективен тромболизис в первые 2 ч от начала симптомов, а уже через 12 ч риск осложнений преобладает над возможной пользой (рис. 4) [2]. При тромболизисе повышается риск развития геморрагических осложнений. Факторами риска развития геморрагических осложнений у больных с ОКС являются: пожилой возраст, женский пол, кровотечения в анамнезе, почечная недостаточность, проводимые интракоронарные вмешательства, недавно проведенная фармакологическая реперфузия, а также терапия инотропами, диуретиками и блокаторами гликопротеиновых ΙΙ, В/ΙΙΙ α-рецепторов [4]. Одним из наиболее тяжелых геморрагических осложнений является внутримозговое кровоизлияние. У пациентов с факторами риска геморрагических осложнений и высоким риском кровотечения ТЛТ противопоказана.

Для проведения тромболизиса применяются фибринолитические средства (активаторы плазминогена), под действием которых циркулирующий в крови неактивный белок плазминоген переходит в активный фрагмент плазмин, вызывающий лизис фибрина и разрушение тромба [4]. Выделяют три поколения тромболитиков (табл. 1):
Ι — стрептокиназа — высокоочищенный белковый препарат активатора плазминогена, вырабатываемый β-гемолитическим стрептококком группы С. Стрептокиназа образует с плазминогеном комплекс, преобразуя плазминоген в плазмин. Не обладает фибриноспецифичностью.
ΙΙ — алтеплаза (препарат Актилизе®) — созданный методом генной инженерии рекомбинантный препарат человеческого тканевого активатора плазминогена. При внутривенном введении избирательно активирует плазминоген, адсорбированный на фибрине. Оказывает фибриноспецифическое действие без существенного снижения содержания фибриногена в плазме крови. По сравнению со стрептокиназой алтеплаза обладает более быстрым и выраженным фибринолитическим эффектом, устойчива к ингибитору активатора плазминогена. Благодаря фибриноспецифичности менее часто на фоне ее применения возникают геморрагические осложнения. Реакции гиперчувствительности редки [5, 6].

ΙΙΙ — тенектеплаза (препарат Метализе®). В результате модификации молекулы алтеплазы был создан новый фибринолитик, обладающий еще более выраженной фибриноспецифичностью и высокой устойчивостью к эндогенному ингибитору активатора плазминогена Ι (ИАП). Период полувыведения препарата был увеличен до 20 мин, что позволяет вводить его однократно болюсом [5].
Таким образом, прямые активаторы плазминогена обладают высокой фибриноспецифичностью, что существенно сокращает время эффективного тромболизиса, и высоким уровнем безопасности вследствие очень низкого системного действия, что снижает риск развития геморрагических осложнений, гипотензии. Т. к. эти препараты не аллергенны, то они могут, в отличие от стрептокиназы, применяться повторно.
Дополнительным преимуществом тенектеплазы является то, что она обладает наибольшей устойчивостью к ИАП 1, вследствие чего возможно проведение тромболизиса путем однократного болюсного введения. В отличие от алтеплазы тенектеплаза в очень малой степени потенцирует коллаген-сенсибилизированную агрегацию тромбоцитов, что снижает риск развития повторной окклюзии коронарной артерии после эффективного тромболизиса [8].
В многоцентровом клиническом исследовании ASSENT-II, в которое были включены почти 16 949 больных с ИМпST, оценивалась эффективность и безопасность ТЛТ в двух группах больных. В одной применяли алтеплазу в дозе ≤100 мг, вводимую в/в течение 90 мин, в другой — тенектеплазу 30–50 мг (в зависимости от массы тела больного) в/в однократно болюсом в течение 5–10 с. Было установлено, что показатели 30-дневной смертности у пациентов обеих групп не различались (6,15% — в группе алтеплазы и 6,18% — в группе тенектеплазы), при этом частота развития нежелательных побочных эффектов была достоверно ниже при использовании тенектеплазы [9].


Перенос ТЛТ на догоспитальный этап обеспечил не только снижение госпитальной летальности у больных с ОКС на 17% [10], но и увеличил продолжительность жизни в среднем на 2,5–3 года [11].
В исследовании ASSENT-III PLUS исследовалась эффективность и безопасность догоспитального тромболизиса тенектеплазой. Было показано, что время от первого появления симптомов до лечения было сокращено на 47 мин по сравнению с пациентами, получавшими лечение в стационаре. У 53% больных отмечалась положительная клиническая картина заболевания, которая выражалась в уменьшении длительности и характера ангинозного приступа и положительной динамике сегмента ST на ЭКГ, что в результате способствовало снижению 30-дневной летальности в группе больных, получивших ТЛТ. Этот показатель возрастал при уменьшении времени проведения тромболизиса с момента появления клинической картины заболевания [12].
Летальность в течение 12 мес у больных с прерванным инфарктом миокарда в результате проведенного тромболизиса на догоспитальном этапе в 5,3 раза ниже в сравнении с группой больных с установленным инфарктом миокарда [13].
Скорая медицинская помощь (СМП) является первой медицинской инстанцией, куда обращаются больные с ОКС. Ежегодно в России СМП выполняет около 50 млн выездов, в т. ч. ежедневно более 25 тыс. по поводу ОКС [14]. Бригада СМП, вне зависимости от профиля, должна в полном объеме провести весь комплекс лечебных мероприятий, а у пациентов с ИМпST при невозможности быстрой госпитализации в специализированный сосудистый центр провести реперфузионную терапию с помощью тромболитиков. ТЛТ в настоящее время является наиболее доступной реперфузионной стратегией для пациентов, проживающих на обширных территориях, при отдаленности специализированных центров, оказывающих высокотехнологичную помощь [15].
Догоспитальный тромболизис с использованием тенектеплазы медиком СМП может быть предпочтительнее вследствие простоты применения и более высокого уровня безопасности.
Целями проспективного когортного многоцентрового клинического исследования РОКС-ВОСТОК явились определение безопасности догоспитальной ТЛТ при ИМпST, а также зависимости летальности от временных промежутков, оценки ее влияния на 30-дневную летальность и частоту основных осложнений при применении рекомбинантных препаратов человеческого тканевого активатора плазминогена.
Материалы и методы. Исследование проводилось в крупных городах Дальневосточного Федерального округа (ДФО): Якутске, Благовещенске, Комсомольске-на-Амуре, Южно-Сахалинске, Петропавловске-Камчатском с 2009 по 2012 г. Нами изучены две группы больных с ИМпST, которые были сопоставимы по полу, возрасту, клинико-анамнестическим показателям. 1-ю группу составили 460 больных с ИМпST, получивших ТЛТ на догоспитальном этапе; 2-ю группу — 553 больных с ИМпST, которым ТЛТ не проводилась в связи с наличием противопоказаний. Для проведения тромболизиса использовались алтеплаза (15 мг в/в болюсом, затем в/в инфузия 0,75 мг/кг, но не более 50 мг в течение 30 мин, далее инфузия 0,5 мг/кг, максимально — 35 мг в течение 60 мин) и тенектеплаза (в/в болюсно за 5–10 с 30 мг при массе тела < 60 кг, 35 мг — при массе тела 60–69 кг, 40 мг — 70–79 кг, 45 мг — 80–89 кг и 50 мг — 90 и более кг). Пациенты включались в исследование при установлении диагноза ОКС с подъемом сегмента ST, при этом выбор препарата был обусловлен наличием последнего в укладке врача СМП. Проведение ТЛТ, согласно протоколу системного тромболизиса, включало применение ацетилсалициловой кислоты — 75 мг, клопидогрела — 300 мг, внутривенное введение гепарина 5 тыс. ед.
Всем больным с ОКС на догоспитальном этапе помимо стандартного клинического осмотра и регистрации ЭКГ в 12 стандартных отведениях проводилось определение биомаркеров некроза миокарда (тропонин Т I крови) в капиллярной крови на экспресс-панели ACON (КНР, Медилинк).
Для оценки эффективности реперфузии нами использованы неинвазивные ЭКГ-критерии. Повторная запись стандартной ЭКГ проводилась через 90 и 180 мин от начала введения тромболитика. Динамика сегмента ST оценивалась по степени его суммарного смещения в информативных отведениях ЭКГ. При этом снижение ST на 50% и более в сравнении с исходным уровнем расценивалось как признак успешной ТЛТ (наличие реперфузии); отсутствие динамики сегмента ST, его снижение менее 50% либо увеличение его элевации — как признак неэффективности ТЛТ.
Оценивались и фиксировались временные параметры, характеризующие работу СМП: время симптом-игла (СИ) — время от дебюта ангинозного приступа до момента начала оказания первой помощи, время транспортировки (ВТ) — время от начала транспортировки до передачи больного врачу приемного покоя, общее время обслуживания вызова (ОВ) — сумма временных интервалов от момента выезда бригады СМП до передачи больного врачу приемного покоя (табл. 2).
Статистическая обработка данных проводилась с помощью пакета прикладных программ IBM SPSS Statistics 19.
Полученные результаты. Снижение смертности от сердечно-сосудистых заболеваний в России в настоящее время зависит от трех главных факторов: информированности населения, обученности врачей первичного звена здравоохранения и правильной маршрутизации пациента [16].
В крупных городах ДФО время от появления симптомов ОКС до начала оказания медицинской помощи колеблется от 25 мин до 3 ч. В крупных городах ДФО пациенты с ИМпST на догоспитальном этапе обслуживаются как специализированными кардиологическими и реанимационными, так и общепрофильными линейными врачебными и фельдшерскими бригадами. Несмотря на это, одноэтапная схема оказания медицинской помощи больным с ИМпST, когда оказывается медицинская помощь одной бригадой СМП, составила 76%, при этом исключительно все больные при одноэтапной схеме обслужены специализированными бригадами СМП. Двухэтапная схема обслуживания больных с ИМпST, по нашим данным, составила 24% случаев. При анализе двухэтапной схемы было установлено, что первой бригадой, оказывающей медицинскую помощь, в 87% случаев была врачебная линейная бригада, в 13% — фельдшерская бригада. Передача вызова специализированной бригаде связана с необходимостью проведения ТЛТ или с необходимостью коррекции нестабильных клинических либо гемодинамических показателей пациента.
Специализированные и врачебные общепрофильные бригады СМП укладываются в рекомендуемые 90 мин для проведения эффективного тромболизиса, но в связи с несвоевременным или поздним вызовом больным СМП это время увеличивается на 86 мин.
СИ и ОВ являются основными временными показателями-предикторами исхода заболевания в группе больных ОКС с подъемом сегмента ST с ТЛТ (табл. 3).
Вероятность летального исхода увеличивается при увеличении времени от дебюта заболевания в группе больных ОКС с подъемом сегмента ST и ТЛТ свыше 88 мин.
Для ОВ точки отсечения распределились следующим образом (рис. 6):
Вероятность летального исхода достоверно увеличивается при времени ОВ в группе ИМпST + ТЛТ, превышающем 85 мин.
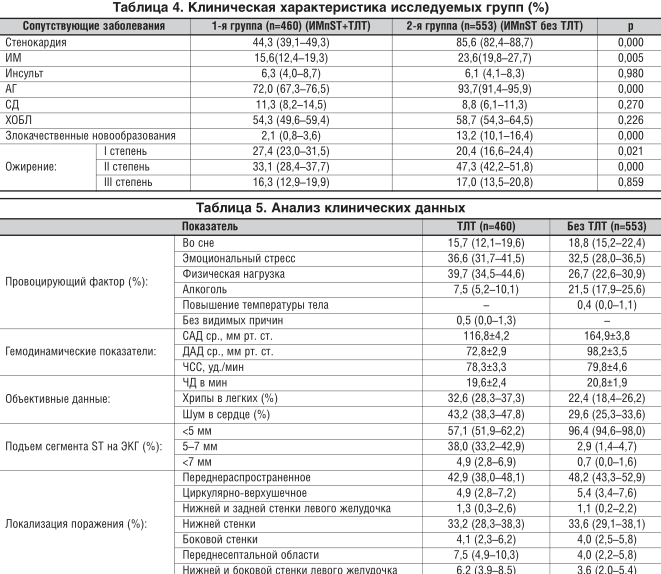
Больные с ОКС, включенные в исследование, страдали артериальной гипертензией (АГ), стенокардией, у 10% был сахарный диабет (СД) 2-го типа, 81% имели ожирение. Сопутствующие соматические заболевания отмечены более чем у половины больных, при этом наиболее часто встречались пациенты с хронической обструктивной болезнью легких (ХОБЛ) (табл. 4). Основными факторами развития клинической картины заболевания в группах являлся физический или/и эмоциональный стресс, а ангинозные боли появлялись и во сне. У 7,5% больных ОКС с подъемом сегмента ST с ТЛТ и у 21,5% пациентов с ОКС с подъемом сегмента ST без ТЛТ провоцирующим фактором был алкоголь (табл. 5).
Уровни систолического (САД) и диастолического (ДАД) артериального давления в группе больных ОКС с подъемом сегмента ST с ТЛТ были существенно ниже по сравнению с группой ОКС с подъемом сегмента ST без ТЛТ. У пациентов обеих групп преобладали ЭКГ-признаки распространенного поражения передней стенки левого желудочка, при этом в группе пациентов, кому была проведена ТЛТ, чаще встречались случаи с подъемом сегмента ST на 5 и более мм.
Положительный результат качественного теста на содержание тропонина Т и/или I получен у больных в группе с ТЛТ в 92,4%, без ТЛТ — в 93,0% случаев.
В группе ОКС с подъемом сегмента ST с ТЛТ изначально больные отмечали дискомфорт в 16,5%, средние по интенсивности боли — в 25,2% и сильные боли — в 58,3% случаев. На 90-й мин у 27,6% больных боли купированы, у 4,7% сохранились сильные боли, у 11% — боли средней интенсивности, у 56,7% пациентов осталось ощущение дискомфорта. У больных ОКС с подъемом сегмента ST без ТЛТ сильный характер указан в 45%, дискомфорт — в 22%, средние по интенсивности боли — в 33%, на 90-й мин от начала лечения боли купированы у 13,2% пациентов, сильные боли сохранились у 23%, у 17,6% отмечены боли средней интенсивности и у 46,2% — ощущение дискомфорта.
На догоспитальном этапе положительная динамика по ЭКГ-признакам наблюдалась у 63% пациентов группы ОКС с подъемом сегмента ST с ТЛТ и 38% больных — группы ОКС с подъемом сегмента ST без ТЛТ (р<0,01). На 30-й день с момента заболевания прерванный ИМ зафиксирован у больных с ТЛТ в 12,9%, без ТЛТ — в 5,2% случаев (р<0,01), развитие Q-образующего ИМ в группе с ТЛТ — в 75,6%, в группе без ТЛТ — в 94,5% (р<0,01), рецидив нефатального ИМ в группе с ТЛТ нами отмечен в 1,5%, а в группе без ТЛТ — в 15,4% случаев (р<0,01).

Неосложненное клиническое течение ИМ (без летальных случаев, рецидивов, прогрессирования недостаточности кровообращения, сложных нарушений ритма и проводимости): в группе с ТЛТ — у 51,2% , в группе без ТЛТ — у 19,8% больных (р<0,01). У 25,2% пациентов с ТЛТ зафиксированы реперфузионные аритмии, а у больных без ТЛТ они отмечены в 5,5% случаев (р<0,01).
В группе больных без ТЛТ уровень 30-дневной летальности составил 85,4%, против 50% у больных с ТЛТ(р<0,001). Общая летальность в группе больных с ТЛТ составила 13,5%, а в группе без ТЛТ — 27,4% (р=0,000). Это составляет 15 спасенных жизней на 100 пациентов, при этом шанс выжить при использовании ТЛТ повышается в 2,4 раза.
В заключение следует отметить, что наше исследование подтвердило зависимость выживаемости больных с ОКС от времени обращения за медицинской помощью. Проведение тромболизиса медиками СМП в течение первых 90–120 мин от появления симптомов рекомбинантными препаратами человеческого тканевого активатора плазминогена является безопасным и позволяет снизить смертность от ОКС с подъемом сегмента ST: 13,5% в группе с ТЛТ по сравнению с 27,4% — в группе без ТЛТ.

Источник
