Ступенчатая терапия хронического болевого синдрома

Боль часто является ведущим симптомом при онкологическом заболевании. Она может быть настолько интенсивной, что бывает просто нестерпимой для пациента. Адекватное обезболивание становится актуальной проблемой для больного и его близких людей.
Лечение ХБС основано на конкретных принципах, соблюдение которых даст положительный результат. Они гласят:
- Незамедлительное начало фармакотерапии при первых же проявлениях боли!
- Препараты и дозировки подбираются ИНДИВИДУАЛЬНО, учитывая характеристики, локализацию и интенсивность болевых ощущений, добиваясь их полного устранения или максимального облегчения состояния пациента.
- Назначение анальгетиков «строго по часам», а не по требованию больного, то есть принимать лекарство не тогда, когда появляется боль, а по расписанию, поддерживая постоянную концентрацию активных веществ в крови.
- Препараты принимают «по восходящей», то есть от самых высоких доз слабых анальгетиков к минимальным дозам сильнодействующих средств.
- Отдавать предпочтение следует не инвазивным фармакологическим формам (капсулы, пластырь и т.д.)
Важно понимать, что на «высоте боли» купировать её очень сложно, поэтому нельзя допускать таких ситуаций!
В России препаратом первой линии в большинстве случаев является Трамадол. Далее пациента переводят на Морфин. Нередко сразу используют внутримышечный путь введения опиоидов. Уколы делаются в ягодичную или дельтовидную мышцу. Инъекция в руку позволяет достичь более быстрого проникновения активного вещества. У внутримышечного введения есть ряд минусов:
- болезненность укола, особенно при повторных инъекциях в одну и туже область (количество введений в сутки может достигать 6 -8 раз и более);
- короткое, по сравнению с пероральным приёмом, действие;
- инфильтрация мягких тканей, что может привести к фиброзным изменениям в мышцах или формированию абсцессов.
В зарубежной практике давно отдано предпочтение трансдермальным терапевтическим системам (ТТС), которые обеспечивают постоянное поступление активного вещества через кожные покровы в кровь. Одного пластыря хватает на 72 часа.
Однако, российские пациенты редко получают пластыри (государство не обеспечивает их необходимого количества). И поэтому наибольшей популярность среди больных на сегодняшний день пользуется метод внутривенной контролируемой анальгезии. Он заключается в том, что человек сам делает себе инъекции по мере необходимости, когда он чувствует усиление боли. При стабилизации болевого синдрома, временной промежуток между введениями растягивается. Преимущества метода следующие:
- полноценное обезболивание, исходя из индивидуальных особенностей и нужд пациента;
- быстрый результат с применением малых доз;
- редкое появление нежелательных реакций;
- положительный психологический момент, так как онкобольной знает, что при необходимости, всегда сможет самостоятельно купировать боль;
- отпадает необходимость привлечения третьих лиц (людей, ухаживающих за больным или медицинских работников).
Как подобрать оптимальную дозу препарата — главный вопрос, который решает врач, занимающейся обезболиванием. Следует понимать, что дозировки сильно различаются у разных пациентов. Подбор медикамента и дозы зависит от многих факторов. Общий статус больного человека должен оцениваться комплексно: учитывается возраст, наличие и выраженность соматической патологии, психоэмоциональный фон, состояние ЦНС и т.д.
У пожилых людей, ослабленных больных и лиц, с заболеваниями головного мозга начальные дозы морфина должны быть ниже на 25-50% от рекомендуемых показателей. Следует знать, что один и тот же препарат будет по-разному действовать на разных пациентов. Некоторые больные по ряду причин лучше реагирует на конкретный анальгетик, чем на его аналоги. Поэтому подбор медикамента может занять какое-то время. Когда выбор будет сделан, преступают к этапу «титрования дозы». Он заключается в назначении стандартной «стартовой» дозировки, с её изменением в большую или меньшую сторону, в зависимости от степени анальгезии и появления побочных эффектов. После установления оптимальной суточной дозы, расписывается схема приёма препарата. Иногда больному может понадобиться дополнительный укол между регулярными инъекциями, например при «прорыве боли».
ВАЖНО понимать: лечение ХБС должно постоянно контролироваться специалистом! В нашей стране эта функция в большинстве случаев возлагается на участковых терапевтов. Если «повезёт» и в поликлинике по месту жительства, куда «прикреплён» пациент будет онколог, то заниматься данной проблемой будет он.
Часто из-за безграмотного назначения анальгетиков или самолечения, что в данном случаи вообще НЕДОПУСТИМО!!!, онкобольной попадает в «порочный круг». Что это значит: изначально пациент не получил адекватного обезболивания, что повлекло усиление боли, вследствие чего повысилась дозировка, а вместе с ней и побочное влияние препарата, состояние пациента ухудшилось, а боль осталась. Особенно важно, чтобы грамотную помощь получали дети и люди, с ограниченными возможностями коммуникации (психически больные, немые и т.д.), ведь они не могут подробно описать, что с ними происходит и часто вынуждены терпеть боль.
Если фармакотерапия, являющаяся первым звеном в лечении ХБС, не помогает или исчерпала свои возможности, её можно дополнить другими видами помощи. Итак, этапы лечения болевого синдрома:
1. Фармакологические средства (если в течение 1-3 дней не удаётся добиться стойкого положительного результата и подобрать «рабочую» эффективную схему терапии, переходят к следующему шагу);
2. Фармакотерапия + электроанальгезия и другие физические способы + детоксикация (на достижение желаемого эффекта отводится 3-5 дней);
3. К вышеописанным методам добавляют регионарные блокады.
Лечение ХБС проводится всегда КОМПЛЕКСНОЕ. Помимо самих анальгезирующих средств, врач назначает адъювантные препараты, которые помогают анальгетикам, либо сами обладают обезболивающим действием. Основными группами являются:
- трициклические антидепрессанты;
- бензодиазепины;
- антиконвульсанты;
- агонисты альфа2-рецепторов;
- кортикостероиды;
- антигистаминные лекарства;
- бисфосфонаты;
- кофеин и другие.
Все эти медикаменты назначаются исключительно доктором, после осмотра пациента и оценки всех имеющихся факторов. Не стоит забывать о таких понятиях, как толерантность (устойчивость) и зависимость (физическая и психическая) от наркотических анальгетиков и сильнодействующих препаратов. (об этих проблемах я буду писать в своих следующих статьях).
Источник
Содержание
Терапия слабой боли — I ступень ВОЗ
Терапия умеренной боли — II ступень лестницы обезболивания ВОЗ
Терапия сильной боли — III ступень лестницы обезболивания ВОЗ
Представляем фрагмент брошюры для врачей «Обезболивание в паллиативной помощи. Практическое руководство для врача», подготовленной благотворительным фондом «Вера». Полная версия брошюры доступна для скачивания по ссылке.
Терапия слабой боли — I ступень лестницы обезболивания ВОЗ
- В каждом конкретном случае необходимо соотносить возможные риски с пользой.
- Парацетамол может быть назначен всем пациентам, если он эффективен и к нему нет противопоказаний; парацетамол усиливает действие опиоидов, но гепатотоксичен.
- При деменции препарат выбора для обезболивания — парацетамол, в случае его неэффективности пациента переводят на морфин (НПВС и трамадол не рекомендуются).
- НПВС показаны при боли, имеющей в своем патогенезе воспалительный компонент (например, при болях в костях). НПВС высокоэффективны, но обладают серьезными побочными эффектами: способствуют образованию язв ЖКТ, усиливают почечную, печеночную недостаточность, повышают риск развития бронхоспазма, гипертонии, инфаркта миокарда и инсульта (особенно у пожилых пациентов).
- Пациенты, получающие глюкокортикоиды, уже находятся в группе высокого риска развития осложнений со стороны ЖКТ; одновременный прием аспирина также значительно повышает риск кровотечения.
- Пациенты, получающие паллиативную помощь, могут иметь недиагностированную почечную недостаточность, прогрессирующую в ходе лечения, в связи с чем необходим мониторинг функции почек; НПВС при этом следует использовать с осторожностью.
- Новые НПВС, селективно ингибирующие циклооксигеназу-2 (ЦОГ-2), могут применяться один раз в день, что позволяет снизить общий объем потребляемых препаратов.
Адъювантная и симптоматическая терапия ХБСРекомендации по назначению адъювантных средств для симптоматической терапии

Нестероидные противовоспалительные препараты для терапии слабой боли (I ступень лестницы обезболивания ВОЗ)
* Анальгин (метамизол натрия) — нет однозначных данных об отнесении данного препарата к НПВС, его назначают при непереносимости других НПВС и парацетамола, не следует сочетать с другими НПВС в течение длительного времени.
Терапия умеренной боли — II ступень лестницы обезболивания ВОЗ
В качестве второй ступени лестницы обезболивания ВОЗ рекомендует кодеин в дозе 30–60 мг 4 раза в день, назначае мый одновременно с парацетамолом. В России нет кодеина в дозировках, необходимых для лечения умеренной боли. Поэтому основным слабым опиоидным анальгетиком является трамадол или трамадол в сочетании с парацетамолом (залдиар). Максимальная суточная доза трамадола составляет 400 мг, у пациентов старше 65 лет — 300 мг. К слабым опиоидам также относятся отечественные препараты: тримеперидин (промедол) и пропионилфенилэтоксиэтилпиперидин (просидол), которые в 2–3 раза слабее морфина. С 2018 года для клинического применения появился новый опиоидный анальгетик тапентадол (палексия), который также в 2–3 раза слабее морфина и назначается для терапии умеренной боли в дозах 50–200 мг/сут.

Опиоидные анальгетики для терапии умеренной боли (II ступень лестницы обезболивания ВОЗ)
* 150, 200 мг только для таблеток трамадола продленного действия.
** Для пациентов старше 65 лет максимальная суточная доза трамадола 300 мг.
*** Для умеренной боли максимальная суточная доза тапентадола до 200 мг, тогда как при сильной боли она составляет 500 мг.
**** При умеренной боли рекомендуется не превышать разовую дозу 20 мг и суточную дозу 80 мг, хотя при сильной боли препарат может использоваться в более высоких дозах.
Комментарии
- Доказано, что из-за генетических особенностей метаболизма у 8–10% людей трамадол не эффективен, но может задерживаться в организме, вызывая тошноту, заторможенность и т.п.
- Трамадол и тапентадол нельзя сочетать с антидепрессанами из-за опасности возникновения серотонинового синдрома.
- При плохой переносимости трамадола следует назначать более сильные опиоиды: просидол до 80 мг/сут, тапентадол до 200 мг/сут. Либо можно сразу назначить сильные опиоиды в низких дозах: морфин быстрого или замедленного высвобождения в таблетках или капсулах (от 10 до 30 мг/сут), оксикодон + налоксон (таргин) в таблетках замедленного высвобождения (5–20 мг/сут по оксикодоу) или ТТС фентанила 12,5 мкг/ч, если пациент не может проглотить таблетку.
- Эффективность трамадола следует признать недостаточной, если его разовая доза 100 мг (в капсулах или таблетках быстрого высвобождения) действует менее 4–6 часов на фоне приема НПВС и других адъювантных средств. Длительность действия трамадола в таблетках пролонгированного действия 100 мг и 200 мг должна быть не меньше 12 часов.
- При недостаточной эффективности трамадола следует переходить на обезболивание более сильными опиоидными анальгетиками. Превышать суточную дозу трамадола 400 мг (300 мг у пожилых пациентов) нецелесообразно.
- Как правило, после неэффективности 400 мг трамадола стартовая доза перорального морфина продленного действия составляет 60 мг/сут (1 таблетка 30 мг — 2 раза в сутки), ТТС фентанила 25 мкг/час, оксикодона+налоксон (таргин) в таблетках продленного действия 40 мг/сут по оксикодону (по 20 мг — 2 раза в сутки), тапентадола (палексия) 150–200 мг/сут.
Терапия сильной боли — III ступень лестницы обезболивания ВОЗ
В России для терапии сильной хронической боли применяются сильные опиоидные анальгетики, которые представлены ниже. Возможно назначение четырех неинвазивных препаратов: морфин быстрого и замедленного высвобождения (капсулы и таблетки), таргин (комбинированный препарат оксикодон + налоксон), ТТС фентанила и палексия (тапентадол).
Важно
Предельно допустимое количество наркотического препарата, разрешенное к выписке на 1 рецепт, определено Приложением 1 Приказа МЗ РФ №1175н.
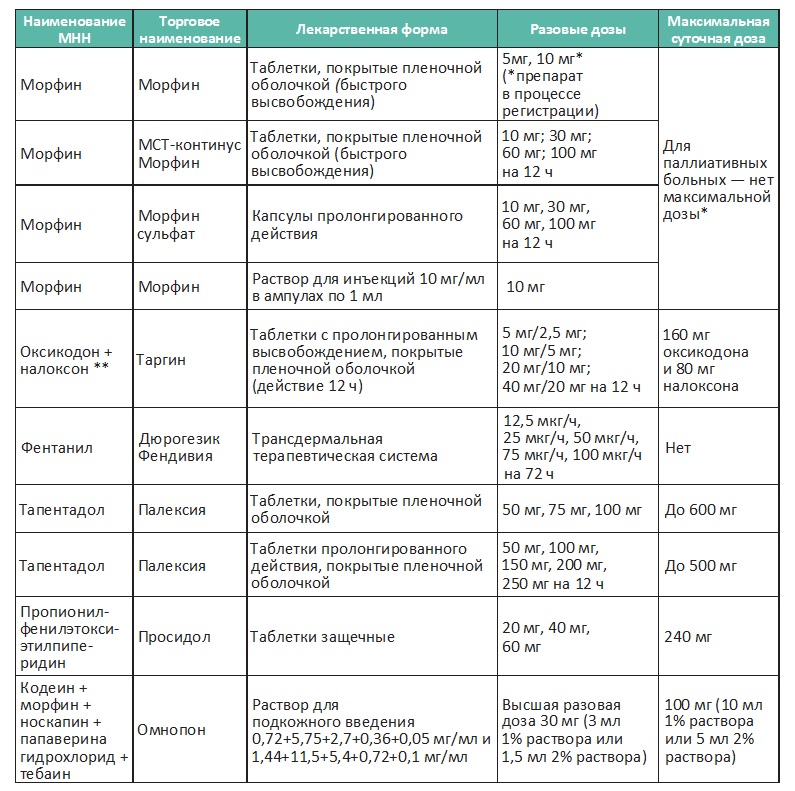
Опиоидные анальгетики для терапии сильной боли (III ступень лестницы обезболивания ВОЗ)
*Морфин в паллиативной медицине не имеет «потолка» анальгетического действия, в отдельных случаях при длительном применении дозы могут возрастать в десятки раз относительно стартовой.
** Оксикодон+налоксон (таргин), тапентадол (палексия) и ТТС фентанила выписываются на рецептурном бланке формы N148-1/у-88.
Читайте дальше: «Нейропатическая боль»
Источник
Хронический болевой синдром (ХБС) — это самостоятельное неврологическое заболевание, характеризующееся длительными болями. Как правило, ХБС возникает вследствие болезни или травмы.
Следует различать боли, обусловленные непосредственно болезнью, и хронический болевой синдром, представляющий собой комплексное расстройство работы ряда органов и систем. «Нормальная», физиологическая боль носит защитный характер. Она стихает одновременно с патологическим процессом, ставшим причиной боли, в то время как симптомы ХБС проявляются независимо от основного заболевания. Именно поэтому современная неврология рассматривает хронический болевой синдром как отдельную проблему, успешное решение которой возможно только при участии специалистов по лечению ХБС, использующих комплексный подход к болезни.
Причины развития
Чаще всего хронический болевой синдром развивается как осложнение заболеваний опорно-двигательного аппарата. Наиболее распространенные причины возникновения ХБС — болезни суставов (остеоартроз, ревматоидный артрит) и фибромиалгия. От хронических болей часто страдают пациенты с туберкулезом позвоночника и различными опухолями.
Считается, что для развития хронического болевого синдрома наличия одного диагноза недостаточно — необходим еще особый тип организации нервной системы. Как правило, ХБС развивается у людей, склонных к депрессиям, ипохондрии, тяжелому пережирванию стрессов.
Важно понимать, что у таких пациентов хронический болевой синдром является проявлением депрессии, ее «маской», а не наоборот, хотя сами больные и их близкие обычно считают именно подавленное настроение и апатию следствием болезненных ощущений.
Не следует, однако, считать хронический болевой синдром проблемой исключительно психологического характера. Психогенная боль, о которой шла речь выше, действительно играет огромную роль в развитии ХБС, но также не менее важны и воспалительный, нейрогенный (обусловленный нарушениями работы нервов, ответственных за передачу болевых импульсов) и сосудистый механизмы формирования хронических болей. Даже такие, казалось бы, далекие от медицины проблемы, как социальная изоляция больных, способны ухудшить течение ХБС. Формируется замкнутый круг: пациент не может встретиться с друзьями, потому что боли в колене или спине не дают выйти из дома, а дефицит неформального общения приводит к еще большему усилению болевых ощущений.
Отдельную проблему представляет собой хронический болевой синдром у онкологических больных. Как правило, он развивается на поздних стадиях онкологических заболеваний, однако сроки появления болей и их интенсивность зависят не только от локализации новообразования и степени распространенности опухолевого процесса, но и от индивидуальной чувствительности пациента к боли, особенностей его психики и конституции.
Диагностика хронического болевого синдрома
Отправной точкой в диагностике ХБС является беседа врача с пациентом и тщательный сбор анамнеза. Важно, чтобы разговор не сводился к формальному перечислению перенесенных и имеющихся болезней: такие события, как смерть близких, потеря работы или даже переезд в другой город заслуживают упоминания не меньше, чем артроз или перенесенное год назад растяжение связок.
Для оценки интенсивности болевых ощущений пациенту может быть предложена шкала вербальных оценок (ШВО) или визуально-аналоговая шкала (ВАШ). Использование этих шкал позволяет врачу понять, насколько серьезна проблема боли для конкретного пациента, и подобрать наиболее подходящий вариант терапии.
Важный этап диагностики хронического болевого синдрома — определение механизма, играющего ключевую роль в формировании ХБС. От того, окажется ли он психогенным, нейрогенным или каким-либо другим, зависит стратегия лечения.
Боль у онкологических больных
У пациентов онкологического профиля болевой синдром может быть связан не только с самим заболеванием, но и с процессом его лечения. Так, хирургические вмешательства нередко приводят к развитию фантомных болей и спаек, химиотерапия повреждает нервную систему и провоцирует развитие болей в суставах. Кроме того, само по себе тяжелое состояние и необходимость соблюдения постельного режима являются факторами риска развития ХБС: у прикованных к кровати больных часто развиваются пролежни. Определение причины усиления болей у тяжелого онкологического пациента является первым шагом на пути к облегчению его состояния и повышению качества жизни.
Лечение хронического болевого синдрома
ХБС — это комплексное заболевание, в основе которого лежит сразу несколько механизмов.
Эффективность традиционных обезболивающих (прежде всего, нестероидных противовоспалительных препаратов, НПВП) при лечении хронического болевого синдрома невелика: они лишь незначительно снижают интенсивность болевых ощущений или не помогают вовсе. Дело в том, что НПВП способны воздействовать лишь на некоторые механизмы развития хронического болевого синдрома, например, на воспаление.
Чтобы повлиять на процессы, идущие непосредственно в центральной нервной системе, пациентам назначают препараты других групп, прежде всего антидепрессанты.
Медикаментозная терапия является лишь одним из направлений комплексного лечения ХБС. Для борьбы с хронической болью активно применяется физио- и психотерапия, техники аутотренига и релаксации. Борьба с основным заболеванием, например, остеоартрозом, играет важную, но не решающую роль в лечении ХБС.
Стратегия лечения хронического болевого синдрома у онкологических больных несколько отличается. Помимо медикаментозных и психотерапевтических методов борьбы с болью им также показано паллиативное лечение: комплекс мер, направленных на повышение качества жизни и минимизацию ущерба, который опухолевый процесс наносит организму. Например, очистка крови от опухолевых токсинов или хирургическое удаление части опухолевой массы могут улучшить самочувствие и, как следствие, стабилизировать эмоциональное состояние, что естественным образом приведет к уменьшению выраженности болей.
Кроме того, для онкологических больных разработаны специальные схемы медикаментозного обезболивания, позволяющие эффективно купировать болевой синдром и повысить, насколько это возможно, качество жизни.
Источник
