Сколько живут с синдромом аперта
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 25 декабря 2015;
проверки требуют 12 правок.
Синдром Апера (Аперта) (акрокраниодисфалангия, акросфеносиндактилия, акроцефалосиндактилия) — врожденная аномалия развития черепа, которая сочетается с отклонением развития кистей рук. Раннее закрытие венечного и стреловидного швов способствует деформации черепа, что приводит к внутричерепной гипертензии[1]. Синдром Апера является одной из форм акроцефалосиндактилии[прим. 1].
Впервые это заболевание описал французский педиатр Эжен Аперт в 1906 году[2]. Заболевание встречается у одного новорожденного на 160 000—200 000[3].
Этиология[править | править код]
Акрокраниодисфалангия — заболевание с аутосомно-доминантным типом наследования[прим. 2]. У детей, родители которых страдают синдромом Аперта, вероятность унаследовать заболевание равна 50%. В 1995 году были опубликованы доказательства, судя по которым, причиной возникновения данного синдрома является нарушение работы фибробластов генов 10-й хромосомы человека[4].
Признаки и симптомы[править | править код]
Синдактилия двух пальцев у младенца
Одним из признаков заболевания является то, что краниосиностоз[прим. 3] сочетается с брахикефалией. В связи с преждевременным срастанием коронарных швов увеличивается внутричерепное давление, что обычно приводит к умственной отсталости. Немаловажными признаками синдрома являются высокий, выпуклый лоб, плоское или вогнутое лицо, в результате чего наблюдается нарушение костей лицевого черепа, что приводит к деформации челюсти, а также синдактилия рук и ног с вовлечением 2, 3 и 4-го пальцев.
Лечение[править | править код]
Радикальных методов лечения не существует.
Симптоматическое лечение данной патологии заключается в хирургическом увеличении объёма черепа, коррекция синдактилии и полидактилии.
Хирургическое лечение включает в себя раннюю краниоэктомию коронарного шва и фронто-орбитальную репозицию для уменьшения проявлений дисморфизма и патологических изменений формы черепа. Операции по поводу синдрома Апера часто состоят из нескольких этапов, последний проводится в подростковом возрасте. Первый этап часто выполняется уже в 3 мес.[5]
Консервативные методы лечения применяют для разработки суставов. Также, для стимуляции психического развития назначают ноотропные препараты: аминалон, пирацетам и другие[1], использовались в эпоху развития науки до проверки лечения методами доказательной медицины.
Примечания[править | править код]
- ↑ Акроцефалосиндактилия — группа наследственных пороков развития черепа и пальцев.
- ↑ Аутосомно-доминантный тип наследования — тип наследования, при котором мутантный аллель доминирует над нормальным аллелем, в связи с чем болезнь или признаки болезни ярко выражены.
- ↑ Краниосиностоз — преждевременное сращение некоторых костей черепа.
Источники[править | править код]
- ↑ 1 2 Л.О. Бадалян. Детская неврология. — Москва: Медицина, 1984. — С. 347—349. — 576 с.
- ↑ Apert’s syndrome (whonamedit.com) (англ.). Дата обращения 13 августа 2010. Архивировано 6 мая 2012 года.
- ↑ Kaplan, L C. Clinical assessment and multispecialty management of Apert syndrome (англ.) // Clinics in plastic surgery : journal. — 1991. — April (vol. 18, no. 2). — P. 217—225. — ISSN 00941298. — PMID 2065483.
- ↑ Wilkie, A O; S. F. Slaney, M. Oldridge, M. D. Poole, G. J. Ashworth, A. D. Hockley, R. D. Hayward, D. J. David, L. J. Pulleyn, P. Rutland. Apert syndrome results from localized mutations of FGFR2 and is allelic with Crouzon syndrome (англ.) // Nature genetics : journal. — 1995. — February (vol. 9, no. 2). — P. 165—172. — doi:10.1038/ng0295-165. — PMID 7719344.
- ↑ Синдром Апера: клинические проявления и этиология — Интернет-сообщество нейрохирургов Росcии. neuro-online.ru. Дата обращения 4 марта 2017.
Источник
Что такое синдром Аперта?
Синдром Аперта (синдром Апера или акроцефалосиндактилия 1 типа) — редкое генетическое заболевание, возникающее при рождении. У больных с синдромом Аперта появляются характерные пороки развития черепа, лица, рук и ног.
Синдром Апера характеризуется краниосиностозом, состоянием, при котором фиброзные суставы (швы) между костями черепа преждевременно закрываются. Это может вызвать поражение лицевых костей и привести к тому, что верхняя часть головы будет выглядеть заостренной. При болезни может наблюдаться сращивание пальцев рук или ног. Пострадавшие дети также могут иметь интеллектуальные нарушения. Серьезность симптомов варьируется.
Синдром Аперта почти всегда является результатом новых генетических изменений (мутаций), которые происходят случайно. Редко болезнь наследуется по аутосомно-доминантному типу. Больные с синдромом могут проходить терапию, направленную на конкретные симптомы, включая реконструктивную хирургию черепа, лица, рук, ног.
Признаки и симптомы

Синдром Аперта характеризуется краниосиностозом, преждевременным закрытием фиброзных суставов (швов) между определенными костями черепа. У детей без краниосиностоза швы позволяют голове расти и расширяться. Затем, эти кости сливаются воедино, образуя череп.
У людей с краниосиностозом мозг все еще растет после преждевременного закрытия этих швов.
Возникающее давление при росте головного мозга может привести к тому, что различные кости черепа и лица деформируются во время развития.
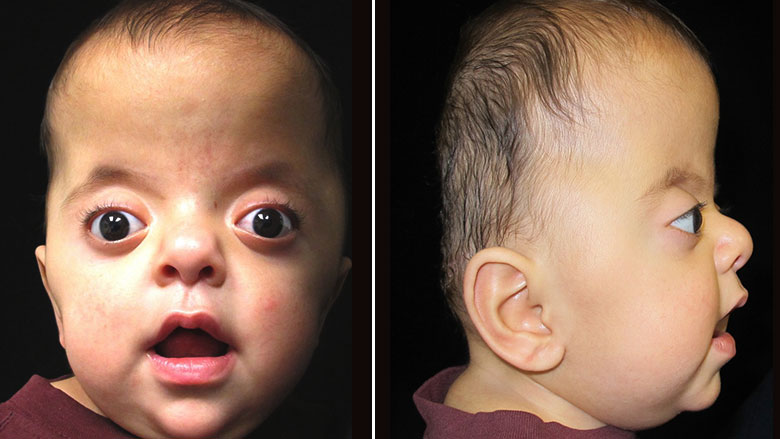
В зависимости от того, какие швы преждевременно закрываются, варьируется степень их тяжести. У большинства больных людей происходит преждевременное закрытие швов между костями, образующими лоб и верхнюю часть черепа. Это приводит к тому, что голова с рождения становится заостренной на верхней части (акроцефалия). Вдобавок, задняя часть черепа может выглядеть сплющенной, с высоким и широким лбом (см. фото выше). На черепе может быть большой «родничок» с поздним закрытием.
У некоторых больных также может быть гидроцефалия, при которой в полостях головного мозга накапливается спинномозговая жидкость. Это может вызвать внутричерепное давление.
Лицевые кости тоже могут быть поражены краниосиностозом. Это может привести к характерным дефектам лица. У пациентов с синдромом Аперта часто наблюдаются широко расставленные глаза (гипертелоризм), выпученные глаза (экзофтальм) или наклоненные вниз глазные щели. У них также могут быть слаборазвитые срединно-лицевые области (гипоплазия верхней челюсти) и расщелина нёба. Правая и левая стороны лица могут быть не симметричными.
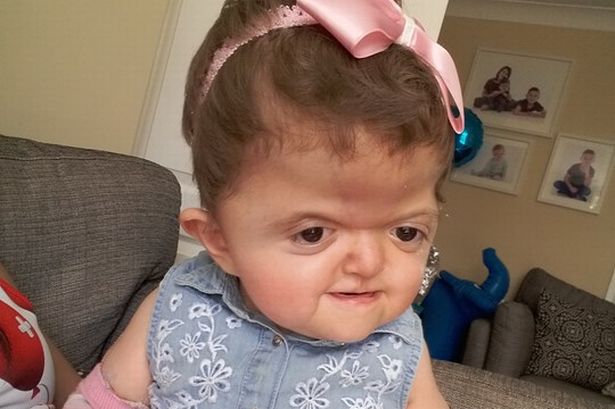
Люди с болезнью могут иметь сплющенный нос с низкой переносицей. У людей бывает задержка роста зубов, скученность зубов или открытый прикус.
Если отверстия между носом и горлом сужены или заблокированы, или трахеальный хрящ поврежден, это может помешать дыханию и глотанию. Люди с этими проблемами могут иметь инфекции верхних дыхательных путей, апноэ во сне, недоедание.
Синдром Аперта имеет несколько характерных пороков развития кисти и стопы. У пострадавших людей могут быть короткие, широкие и большие пальцы ног, отклоняющиеся наружу. Они также могут иметь частичное или полное слияние (синдактилию) определенных пальцев рук и ног. Многие больные люди имеют полное слияние костей второго и четвертого пальцев и один единственный сплошной ноготь («варежкообразная» синдактилия). Однако возможны и другие слияния.
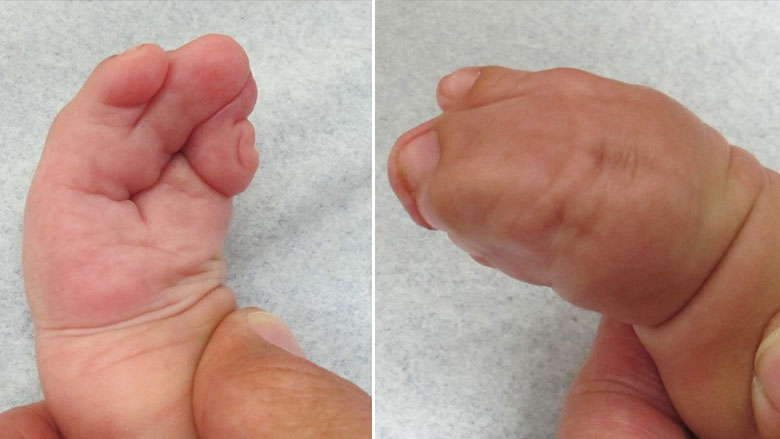
Суставы пальцев становятся жесткими к четырем годам. В ногах синдактилия также обычно затрагивает вторые, третьи и четвертые пальцы. Ногти на ногах могут быть частично непрерывными или отдельными. Как правило, синдром поражает верхние конечности сильнее, чем нижние.
Синдром Аперта может влиять и на другие системы органов (см. таблицу).
| Скелетная система |
|
| Нервная система |
|
| Уши |
|
| Сердечно-сосудистая система |
|
| Брюшная полость |
|
| Почки и мочеполовая система |
|
Причины
Синдром Аперта возникает в результате изменения (мутации) гена рецептора фактора роста фибробластов 2 (англ. Fibroblast growth factor receptor 2, сокр. FGFR2). Этот ген играет важную роль в развитии скелета. Гены предоставляют инструкции для создания белков, играющих разные роли в организме. Когда происходит мутация гена, белковый продукт может не работать должным образом. При синдроме Апера мутации в FGFR2 приводят к тому, что эти рецепторы неправильно связываются с факторами роста фибробластов. Это влияет на формирование нормальных швов в мозге и может препятствовать развитию многих других структур в организме. Это неправильное образование является причиной пороков развития, наблюдаемых при синдроме Аперта.
Почти у всех зарегистрированных пациентов расстройство было вызвано одной из двух специфических мутаций гена FGFR2. (Эти мутации обозначены как «Ser252Trp» и «Pro253Arg».) Эти мутации могут вызывать слегка отличающиеся проявления, включая степень выраженности синдактилии (сращивание пальцев). Различные мутации в гене FGFR2 могут вызывать несколько других связанных расстройств, включая синдром Пфайффера, синдром Крузона и синдром Джексона-Вейсса.
У 95% пациентов синдром Апера возникает в результате новой мутации в гене FGFR2. Эти новые мутации появляются случайно по неизвестным причинам (спорадически). Сообщалось, что отдельные случаи заболевания связаны с увеличением возраста отца.
Редко синдром наследуется по аутосомно-доминантному типу. Доминантные генетические нарушения возникают, когда необходима только одна копия мутации, чтобы вызвать конкретное заболевание. Риск передачи мутации от больного родителя к потомству составляет 50% для каждой беременности. Риск одинаков для мужчин и женщин.
Затронутые группы населения
Синдром Аперта, по оценкам, встречается примерно у одного из 65 000 новорожденных. Мужчины и женщины болеют в относительно равных количествах. С тех пор, как расстройство было первоначально описано в 1894 и 1906 годах было зарегистрировано более 300 новых случаев. Сообщалось, что у людей из Азии самый высокий уровень заболеваемости данным синдромом.
Диагностика
Диагноз чаще всего ставится при рождении или в младенчестве. Пациенты диагностируются посредством клинической оценки и различных специализированных тестов. Определяются физические признаки, такие как аномалии лица или синдактилия.
Скелетные аномалии и врожденные пороки сердца обнаруживаются с помощью визуализации, например компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ). Нарушение слуха может быть обнаружено во время исследования слуха у новорожденного.
Люди могут также пройти тест на мутации в гене FGFR2, что может обеспечить генетическим диагнозом синдрома Апера.
В некоторых случаях признаки синдрома Аперта могут быть обнаружены до рождения. Это можно сделать с помощью пренатального 2D или 3D ультразвукового исследования или магнитно-резонансной томографии (МРТ). Ультразвуковое исследование (УЗИ) — неинвазивная процедура, позволяющая получить изображение плода. Процедура может обнаружить различия в форме черепа, аномалии лица и синдактилию. МРТ плода может обеспечить большую детализацию мозга плода, чем УЗИ.
Схожие по симптомам расстройства
Симптомы следующих расстройств могут быть похожи на симптомы синдрома Аперта. Сравнения могут быть полезны для дифференциальной диагностики.
- Синдром Карпентера — редкое генетическое заболевание, связанное с краниосиностозом, полидактилией или синдактилией. Макушка головы может казаться необычно заостренной (акроцефалия) или голова может казаться короткой и широкой (брахицефалия). Вдобавок, черепные швы часто сливаются неравномерно, в результате чего голова и лицо кажутся асимметричными от одной стороны к другой. В некоторых случаях присутствуют дополнительные физические отклонения, такие как низкий рост, врожденные пороки сердца, легкое или умеренное ожирение, пупочная грыжа или крипторхизм. Многие люди с расстройством страдают от легкой до умеренной умственной отсталости.
- Синдром Крузона — редкое наследственное заболевание, связанное с краниосиностозом. У людей с синдромом Крузона также имеются пороки развития средней части лица, выпуклые глаза и закупорка дыхательных путей, приводящие к затруднению дыхания и глотанию. У некоторых больных голова очень большая (гидроцефалия). Синдром Крузона обычно не связан с умственной отсталостью или проблемами затрагивающими руки, ноги, кисти или ступни. Синдром Крузона вызывается изменениями в одном из генов FGFR, обычно FGFR2, и наследуется по аутосомно-доминантному типу.
- Синдром Джексона-Вейсса (СДВ) — редкое наследственное заболевание, характеризующееся краниосиностозом и аномалиями ног. Диапазон и серьезность симптомов и признаков сильно различаются, даже среди затронутых членов одной семьи. Первичные признаки могут включать необычно плоские, недоразвитые срединно-лицевые области (гипоплазия средней части лица), аномально широкие большие пальцы ног и/или порок развития или слияние определенных костей в ступнях. СДВ может возникать спорадически или наследоваться по аутосомно-доминантному типу.
- Синдром Пфайффера — редкое генетическое заболевание, характеризующееся краниосиностозом и аномально широкими и отклоненными медиально большими пальцами рук и ног. У большинства пострадавших также наблюдаются выпученные глаза и кондуктивная потеря слуха. Существует три формы синдрома Пфайффера. Типы II и III являются более серьезными. Синдром Пфейффера является аутосомно-доминантным расстройством, связанным с мутациями в генах FGFR2 и FGFR1.
Лечение
Лечение синдрома Аперта варьируется в зависимости от того, какие симптомы наблюдаются у больного. Лечение может потребовать ухода со стороны группы медицинских специалистов, включая педиатров и хирургов, нейрохирургов, врачей, специализирующихся на заболеваниях скелета, суставов и мышц (ортопедов), врачей, специализирующихся на заболеваниях ушей, носа и горла (отоларингологов), врачей, специализирующихся на нарушениях сердечной деятельности (кардиологов).
Специальные методы лечения синдрома Аперта являются симптоматическими и поддерживающими. Краниосиностоз и гидроцефалия могут привести к ненормально повышенному давлению внутри черепа и мозга. В таких случаях для коррекции краниосиностоза может быть рекомендовано раннее хирургическое вмешательство (в течение 2-4 месяцев после рождения). Для пациентов с гидроцефалией операция может также включать введение трубки (шунта) для оттока избыточной спинномозговой жидкости (СМЖ) из головного мозга. СМЖ сливается в другую часть организма, где он абсорбируется.
Корректирующая и реконструктивная хирургия может быть рекомендована для коррекции черепно-лицевых пороков развития. Хирургия также может помочь исправить полидактилию и синдактилию, а также другие скелетные дефекты или физические отклонения. Для больных с врожденными пороками сердца может потребоваться лечение определенными препаратами, хирургическое вмешательство и/или другие терапевтические меры. Для некоторых больных с нарушениями слуха полезны слуховые аппараты.
Раннее вмешательство может быть важным для обеспечения того, чтобы дети с синдромом Аперта полностью раскрыли свой потенциал. Специальные терапевтические мероприятия, такие как физиотерапия, трудотерапия и специализированное обучение также будут полезными.
Для пострадавших лиц и их семей рекомендуется генетическое консультирование. Генетический консультант сможет объяснить причины заболевания. Он также может обсудить возможность рождения новых детей с заболеванием. Дополнительно, для всей семьи необходима психосоциальная поддержка.
Прогноз
Прогноз для детей с синдромом Апера зависит от того, насколько серьезным является состояние и на какие системы организма оно повлияло. Заболевание может быть более серьезным, если повлияет на дыхательную систему ребенка или если внутри черепа вырастит давление, но эти проблемы можно исправить хирургическим путем.
Дети с синдромом часто имеют проблемы с обучением. Некоторые дети страдают более серьезно, чем другие.
Поскольку тяжесть болезни может варьироваться в широких пределах, сложно прогнозировать продолжительность жизни. Заболевание может не оказывать существенного влияния на продолжительность жизни ребенка, особенно если у него нет пороков сердца.
Источник
Синдром Апера – генетическое заболевание, характеризующееся нарушениями процессов окостенения черепа и связанными с этим вторичными расстройствами, а также многочисленными пороками развития скелета и конечностей. Симптомами этого состояния являются карликовый рост, башенная форма черепа, расширенная переносица, незаращение твердого нёба, синдактилии на руках и ногах. Диагностика синдрома Апера производится по характерной клинической картине патологии, на основании рентгенологических данных и молекулярно-генетических исследований. Специфического лечения заболевания не существует, применяют поддерживающую терапию, проводят хирургические вмешательства паллиативного характера.
Общие сведения
Синдром Апера (акроцефалосиндактилия 1 типа) – генетическая патология, обусловленная нарушением образования некоторых видов соединительной ткани, главным образом костной. Впервые данное состояние было описано в 1906 году французским педиатром Э. Апером, дальнейшие исследования подтвердили генетическую природу этого заболевания. Этиология и молекулярно-генетические механизмы развития синдрома Апера были определены значительно позднее – лишь в 1995 году. Данная патология может наследоваться по аутосомно-доминантному механизму, однако в подавляющем большинстве случаев ее причиной являются спонтанные мутации в половых клетках родителей (так называемые герминативные мутации).
Синдром Апера с одинаковой частотой поражает как мальчиков, так и девочек, его встречаемость составляет в среднем 1 случай на 160 000-200 000 новорожденных. Врачи-генетики в настоящее время относят синдром Апера к особой группе наследственных заболеваний – акроцефалосиндактилиям, характеризующиеся одновременным поражением костей черепа и конечностей. Особенностью этой патологии является важность ее как ранней диагностики, поскольку паллиативные мероприятия в раннем возрасте могут в значительной степени влиять на дальнейшее интеллектуальное развитие больного.
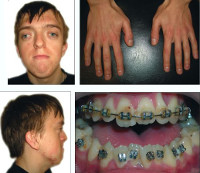
Синдром Апера
Причины синдрома Апера
Синдром Апера, согласно последним научным данным, обусловлен мутациями гена FGFR2, расположенного на 10 хромосоме. Он кодирует белок-рецептор фактора роста фибробластов-2, который оказывает значительное влияние на развитие клеток соединительных тканей, в том числе и костной. Значительный размер (20 экзонов) и специфическое расположение гена делают его уязвимым к различного рода повреждениям, которые затем фенотипически проявляются наследственными заболеваниями. Помимо синдрома Апера дефекты гена FGFR2 приводят к развитию таких патологий, как синдром Бира-Стивенсона, синдром Пфайффера, синдром Сетре-Чотзена, краниофациально-скелетно-дерматологическая дисплазия и ряду других. Поэтому исследования данного гена довольно распространены в современной генетике.
Как показали исследования 1995-2000 годов, наиболее часто (в 96% случаев) к развитию синдрома Апера приводят мутации в области 7 экзона гена FGFR2. При этом на долю мутации S252W приходится порядка 74-76% от всех случаев заболевания, а примерно 21-23% вызываются дефектом P253R. Таким образом, причиной подавляющего большинства случаев синдрома Апера являются всего лишь два типа мутации, что упрощает молекулярно-генетическую диагностику этого состояния. Так как эти дефекты относятся к миссенс-мутациям, полученный в результате трансляции такого гена рецептор к фактору роста фибробластов имеет нарушенную структуру и неспособен выполнять свои функции. Это приводит к нарушению процессов окостенения черепа, в частности – к преждевременному зарастанию швов и остановке нормального роста черепной коробки. Дефект рецепторов при синдроме Апера также становится причиной пороков развития иных структур, где участвуют фибробласты (стенки сосудов крупного калибра, сердце, кости лицевого черепа, трахея). Наследуется это состояние по аутосомно-доминантному механизму, но чаще всего имеют место спонтанные мутации.
Кроме того, при синдроме Апера возникает аномальная экспрессия гена KGFR, тоже расположенного на 10 хромосоме. Он кодирует последовательность белка, являющегося рецептором к фактору роста кератоцитов. Никаких мутаций или других нарушений в структуре KGFR при синдроме Апера выявлено не было, лишь его чрезмерная активность, приводящая к увеличению количества кодируемых им рецепторов. Возможно, это явление объясняется сложными взаимоотношениями генов или же рецептор к фактору роста фибробластов 2 обладает супрессирующим действием на ген KGFR. Результатом аномальной экспрессии этого гена становятся фенотипические нарушения формирования конечностей – различные формы синдактилии, всегда встречающиеся при синдроме Апера, иногда полидактилия.
Симптомы синдрома Апера
Некоторые проявления синдрома Апера заметны с самого рождения – например, синдактилия, которая может быть полной или в виде перепонок. Как правило, срастаются 2, 3 и 4 пальцы на кистях, иногда аналогичный порок возникает и на пальцах ног. Среди неонатологов симптом иногда носит название «среднего пальца» – в тяжелых случаях эти три пальца прочно срастаются между собой и имеют один общий ноготь. Другим постоянным симптомом синдрома Апера, обнаруживающимся сразу после рождения или в первые месяцы жизни, является раннее развитие синостоза костей черепа. Чаще всего происходит срастание венечного или стреловидного шва, что по мере роста головного мозга приводит к деформации черепа по типу «башенной». Из-за черепного синостоза у больных синдромом Апера наблюдается хроническое повышение внутричерепного давления, становящееся причиной задержки умственного развития, головных болей, тошноты и рвоты.
Помимо деформации черепа о наличии синдрома Апера свидетельствует характерный внешний вид больных. У них обычно обнаруживается плоский или выпуклый лоб, гипертелоризм и экзофтальм, может развиваться косоглазие. Деформации затрагивают и кости лицевого черепа – переносица расширена, челюсти нередко недоразвиты, наблюдается нарушение прикуса. Из других симптомов синдрома Апера иногда регистрируются нарушения дыхания (из-за недоразвития верхней челюсти, сужения хоан или трахеи), незаращение твердого нёба, врожденные пороки сердца, аномалии развития позвонков, почек, прямой кишки.
У взрослых лиц, страдающих синдромом Апера, может возникать атрофия зрительных нервов вплоть до полной слепоты. Интеллектуальное развитие больных часто отстает от возрастной нормы, однако достоверно неизвестно, обусловлено это генетическими нарушениями или вторичными факторами (хронической внутричерепной гипертензией). Практически всегда при синдроме Апера наблюдается карликовый рост. При соответствующем паллиативном лечении и уходе больные могут доживать до преклонного возраста, но риск внезапной смерти из-за поражений дыхательной, нервной и сердечно-сосудистой систем у них намного выше, чем в популяции.
Диагностика синдрома Апера
Диагностика синдрома Апера производится на основании осмотра и изучения настоящего статуса пациента, рентгенологических исследований, молекулярно-генетических анализов. При осмотре у больного выявляется синдактилия (у лиц старшего возраста могут обнаруживаться следы ее хирургической коррекции), деформация черепа – башенный череп или брахикефалия, характерный внешний вид лица. С возрастом у больных синдромом Апера могут нарастать признаки нарушения дыхания, при ЭхоКГ нередко определяются пороки сердца и сосудов – стеноз легочного ствола или аорты, дефекты межжелудочковой перегородки. Иногда на этом фоне выявляются признаки сердечной недостаточности. Также возможно наличие иных пороков развития – аномалий позвонков, глухоты, слепоты (из-за катаракты, пигментного ретинита, атрофии зрительных нервов), патологий почек и поджелудочной железы. Из-за столь широкого спектра возможных нарушений больные синдромом Апера нуждаются в тщательном и всестороннем медицинском обследовании.
Рентгенологическими методиками уже у маленьких детей можно обнаружить синостоз костей черепа в области венечного или стреловидного шва. В дальнейшем при помощи рентгенографии можно определить характерную для синдрома Апера деформацию черепной коробки, пороки развития костей лицевого черепа, аномалии позвонков и другие нарушения. Наиболее достоверным диагностическим методом при этом состоянии является молекулярно-генетический анализ. Как правило, для выявления синдрома Апера производят секвенирование 7 экзона гена FGFR2, иногда используют менее затратные техники, ориентированные только на поиск наиболее распространенных мутаций (S252W и P253R), приводящих к этому заболеванию. Подобные методики более дешевые и быстрые в выполнении, обладают точностью на уровне 95%, возможно их использование в качестве пренатальной диагностики этого состояния. Подобный анализ особенно актуален, если посредством профилактических УЗИ у плода выявляются нарушения, предположительно связанные с синдромом Апера – пороки развития черепа, сердца, верхних или нижних конечностей.
Лечение синдрома Апера
Специфического лечения синдрома Апера на сегодняшний день не существует, однако паллиативные и симптоматические мероприятия могут значительно облегчить состояние больного и улучшить качество его жизни. Особенно важно как можно раньше диагностировать это заболевание по той причине, что своевременная хирургическая коррекция черепного синостоза позволит избежать значительного роста внутричерепного давления. По многочисленным данным, после таких операций, произведенных в раннем детстве, признаки умственной неполноценности у больных синдромом Апера были выражены значительно слабее, иногда сохранялся нормальный интеллект. Поэтому борьба с внутричерепной гипертензией играет центральную роль в паллиативном лечении этого состояния. Если же у пациентов имеется умственная отсталость, то ее выраженность снижается путем психокоррекционной работы.
Другой часто выполняемой паллиативной хирургической операцией при синдроме Апера является вмешательство для разделения сросшихся пальцев на руках и ногах. Это относительно несложная процедура при перепончатом типе сращения, однако при более тяжелых формах порока операция значительно усложняется. При синдроме Апера также может потребоваться помощь хирургов в случае пороков сердца, сужения хоан или трахеи, нарушения формирования прямой кишки и других проявлений этого генетического заболевания. Больные нуждаются в регулярных медицинских обследованиях у специалистов различного профиля.
Прогноз и профилактика синдрома Апера
Прогноз синдрома Апера неопределенный по причине очень широкого спектра проявлений и значительного диапазона их выраженности. На прогноз также оказывают влияние такие факторы, как своевременность диагностики заболевания, объем паллиативного и симптоматического лечения. При относительно легких случаях синдрома Апера или правильной терапии этого состояния больные могут доживать до преклонного возраста. При этом возможно снижение интеллекта и появляющиеся с возрастом нарушения все новых органов и систем, что негативно сказывается на качестве жизни пациентов. В тяжелых случаях наблюдается летальный исход в раннем детстве из-за врожденных пороков сердца или полиорганной недостаточности.
Профилактика синдрома Апера возможна только в качестве пренатальной диагностики, которая может производиться как ультразвуковыми методиками, так и путем молекулярно-генетического анализа. Обычно проявления патологии сначала обнаруживаются на профилактических УЗИ, а затем диагноз подтверждается врачом-генетиком. Если данное состояние удается выявить на ранних сроках беременности, то ставится вопрос о ее прерывании.
Источник
