Синдром вторичного индуцированного иммунодефицита презентация

- Размер: 2.2 Mегабайта
- Количество слайдов: 34
Описание презентации Презентация Первичные и вторичные иммунодефицитные состояния по слайдам
 — это нарушения иммунного статуса, которые обусловлены дефектом одного или нескольких механизмов иммунного ответа. Проблема наследственных, или врожденных, первичных иммунодефицитов представляет собой сложную и специальную задачу. Наиболее тяжелые формы выявляются у детей грудного возраста, у которых нарушения иммунной системы представляют собой фактор риска и заканчиваются летальным исходом.
— это нарушения иммунного статуса, которые обусловлены дефектом одного или нескольких механизмов иммунного ответа. Проблема наследственных, или врожденных, первичных иммунодефицитов представляет собой сложную и специальную задачу. Наиболее тяжелые формы выявляются у детей грудного возраста, у которых нарушения иммунной системы представляют собой фактор риска и заканчиваются летальным исходом.
 Различают иммунодефициты, обусловленные: — нарушениями гуморального звена иммунитета (гипо- и агаммаглобулинемии и др. ); — нарушениями функции тимуса и клеточного иммунитета; — комбинированные иммунодефициты; — дефекты фагоцитоза; — дефицит системы комплемента; — дефицит системы интерлейкинов; — аллельные факторы главного комплекса гистосовместимости; — общий вариабельный иммунодефицит.
Различают иммунодефициты, обусловленные: — нарушениями гуморального звена иммунитета (гипо- и агаммаглобулинемии и др. ); — нарушениями функции тимуса и клеточного иммунитета; — комбинированные иммунодефициты; — дефекты фагоцитоза; — дефицит системы комплемента; — дефицит системы интерлейкинов; — аллельные факторы главного комплекса гистосовместимости; — общий вариабельный иммунодефицит.
 связаны с генетическим блоком развития иммунной системы в онтогенезе , который реализуется на различных стадиях развития и дифференцировки стволовой клетки. Основное значение имеют — функциональные и структурные нарушения вилочковой железы — аномалии хромосом (14-й, 18-й, 20-й).
связаны с генетическим блоком развития иммунной системы в онтогенезе , который реализуется на различных стадиях развития и дифференцировки стволовой клетки. Основное значение имеют — функциональные и структурные нарушения вилочковой железы — аномалии хромосом (14-й, 18-й, 20-й).
 Возможны также генетические дефекты мембранных структур. Около 1/3 первичных иммунодефицитов сцеплены с полом и передаются по наследству. Целый ряд подобных состояний может быть обусловлен внутриутробной инфекцией (например, коревой краснухой, когда развивается гиперпродукция Ig. M и дефицит Ig A ). Значимую роль в развитии подобных заболеваний играют вирусы.
Возможны также генетические дефекты мембранных структур. Около 1/3 первичных иммунодефицитов сцеплены с полом и передаются по наследству. Целый ряд подобных состояний может быть обусловлен внутриутробной инфекцией (например, коревой краснухой, когда развивается гиперпродукция Ig. M и дефицит Ig A ). Значимую роль в развитии подобных заболеваний играют вирусы.
 Нарушения гуморального звена иммунной системы могут проявляться в виде селективного дефицита отдельных классов иммуноглобулинов либо в виде комбинированного иммунодефицита. Клиническим примером данной патологии могут быть: — болезнь Брутона (проявляется преимущественно у мальчиков, характеризуется нарушением синтеза иммуноглобулинов); — синдром Блума (нарушение дифференцировки В-лимфоцитов); — гипогаммаглобулинемия с нарушением роста и т. п. Подобные состояния предрасполагают к бактериальным инфекциям, тяжелому течению вирусных заболеваний, нарушениям формирования костной системы и т. п.
Нарушения гуморального звена иммунной системы могут проявляться в виде селективного дефицита отдельных классов иммуноглобулинов либо в виде комбинированного иммунодефицита. Клиническим примером данной патологии могут быть: — болезнь Брутона (проявляется преимущественно у мальчиков, характеризуется нарушением синтеза иммуноглобулинов); — синдром Блума (нарушение дифференцировки В-лимфоцитов); — гипогаммаглобулинемия с нарушением роста и т. п. Подобные состояния предрасполагают к бактериальным инфекциям, тяжелому течению вирусных заболеваний, нарушениям формирования костной системы и т. п.
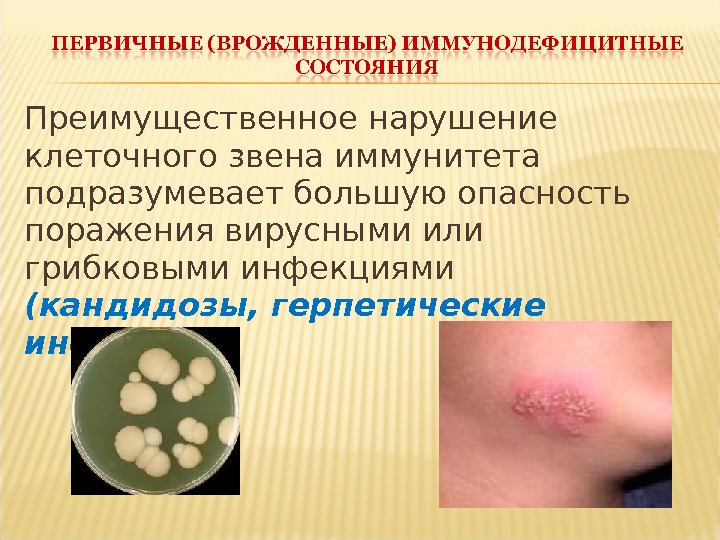 Преимущественное нарушение клеточного звена иммунитета подразумевает большую опасность поражения вирусными или грибковыми инфекциями (кандидозы, герпетические инфекции).
Преимущественное нарушение клеточного звена иммунитета подразумевает большую опасность поражения вирусными или грибковыми инфекциями (кандидозы, герпетические инфекции).

 К основным формам относятся: — синдром Незелофа (уменьшение Т-лимфоцитов в результате полного отсутствия лимфоцитов в вилочковой железе и опустошения тимусзависимых зон в лимфоузлах); — синдром Ди. Джорджи (уменьшение содержания лимфоцитов в результате нарушения эмбрионального развития вилочковой железы); — иммунодефицит при карликовом росте ; -иммунодефицит при синдроме Дауна (Т-клеточный дефицит, усиливающийся по мере развития ребенка).
К основным формам относятся: — синдром Незелофа (уменьшение Т-лимфоцитов в результате полного отсутствия лимфоцитов в вилочковой железе и опустошения тимусзависимых зон в лимфоузлах); — синдром Ди. Джорджи (уменьшение содержания лимфоцитов в результате нарушения эмбрионального развития вилочковой железы); — иммунодефицит при карликовом росте ; -иммунодефицит при синдроме Дауна (Т-клеточный дефицит, усиливающийся по мере развития ребенка).
 Комбинированные иммунодефициты развиваются при сочетании нарушений Т- и В-звеньев иммунитета. Ведущая роль здесь принадлежит дефекту Т-клеток, нарушения В-системы обусловлены как отсутствием супрессорного эффекта, так и усилением его активности.
Комбинированные иммунодефициты развиваются при сочетании нарушений Т- и В-звеньев иммунитета. Ведущая роль здесь принадлежит дефекту Т-клеток, нарушения В-системы обусловлены как отсутствием супрессорного эффекта, так и усилением его активности.
 Подобные иммунодефициты предрасполагают к бактериальным, вирусным и грибковым заболеваниям. Значительные расстройства могут быть летальны уже в детском возрасте. Примеры комбинированных иммунодефицитов: — синдром Луи Бар (связан с дефектом вилочковой железы; — летальный исход обычно вызывают инфекции и злокачественные новообразования; — синдром Вискотта — Олдрича (отмечается опустошение тимусзависимых зон селезенки и лимфатических узлов;
Подобные иммунодефициты предрасполагают к бактериальным, вирусным и грибковым заболеваниям. Значительные расстройства могут быть летальны уже в детском возрасте. Примеры комбинированных иммунодефицитов: — синдром Луи Бар (связан с дефектом вилочковой железы; — летальный исход обычно вызывают инфекции и злокачественные новообразования; — синдром Вискотта — Олдрича (отмечается опустошение тимусзависимых зон селезенки и лимфатических узлов;
 Примеры комбинированных иммунодефицитов: — к летальному исходу приводят инфекции, геморрагии и злокачественные формы); — синдром Гуда (с развитием опухоли вилочковой железы); — иммунодефициты, обусловленные нарушением обмена веществ; — синдром «голых лимфоцитов» (характеризуется отсутствием на мембране лимфоцитов антигенов 1-го класса HLA).
Примеры комбинированных иммунодефицитов: — к летальному исходу приводят инфекции, геморрагии и злокачественные формы); — синдром Гуда (с развитием опухоли вилочковой железы); — иммунодефициты, обусловленные нарушением обмена веществ; — синдром «голых лимфоцитов» (характеризуется отсутствием на мембране лимфоцитов антигенов 1-го класса HLA).
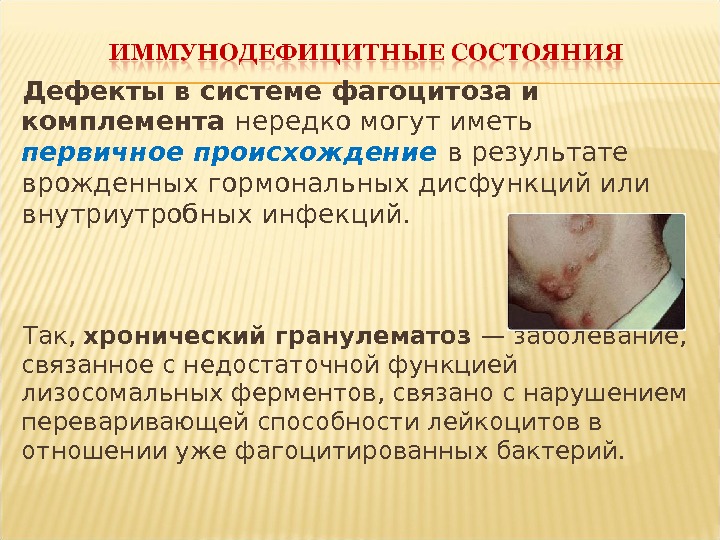 Дефекты в системе фагоцитоза и комплемента нередко могут иметь первичное происхождение в результате врожденных гормональных дисфункций или внутриутробных инфекций. Так, хронический гранулематоз — заболевание, связанное с недостаточной функцией лизосомальных ферментов, связано с нарушением переваривающей способности лейкоцитов в отношении уже фагоцитированных бактерий.
Дефекты в системе фагоцитоза и комплемента нередко могут иметь первичное происхождение в результате врожденных гормональных дисфункций или внутриутробных инфекций. Так, хронический гранулематоз — заболевание, связанное с недостаточной функцией лизосомальных ферментов, связано с нарушением переваривающей способности лейкоцитов в отношении уже фагоцитированных бактерий.
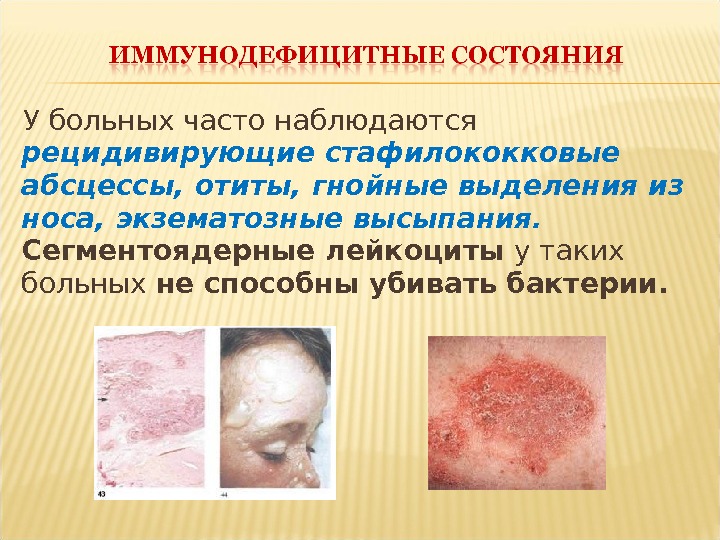 У больных часто наблюдаются рецидивирующие стафилококковые абсцессы, отиты, гнойные выделения из носа, экзематозные высыпания. Сегментоядерные лейкоциты у таких больных не способны убивать бактерии.
У больных часто наблюдаются рецидивирующие стафилококковые абсцессы, отиты, гнойные выделения из носа, экзематозные высыпания. Сегментоядерные лейкоциты у таких больных не способны убивать бактерии.
 К заболеваниям, относящимся к наследственной патологии , относится также синдром Шедиака — Хигаши. Характеризуется рецидивирующими инфекциями, гепатоспленомегалией, нарушениями ЦНС, часто сочетающимися с имфопролиферативным раком. Иммунологическое обследование в данном случае выявляет снижение хемотаксиса нейтрофилов и активности NK-клеток ; нарушение переваривающей способности нейтрофилов за счет дефекта лизосомальных ферментов.
К заболеваниям, относящимся к наследственной патологии , относится также синдром Шедиака — Хигаши. Характеризуется рецидивирующими инфекциями, гепатоспленомегалией, нарушениями ЦНС, часто сочетающимися с имфопролиферативным раком. Иммунологическое обследование в данном случае выявляет снижение хемотаксиса нейтрофилов и активности NK-клеток ; нарушение переваривающей способности нейтрофилов за счет дефекта лизосомальных ферментов.
 Недостаточность факторов системы комплемента, в норме активно влияющих на функцию иммунокомпетентных клеток, отмечается при развитии целого ряда заболеваний, поскольку рецепторы для компонентов системы комплемента имеются практически на всех ммунокомпетентных клетках (В-лимфоцитах, Т-лимфоцитах, нейтрофилах, макрофагах, эозинофилах, эритроцитах, NK-клетках, клетках эндотелия и т. п. ).
Недостаточность факторов системы комплемента, в норме активно влияющих на функцию иммунокомпетентных клеток, отмечается при развитии целого ряда заболеваний, поскольку рецепторы для компонентов системы комплемента имеются практически на всех ммунокомпетентных клетках (В-лимфоцитах, Т-лимфоцитах, нейтрофилах, макрофагах, эозинофилах, эритроцитах, NK-клетках, клетках эндотелия и т. п. ).
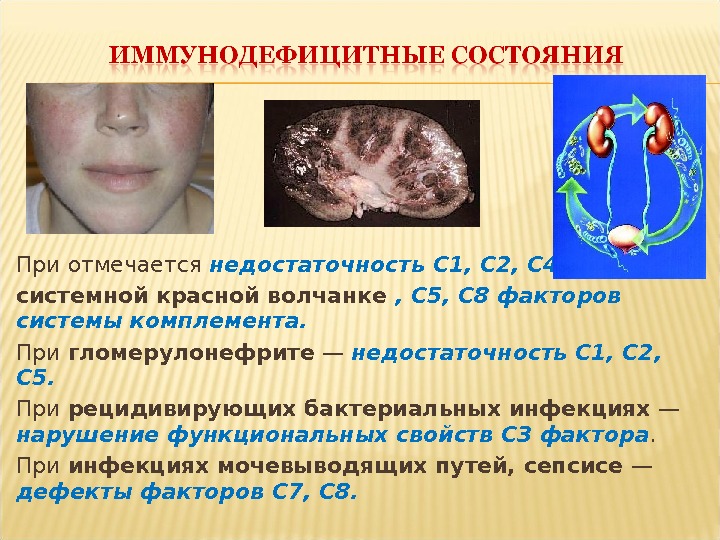 При отмечается недостаточность С 1, С 2, С 4 системной красной волчанке , С 5, С 8 факторов системы комплемента. При гломерулонефрите — недостаточность С 1, С 2, С 5. При рецидивирующих бактериальных инфекциях — нарушение функциональных свойств С 3 фактора. При инфекциях мочевыводящих путей, сепсисе — дефекты факторов С 7, С 8.
При отмечается недостаточность С 1, С 2, С 4 системной красной волчанке , С 5, С 8 факторов системы комплемента. При гломерулонефрите — недостаточность С 1, С 2, С 5. При рецидивирующих бактериальных инфекциях — нарушение функциональных свойств С 3 фактора. При инфекциях мочевыводящих путей, сепсисе — дефекты факторов С 7, С 8.
 Общий вариабельный иммунодефицит может характеризоваться: — В-клеточным дефицитом с нарушением дифференцировки данных клеток; — дефектом Т-клеток с преобладанием Т-супрессоров и дефицитом Т-хелперов; — выработкой антител к Т- или В-лимфоцитам. — инфекциями верхних дыхательных путей, гиперплазией тонкого кишечника, анемией и остеопатией. Примером данной патологии является болезнь Дункан (наследственное заболевание, в основе которого лежит снижение иммунного ответа на вирус Эпштейн — Барр и как результат развитие инфекционного мононуклеоза и В-клеточной лимфомы ).
Общий вариабельный иммунодефицит может характеризоваться: — В-клеточным дефицитом с нарушением дифференцировки данных клеток; — дефектом Т-клеток с преобладанием Т-супрессоров и дефицитом Т-хелперов; — выработкой антител к Т- или В-лимфоцитам. — инфекциями верхних дыхательных путей, гиперплазией тонкого кишечника, анемией и остеопатией. Примером данной патологии является болезнь Дункан (наследственное заболевание, в основе которого лежит снижение иммунного ответа на вирус Эпштейн — Барр и как результат развитие инфекционного мононуклеоза и В-клеточной лимфомы ).
 Различают: I. Протозойные и глистные болезни (малярия, трипаносомоз, лейшманиоз, шистосомоз, трихинеллез и др. ). Развитие иммунодефицита при паразитарных инфекциях включает в себя: — угнетение функции макрофагов (малярия); — гиперактивацию Т-супрессоров (трипаносомоз); — нарушение иммунорегуляции и выработку лимфоцитотоксинов (Trichinello spiralis) или супрессирующих факторов, угнетающих иммунные реакции (шисто- и трипаносомы).
Различают: I. Протозойные и глистные болезни (малярия, трипаносомоз, лейшманиоз, шистосомоз, трихинеллез и др. ). Развитие иммунодефицита при паразитарных инфекциях включает в себя: — угнетение функции макрофагов (малярия); — гиперактивацию Т-супрессоров (трипаносомоз); — нарушение иммунорегуляции и выработку лимфоцитотоксинов (Trichinello spiralis) или супрессирующих факторов, угнетающих иммунные реакции (шисто- и трипаносомы).
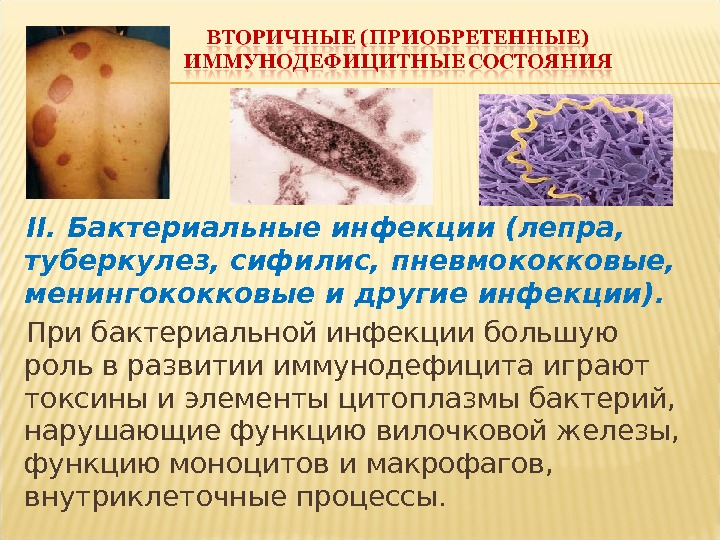 II. Бактериальные инфекции (лепра, туберкулез, сифилис, пневмококковые, менингококковые и другие инфекции). При бактериальной инфекции большую роль в развитии иммунодефицита играют токсины и элементы цитоплазмы бактерий, нарушающие функцию вилочковой железы, функцию моноцитов и макрофагов, внутриклеточные процессы.
II. Бактериальные инфекции (лепра, туберкулез, сифилис, пневмококковые, менингококковые и другие инфекции). При бактериальной инфекции большую роль в развитии иммунодефицита играют токсины и элементы цитоплазмы бактерий, нарушающие функцию вилочковой железы, функцию моноцитов и макрофагов, внутриклеточные процессы.
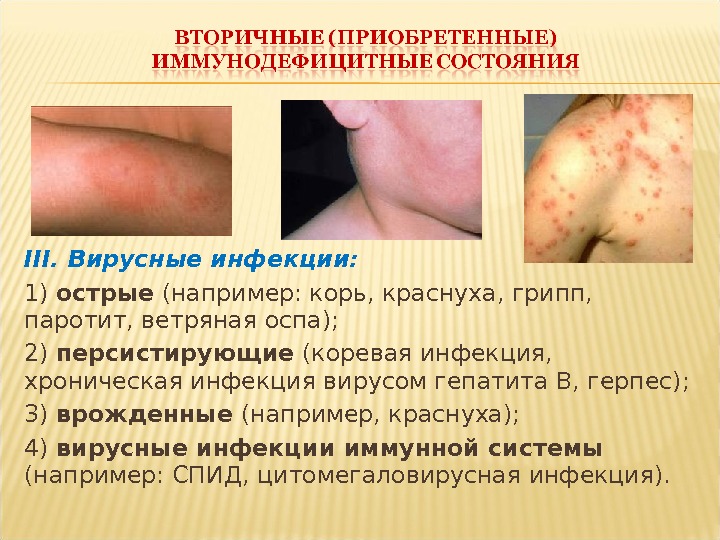 III. Вирусные инфекции: 1) острые (например: корь, краснуха, грипп, паротит, ветряная оспа); 2) персистирующие (коревая инфекция, хроническая инфекция вирусом гепатита В, герпес); 3) врожденные (например, краснуха); 4) вирусные инфекции иммунной системы (например: СПИД, цитомегаловирусная инфекция).
III. Вирусные инфекции: 1) острые (например: корь, краснуха, грипп, паротит, ветряная оспа); 2) персистирующие (коревая инфекция, хроническая инфекция вирусом гепатита В, герпес); 3) врожденные (например, краснуха); 4) вирусные инфекции иммунной системы (например: СПИД, цитомегаловирусная инфекция).
 III. Вирусные инфекции: Механизмы формирования иммунодефицитов при данных инфекциях довольно многообразны, но основными из них являются: — непосредственное поражение вирусом лимфоцитов или макрофагов (вирусом Эпштейн — Барр, вирусом иммунодефицита человека); — иммуносупрессия, индуцированная Т-супрессорами под влиянием жизнедеятельности вирусов в тканевых клетках; — модификация мембран лимфоцитов, вызванная вирусом, иммунными комплексами, антителами, интерфероном.
III. Вирусные инфекции: Механизмы формирования иммунодефицитов при данных инфекциях довольно многообразны, но основными из них являются: — непосредственное поражение вирусом лимфоцитов или макрофагов (вирусом Эпштейн — Барр, вирусом иммунодефицита человека); — иммуносупрессия, индуцированная Т-супрессорами под влиянием жизнедеятельности вирусов в тканевых клетках; — модификация мембран лимфоцитов, вызванная вирусом, иммунными комплексами, антителами, интерфероном.
 IV. Нарушения питания (голодание), несбалансированное питание и нарушение обмена веществ. При данных процессах повышается опасность инфекционных заболеваний. Концентрации иммуноглобулинов могут долго сохраняться на должном уровне , однако снижен уровень первичного иммунного ответа. Далее процесс затрагивает функциональную активность лимфоцитов. Гистологически выявляется атрофия вилочковой железы , клеточное опустошение в иммунных зонах.
IV. Нарушения питания (голодание), несбалансированное питание и нарушение обмена веществ. При данных процессах повышается опасность инфекционных заболеваний. Концентрации иммуноглобулинов могут долго сохраняться на должном уровне , однако снижен уровень первичного иммунного ответа. Далее процесс затрагивает функциональную активность лимфоцитов. Гистологически выявляется атрофия вилочковой железы , клеточное опустошение в иммунных зонах.
 Иммунодефицит может быть обусловлен дефицитом неорганических веществ в продуктах питания, особенно это касается железа, меди и цинка. Дефицит железа приводит к нарушению Т-клеточной функции (снижается продукция лимфокинов), подавлению активности нейтрофилов и появлению опасности рецидивирующих бактериальных инфекций.
Иммунодефицит может быть обусловлен дефицитом неорганических веществ в продуктах питания, особенно это касается железа, меди и цинка. Дефицит железа приводит к нарушению Т-клеточной функции (снижается продукция лимфокинов), подавлению активности нейтрофилов и появлению опасности рецидивирующих бактериальных инфекций.
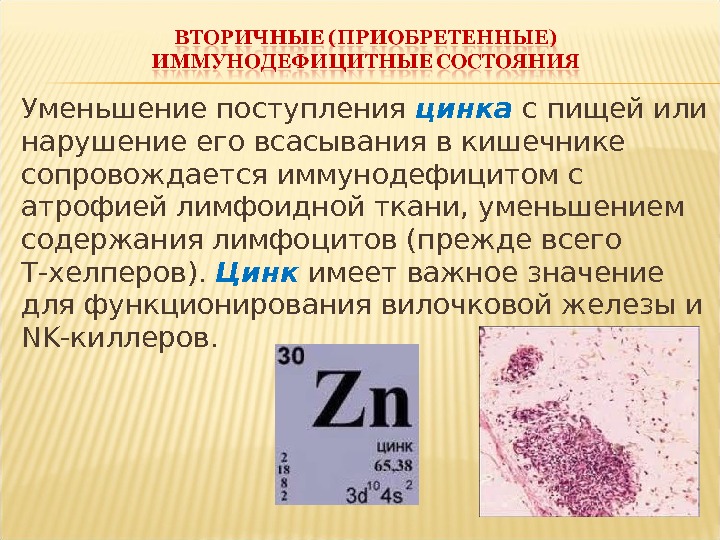 Уменьшение поступления цинка с пищей или нарушение его всасывания в кишечнике сопровождается иммунодефицитом с атрофией лимфоидной ткани, уменьшением содержания лимфоцитов (прежде всего Т-хелперов). Цинк имеет важное значение для функционирования вилочковой железы и NK-киллеров.
Уменьшение поступления цинка с пищей или нарушение его всасывания в кишечнике сопровождается иммунодефицитом с атрофией лимфоидной ткани, уменьшением содержания лимфоцитов (прежде всего Т-хелперов). Цинк имеет важное значение для функционирования вилочковой железы и NK-киллеров.
 Дефицит меди снижает фагоцитарную активность, вызывает нейтропению, замедляет пролиферативную активность лимфоцитов. Дети с врожденным дефицитом меди (болезнь Менкеса) погибают в раннем возрасте от инфекций.
Дефицит меди снижает фагоцитарную активность, вызывает нейтропению, замедляет пролиферативную активность лимфоцитов. Дети с врожденным дефицитом меди (болезнь Менкеса) погибают в раннем возрасте от инфекций.
 Дефицит магния сопровождается снижением уровня Ig. G и Ig. M. Большую роль играют витамины. Недостаточность витаминов приводит к существенным нарушениям гуморального и клеточного иммунитета , так как многие витамины ( группы В и Е ) являются коферментами метаболизма лимфоцитов, витамины Е и С — антиоксидантами и т. д. Влияют также физические и химические факторы , самым сильным из которых является радиация. Если слабые дозы стимулируют рост и митозы клеток, то высокие оказывают иммунодепрессивное воздействие.
Дефицит магния сопровождается снижением уровня Ig. G и Ig. M. Большую роль играют витамины. Недостаточность витаминов приводит к существенным нарушениям гуморального и клеточного иммунитета , так как многие витамины ( группы В и Е ) являются коферментами метаболизма лимфоцитов, витамины Е и С — антиоксидантами и т. д. Влияют также физические и химические факторы , самым сильным из которых является радиация. Если слабые дозы стимулируют рост и митозы клеток, то высокие оказывают иммунодепрессивное воздействие.
 V. Хронические соматические заболевания. Могут вызывать иммунодефицитные состояния вследствие длительного напряжения иммунных реакций. Например, сахарный диабет, хронический панкреатит, хронические бронхиты и пневмонии и т. п. VI. Ятрогенные иммунодефициты. Удаление миндалин (особенно у детей) и не всегда обоснованная аппендэктомия (т. е. удаление лимфоидных органов) могут вызывать серьезные изменения в иммунологической реактивности.
V. Хронические соматические заболевания. Могут вызывать иммунодефицитные состояния вследствие длительного напряжения иммунных реакций. Например, сахарный диабет, хронический панкреатит, хронические бронхиты и пневмонии и т. п. VI. Ятрогенные иммунодефициты. Удаление миндалин (особенно у детей) и не всегда обоснованная аппендэктомия (т. е. удаление лимфоидных органов) могут вызывать серьезные изменения в иммунологической реактивности.
 VII. Иммунотоксическое действие лекарств. В большом количестве экспериментальных работ и клинических наблюдений обнаружено иммунодепрессивное влияние даже коротких курсов таких антибиотиков, как пенициллин, стрептомицин, тетрациклины, противотуберкулезные и противогрибковые антибиотики.
VII. Иммунотоксическое действие лекарств. В большом количестве экспериментальных работ и клинических наблюдений обнаружено иммунодепрессивное влияние даже коротких курсов таких антибиотиков, как пенициллин, стрептомицин, тетрациклины, противотуберкулезные и противогрибковые антибиотики.
 VII. Иммунотоксическое действие лекарств. Эффекты антибиотиков: — дефекты формирования первичного иммунного ответа (скорость образования антител); — существенное снижение противовирусного иммунитета (особенно против вируса гриппа, розового и отрубевидного лишая); — снижение цитотоксической активности Т-лимфоцитов; — значительное уменьшение фагоцитарной активности фагоцитов (нейтрофилов и макрофагов).
VII. Иммунотоксическое действие лекарств. Эффекты антибиотиков: — дефекты формирования первичного иммунного ответа (скорость образования антител); — существенное снижение противовирусного иммунитета (особенно против вируса гриппа, розового и отрубевидного лишая); — снижение цитотоксической активности Т-лимфоцитов; — значительное уменьшение фагоцитарной активности фагоцитов (нейтрофилов и макрофагов).
 Особенно опасные иммунодефицитные состояния формируются у рабочих, занятых в производстве и на расфасовке антибиотиков и других иммунодепрессивных препаратов. Иногда иммунодепрессивное влияние антибиотиков оказывается весьма полезным. Например, при лечении ангин , вызываемых гемолитическим стрептококком типа А , показаны и даже предпочтительны именно антибиотики пенициллинового ряда, применение которых одновременно снижает опасность развития ревматизма. Кроме антибиотиков, иммуносупрессивными свойствами обладают классические иммунодепрессанты и цитостатики , использующиеся в терапии аутоиммунных, лимфопролиферативных и онкологических заболеваний, при трансплантациях и др.
Особенно опасные иммунодефицитные состояния формируются у рабочих, занятых в производстве и на расфасовке антибиотиков и других иммунодепрессивных препаратов. Иногда иммунодепрессивное влияние антибиотиков оказывается весьма полезным. Например, при лечении ангин , вызываемых гемолитическим стрептококком типа А , показаны и даже предпочтительны именно антибиотики пенициллинового ряда, применение которых одновременно снижает опасность развития ревматизма. Кроме антибиотиков, иммуносупрессивными свойствами обладают классические иммунодепрессанты и цитостатики , использующиеся в терапии аутоиммунных, лимфопролиферативных и онкологических заболеваний, при трансплантациях и др.
 Препараты, содержащие гормоны кортикостероиды , обладают иммунодепрессивным действием. Следует помнить, что некоторые сульфаниламиды могут существенно подавлять иммунную систему (например, бисептол). После отмены препарата происходит постепенное восстановление иммунологических показателей. При физиотерапевтических воздействиях возникает фаза стимуляции, а затем иммунодепрессии.
Препараты, содержащие гормоны кортикостероиды , обладают иммунодепрессивным действием. Следует помнить, что некоторые сульфаниламиды могут существенно подавлять иммунную систему (например, бисептол). После отмены препарата происходит постепенное восстановление иммунологических показателей. При физиотерапевтических воздействиях возникает фаза стимуляции, а затем иммунодепрессии.
 VIII. Постстрессовые иммунодефицитные состояния. IX. Последствия ожогов. В первые дни после ожогов снижается уровень сывороточных иммуноглобулинов. Они восстанавливаются спустя 1— 2 недели (сначала Ig М , затем Ig A и Ig G ). Нарушение клеточного звена иммунитета заключается в снижении общего числа зрелых Т-лимфоцитов, Т-хелперов, Т-киллеров. Снижается активность системы комплемента.
VIII. Постстрессовые иммунодефицитные состояния. IX. Последствия ожогов. В первые дни после ожогов снижается уровень сывороточных иммуноглобулинов. Они восстанавливаются спустя 1— 2 недели (сначала Ig М , затем Ig A и Ig G ). Нарушение клеточного звена иммунитета заключается в снижении общего числа зрелых Т-лимфоцитов, Т-хелперов, Т-киллеров. Снижается активность системы комплемента.
 Х. Последствия травм, хирургических вмешательств. Крупные хирургические операции под наркозом приводят к существенным иммунным нарушениям. Показатели периферической крови достигают нормы только спустя 10 часов после применения наркотических препаратов; выработка антител восстанавливается через месяц. Сама операционная травма ведет к возникновению иммунодефицитов, возможно, обусловленных гормональной реакцией организма на вмешательство и супрессией макрофагов.
Х. Последствия травм, хирургических вмешательств. Крупные хирургические операции под наркозом приводят к существенным иммунным нарушениям. Показатели периферической крови достигают нормы только спустя 10 часов после применения наркотических препаратов; выработка антител восстанавливается через месяц. Сама операционная травма ведет к возникновению иммунодефицитов, возможно, обусловленных гормональной реакцией организма на вмешательство и супрессией макрофагов.
Источник
1. Вторичные иммунодефициты
2. Вторичные иммунодефициты (ВИД)
Вторичные иммунодефициты (ВИД) — это
нарушения иммунитета, возникшие в
результате неблагоприятного воздействия
на организм эндогенных или экзогенных
факторов. Вторичные иммунодефициты
характеризуются тем, что они возникают в
позднем постнатальном периоде или в
зрелом возрасте. Эти состояния
развиваются на фоне ранее нормально
функционировавшей иммунной системы
(генетически недефектной системы).
3. Вторичные иммунодефициты (ВИД)
I.
Классификация ВИД.
По темпам развития:
1. острый иммунодефицит (обусловлен
острым инфекционным заболеванием,
тяжелой травмой, интоксикацией и др.);
2. хронический иммунодефицит (развивается
на фоне хронических воспалительных
заболеваний, аутоиммунных нарушений,
опухолевого роста, персистирующей
вирусной инфекции и др.).
4. Вторичные иммунодефициты (ВИД)
Классификация ВИД.
По характеру нарушения в иммунной системе:
1. нарушение клеточного иммунитета;
2. нарушение гуморального иммунитета;
3. нарушение системы фагоцитов;
4. нарушение системы комплемента;
5. комбинированные дефекты.
III. По распространенности иммунных нарушений:
1. местный иммунодефицит;
2. системный иммунодефицит.
II.
5. Вторичные иммунодефициты (ВИД)
Классификация ВИД.
IV.
По степени тяжести:
1.
2.
3.
компенсированный (легкий);
Клинически проявляется в виде частых ОРЗ, пневмоний,
пиодермии, гайморитов и поражений других органов и тканей,
высокой чувствительности к детским инфекциям.
субкомпенсированный (средней тяжести);
Эта форма характеризуется развитием хронических
инфекционно-воспалительных процессов. При этой форме
наблюдаются хронические бронхиты, пневмонии,
пиелонефриты, отиты, энтероколиты и другие тяжелые
заболевания.
декомпенсированный (тяжелый).
Проявляется в виде развития генерализованных инфекций,
вызванных патогенной и условно-патогенной микрофлорой,
злокачественных новообразований и др.
6. Вторичные иммунодефициты (ВИД)
Среди ВИД выделяют две формы:
• Приобретенно-индуцированную, вызванную
конкретным фактором: вирусом, ионизирующим
излучением, развивающуюся после цитостатической
или кортикостероидной терапии, травмы и др. Эта
форма является вторичной по отношению к основному
заболеванию (сахарному диабету, заболеванию
печени, почек, злокачественному процессу).
• Спонтанную (характеризующуюся отсутствием явной
причины, вызвавшей иммунные расстройства).
В количественном отношении спонтанная форма
является доминирующей среди вторичных
иммунодефицитов.
7. Вторичные иммунодефициты (ВИД)
К развитию ВИД могут приводить следующие факторы:
1.
2.
3.
4.
5.
6.
7.
Протозойные инвазии и гельминтозы (малярия, токсоплазмоз,
лейшманиоз, трихинеллез, аскаридоз и др.).
Бактериальные инфекции (стафилококковая, пневмококковая,
менингококковая, туберкулез и др.)
Вирусные инфекции (корь, краснуха, грипп, ветряная оспа,
хронические гепатиты, подострый склерозирующий панэнцефалит,
ВИЧ- и цитомегаловирусная инфекции).
Нарушение питания (белково-энергетическая недостаточность.
Дефицит микроэлементов (Zn, Си, Fе и др.), витаминов (А, С, Е,
фолиевой кислоты); кахексия, потеря белка через кишечник или
почки, врожденные нарушения метаболизма (ожирение).
Злокачественные новообразования, особенно
лимфопролиферативные заболевания.
Аутоиммунные заболевания;
Состояния, сопровождающиеся потерей иммунокомпетентных клеток
и иммуноглобулинов (кровотечения, ожоги, нефрит).
8. Вторичные иммунодефициты (ВИД)
К развитию ВИД могут приводить следующие факторы:
8.
Экзогенные и эндогенные интоксикации (отравления,
тиреотоксикоз, декомпенсированный сахарный диабет).
9.
Физические воздействия на организм (ионизирующее излучение,
СВЧ и др.).
10. Воздействие химических веществ на организм (наркотики,
гербициды, пестициды и др.);
11. Длительное применение лекарственных веществ (химиотерапия,
цитостатики, кортикостероиды);
12. Физические и психо-эмоциональные перегрузки (стресс,
спортивные перегрузки, психические травмы);
13. Тяжелые травмы и хирургические операции.
Следует заметить, что в детском и в пожилом возрасте, а также при
беременности наблюдаются иммунодефицитные состояния,
которые являются «естественными» (естественные
иммунодефициты).
9. Вторичные иммунодефициты (ВИД)
Клиническими признаками, позволяющими
заподозрить иммунодефицитное
состояние, являются:
1.
2.
хронические, часто рецидивирующие, вялотекущие
инфекционно-воспалительные процессы любой
локализации, трудно поддающиеся традиционному
лечению, вызванные условно-патогенными или
оппортунистическими микробами с атипичными
биологическими свойствами, часто с
множественной устойчивостью к антибиотикам;
слабая температурная реакция или ее отсутствие
при остром инфекционном заболевании.
10. Вторичные иммунодефициты (ВИД)
Лабораторные данные:
1.
2.
3.
4.
Важны в постановке и подтверждении диагноза ИД;
Необходимы для выбора адекватной терапии;
Важны в контроле эффективности и правильности
проведения иммунотерапии и своевременной ее
коррекции;
Данные иммунного статуса являются
прогностическими критериями течения заболевания
(выздоровления, прогрессирования заболевания,
развития осложнений)
11. Вторичные иммунодефициты (ВИД)
Лечение:
—
1.
2.
3.
4.
Назначение препарата и схема его применения в каждом
конкретном случае определяется врачом в зависимости от:
Клинических проявлений заболевания
Тяжести заболевания
Сопутствующей патологии
Характера выявленного иммунного дефекта
Цель назначения иммунопрепаратов:
Восстановление иммунных нарушений;
Стимуляция активности неповрежденных факторов
иммунитета;
Включение в защитные реакции резервов иммунной системы;
Профилактика развития патологических иммунных реакций
(аутоиммунных, аллергических реакций)
12. Вторичные иммунодефициты (ВИД)
Лечение:
A. При нарушениях в системе моноцитарно-макрофагальных клеток
показано применение препаратов, оказывающих преимущественное
воздействие на этот тип клеток. К высокоэффективным препаратам
последнего поколения относятся:
— полиоксидоний;
— ликопид;
— интерфероны (гамма-интерферон);
— миелопид (фракция МП-3);
— рибомунил и др.
При тяжелых формах поражения моноцитарно-макрофагальной системы
используются препараты, содержащие колониестимулирующие факторы:
— лейкомакс;
— нейпоген;
— с заместительной целью применяется лейкомасса.
13. Вторичные иммунодефициты (ВИД)
Лечение:
Б.
При нарушениях в Т-клеточном звене
иммунитета используются препараты,
активирующие функцию Т-клеток (НКклеток). Этими свойствами обладают:
— тактивин;
— тимоген;
— имунофан;
— миелопид (фракция МП-1) и др.
14. Вторичные иммунодефициты (ВИД)
Лечение:
B. При нарушениях гуморального иммунитета применяют
препараты, активирующие функции В-лимфоцитов, а также Тклеток и макрофагов. Препаратом, действующим на В-клетки,
является миелопид.
С заместительной целью при гипогаммаглобулинемиях
используются препараты иммуноглобулинов:
— сандоглобулин;
— октагамом;
— интраглобулин;
— иммуноглобулин нормальный человеческий для внутривенного
введения;
— пентаглобин и др.
15. Вторичные иммунодефициты (ВИД)
Лечение:
Принципы
воздействия
иммуномодуляторов
на иммунную систему
16. Вторичные иммунодефициты (ВИД)
1.
2.
3.
Принципы иммунотерапии:
Главным обоснованием для назначения
иммунотропных препаратов является клиническая
картина заболевания, характеризующаяся наличием
хронических, вялотекущих и трудноподдающихся
традиционному лечению инфекционновоспалительных процессов.
Иммуномодуляторы назначают в комплексе с
антибиотиками, противогрибковыми,
противопротозойными или противовирусными
средствами.
Целесообразно раннее назначение иммунотропных
препаратов — начиная с первого дня применения
химиотерапевтического этиотропного средства.
17. Вторичные иммунодефициты (ВИД)
Принципы иммунотерапии:
4.
5.
6.
Больным ВИД с лабораторно невыявленными нарушениями
иммунного статуса, оправданным является назначение
препаратов, стимулирующих моноцитарно-макрофагальное
звено иммунитета. Основанием для назначения иммунотропного
препарата является клиническая картина заболевания.
Проведение иммунотерапии целесообразно сопровождать
этапными иммунограммами.
Иммунотропные вещества могут применяться в виде
монотерапии при проведении иммунореабилитационных
мероприятий, в частности, при неполном выздоровлении после
перенесенного острого инфекционного заболевания.
Думается, что соблюдение этих принципов поможет врачам всех
специальностей эффективно лечить больных с нарушениями
иммунитета.
