Синдром утечки воздуха у новорожденных
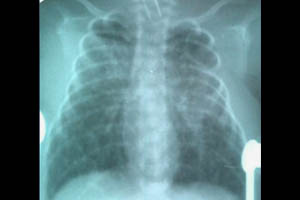
Синдром утечки воздуха (СУВ) — группа патологических состояний, характеризующихся скоплением газа вне альвеолярного пространства.
Чаще всего нарушение целостности альвеол происходит в результате повреждения респираторного эпителия альвеол и терминальных воздухоносных путей высоким внутрилёгочным давлением.
Нозологические формы СУВ:
— интерстициальная легочная эмфизема;
— пневмоторакс;
— пневмомедиастинум;
— пневмоперикард;
— пневмоперитонеум;
— подкожная эмфизема.
Перечисленные нозологии могут возникать изолированно или в сочетании друг с другом. Летальность в группе детей с СУВ при разных формах достигает 50%. У выживших детей высока частота развития хронической патологии легких и тяжелых неврологических расстройств, как следствие внутричерепных кровоизлияний.
Интерстициальная легочная эмфизема
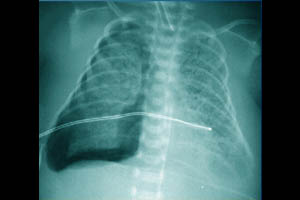
При развитии интерстициальной легочной эмфиземы (ИЛЭ) воздух через поврежденный альвеолярный эпителий проникает в интерстициальное пространство легких. Наиболее часто ИЭЛ встречается у недоношенных детей с массой тела менее 1000 г. К факторам риска относят:
— респираторный дистресс-синдром;
— морфофункциональная незрелость лёгких;
— аспирационный синдром;
— врожденные пневмонии;
— диспозиция эндотрахеальной трубки (однолегочная вентиляция).
При ИЛЭ разрывы эпителия альвеол и мелких дыхательных путей приводят к скоплению пузырьков газа в интерстициальном пространстве легочной ткани. Интерстициальный газ становится причиной механической компрессии альвеол вплоть до их ателектазирования, что приводит к снижению растяжимости легких и нарушению вентиляционно-перфузионных отношений. Шунтирование крови на «неработающих» альвеолах и механическое сдавление сосудов интерстициальным газом приводит к повышению давления в легочной артерии и развитию вторичной легочной гипертензии. Описанный патологический процесс ведет к необходимости увеличения параметров вентиляции, что, по сути, замыкает «порочный круг» патогенеза ИЛЭ.
Диагноз ИЛЭ ставится на основании клинических, рентгенологических и лабораторных данных. Иногда ИЛЭ диагностируется после дренирования пневмоторакса и расправления пострадавшего легкого. В большинстве случаев, выявлению ИЛЭ предшествует ухудшение состояния ребенка, снижение оксигенации, необходимость увеличения параметров ИВЛ, десинхронизация с аппаратной вентиляцией, тенденция к артериальной гипотензии. При объективном осмотре у ребенка могут наблюдаться вздутие грудной клетки, крепитирующие хрипы на стороне поражения. Лабораторно выявляются гиперкапния, гипоксемия и ацидоз. Классическая рентгенография грудной клетки в прямой проекции лежа позволяет четко диагностировать ИЛЭ, которая проявляется в двух основных формах: линейной и кистозноподобной. Часто эти две формы выявляются вместе. Линейная ИЛЭ визуализируется как неразветвленные тени длиной от 3 до 8 мм, ширина их редко превышает 2мм. Кистозноподобная форма представляет собой округлые, иногда овальные, тени от 1 до 4 мм в диаметре. Иногда данная рентгенологическая картина ошибочно интерпретируется как нормально аэрированное легкое, окруженное экссудатом, как при аспирационном синдроме или отеке легких. Линейную форму необходимо дифференцировать от «воздушных бронхограмм» при РДС. «Воздушные бронхограммы» представляют собой протяжённые разветвлённые тени, напоминающие трахеобронхиальное дерево, постепенно уменьшающиеся и исчезающие к периферии. Линейная форма ИЛЭ видна в дистальных отделах лёгких, в стороне от бронхов и не имеет ответвлений.
ИЛЭ следует дифференцировать с врождёнными кистозными аномалиями (лобарная эмфизема, кистоаденоматоз) и гиперинфляцией лёгких.
Одним из методов лечения является терапия положением. Ребенок укладывается на бок на сторону поражения. При этом достигается определенное сжатие дыхательных путей с пораженной стороны и наоборот, увеличение вентиляции и оксигенации в условно здоровом легком. Неотъемлемая часть этой методики — постепенное снижение параметров вентиляции. Пиковое и среднее давление в дыхательных путях должны быть снижены до минимума, позволяющего поддерживать приемлемые газы крови: PaO2 35–55 мм рт.ст., PaCO2 до 65 мм рт.ст., pH более 7,2. Для обеспечения целевой оксигенации после снижения PIP можно увеличить FiO2. Стратегия ограничения дыхательного объёма предусматривает постепенное его снижение на фоне синхронизированной вентиляции до потенциально безопасных значений — 4–6 мл/кг. Для минимизации баротравмы и волюмотравмы рекомендуют использовать режимы триггерной вентиляции: SIMV, А/С, PRVC. При развитии ИЛЭ показан перевод пациента на ВЧО ИВЛ, тем самым снижается вероятность образования воздушных ловушек, достигается равномерность вентиляции, максимальное расправление ателектазированных участков легких и снижается избыточное давление в перераздутых альвеолах.
Селективная бронхиальная интубация, декларированная некоторыми авторами как метод лечения при ИЛЭ, у новорожденных бывает технически трудновыполнима при поражении правого легкого, в то время как СУВ в 2/3 случаев отмечается именно справа.
Смертность, связанная с ИЛЭ, достигает 67% у детей, находящихся на ИВЛ. Раннее выявление (до 48 часов после рождения) увеличивает эту цифру до 100%, поскольку прямо коррелирует с тяжестью паренхиматозного поражения легких. Осложнениями ИЛЭ являются другие вид СУВ, воздушная эмболия, хронические легочные заболевания, внутрижелудочковые кровоизлияния, перевентрикулярная лейкомаляция. Основными методами профилактики ИЛЭ являются: выполнение клинических рекомендаций и протоколов по базовой помощи и первичной реанимации в родовом зале, по ведению детей с РДС.
Пневмоторакс
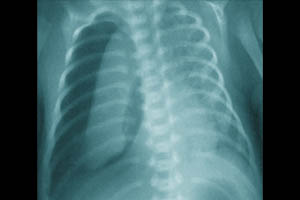
Пневмоторакс — это вид СУВ, при котором воздух проникает в плевральную полость вследствие нарушения целостности висцеральной плевры.
У 1% новорожденных встречаются спонтанные ненапряженные пневмотораксы, как результат перерастяжения и разрыва альвеол из-за сильного повышения внутрилёгочного давления во время первых нескольких вдохов.
Заподозрить спонтанный пневмоторакс у новорожденного можно по следующим симптомам: тахипноэ, увеличение грудной клетки в переднезаднем размере, асимметрия грудной клетки, ослабление дыхания, коробочный оттенок звука на стороне пораженного легкого, перкуторное смещение границ сердечно тупости, приглушенность сердечных тонов. Как правило, такие пневмотораксы купируются самостоятельно, но требуют интенсивного наблюдения за пациентом. Наибольшую опасность представляют собой напряженные пневмотораксы с выраженной компрессией легкого на стороне поражения и смещением средостения в здоровую сторону. Причинами подобных пневмотораксов являются заболевания, характеризующиеся неравномерной растяжимостью различных участков легкого: синдром аспирации мекония, гипоплазия легких, буллезная мальформация легких. Пневмоторакс может стать осложнением респираторной терапии или возникнуть в результате травмы легкого (катетеризация подключичной и яремной вен методом Сельдингера, санация трахеобронхиального дерева).
Клиническая картина напряженного пневмоторакса: тахипноэ, цианоз, втяжение уступчивых мест грудной клетки, десинхронизация с аппаратом ИВЛ, артериальная гипотензия, нарушение сердечного ритма, выраженная асимметрия грудной клетки (выбухание на стороне поражения), ослабление дыхания, коробочный перкуторный звук, перкуторные и аускультативные признаки смещения средостения в здоровую сторону, вздутие живота. Диагноз основывается на клинических данных, рентгенологическом обследовании, результате диагностической плевральной пункции, данных трансиллюминации. Последний метод требует строгих условий выполнения: относительно затемненная комната или возможность создать локальное затемнение и яркий источник холодного света малого диаметра (сильный фонарик, веновизор, светопроводник от эндоскопа). Источник света прикладывают к грудной клетке ребенка: если в плевральной полости воздуха нет, то свет будет образовывать небольшое кольцо вокруг источника света; в случае внелегочного скопления воздуха будет широкое распространение света по грудной клетке. В случае развития явной клинической картины напряженного пневмоторакса, не следует терять время на проведения дополнительного обследования, а срочно провести декомпрессию легкого. Процедура выполняется в стерильных условиях. Положение ребенка на спине. При использовании бокового доступа необходимо фиксировать руку на стороне поражения за головой. Место пункции: IV-V межреберье по переднеаксиллярной линии, по верхнему краю нижележащего ребра. Анатомическим ориентиром является сосок, располагающийся на уровне IV межреберья. Для пункции используют иглу (18G), катетер — «бабочку» (18G) или сосудистый катетер на игле (20–18G). Для дренирования с помощью торакоцентеза используются дренажные трубки 8–10 Fr или торакальные канюли 10–12 Fr. Иглу или катетер соединяют со шприцем посредством переходника с зажимом (3-ходового крана). Иглу (катетер) медленно продвигается под углом 45° в краниальном направлении, подтягивая поршень шприца на себя. При свободном поступлении воздуха в шприц воздух удаляется из плевральной полости. В случае пункции сосудистым катетером, катетер продвигается по игле на необходимую глубину, игла удаляется, и канюля соединяется с трубкой системы аспирации. Катетер фиксируется к коже. Глубина введения дренажной трубки или катетера 2–4 см в зависимости от массы тела. Дренаж фиксируют с помощью лейкопластыря, при проведении торакоцентеза — трубка закрепляется 1–2 швами. Контролируют положение дренажа рентгенологически, при наличии остаточного воздуха изменяют положение дренажа или ставят второй. Рентгенологический контроль состояния лёгких и положения дренажа после стабилизации пациента осуществляют не реже одного раза в сутки. Если лёгкие расправились и дренаж не функционирует в течение 12 ч, то его следует пережать. Если еще через 12 ч на рентгенограмме лёгкое расправлено и воздуха в плевральной полости нет, дренаж удаляют. Манипуляция проводится под местной или общей анестезией.
В экстренных случаях, при правостороннем пневмотораксе, для пункции можно использовать II–III межреберье по среднеключичной линии.
В связи с высокой частотой развития пневмоторакса у новорожденных детей, в отделениях, где оказывается помощь таким пациентам, следует всегда «держать под рукой» набор для пункции и дренирования плеврального пространства. В целях профилактики пневмоторакса необходимо выполнение протоколов ведения детей с респираторными проблемами, быть особенно осторожными во время ручной вентиляции (техника вентиляции, показания манометра, наличие клапана ПДКВ), использовать графический мониторинг при проведении инвазивной ИВЛ.
Пневмоперикард
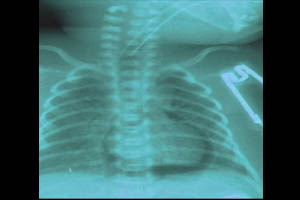
Более «грозной» формой СУВ является пневмоперикард — скопление воздуха в полости сердечной сумки. Летальность при этой форме СУВ достигает 90%. Клинически проявляется тампонадой сердца: генерализованный цианоз, глухость сердечных тонов, ослабление пульса, падение артериального давления. На рентгенограмме пневмоедиастинум и пневмоперикард выглядят как воздушный ореол с ровными краями (темный ободок) вокруг тени сердца. Дифференцировать пневмоперикард от пневмомедиастинума позволяет полоска воздуха вдоль нижней поверхности сердца над диафрагмой. Основной метод лечения — пункционное удаление воздуха из перикарда. Во избежание осложнений, данную манипуляцию следует проводить под контролем УЗИ.
Пневмомедиастинум

Пневмомедиастинум чаще всего сочетается с другими формами СУВ и характеризуется накоплением воздуха в средостении, имеет различные варианты клинического течения. У новорожденных часто отмечается сочетание пристеночного спонтанного пневмоторакса и пневмомедиастинума. Клинически определяется приглушенность тонов сердца, перкуторный коробочный звук над грудиной. Лечение симптоматическое.
Пневмоперитонеум
Пневмоперитонеум обычно является результатом перфорации полого органа на фоне течения некротизирующего энтероколита, но может быть и вариантом СУВ. В этом случае пневмоперитонеум развивается у вентилируемых новорожденных, уже имеющих пневмоторакс и пневмомедиастинум. Лечение пневмоторакса приводит к спонтанному разрешению пневмоперитонеума.
Подкожная эмфизема
Подкожная эмфизема – скопление воздуха в подкожной клетчатке, у новорожденных встречается редко и, в основном, при нарушении техники дренирования плевральных полостей. Характерен симптом «хруста» при пальпации кожи. Лечения данный вид СУВ не требует.
Источник
I. Определение. Синдромы утечки воздуха из легких (интерстициальная эмфизема легких, пневмомедиастинум, пневмоторакс, пневмоперикард) объединяют заболевания с единым патогенезом. Перерастяжение альвеол и нижних дыхательных путей может привести к их разрыву и проникновению воздуха в окружающие ткани.
II. Частота. Хотя точную частоту синдромов утечки воздуха из легких установить трудно, отмечено, что чаще всего они встречаются у новорожденных с заболеваниями легких, которым проводится искусственная вентиляция легких в условиях отделения интенсивной терапии. В целом, чем тяжелее заболевание легких, тем выше частота утечки воздуха из легких. Поскольку синдромы утечки воздуха из легких чаще всего наблюдают у новорожденных, которым проводится механическая вентиляция легких, считают, что все они возникают спонтанно.
III. Патофизиология. Перерастяжение нижних отделов дыхательных путей — ведущий патогенетический фактор при всех синдромах утечки воздуха легких — может быть результатом неравномерной альвеолярной вентиляции, образования «воздушных ловушек» или необоснованного применения положительного давления в конце выдоха при проведении новорожденным искусственной вентиляции легких. Когда объем воздуха в легких начинает превышать допустимые физиологические пределы, на стенку альвеолы во всех направлениях оказывают действие механические силы, которые в конечном счете могут привести к ее разрыву.
А. Интерстициальная эмфизема легких (ИЭЛ). ИЭЛ может предшествовать возникновению всех остальных синдромов утечки воздуха из легких. В результате перерастяжения и разрыва альвеол воздух проникает в периваскулярные ткани легких. В интерстициальном пространстве воздух распространяется по соединительной ткани вокруг осей сосудов, особенно вен. Попав в интерстициальное пространство, воздух двигается вдоль бронхиол, лимфатических сосудов, периваскулярных тканей или непосредственно через интерстиций легких к висцеральной плевре. Экстрапульмональный воздух либо накапливается в интерстиции (ИЭЛ), либо прорывается через плевру в средостение (пневмомедиастинум), полость перикарда (пневмоперикард) или плевральное пространство (пневмоторакс). Развитие синдромов утечки воздуха из легких не происходит в строго определенной последовательности. ИЭЛ может прогрессировать, приводя к пневмотораксу или пневмомедиастинуму, но может существовать и как самостоятельное заболевание. И наоборот, не во всех случаях развитию пневмоторакса предшествует ИЭЛ.
Б. Баротравма вследствие механической вентиляции легких. Баротравма является одним из ведущих этиологических факторов синдромов утечки воздуха из легких. Если перерастяжение легких — главное звено патогенеза, баротравма — наиболее частая причина перерастяжения легких. Баротравма возникает в тех случаях, когда нельзя избежать применения положительного давления в дыхательных путях у тяжелобольных новорожденных, которым требуется проведение искусственной вентиляции легких.
1. Максимальное давление на вдохе (МДВ), положительное давление в конце выдоха (ПДКВ), время вдоха (Ввд), частота дыхания и форма кривой давления на вдохе играют важную роль в возникновении баротравмы легких. Бывает трудно определить, какой из этих параметров обладает наиболее повреждающим действием и играет главную роль в развитии утечки воздуха из легких. Частые и выраженные колебания давления в легких, возникающие при перемежающейся вентиляции под положительным давлением (ПВПД), могут играть большее значение, чем само расширяющее давление; время вдоха (Ввд) — большее значение, чем положительное давление в конце выдоха (ПДКВ); расширяющее давление — большее значение, чем все перечисленное выше.
2. Непреднамеренное ПДКВ вследствие большой частоты дыхания (обычно более 80—100 вдохов/мин) и короткого выдоха может также являться причиной баротравмы легких. Несмотря на большие успехи в области применения искусственной вентиляции легких и мониторинга давления в дыхательных путях, баротравма остается главным недостатком этого метода лечения. Обдуманное применение параметров вентиляции и подбор их с учетом уменьшения риска баротравмы легких имеют крайне важное значение в интенсивной терапии новорожденных.
В. Другие причины перерастяжения легких. Баротравма — не единственная причина перерастяжения легких. Образование «воздушных ловушек» вследствие клапанного механизма может произойти при аспирации мекония или при частичной обтурации дыхательных путей слизистыми пробками. К другим причинам перерастяжения и разрыва альвеол сразу после рождения относятся ошибочная интубация правого главного бронха или развитие высокого раскрывающего давления в легких во время первого вдоха.
IV. Клинические проявления. Обычно во всех случаях ухудшения клинического состояния новорожденного, которому проводится искусственная вентиляция легких, следует подозревать один из синдромов утечки воздуха из легких, каждый из которых проявляется различными симптомами.
А. Интерстициальная эмфизема легких (ИЭЛ). Этот синдром встречается исключительно у новорожденных, находящихся на искусственной вентиляции легких. Развивается обычно в первые 24 ч жизни и имеет плохой прогноз. С возрастом (дни) частота ИЭЛ снижается, но она может возникнуть в любой момент во время проведения искусственной вентиляции легких. Состояние ребенка может ухудшиться внезапно, но гораздо чаще заболевание проявляется медленным прогрессивным ухудшением пoкaзaтeлeй газов артериальной крови и необходимостью увеличения параметров вентиляции. У таких больных неизбежно блокируется диффузия газов в легких вследствие отделения альвеолярной мембраны от капиллярного русла воздухом в интерстициальном пространстве. Увеличение параметров вентиляции при ухудшении газов крови может привести к нарастанию ИЭЛ и внезапному ухудшению состояния ребенка. У новорожденных с тяжелой ИЭЛ состояние ухудшается внезапно и быстро, но если ИЭЛ прогрессирует до развития пневмоторакса, оно может улучшиться.
Б. Пневмоторакс
1. У доношенного новорожденного, которому искусственная вентиляция легких не проводится, может развиться спонтанный пневмоторакс. Обычно это происходит сразу после рождения, так как для расправления спавшихся альвеол требуется большая величина раскрывающего давления. В этих случаях симптомов утечки воздуха из легких у новорожденных может не быть или она проявляется классической картиной респираторного дистресс-синдрома (стонущий выдох, раздувание крыльев носа и втяжение уступчивых мест грудной клетки).
2. У новорожденного, находящегося на искусственной вентиляции легких, состояние, как правило, ухудшается внезапно и быстро: появляются цианоз, гипоксемия, гиперкапния и респираторный ацидоз. Чаще всего это осложнение развивается сразу после начала искусственной вентиляции легких или когда состояние больного начинает улучшаться и возрастает растяжимость легких. В обоих случаях можно наблюдать и другие симптомы, такие как ослабление дыхания на стороне пневмоторакса, смещение верхушечного толчка в противоположную сторону и асимметрия грудной клетки. Весь персонал, ответственный за оказание помощи новорожденным, которым проводится искусственная вентиляция легких, должен быть исключительно внимателен в отношении развития пневмоторакса.
В. Пневмомедиастинум. Пневмомедиастинум, за исключением тех случаев, когда он сочетается с пневмотораксом, как правило, протекает совершенно бессимптомно. Спонтанный пневмомедиастинум может возникнуть у доношенных новорожденных, не находящихся на искусственной вентиляции легких, и проявляться легким синдромом дыхательных расстройств. К физикальным данным наряду с респираторным дистрессом относятся увеличение переднезаднего размера грудной клетки и приглушенные тоны сердца.
Г. Пневмоперикард. Считают, что возникновению пневмоперикарда всегда предшествует пневмомедиастинум, но это не всегда так. Клинические проявления пневмоперикарда могут полностью отсутствовать, а могут выражаться в резвернутой картине тампонады сердца. Первым симптомом может быть падение артериального или пульсового давления. Отмечаются также тахикардия и глухость тонов сердца.
V. Диагноз. Для своевременной диагностики синдромов утечки воздуха из легких необходима большая степень настороженности. Исходя из клинических данных, синдром утечки воздуха из легких следует заподозрить при ухудшении состояния ребенка или появлении у него синдрома дыхательных расстройств. Точный диагноз любого из синдромов утечки воздуха из легких устанавливают на основании данных рентгенографии грудной клетки. Для этого необходимо сделать рентгенограммы в переднезадней и боковой или косой проекциях.
A. Интерстициальная эмфизема легких. На рентгенограмме грудной клетки у новорожденных с ИЭЛ обычно выявляются участки повышения прозрачности легочных полей линейной или кистообразной формы. Линейные участки повышенной прозрачности имеют различную длину и не ветвятся; они определяются как на периферии, так и в медиальных зонах, и могут быть ошибочно приняты за воздушные бронхограммы. Участки повышенной прозрачности, имеющие форму кист, варьируют от 1 до 4 мм в диаметре и могут локализоваться в отдельных долях легкого.
Б. Пневмоторакс. Этот диагноз можно поставить с помощью трансиллюминации, не прибегая к рентгенографии грудной клетки. Прикладывание к грудной клетке ребенка световода, соединенного системой волоконной оптики с источником света, вызывает свечение пораженной половины. Несмотря на то что трансиллюминацию удобно применять для неотложной диагностики, она не может заменить полностью рентгенографию грудной клетки, являющуюся основным методом выявления пневмоторакса. К рентгенографическим признакам пневмоторакса относятся наличие воздуха в плевральной полости, разделяющего висцеральный и париетальный листики плевры, коллапс легкого на стороне поражения, смещение средостения в противоположную сторону и смещение вниз диафрагмы. У новорожденных с РДС растяжимость легких бывает настолько низкой, что легкое на стороне пневмоторакса не спадается, а отмечается лишь небольшое смещение органов средостения. На фронтальном снимке классической рентгенографической картины пневмоторакса может и не быть, если большое количество воздуха скапливается в плевральной полости непосредственно за грудиной. В этом случае свободный газ за грудиной выявляют с помощью снимков в боковой проекции и в положении больного на здоровом (предположительно) боку.
B. Пневмомедиастинум. Рентгенографически пневмомедиастинум проявляется в нескольких вариантах. Классическая картина напоминает расправленный ветром треугольный парус с долей тимуса, приподнятой над сердцем. В других случаях на фронтальном снимке вокруг тени сердца может наблюдаться ореол или любые признаки пневмомедиастинума могут отсутствовать полностью. Скопление воздуха в переднем средостении позволяет выявить боковой снимок, но при этом бывает трудно отличить пневмомедиастинум от пневмоторакса. Г. Пневмоперикард. Рентгенографическая картина пневмоперикарда является наиболее типичной из всех синдромов утечки воздуха из легких. Широкая рентгенопрозрачная полоса в виде ореола полностью окружает сердце, включая диафрагмальную поверхность. Такую картину легко отличить от проявлений любого другого синдрома утечки воздуха из легких по характерному расположению воздуха вокруг сердца, выявляемого во всех проекциях.
VI. Лечение
А. Профилактика. Лучший метод лечения синдромов утечки воздуха из легких — это их профилактика. В профилактике баротравмы легких большую роль играют обдуманное применение искусственной вентиляции легких с тщательным подбором оптимальных значений расширяющего давления, ПДКВ, времени вдоха и своевременное смягчение параметров вентиляции для постепенного перевода ребенка на самостоятельное дыхание при улучшении его состояния. Однако, несмотря на высококвалифицированное проведение искусственной вентиляции легких новорожденным, синдромы утечки воздуха из легких остаются одной из главных проблем неонатальных центров.
Б. Интерстициальная эмфизема легких. По вопросу о лечении ИЭЛ нет единого мнения.
1. Уменьшение баротравмы. Как только диагностирована ИЭЛ, необходимо попытаться смягчить параметры вентиляции и уменьшить баротравму легких. Для этого следует уменьшить максимальное давление на вдохе, ПДКВ или сократить время вдоха. Все эти действия позволят уменьшить баротравму и, возможно, тяжесть ИЭЛ. В это время не удастся избежать некоторой степени гиперкапнии и гипоксии.
2. В некоторых случаях при односторонней ИЭЛ эффективным может оказаться «шинирование» пораженной половины грудной клетки (укладывание ребенка на больной бок под углом 90°).
3. Другие методы лечения. К инвазивным методам лечения относятся коллабирование легкого на стороне поражения или на стороне более выраженной ИЭЛ при двустороннем процессе путем селективной интубации бронхов и даже введение в плевральную полость дренажной трубки еще до развития пневмоторакса.
4. Струйная вентиляция легких. В настоящее время проводятся клинические испытания высокочастотной струйной и осцилляторной вентиляции легких.
В. Пневмоторакс. Лечение пневмоторакса будет зависеть от клинической ситуации, в которой он развился.
1. Дополнительная оксигенация. Для доношенного новорожденного с умеренно выраженными симптомами пневмоторакса достаточной может оказаться лишь дополнительная оксигенация (обычно 100% кислородом через палатку). Этот метод лечения не подходит для недоношенных новорожденных из-за риска развития ретинопатии недоношенных.
2. Декомпрессия. Новорожденному с симптомами напряженного пневмоторакса или находящемуся на искусственной вентиляции легких показано немедленное удаление воздуха из плевральной полости. В конечном счете требуется введение в плевральную полость дренажной трубки соответствующего размера.
Г. Пневмомедиастинум. Специальных методов лечения пневмомедиастинума не существует. Следует противостоять соблазну дренировать средостение, так как это не принесет пользы и породит больше проблем, чем разрешит. Если вы считаете, что наличие у новорожденного пневмомедиастинума отражается на его состоянии, обеспечьте дополнительную оксигенацию с целью вымывания из легких и средостения азота (только для доношенных детей).
Д. Пневмоперикард. Пневмоперикард необходимо лечить. Лечение заключается в постоянном дренировании полости перикарда или повторных пункциях перикарда.
Источник
