Синдром укороченного qt чем опасен
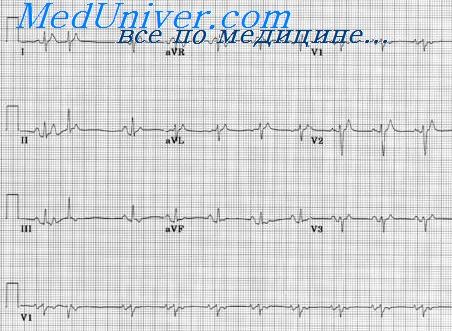
Синдром укороченного интервала QT (SQTS — short Q-T syndrome) — наследственная электрическая болезнь сердца, которая характеризуется укороченным интервалом QT и пароксизмальными тахиаритмиями как результатом ускоренной реполяризации миокарда (предсердий и желудочков) вследствие врожденных сердечных каналопатий. Для понимания сущности SQTS необходимо помнить, что интервал QT представляет собой графическое отражение реполяризации желудочков на ЭКГ и что существует постоянная взаимосвязь между эффективным рефрактерным периодом (ЭРП) желудочков и интервалом QT.
Были описаны три основных генетических варианта SQTS и все они связаны с мутациями генов калиевых каналов, которые (мутации) приводят к ускоренному току ионов калия (через калиевые каналы), что, в свою очередь, вызывает укорочение продолжительности потенциала действия. Синдром SQTS первого типа обусловлен мутациями в гене KCNH2 (HERG), SQTS второго типа — в гене KCNQ1, SQTS третьего типа — в гене KCNJ2.
Во всех опубликованных на сегодняшний день статьях о синдроме укороченного интервала QT диагноз SQTS был основан на зарегистрированном на ЭКГ при нормальной ЧСС интервале QT не более 320 мс (однако по последним данным при SQTS интервал QT может быть более 320 мс). Интервал Q-T традиционно корригируется с частотой сердечных сокращений, а у больных с SQTS при изменении ЧСС интервал QT изменяется минимально. Корригированный интервал Q-T (рассчитываемый по формуле Bazett — QTс = QT / (RR)0,5 при RR < 1000 мс) для постановки диагноза SQTS следует определять при частоте сердечных сокращений менее 100 уд/мин. Это особенно важно при диагностике данного синдрома у детей, так как у них даже в состоянии покоя наблюдается более высокая ЧСС.
SQTS обычно возникает у молодых людей без сопутствующей сердечно-сосудистой патологии. Основными клиническими проявлениями заболевания являются синкопальные состояния, обусловленные пароксизмами желудочковой тахикардии, что сопровождается повышенным риском внезапной сердечной смерти ( ВСС), случаи которой описаны у больных всех возрастных групп. Достаточно часто заболевание проявляется также пароксизмами мерцательной аритмии. Таким образом, наличие в семье случаев внезапной смерти в молодом возрасте, синкопальных состояний неясной этиологии требует исключения SQTS.
Диагностика SQTS производится с помощью измерения интервала QT в 12 отведениях на ЭКГ. При интервале QTс менее 350 мс необходимо проводить дифференциальную диагностику, в том числе со вторичным SQTS, приводящему к обратимому укорочению интервала QT) и возникающему на фоне гиперкалиемии, гиперкальциемии, ацидоза, отравлении препаратами наперстянки и гипертермии. Кроме того, гормоны стресса, такие как ацетилхолин и катехоламины или тестостерон, также могут быть причиной укорочения интервала QT. Таким образом, для постановки диагноза SQTS необходимо учитывать не только длину интервала QT, но анамнез заболевания, клинические проявления, данные ЭКГ, в том числе и морфологию зубца T (по данным ЭКГ у всех пациентов с интервалом QT менее 320 мс наблюдается укорочение или отсутствие сегмента ST, часто высокий, узкий и симметричный зубец Т в правых прекордиальных отведениях).
Проведение электрофизиологического исследования (ЭФИ — эпикардиальная или эндокардиальная, или чреспищеводная электрическая стимуляция сердца) бессимптомным больным имеет значение в стратификации риска ВСС. Исследование позволяет подтвердить укорочение эффективных рефрактерных периодов миокарда предсердий и желудочков, который обычно составляет 120 — 180 мс. Индукция фибрилляции желудочков (ФЖ) и фибрилляции предсердий (ФП) при проведении ЭФИ регистрируется при этом заболевании в 90% случаев.
В клинической практике целесообразно выделение диагноза SQTS как основного у больных группы риска (лица с отягощенным семейным анамнезом по случаям внезапной сердечной смерти и/или синкопальными состояниями неясной этиологии), при отсутствии характерных признаков других заболеваний типа синдрома Бругада, аритмогенной дисплазии правого желудочка и др., более полно клинически очерченных на сегодняшний день.
В настоящее время генетический скрининг SQTS находится в стадии исследования. В связи с этим решающая роль отводится анализу ЭКГ больных и прогнозированию на основании ее параметров возникновения аритмий, угрожающих жизни, так как зачастую первым симптомом данного заболевания является внезапная сердечная смерть у физически здоровых людей. Риск внезапной смерти присутствует на протяжении всей жизни, как у детей в возрасте до одного года, так и у взрослых пациентов старше 60 лет.
Общепринятые принципы лечения пациентов с SQTS не определены. В настоящее время терапией выбора при предотвращении ВСС у больных SQTS является имплантация кардиовертера-дефибриллятора (КВД). Эффективным для удлинения интервала QT эффективным признан хинидин, который нормализует соотношение интервала QT и ЧСС, а также ЭРП желудочков (не эффективными являются антиаритмические препараты, такие как ибутилид, соталол, флекаинид). К тому же хинидин может быть использован как дополнение к КВД у пациентов с пароксизмами ФП, ФЖ и желудочковых тахикардий.
Источник
- 1 Синдром укороченного интервала QT
- 1.1 Введение
- 1.1.1 Эпидемиология
- 1.1.2 Этиология
- 1.2 Классификация
- 1.3 Диагностика
- 1.4 Дифференциальная диагностика
Синдром укороченного интервала QT
Введение
Синдром укороченного интервала QT (Short QT Syndrome; ShortQTS) является редким заболеванием, распространённость которого в популяции в настоящее время неизвестна. Связь укороченного интервала QT с пароксизмами мерцательной аритмии и фибрилляцией желудочков впервые описана I. Gussak в 2000г.
Основными клиническими проявлениями заболевания являются синкопальные состояния, обусловленные пароксизмами желудочковой тахикардии, что сопровождается повышенным риском внезапной сердечно-сосудистой смерти, случаи которой описаны у больных всех возрастных групп. Достаточно часто заболевание проявляется также пароксизмами мерцательной аритмии.
Наследование заболевания осуществляется по аутосомно-доминантному типу.
Эпидемиология
Распространённость заболевания в популяции неизвестна.
Этиология
Укорочение интервала QT вызывают мутации в генах калиевых каналов, приводящие к усилению генерируемых ими токов К+, укорочению длительности фазы реполяризации потенциала действия и уменьшению продолжительности рефрактерных периодов возбудимых тканей сердца, что сопровождается уменьшением длины волны возбуждения, предрасполагающем к возникновению аритмий по механизму re-entry.
Классификация
Описаны 3 молекулярно-генетических типа синдрома (табл. 1). Данные мутации обнаруживают лишь у 20% больных синдромом укороченного интервала QT.Таблица 1. Молекулярно-генетическая классификация синдрома укороченного интервала QT
Диагностика
Характерными изменениями ЭКГ при данном синдроме являются уменьшение продолжительности интервалов QT/QTc и высокий симметричный зубец T в правых прекордиальных отведениях (рис. 1) Описывают также проявления обратной частотной зависимости величины интервала QT — укорочение этого показателя при снижении частоты сердечного ритма.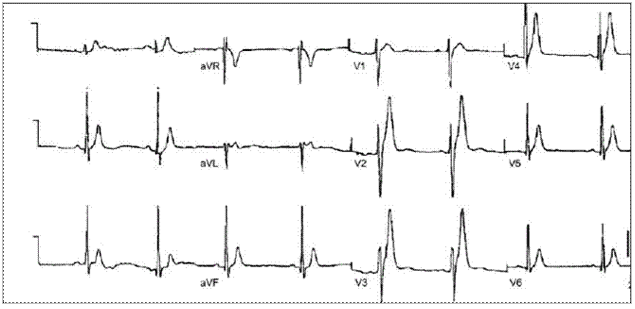
Рис. 1. ЭКГ пациента с синдромом укороченного интервала QT. Высокоамплитудные симметричные зубцы T в V2–V4. QT = 220 мс.В настоящее время диагностически значимой считается продолжительность QTc ≤330 мс.
Диагноз синдрома укороченного интервала QT также правомочен при продолжительности QTс <360 мс в тех случаях, когда выявлена генетическая мутация, и/или семейный анамнез отягощен случаями внезапной сердечно-сосудистой смерти, и/или синдром укороченного интервала QT установлен у родственников больного, а также у тех лиц, которые пережили ВСС при отсутствии у них органического поражения сердца.
Проведение ЭФИ бессимптомным больным имеет значение в стратификации риска ВСС. Исследование позволяет подтвердить укорочение эффективных рефрактерных периодов миокарда предсердий и желудочков, который обычно составляет 120–180 мс. Индукция ФЖ и ФП при проведении ЭФИ регистрируется при этом заболевании в 90% случаев.
В настоящее время рутинное проведение молекулярно-генетических исследований для диагностики заболевания не рекомендовано. Целесообразно проведение селективных молекулярно-генетических исследований близких родственников больного при обнаружении у него патогномоничной данному заболеванию мутации.
Дифференциальная диагностика
Синдром укороченного интервала QT следует дифференцировать от других возможных причин синкопальных состояний, учитывая относительно молодой возраст больных, прежде всего, от эпилепсии и вазо-вагальных обмороков, а также от других врождённых желудочковых нарушений ритма сердца.
Источник
Синдром короткого интервала QT. Клиника синдрома короткого интервала QT
Первое сообщение о синдроме короткого QT (CK QT, или SQTS) у 4 пациентов с интервалом QT < 300 мсек было вызвано возникновением ФП во время брюшной операции у девочки с очень коротким интервалом QT. Через несколько лет были опубликованы данные о новых случаях, вызвавшие большой интерес. Информации о CK QT пока еще мало.
Идентифицированы три различных гена с мутациями, вызывающими СК QT. Все они связаны с другими каналопатиями с вовлечением потока К+ увеличение функции. CK QT и СУ QT действительно близко связаны.
SQT1 связан с мутацией KCNH2 (ген дли LQT2), приводящей к увеличению тока IKr. SQT2 связан с мутацией KCNQ1 (ген для LQT1), вызывающей увеличение тока IK. SQT3 связан С мутацией KCNJ2 (ген синдрома Andersen-Tawil), приводящей к увеличению тока Ik1.
Помимо очевидно отличающейся формы волны Т при SQT3, характеризующейся почти нормальной фазой нарастания и быстрой фазой снижения, нет никаких отличительных особенностей для определения CK QT. Однако это может свидетельствовать о недостаточности знаний в этом вопросе.
Основной признак синдрома короткого интервала QT — короткий интервал QT. О вероятном наличии «молчаливых» носителей мутации, довольно распространенных при LQT6, в настоящее время отсутствуют сообщения для СК QТ. Недавно абсолютной величиной, указывающей на СК QТ, считали интервал QТ 300-320 мсек, с небольшим разбросом данных.

Однако эти измерения должны быть сделаны при ЧСС < 80 уд/мин, поскольку один из отличительных признаков СК QТ зависит от ЧСС. Важно, что у детей трудно определить СК QT. В диагностическом процессе необходимо исключить вторичные причины СК QT, такие как гиперкальциемия, гиперкалиемия, гипертермия, ацидоз и применение дигоксина.
Другое основное клиническое проявление синдрома короткого интервала QТ — частый предсердный и желудочковый ритмы, в т.ч. фибрилляция. СК QT следует подозревать у больных с коротким интервалом QT(< 350 мсек) и ФП либо первичной ФЖ, с семейным анамнезом ВСС или остановкой сердца, или SIDS. Недавно поступило сообщение о 3 младенцах в возрасте < 1 года с мутацией KCNQ1 и эффектами, типичными для СК QT, которым был поставлен диагноз SIDS.
Таким образом, синдром короткого интервала QT следует рассматривать как одну из каналопатий, вызывающих синдром ВС у детей, где СУ QT также играет существенную роль. Эта концепция была подтверждена недавней информацией о выявлении у младенца с мутацией KCNQI укорочения продолжительности ПД с сердечными симптомами во внутриутробном периоде и диагностированным СК QТ после кесаревого сечения.
У немногих пациентов, которым проводили электрофизиологическое исследование, эффективные рефрактерные периоды предсердий и желудочков были короткими (140-150 мсек). Почти у всех этих пациентов индуцировали ФЖ или трепетание.
Пока не ясно, как вести больных с синдромом короткого интервала QТ, что в значительной степени связано с небольшим количеством пациентов и ограниченным периодом наблюдения. Учитывая высокий риск ВСС и недостаток лекарственных средств с доказанной эффективностью в предотвращении ВСС, рекомендуют установить ИКД для вторичной профилактики ФЖ. ИКД следует рекомендовать также пациентам в целях первичной профилактики ФЖ. Решение об установке ИКД является трудным, т.к. отсутствуют параметры стратификации пациентов с высоким риском ВС.
Есть сообщения о неоправданных нанесениях электрических разрядов ИКД из-за неадекватной оценки им зубца Т, что также создает проблему профилактической имплантации прибора.
Идет постоянный поиск антиаритмических средств, особенно для детей. Соталол, ибутилид и флекаинид оказались неэффективными, но хинидин нормализовал интервал QT в покое у небольшого количества пациентов. Эти изменения сопровождались удлинением эффективного рефрактерного периода желудочков.
— Также рекомендуем «Генетические болезни миокарда. Наследственные причины кардиомиопатий»
Оглавление темы «Наследственные нарушения ритма и поражения миокарда»:
1. Генетика синдрома удлиненного интервала QT. Лечение синдрома удлиненного интервала QT
2. Фенотип синдрома удлиненного интервала QT. Риск развития синдрома удлиненного интервала QT
3. Синдром Brugada. Генетические основы синдрома Бругада
4. Прогноз синдрома Бругада. Катехоламинергическая полиморфная желудочковая тахикардия (KПЖТ)
5. Аутосомно-доминантная форма катехоламинергической полиморфной желудочковой тахикардии. Аутосомно-рецессивная KПЖТ
6. Синдром короткого интервала QT. Клиника синдрома короткого интервала QT
7. Генетические болезни миокарда. Наследственные причины кардиомиопатий
8. Гипертрофия миокарда. Мутация саркомеров при гипертрофической кардиомиопатии (ГКМП)
9. Мутация белков толстых филаментов миокарда. Альфа-изоформа МНС предсердий и желудочков сердца
10. Предрасположенность к аритмиям при ГКМП. Титин при гипертрофической кардиомиопатии
Источник
Смерть человека — всегда горе. Но когда она, не оставив признаков на вскрытии, настигает здоровых людей в расцвете лет, это горе исключительное. Однако соболезнуя родственникам умершего, врач-кардиолог в такой ситуации одновременно испытывает надежду, что с каждым годом таких смертей будет все меньше, поскольку область медицины, связанная с кардиопатиями, приводящими к таким трагедиям, сегодня быстро и успешно развивается. Этой теме был посвящен доклад руководителя Центра синкопальных состояний и сердечных аритмий у детей и подростков ФМБА России профессора Леонида Михайловича МАКАРОВА и врача центра, кандидата медицинских наук Веры Николаевны КОМОЛЯТОВОЙ, представленный на II Международном конгрессе «Актуальные вопросы критических состояний у детей и стимуляционные образовательные программы».
Неполадки в каналах, обрывающие жизнь
Внезапной считают ненасильственную смерть, наступающую на фоне кажущегося здоровья при отсутствии каких-либо тревожных предвестников. Внезапная сердечная смерть (ВСС) — это естественная смерть, связанная с кардиальными причинами, которой предшествует потеря сознания в течение до 24 часов после появления симптомов. Время и характер смерти являются неожиданными, независимо от того, страдал ли пациент заболеваниями сердца ранее или недуг проявился впервые. Значительно чаще (в 70—80% случаев) ВСС поражает мужчин.
ВСС сегодня является предметом активного изучения в развитых странах, поскольку она составляет более 95% любой внезапной смерти людей молодого возраста, верхняя граница которого обычно обозначается как 45 лет. И хотя, казалось бы, «лидировать» среди оставшихся 5% должны цереброваскулярные катастрофы и разрывы крупных сосудов, в этой группе различные заболевания наблюдаются с незначительно отличающейся частотой.
В России доля ВСС у лиц в возрасте 1—45 лет составляет примерно 6,5%. Только в Москве ежегодно внезапно умирает вне ЛПУ более 2,5 тысячи молодых людей. Примерно такая же ситуация зафиксирована и в развитых странах. Но если проанализировать данные по внезапной смерти во всех возрастных категориях, то здесь общий процент умерших от общего числа смертей в России составляет примерно 40%. Это более чем в четыре раза выше аналогичного показателя в развитых странах. Причины здесь явно не только в недостатках отечественного здравоохранения и медицинской безграмотности населения, но и нежелании значительной части россиян (по разным оценкам, около 30%) заботиться о своем здоровье.
Причиной большинства случаев ВСС, особенно у людей моложе 30 лет, является группа заболеваний, называемых первичными или врожденными каналопатиями, которые не сопровождаются структурными изменениями миокарда и проявляются преимущественно электрофизиологическими нарушениями в кардиомиоцитах. Для этой группы состояний высокий риск ВСС характерен из-за развития жизнеугрожающих нарушений ритма или проводимости в сердце.
Если в основе первичных каналопатий лежат мутации генов, кодирующих белки ионных каналов, экспрессирующихся в миокарде, то вторичные каналопатии характерны для любых возрастов. Наступают же они в результате воздействия неблагоприятных факторов, главным образом, побочных эффектов лекарств, но также низкобелковой диеты, миокардитов, внутричерепных кровоизлияний и других причин. Распространенность вторичных каналопатий очень велика.
Например, пациенты, проходящие психофармакотерапию, подвержены в 2 раза более высокому риску ВСС. Тем не менее опасность первичных каналопатий значительно выше, чем вторичных, так как эти заболевания, несмотря на существенные успехи поддерживающего лечения, остаются абсолютно неизлечимыми. Вторичные же каналопатии обычно проходят после отмены фармакопрепаратов или прекращения действия иных повреждающих факторов.
К наиболее изученным в настоящее время относятся 4 первичные каналопатии: синдром Бругада, синдромы удлиненного и укороченного интервала QT, а также катехоламинергическая полиморфная желудочковая тахикардия.
Синдром удлиненного интервала QT (CУИ QT)
В норме интервал QT отражает электрическую систолу желудочков (время от начала комплекса QRS до конца зубца Т), причем нормализированный по частоте сердечного ритма, так называемый корригированный интервал QT, составляет 340—450 мс для женщин и 340—430 для мужчин.
ЭКГ-признаки СУИ QT — это удлинение интервала QT более нормы, альтернация зубца Т, то есть изменение его формы, полярности, амплитуды.
В отсутствие лечения риск ВСС при врожденном СУИ QT достигает 85% (причина — фатальные фибрилляция и аритмии желудочков). При этом 20% детей умирает в течение года после первой потери сознания, и более половины — в первое десятилетие жизни.
Заболевание вызывают мутации в 8 генах, кодирующих калиевые и натриевые каналы сердца. В клинической картине доминируют приступы стрессиндуцированных потерь сознания (синкопе), имеющие типичных предвестников. Внезапная общая слабость, потемнение в глазах, сердцебиение, тяжесть за грудиной, за которыми следует быстрое, без амнезии и сонливости, восстановление сознания. Бессознательное состояние длится 1—2 минуты и в половине случаев сопровождается эпилептиформными судорогами. Критерием для уточнения диагноза являются также случаи выявления подобного синдрома в семье.
Синдром короткого интервала QT (СКИ QT)
Основной ЭКГ признак — укорочение интервала QT менее 340 мс (зачастую даже менее 300 мс), а также высокие и заостроенные зубцы Т.
СКИ QT столь же высоко, как и СУИ QT, ассоциировано с увеличенным риском ВСС по причине фибрилляции желудочков. Хотя причиной этого заболевания являются нарушения в тех же генах, которые ответственны за СКУ QT, функциональные эффекты мутаций, приводящих к синдрому СКИ QT, диаметрально противоположны. Измененные калиевые каналы характеризуются не блокадой, а увеличением калиевых токов, а, следовательно, скорости реполяризации, что и проявляется на ЭКГ укорочением интервала QT. В итоге же, как и при удлиненном QT, нарушение нормальной продолжительности реполяризации в миокарде приводит к негомогенности электрических процессов, что является субстратом для развития жизнеугрожающих аритмий, а также синкопальных состояний, протекающих с теми же проявлениями, что и при СУИ QT. Из-за наследственной природы заболевания в семьях пациентов прослеживаются случаи ВСС.
Синдром Бругада
Так называют генетически детерминированное нарушение сердечного ритма. Оно характеризуется синкопальными состояниями, подъемом сегмента ST над изоэлектрической линией в отведениях V1—V3, полной или неполной блокадой правой ножки пучка Гиса и высоким риском развития жизнеугрожающих желудочковых тахиаритмий, обычно развивающихся в вечерние и ночные часы, когда больной находится во сне или в спокойном состоянии.
Изменения сегмента ST могут быть 2-х типов: сводчатый и седловидный. Наибольшей диагностической значимостью и в то же время повышенной прогностической неблагоприятностью обладает первый тип. Но он встречается достаточно редко. Кроме того, даже у больных с подтвержденным диагнозом изменения «сводчатого» типа выявляются непостоянно. Наличие же у больного изменений на ЭКГ «седловидного» ST позволяет только заподозрить синдром Бругада. Для верификации диагноза необходимы нагрузочные пробы с лекарственной нагрузкой (антиаритмические препараты IA класса).
Известны 5 генов, мутации которых ответственны за развитие этого состояния. Ионными механизмами синдрома Бругада является потеря функции натриевых каналов, что приводит к преждевременной реполяризации эпикарда. Чаще всего указанный синдром развивается на 3—4-й декаде жизни. Случаи внезапной смерти у родственников больных синдромом Бругада обычно происходили также во сне или при внезапном пробуждении практически здоровых мужчин 30—50 лет.
Катехоламинергическая полиморфная желудочковая тахикардия (КПЖТ)
Среди известных каналопатий является наиболее опасной и сложной. Основные ЭКГ-признаки — три и более широких комплекса QRS (в разных возрастах — превышения нормальной продолжительности от 60 до 120 мс); дискордантные отношения между главным зубцом QRS и конечной частью желудочкового комплекса RS-T и Т; частота желудочковых сокращений от 150 до 250 уд/мин; отсутствие Р-волны перед QRS-комплексом; стабильно короткий интервал R-R; внезапное начало и окончание тахикардии.
Обмороки вызываются исключительно физическими нагрузками или эмоциональным стрессом, болезнь дебютирует в возрасте 6—8 лет. У одной трети пациентов с КПЖТ есть семейная история преждевременной внезапной смерти или синкопальных состояний, вызванных стрессом. Причина заболевания — мутации генов, кодирующих белки, ответственные за чресканальный транспорт ионов кальция.
Лечение лекарственное, электроимпульсное и хирургическое
Наиболее распространенными препаратами в фармакотерапии каналопатий являются ?-адреноблокаторы (пропранолол по 1—3 мг/кг или 120—1000 мг/сут), устраняющие аритмогенные симпатические влияния на проводящую систему сердца, подавляющие гетерогенный автоматизм, стабилизирующие содержание калия в миокарде. ?-адреноблокаторы могут назначаться в сочетании с препаратами магния и блокаторами кальциевых каналов, в частности, верапамилом. Также могут быть использованы препараты калия и блокаторы натриевых каналов (мексилетин, флекаинид).
В лечении каналопатий, поскольку уже известны конкретные мутации, вызывающие те или иные варианты синдромов, разрабатывается генспецифическая терапия. Например, доказано существование нескольких типов CУИ QT. 1-й тип данного синдрома запускает мутация гена KVLQT1, кодирующего структуру ?-субъединицы медленных калиевых каналов кардиомиоцитов, обеспечивающих медленный компонент калиевого тока фазы реполяризации. При 2-м типе CУИ QT повреждается ген HERG, кодирующий структуру ?-субъединицы быстрых калиевых каналов, определяющих быстрый компонент калиевого тока. 3-й тип синдрома связан с мутацией гена SCN5A, кодирующего структуру белка натриевых каналов, обеспечивающих натриевый ток фазы реполяризации.
Установлено, что ?-адреноблокаторы наиболее эффективны при синдроме 1-го типа, препараты калия — 2-го типа, а блокаторы натриевых каналов (мексилетин) — 3-го типа. При неэффективности фармакотерапии имплантируются электрокардиостимуляторы или кардиовертеры-дефибрилляторы в сочетании с применением ?-адреноблокаторов. Кардиовертеры-дефибрилляторы используют у пациентов с врожденными каналопатиями при высоком риске ВСС, особенно при указании в анамнезе на фибрилляцию желудочков. После имплантации кардиовертера-дефибриллятора риск внезапной смерти при тяжелом течении каналопатий снижается до 1—5%.
При непереносимости или неэффективности ?-адреноблокаторов, отсутствии эффекта от электрокардиостимулятора и невозможности имплантировать кардиовертер-дефибриллятор пациентам с указанными синдромами выполняют левостороннюю шейно-грудную симпатэктомию, что обеспечивает устранение дисбаланса симпатической иннервации сердца.
Но третья сестренка будет жить!
Для успешной борьбы с теми сердечными заболеваниями, о которых идет речь, крайне важными являются мероприятия в области организации здравоохранения. В первую очередь это относится к усовершенствованию работы уже действующих и созданию новых специализированных центров, в задачи которых входит лечение и профилактика жизнеугрожающих аритмий, обучение врачей первичного звена, научно-медицинские исследования.
Одним из немногих подобных учреждений в России стал Центр синкопальных состояний и сердечных аритмий у детей и подростков Федерального медико-биологического агентства (ЦСССА), организованный на базе Детской клинической больницы №38 ФМБА России в 2007 году. О том, зачем нужны подобные центры и как они работают, лучше всего расскажет такой случай.
С интервалом в 4 месяца две девочки-близнеца (4 года 7 месяцев и 4 года 10 месяцев) внезапно умерли при одних и тех же обстоятельствах: когда бежали навстречу матери, пришедшей, чтобы забрать их из детского сада, который находится в одном из крупных городов России. Хотя вторая из этих близнецов прошла, казалось бы, тщательное обследование, у нее не было выявлено каких-либо реальных причин смерти, в том числе и повышенного риска жизнеугрожающей аритмии. А посмертный диагноз был сформулирован как иммунодефицитное состояние.
Через год после этих событий, в середине 2009 года, в этой семье мама все-таки решилась родить еще девочку. Естественно возник вопрос — насколько велик для нее риск внезапной смерти? После обследования в ведущих клиниках региона, а затем и Москвы, врачи не определили каких-либо опасных изменений в организме ни у этого ребенка, ни (судя по оценке медицинских документов, сделанной после смерти близнецов) у обеих ее старших сестер.
Чтобы разобраться в ситуации, потребовалась консультация Л.М. Макарова. Проанализировав электрокардиограммы погибших девочек, он выявил у них признаки редкого, но крайне опасного в детском возрасте врожденного заболевания проводящей системы сердца — болезнь Лева—Ленегра. Раннее обнаружение и лечение этого заболевания, возможно, могло бы спасти жизнь, по крайней мере, одной из сестер.
При обследовании в ЦСССА третьей из сестер очевидных признаков аналогичного заболевания не было выявлено. Однако в совместном обследовании с профессором Центра молекулярной генетики Е.В. Заклязьминской была обнаружена мутация в гене SCN5A, ответственном за это заболевание. Сейчас ребенок периодически обследуется в ЦСССА c применением новейших диагностических тестов, решается вопрос о необходимости имплантации электрокардиостимулятора.
ЦСССА работает в режиме амбулаторного подразделения, где ежегодно наблюдаются и лечатся около тысячи пациентов. Большинство методов лечения и диагностики, используемых в центре (например, частотная динамика QT, турбулентность ритма сердца, микровольтная альтернация Т зубца и др.), основаны на собственных разработках, являются приоритетными в России, а часто и в мире. Многие разработанные сотрудниками центра методики давно стали стандартными для большинства клиник в нашей стране.
Сотрудники центра участвовали в создании практически всех российских рекомендаций по диагностике и лечению жизнеугрожающих аритмий у детей за последние 20 лет. Руководитель ЦСССА профессор Л.М. Макаров является президентом Российского холтеровского общества (РОХМИНЭ). Авторитет российских специалистов, которых объединяет под руководством Л.М. Макарова эта общественная организация (в том числе ведущих сотрудников ЦСССА), позволил получить право на проведение в России одного из наиболее авторитетных в мире съезда кардиологов — XIV Международного конгресса по неинвазивной электрокардиологии. Он состоится в Москве 26—28 апреля 2011 года (www.ISHNE2011.ru), и его почетными президентами должны стать лауреаты Нобелевской премии Е.И. Чазов (Россия) и Б. Лаун (США).
Этот конгресс проводится раз в два года и никогда не повторяется в одной стране дважды. В Россию приедут все ведущие специалисты по проблеме внезапной смерти, ранней диагностике и лечению больных с сердечными заболеваниями. Участие российских врачей в этом форуме позволит поднять на уровень мировых стандартов знания наших специалистов, внедрить в практику последние технологии, а в итоге более успешно бороться с опаснейшими сердечными заболеваниями.
Александр РЫЛОВ
ВСС — это и патофизиологический механизм, и клинический диагноз. По Международной классификации болезней ВОЗ (2007), диагноз I 46.1 означает внезапную сердечную смерть, I 46.0 — остановку сердца с успешной реанимацией, а I 46.9 — остановку сердца неспецифическую, то есть такую, где причина осталась непонятной.
Проблема внезапной сердечной смерти — одна из наиболее актуальных в клинической медицине. Наибольшую группу составляют, во-первых, дети и лица молодого возраста, страдающие врожденными (или первичными) каналопатиями, во-вторых, пациенты зрелого и пожилого возраста, перенесшие инфаркт миокарда и другие коронарные кризы, страдающие ишемической болезнью сердца и сердечной недостаточностью с низкой фракцией выброса.
По результатам вскрытий органических нарушений не обнаруживается примерно у 40% молодых людей, погибших от ВСС. У трети пациентов подобная смерть является первым проявлением болезни. У лиц старше 30 лет в качестве причины ВВС преобладает ИБС, а моложе — группа заболеваний, называемых первичными каналопатиями.
По данным американского Регистра внезапной смерти, связанной с физической нагрузкой у молодых лиц, за период с 2000 по 2006 год выживаемость в последние 3 года анализа практически удвоилась по сравнению с таковой в начальный период исследования. При этом только в 2006 году при успешном восстановлении жизнедеятельности после остановки сердца отмечено одинаковое число случаев применения автоматических наружных дефибрилляторов, расположенных в общественных местах, и электрических дефибрилляций, выполненных специализированными бригадами скорой помощи.
Несомненна провоцирующая роль алкоголя как этиологического фактора алкогольной кардиомиопатии, угрожающих жизни аритмий при первичных каналопатиях, мерцательной аритмии, развитии так называемого синдрома праздничного сердца. Алкоголь нарушает электрическую стабильность миокарда, вариабельность интервала QT, что может способствовать развитию опасных желудочковых аритмий и внезапной сердечной смерти (ВСС). Это подчеркивает необходимость учета употребления алкоголя как значимого фактора в определении риска ВСС и разработке мер по ее профилактике.
Практически при всех каналопатиях во всем мире 30—40% больных из-за ошибок диагностики начинают проходить лечение от эпилепсии, поскольку основные проявления этих патологий — обмороки, зачастую с сопутствующими судорогами. И если вовремя не распознать болезнь, не все эти пациенты, к сожалению, успевают попасть к кардиологу.
Источник
